26/01/2023
En el fascinante mundo de la química, cada reacción es como una receta culinaria, donde los ingredientes, o reactivos, se combinan para formar nuevos platos, o productos. Pero, ¿qué sucede si no tenemos las cantidades exactas de todos los ingredientes que la receta pide? En la cocina, podríamos quedarnos sin pastel. En la química, nos encontramos con un concepto fundamental: el reactivo limitante. Comprender este principio es crucial no solo para los químicos de laboratorio, sino para cualquiera que desee entender cómo se optimizan los procesos y cómo se determina la cantidad máxima de algo que se puede producir a partir de unos recursos dados. Este conocimiento es la piedra angular para predecir rendimientos, minimizar desperdicios y, en última instancia, dominar el arte de las transformaciones químicas.
La mayoría de las veces, cuando se lleva a cabo una reacción química, los reactivos no se presentan en las cantidades estequiométricamente perfectas que indica su ecuación balanceada. Imagina que estás construyendo bicicletas: necesitas dos ruedas y un cuadro para cada una. Si tienes 10 ruedas y 3 cuadros, ¿cuántas bicicletas puedes armar? Rápidamente te das cuenta de que solo puedes hacer 3 bicicletas, porque los cuadros son el factor que te detiene. Las ruedas te sobrarían. En química, este 'cuadro' que se agota primero es lo que conocemos como el reactivo limitante.
- ¿Qué es Exactamente el Reactivo Limitante?
- La Importancia del Reactivo Limitante en la Vida y la Industria
- ¿Cómo Determinar el Reactivo Limitante? Un Enfoque Paso a Paso
- El Rendimiento Teórico: El Máximo Posible
- ¿Cómo Afecta la Cantidad de los Reactivos al Rendimiento de la Reacción?
- Tabla Comparativa: Reactivo Limitante vs. Reactivo en Exceso
- Preguntas Frecuentes (FAQ)
- ¿Por qué es tan importante balancear la ecuación química antes de determinar el reactivo limitante?
- ¿Puede haber más de un reactivo limitante en una reacción?
- ¿Qué es el rendimiento porcentual y cómo se relaciona con el reactivo limitante?
- ¿Es posible que no haya un reactivo limitante?
- ¿Qué significa que el reactivo limitante da un 'salto' en las cantidades?
- Conclusión
¿Qué es Exactamente el Reactivo Limitante?
El reactivo limitante es aquel que, en una reacción química, se consume por completo en primer lugar. Su presencia, o más bien su agotamiento, es lo que 'limita' la cantidad total de producto que se puede formar. Una vez que este reactivo se acaba, la reacción se detiene, sin importar cuánto de los otros reactivos (los reactivos en exceso) todavía quede disponible. Es el 'cuadro' de nuestra analogía de las bicicletas, el ingrediente que dicta el ritmo y el final de la producción.
Este concepto es vital porque la cantidad de producto que se obtiene está directamente determinada por la cantidad inicial del reactivo limitante. Si duplicas la cantidad del reactivo limitante (asumiendo que los demás reactivos están en exceso), podrías duplicar la cantidad de producto. Si lo reduces a la mitad, la producción se reducirá a la mitad. Es el 'cuello de botella' de la reacción.
La Importancia del Reactivo Limitante en la Vida y la Industria
Más allá de los libros de texto, el concepto de reactivo limitante tiene aplicaciones prácticas inmensas. En la industria, por ejemplo, donde la eficiencia y la rentabilidad son clave, los químicos utilizan este principio para asegurarse de que un reactivo particularmente costoso sea completamente consumido en el transcurso de una reacción. Esto maximiza el aprovechamiento de la inversión y minimiza el desperdicio de materiales valiosos. Pensemos en la fabricación de medicamentos, donde los precursores pueden ser muy caros; identificar y controlar el reactivo limitante es fundamental para optimizar el proceso y reducir costos.
Pero no solo se limita a la industria química. En la vida cotidiana, aunque no lo llamemos por su nombre técnico, aplicamos este concepto intuitivamente. Al cocinar, si una receta pide 2 huevos y 1 taza de harina para un pastel, pero solo tienes 1 huevo, el huevo es tu 'reactivo limitante' y no podrás hacer el pastel completo. En la agricultura, la disponibilidad de un nutriente específico en el suelo (nitrógeno, fósforo) puede ser el factor limitante para el crecimiento de los cultivos, incluso si hay abundante agua y luz solar.
¿Cómo Determinar el Reactivo Limitante? Un Enfoque Paso a Paso
Determinar el reactivo limitante es una habilidad fundamental en estequiometría. Aquí te presentamos un método sistemático para hacerlo:
Ajusta la Ecuación Química
Antes de cualquier cálculo, asegúrate de que la ecuación química esté balanceada. Esto significa que el número de átomos de cada elemento debe ser el mismo en ambos lados de la ecuación (reactivos y productos). La ecuación balanceada te proporciona las proporciones molares correctas entre los reactivos y los productos, que son esenciales para los cálculos estequiométricos.
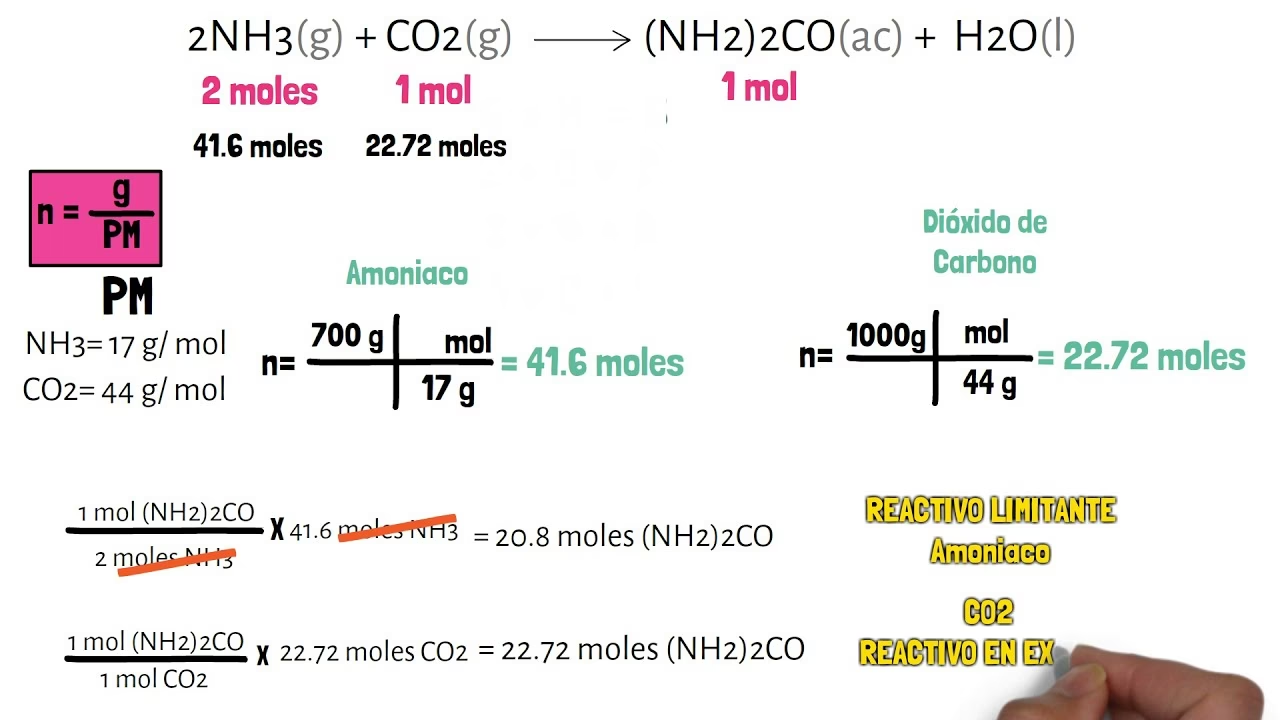
Convierte las Cantidades Dadas a Moles
Generalmente, las cantidades de los reactivos se dan en gramos. Para realizar cálculos estequiométricos, necesitas convertir estas masas a moles utilizando la masa molar de cada sustancia. Los moles son la 'moneda' de la química, ya que las relaciones en la ecuación balanceada se expresan en términos de moles.
Calcula la Cantidad de Producto que Cada Reactivo Podría Producir
Una vez que tienes los moles de cada reactivo, utiliza las relaciones molares de la ecuación balanceada para calcular cuántos moles (o gramos) de un producto específico se podrían formar si *cada* reactivo se consumiera por completo. Haz este cálculo para cada reactivo de forma independiente.
Por ejemplo: Si la reacción es A + 2B → C, y tienes 10 moles de A y 15 moles de B:
- Con 10 moles de A, se formarían 10 moles de C (basado en la relación 1:1 entre A y C).
- Con 15 moles de B, se formarían 7.5 moles de C (basado en la relación 2:1 entre B y C).
Identifica el Reactivo Limitante
El reactivo que produce la menor cantidad de producto es el reactivo limitante. En el ejemplo anterior, B es el reactivo limitante porque solo puede producir 7.5 moles de C, mientras que A podría producir 10 moles de C. El reactivo con el 'menor número de moles de reacción' (la menor proporción de moles disponibles respecto a su coeficiente estequiométrico) es el que se agota primero.
Calcula la Cantidad de Reactivo en Exceso (Opcional pero Útil)
Una vez identificado el reactivo limitante, puedes calcular cuánto del reactivo en exceso reaccionó y cuánto queda sin reaccionar. Esto se hace usando la estequiometría con el reactivo limitante para determinar cuánto del reactivo en exceso se *necesitaba*, y luego restando esa cantidad de la cantidad inicial del reactivo en exceso.

¿Cómo se calcula el rendimiento? A grandes rasgos, el rendimiento es el resultado de dividir la producción real entre la capacidad productiva para un período de tiempo determinado.
El Rendimiento Teórico: El Máximo Posible
La cantidad de producto que se obtiene cuando reacciona todo el reactivo limitante se denomina rendimiento teórico de la reacción. Este es el rendimiento máximo posible que se puede alcanzar bajo las condiciones ideales, asumiendo una reacción completa y sin pérdidas. En la práctica, el rendimiento real de una reacción casi siempre es menor que el rendimiento teórico debido a factores como reacciones secundarias, impurezas o pérdidas durante la purificación del producto. La importancia del reactivo limitante es que nos da la base para calcular este rendimiento teórico, una referencia crucial para evaluar la eficiencia de cualquier proceso químico.
¿Cómo Afecta la Cantidad de los Reactivos al Rendimiento de la Reacción?
La cantidad de los reactivos afecta directamente el rendimiento de la reacción a través del reactivo limitante. Cuanta más cantidad tengamos del reactivo limitante, mayor será la cantidad de producto que podremos formar, hasta que otro factor se convierta en limitante. La relación es directa: si duplicamos la cantidad del reactivo limitante, idealmente duplicaremos el rendimiento teórico. Es crucial entender que los reactivos en exceso, por mucha cantidad que haya de ellos, no aumentarán la cantidad de producto una vez que el reactivo limitante se ha agotado. La reacción se detiene, y los reactivos en exceso simplemente quedan sin reaccionar.
En términos de 'moles de reacción' (una forma de visualizar cuántas 'veces' puede ocurrir la reacción con cada reactivo), el reactivo con el menor valor de moles disponibles dividido por su coeficiente estequiométrico es el limitante. Este valor representa el número máximo de 'unidades' de reacción que se pueden completar. Por lo tanto, el reactivo que permite que la reacción se lleve a cabo el menor número de veces es el que la limita.
Tabla Comparativa: Reactivo Limitante vs. Reactivo en Exceso
| Característica | Reactivo Limitante | Reactivo en Exceso |
|---|---|---|
| Definición | Se consume completamente durante la reacción. | Parte de él queda sin reaccionar al finalizar la reacción. |
| Cantidad de Producto | Determina la cantidad máxima de producto formado. | No determina la cantidad de producto una vez que el limitante se agota. |
| Consumo | Se agota primero. | Se consume parcialmente. |
| Función Principal | Controla el rendimiento teórico de la reacción. | Asegura la reacción completa del reactivo limitante. |
| Optimización Industrial | Se busca que sea el reactivo más costoso para asegurar su consumo total. | Generalmente, se usa en mayor cantidad si es barato o fácil de recuperar. |
Preguntas Frecuentes (FAQ)
¿Por qué es tan importante balancear la ecuación química antes de determinar el reactivo limitante?
Balancear la ecuación química es el primer paso y el más crítico porque establece las proporciones estequiométricas correctas (relaciones molares) entre los reactivos y los productos. Sin una ecuación balanceada, cualquier cálculo de moles o de producto sería incorrecto, llevando a una identificación errónea del reactivo limitante y un cálculo de rendimiento teórico impreciso.
¿Puede haber más de un reactivo limitante en una reacción?
No, por definición, solo puede haber un reactivo limitante en una reacción. Es aquel que se consume completamente primero y detiene la reacción. Todos los demás reactivos que no se agotan por completo son reactivos en exceso.
¿Qué es el rendimiento porcentual y cómo se relaciona con el reactivo limitante?
El rendimiento porcentual es la relación entre el rendimiento real (la cantidad de producto obtenida experimentalmente) y el rendimiento teórico (la cantidad máxima de producto que se podría obtener según el reactivo limitante), multiplicado por 100. Se calcula como: (Rendimiento Real / Rendimiento Teórico) x 100%. El reactivo limitante es fundamental para calcular el rendimiento teórico, que a su vez es necesario para determinar el rendimiento porcentual, una medida clave de la eficiencia de una reacción.
¿Es posible que no haya un reactivo limitante?
Sí, es teóricamente posible, pero extremadamente raro en la práctica. Ocurriría si todos los reactivos se encuentran en proporciones estequiométricamente exactas, es decir, si todos se consumen por completo al mismo tiempo. En un laboratorio o entorno industrial, esto es muy difícil de lograr con precisión, por lo que casi siempre habrá un reactivo limitante y uno o más reactivos en exceso.
¿Qué significa que el reactivo limitante da un 'salto' en las cantidades?
Esta frase se refiere a cómo el reactivo limitante impone un límite abrupto o un 'salto' en la cantidad de producto que se puede formar. Por ejemplo, si tienes los ingredientes para hacer 10 pasteles y solo un ingrediente para hacer 5, ese ingrediente 'salta' y limita la producción a 5 pasteles, no a 10. Su agotamiento provoca un cambio repentino en la disponibilidad de la reacción para continuar.
Conclusión
El concepto de reactivo limitante es mucho más que una simple regla química; es una herramienta esencial para comprender y controlar los procesos de transformación de la materia. Desde el laboratorio de investigación hasta las grandes plantas industriales, pasando por las decisiones cotidianas en el hogar, identificar el reactivo limitante nos permite predecir resultados, optimizar el uso de recursos y maximizar la eficiencia. Al dominar este principio, no solo profundizamos nuestra comprensión de la estequiometría, sino que también desarrollamos una mentalidad analítica que es invaluable en cualquier campo que requiera la gestión y transformación de recursos. La próxima vez que veas una reacción química, recuerda que en el corazón de su producción hay un 'director de orquesta' silencioso pero poderoso: el reactivo limitante.
Si quieres conocer otros artículos parecidos a El Reactivo Limitante: La Clave de Toda Reacción Química puedes visitar la categoría Química.

