20/02/2026
En el vasto universo de la química, los iones desempeñan un papel fundamental, siendo los pilares de innumerables reacciones y procesos vitales. Si bien en nuestros estudios iniciales aprendemos sobre átomos neutros, la realidad es que muchos elementos existen en formas cargadas, conocidas como iones. Estos se dividen en dos categorías principales: los cationes y los aniones, cada uno con una carga eléctrica opuesta pero complementaria. Comprender cómo se forman, cómo identificarlos y cómo calcular su carga es esencial no solo en el laboratorio, sino también en diversas aplicaciones del mundo real.
Este artículo te guiará a través de una exploración profunda de los cationes y aniones. Abordaremos sus definiciones, la importancia de su identificación en campos como la química analítica, la ciencia forense y la ciencia ambiental, y te mostraremos los métodos prácticos más comunes para su detección. Además, te explicaremos el proceso para determinar su carga eléctrica y profundizaremos en el catión de sodio, un ejemplo crucial por su relevancia biológica y química. Prepárate para desentrañar los secretos de estas partículas cargadas que definen gran parte de nuestro entorno.
- ¿Qué Son los Cationes y Aniones?
- La Importancia de su Identificación
- Métodos de Identificación Práctica
- Aplicaciones Reales de la Identificación Iónica
- Calculando Cationes y Aniones: La Ciencia Detrás de la Carga
- El Catión Sodio (Na+): Un Caso de Estudio Esencial
- Preguntas Frecuentes (FAQ)
- Conclusión
¿Qué Son los Cationes y Aniones?
Para adentrarnos en el mundo de los iones, primero debemos comprender qué son exactamente. Los iones son átomos o moléculas que han ganado o perdido uno o más electrones, lo que les confiere una carga eléctrica neta. Esta carga es lo que los distingue de los átomos neutros.
Cationes: Iones con Carga Positiva
Un catión es un ion con carga positiva. Se forma cuando un átomo neutro pierde uno o más electrones de sus capas más externas. La pérdida de electrones significa que el átomo ahora tiene más protones (cargas positivas) que electrones (cargas negativas), resultando en una carga neta positiva. La magnitud de esta carga dependerá directamente del número de electrones perdidos. Por ejemplo, si un átomo pierde un electrón, se convierte en un catión con carga +1; si pierde dos, tendrá una carga +2, y así sucesivamente. La tendencia de un átomo a perder electrones se conoce como electropositividad.
Aniones: Iones con Carga Negativa
Por otro lado, un anión es un ion con carga negativa. Se forma cuando un átomo neutro gana uno o más electrones. Al ganar electrones, el átomo tiene más electrones que protones, lo que resulta en una carga neta negativa. De manera similar a los cationes, la carga del anión dependerá del número de electrones ganados. Si gana un electrón, la carga será -1; si gana dos, será -2, y así. La tendencia de un átomo a ganar electrones se denomina electronegatividad.
Los iones pueden formarse de diversas maneras, como la disociación iónica en soluciones acuosas o mediante la aplicación de energía. Compuestos iónicos, ácidos, bases y sales se disocian naturalmente en aniones y cationes cuando se disuelven en agua. Incluso el agua pura exhibe una ionización espontánea en iones hidronio (H3O+) e hidróxido (OH-). En compuestos iónicos, como el cloruro de sodio (sal de mesa), los pares de electrones en las capas más externas son capturados por un solo átomo, molécula o grupo funcional, creando una distribución asimétrica de la nube electrónica. Estos compuestos se conocen como electrófilos. Ejemplos comunes de electrófilos incluyen el ion hidronio (H3O+), trifluoruro de boro (BF3), cloruro de aluminio (AlCl3), así como moléculas diatómicas de halógenos como el flúor (F2), cloro (Cl2), bromo (Br2) y yodo (I2).
Además de la disociación en solución, los iones también pueden formarse cuando los átomos son sometidos a una corriente eléctrica (como en la electrólisis) o a radiación de alta energía. Un ejemplo natural de esto es cómo los rayos ultravioleta pueden desplazar electrones de los gases en la atmósfera, causando su ionización.
La Importancia de su Identificación
Saber identificar cationes y aniones es crucial en la química analítica. Esta habilidad permite descartar la presencia de ciertas sustancias químicas o impurezas en una muestra. Su utilidad se extiende a diversos campos, incluyendo la fabricación, la ciencia forense y la ciencia ambiental. Por ejemplo, en el control de calidad de productos, la identificación de iones puede asegurar la pureza de los materiales. En la investigación forense, ayuda a identificar sustancias desconocidas en escenas de crimen. Y en la ciencia ambiental, es fundamental para detectar contaminantes en el agua o el suelo.

Métodos de Identificación Práctica
Para identificar cationes y aniones en un laboratorio, se utilizan principalmente dos métodos cualitativos: las pruebas de llama y las reacciones de precipitación. Estos experimentos son accesibles incluso en entornos educativos y proporcionan resultados visuales claros.
Prueba de Llama para Cationes
La prueba de llama es un método cualitativo utilizado para identificar la presencia de ciertos cationes metálicos. Cuando los iones metálicos son expuestos a una llama caliente, sus electrones se excitan y saltan a niveles de energía más altos. Al regresar a sus niveles de energía originales, emiten luz con longitudes de onda características, que se manifiestan como colores específicos en la llama. Este fenómeno es único para cada elemento y permite su identificación.
Reacciones de Precipitación para Aniones
Las reacciones de precipitación son otra herramienta cualitativa útil, principalmente para identificar aniones. En estas reacciones, se añade un reactivo específico a una solución que contiene el ion desconocido. Si se forma un compuesto insoluble (un precipitado), esto indica la presencia del anión. La formación y el color del precipitado son clave para la identificación.
Materiales y Precauciones de Seguridad
Para llevar a cabo estos experimentos de forma segura y efectiva, es fundamental contar con el equipo adecuado y seguir estrictas precauciones. Muchos de los productos químicos utilizados son corrosivos y pueden producir vapores nocivos. Siempre se deben usar gafas de seguridad, guantes de goma y otra vestimenta protectora. Es recomendable trabajar bajo una campana de extracción cuando se diluyen productos químicos para evitar la inhalación de vapores.
Equipo Necesario:
- Tubos de ensayo
- Probetas graduadas
- Matraces volumétricos o Erlenmeyer
- Vasos de precipitados
- Mechero Bunsen
- Palillos de madera (o varillas de ignición)
- Encendedor o cerillas
- Gafas de seguridad
Sustancias Químicas para Pruebas:
Se utilizarán soluciones de composición conocida para demostrar los colores específicos que producen ciertos iones. Para las pruebas de llama, se pueden usar sales de los siguientes cationes:
- Cu2+ (Cobre(II))
- Ca2+ (Calcio)
- K+ (Potasio)
- Na+ (Sodio)
Para las reacciones de precipitación, se pueden probar los siguientes aniones:
- OH- (Hidróxido)
- SO42- (Sulfato)
- CO32- (Carbonato)
- Cl- (Cloruro)
- Br- (Bromuro)
- I- (Yoduro)
- NO3- (Nitrato)
Y los siguientes cationes:
- H+ (Hidrógeno)
- Ca2+ (Calcio)
- Cu2+ (Cobre(II))
- Fe3+ (Hierro(III))
- Fe2+ (Hierro(II))
- NH4+ (Amonio)
Se recomienda tener acceso a las siguientes soluciones para las pruebas:
- Cloruro de cobre
- Carbonato de potasio
- Yoduro de potasio
- Sulfato de cobre(II)
- Cloruro de hierro(III)
- Sulfato de hierro(II)
- Nitrato de plomo
- Sulfato de magnesio
Además, se necesitarán reactivos generales:
- Papel indicador de pH de rango completo
- Solución de amoníaco, 2 mol dm–3
- Solución de hidróxido de sodio, 0.4 mol dm–3
- Solución de ácido clorhídrico, 0.4 mol dm–3
- Solución de cloruro de bario, 0.1 mol dm–3
- Solución de agua de cal, 0.02 mol dm–3
- Ácido nítrico, 0.4 mol dm–3
- Solución de nitrato de plata, 0.1 mol dm–3
Realizando el Experimento: Pasos Clave
Paso 1: Preparación de las soluciones
Antes de iniciar, asegúrate de que el mechero Bunsen esté correctamente conectado al suministro de gas y no haya fugas. Remoja los palillos de madera en agua destilada antes de sumergirlos en las soluciones de prueba. Puedes usar hasta tres palillos por tubo de ensayo. Diluye las soluciones si es necesario o utiliza soluciones estándar ya diluidas. Calcula la molaridad basándote en el volumen de las muestras. Utiliza la probeta graduada y el matraz para mezclar las soluciones y vierte cada una en un tubo de ensayo separado, etiquetándolos correctamente.
Paso 2: Realización de las pruebas de llama para cationes
Enciende el mechero Bunsen y ajusta la válvula de gas y el collar del quemador hasta obtener una llama azul y no luminosa. Uno por uno, introduce los palillos previamente humedecidos con las soluciones iónicas en la llama y observa cuidadosamente los cambios de color. Registra tus observaciones en una tabla. Por ejemplo:
| Catión | Color de la Llama |
|---|---|
| Sodio (Na+) | Naranja brillante / Amarillo intenso |
| Potasio (K+) | Lila / Violeta |
| Calcio (Ca2+) | Rojo ladrillo / Naranja rojizo |
| Cobre (Cu2+) | Verde-azul (verde esmeralda) |
| Litio (Li+) | Rojo carmesí |
| Estroncio (Sr2+) | Rojo intenso |
| Bario (Ba2+) | Verde amarillento |
Paso 3: Realización de reacciones de precipitación para aniones
- Aniones cloruro (Cl-): En un tubo de ensayo con solución de cloruro de cobre, añade unas gotas de ácido nítrico diluido. Luego, agrega unas gotas de solución de nitrato de plata. Observarás la formación de un precipitado blanco, que es cloruro de plata (AgCl). El cloruro de plata es soluble en solución de amoníaco.
- Aniones yoduro (I-): En un tubo de ensayo separado con yoduro de potasio, añade unas gotas de ácido nítrico diluido, seguido de unas gotas de solución de nitrato de plata. Se formará un precipitado amarillo de yoduro de plata (AgI).
- Aniones sulfato (SO42-): Añade unas gotas de cloruro de bario a una solución de sulfato de magnesio. Se formará un precipitado lechoso de sulfato de bario (BaSO4).
Puedes experimentar con otras soluciones para observar si se forman precipitados. Para las reacciones que no forman precipitados, también puedes usar papeles indicadores para probar la acidez o alcalinidad de las soluciones, lo que puede dar pistas sobre la presencia de ciertos iones (como OH- o H+).
Observaciones y Resultados Esperados
Este experimento se basa principalmente en observaciones cualitativas. Para ambas pruebas, la de llama y la de precipitación, registra cuidadosamente tus observaciones en una tabla. Utiliza la tabla periódica como referencia para determinar las cargas y la reactividad de los elementos. Es útil anotar esta información junto con tus observaciones. Los resultados dependerán en gran medida de los productos químicos utilizados. Una tabla como la siguiente puede ser útil para organizar tus datos:
| Nombre de la Solución Química | Cationes Presentes | Aniones Presentes | Cambio Observado (Color de Llama/Precipitado) |
|---|---|---|---|
| Cloruro de Cobre | Cu2+ | Cl- | Llama verde-azul; Precipitado blanco con AgNO3 |
| Yoduro de Potasio | K+ | I- | Llama lila; Precipitado amarillo con AgNO3 |
| Sulfato de Magnesio | Mg2+ | SO42- | Llama incolora; Precipitado lechoso con BaCl2 |
| ... | ... | ... | ... |
Aplicaciones Reales de la Identificación Iónica
La identificación de cationes y aniones es un método cualitativo fundamental que permite descartar o identificar ciertos tipos de iones basándose en cambios de color observados en pruebas de llama y precipitaciones. Aunque son pruebas sencillas que se pueden realizar fácilmente en un laboratorio de química de secundaria, su utilidad va mucho más allá de los propósitos académicos y tiene importantes aplicaciones en el mundo real.

- Química Forense: Estas pruebas se utilizan a menudo en la química forense para identificar sustancias desconocidas que puedan contaminar la escena de un crimen. La simplicidad de la prueba permite realizarla in situ con ciertos reactivos para descartar o identificar sustancias particulares.
- Ciencia Ambiental: Es extremadamente útil en la ciencia ambiental, ya que permite a los expertos identificar diferentes contaminantes en muestras de agua, suelo o aire. Esto es crucial para la evaluación de la calidad ambiental y la gestión de la contaminación.
- Industria Manufacturera: En la industria manufacturera, los experimentos de identificación de cationes y aniones pueden formar parte del proceso de control de calidad. Ayudan a asegurar que las materias primas o los productos finales contengan los iones deseados en las proporciones correctas y estén libres de impurezas.
Calculando Cationes y Aniones: La Ciencia Detrás de la Carga
Para calcular la carga de un catión o un anión, es fundamental entender que estos son iones con cargas opuestas, formados por la ganancia o pérdida de electrones. La clave reside en el número de electrones que un átomo neutro ha perdido o ganado.
Cálculo de Cationes:
- Identificar el Átomo: Determina el elemento químico del átomo que forma el catión.
- Conocer el Número Atómico (Z): Encuentra el número atómico del átomo en la tabla periódica. El número atómico indica el número de protones en el núcleo del átomo. En un átomo neutro, el número de electrones es igual al número de protones.
- Determinar la Carga: Cuenta cuántos electrones ha perdido el átomo. Cada electrón perdido resulta en una carga positiva igual a la cantidad de electrones perdidos.
- Escribir el Símbolo: Representa el ion con el símbolo del elemento, seguido de un superíndice con la carga positiva.
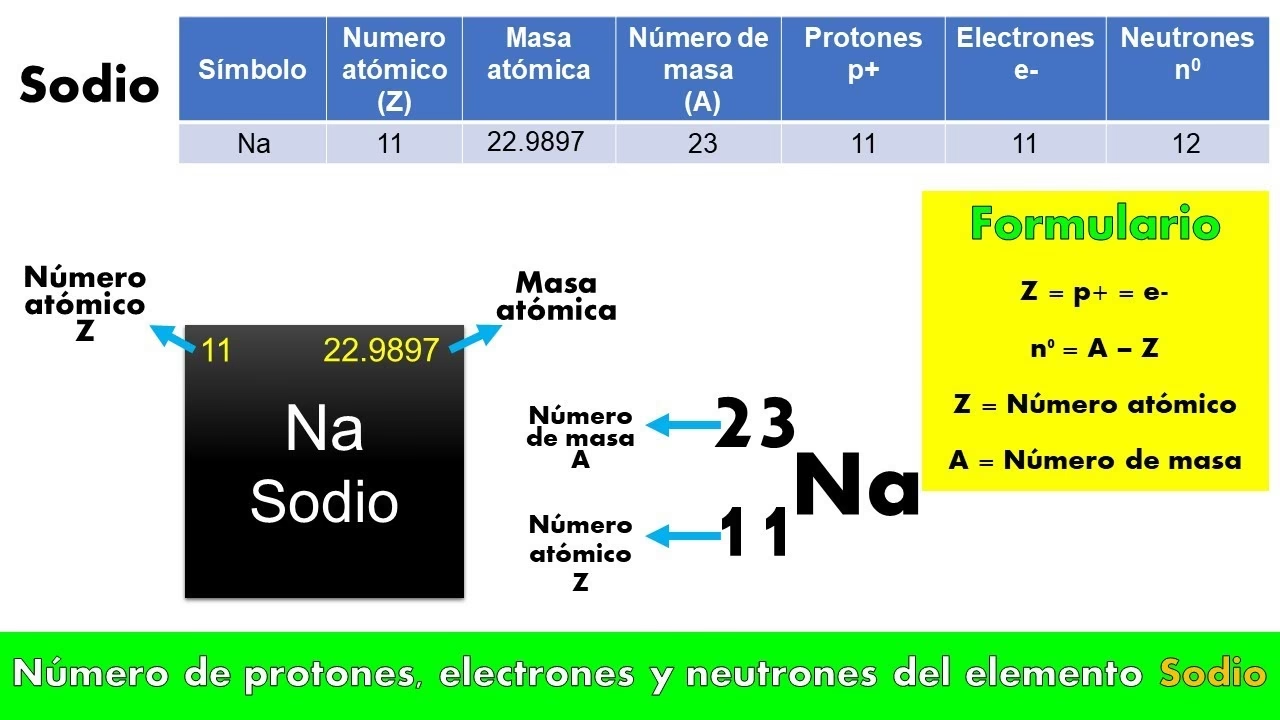
Ejemplo: Catión de Sodio (Na+)
- Átomo: Sodio (Na)
- Número Atómico: Z = 11 (lo que significa 11 protones).
- Electrones en átomo neutro: 11 electrones.
- Carga: El ion Na+ tiene una carga de +1. Esto significa que el átomo de sodio ha perdido 1 electrón.
- Electrones en Na+: 11 protones - 1 electrón perdido = 10 electrones.
- Símbolo: Na+
Cálculo de Aniones:
- Identificar el Átomo: Determina el elemento químico del átomo que forma el anión.
- Conocer el Número Atómico (Z): Encuentra el número atómico del átomo.
- Determinar la Carga: Cuenta cuántos electrones ha ganado el átomo. Cada electrón ganado resulta en una carga negativa igual a la cantidad de electrones ganados.
- Escribir el Símbolo: Representa el ion con el símbolo del elemento, seguido de un superíndice con la carga negativa.
Ejemplo: Anión de Cloruro (Cl-)
- Átomo: Cloro (Cl)
- Número Atómico: Z = 17 (lo que significa 17 protones).
- Electrones en átomo neutro: 17 electrones.
- Carga: El ion Cl- tiene una carga de -1. Esto significa que el átomo de cloro ha ganado 1 electrón.
- Electrones en Cl-: 17 protones + 1 electrón ganado = 18 electrones.
- Símbolo: Cl-
El Catión Sodio (Na+): Un Caso de Estudio Esencial
El sodio, con el símbolo químico Na (derivado del latín natrium), es un elemento químico con número atómico 11. Fue descubierto en 1807 por Humphry Davy. Es un metal alcalino blando, untuoso y de color plateado, extremadamente abundante en la naturaleza, especialmente en la sal marina. Es un elemento altamente reactivo: arde con una llama amarilla característica, se oxida rápidamente en presencia de oxígeno y reacciona violentamente con el agua.
Características del Sodio Elemental
Al igual que otros metales alcalinos, el sodio es un metal ligero y de color plateado que no se encuentra libre en la naturaleza debido a su alta reactividad. Flota en el agua y la descompone, liberando hidrógeno y formando un hidróxido. En condiciones apropiadas, puede reaccionar espontáneamente con el agua y no suele arder en contacto con el aire por debajo de los 40 °C.
El Papel Biológico del Sodio
El sodio es un elemento esencial para todos los animales y algunas plantas. En los seres vivos, el catión sodio (Na+) desempeña un papel fundamental en el metabolismo celular. Es el principal catión en el líquido extracelular (LEC) y, como tal, contribuye significativamente a la presión osmótica del LEC y a su volumen. La concentración plasmática normal de sodio en humanos es de 135-145 mmol/L.
Una de sus funciones más críticas es en la transmisión del impulso nervioso, a través del mecanismo de la bomba de sodio-potasio. Esta bomba, presente en las membranas celulares, bombea activamente tres iones de sodio fuera de la célula a cambio de dos iones de potasio hacia el interior. Esta diferencia de concentración iónica a través de la membrana celular es crucial para generar el potencial de acción, que permite la transmisión de señales nerviosas.
Además de la transmisión nerviosa, el sodio participa en:
- La contracción muscular.
- El equilibrio ácido-base del organismo.
- La absorción de nutrientes por las membranas celulares.
- El mantenimiento del volumen y la osmolaridad de los fluidos corporales.
Desequilibrios de Sodio: Hipernatremia e Hiponatremia
Los desequilibrios en la concentración de sodio en la sangre pueden tener graves consecuencias para la salud:
- Hipernatremia: Se produce cuando la concentración de sodio en plasma es superior a 145 meq/L. Las causas principales incluyen una acción insuficiente de la hormona vasopresina (ADH), pérdidas excesivas de agua o un balance positivo de sal. Los síntomas predominantes son la sed intensa, poliuria (aumento del volumen de orina), diarrea y sudoración. Valores superiores a 160 meq/L pueden causar trastornos neurológicos graves, como irritabilidad muscular, alteraciones del nivel de conciencia, coma e incluso convulsiones.
- Hiponatremia: Se considera hiponatremia cuando la concentración de sodio en plasma es inferior a 135 meq/L. Las causas principales incluyen grandes pérdidas de sodio (por diuréticos, enfermedades renales), o un aumento excesivo de la ingesta o aporte de agua al organismo. Los síntomas comunes son náuseas, vómitos, calambres musculares, alteraciones visuales, cefalea y letargo. Una disminución por debajo de 125 meq/L se considera potencialmente fatal y puede provocar convulsiones y coma.
El cuerpo humano cuenta con complejos mecanismos reguladores, principalmente a través de los osmorreceptores en el hipotálamo y la acción de la hormona vasopresina, para mantener el balance óptimo de sal y agua. Una corrección demasiado rápida de la hipernatremia, por ejemplo, puede resultar en daño cerebral debido al edema celular, ya que el agua se mueve rápidamente hacia el interior de las células con alto contenido osmolar.
Sodio en la Dieta y Precauciones
La mayor fuente de sodio en la dieta es el cloruro de sodio (sal común), del cual el sodio constituye el 40%. Sin embargo, todos los alimentos contienen sodio de forma natural, siendo más predominante en alimentos de origen animal que vegetal. Se estima que el requerimiento diario de sodio es de aproximadamente 500 mg/día. La mayoría de las personas consumen mucho más sodio de lo que necesitan fisiológicamente, lo cual, para individuos sensibles a la sal, puede tener efectos negativos en la presión arterial y la salud cardiovascular.

En su forma metálica, el sodio es extremadamente reactivo y explosivo en contacto con el agua y muchos otros elementos. Por ello, debe manipularse siempre con sumo cuidado y almacenarse en una atmósfera inerte, generalmente de argón, evitando cualquier contacto con el agua y otras sustancias reactivas como el oxígeno. La reacción del sodio con el agua (2Na + 2H2O → 2NaOH + H2 (g) + Energía) libera hidrógeno y una cantidad considerable de energía, lo que puede provocar explosiones del hidrógeno generado. Es crucial trabajar con precaución y con el equipo de protección necesario.
Preguntas Frecuentes (FAQ)
¿Por qué los átomos forman iones?
Los átomos forman iones para alcanzar una configuración electrónica más estable, similar a la de los gases nobles. Esto se logra ganando o perdiendo electrones para completar su capa de valencia.
¿Cuál es la diferencia principal entre un catión y un anión?
La diferencia principal radica en su carga eléctrica: los cationes tienen carga positiva (por pérdida de electrones), mientras que los aniones tienen carga negativa (por ganancia de electrones).
¿Se pueden identificar todos los cationes y aniones con pruebas de llama y precipitación?
No, estas pruebas son cualitativas y útiles para la identificación de un rango limitado de iones específicos que producen colores distintivos en la llama o forman precipitados reconocibles. Para una identificación más precisa y cuantitativa, se requieren técnicas analíticas más avanzadas.
¿Qué significa que el sodio es un electrolito esencial?
Significa que el sodio, en su forma iónica (Na+), es crucial para mantener funciones corporales vitales como el equilibrio hídrico, la función nerviosa y muscular. Los electrolitos son minerales que llevan una carga eléctrica cuando se disuelven en líquidos corporales.
Conclusión
La identificación y el cálculo de cationes y aniones son habilidades fundamentales en química, con aplicaciones que trascienden el laboratorio. A través de técnicas sencillas como las pruebas de llama y las reacciones de precipitación, podemos determinar la presencia de iones específicos basándonos en cambios de color predecibles y la formación de precipitados. Hemos visto cómo los cationes se forman por la pérdida de electrones y los aniones por su ganancia, y cómo esta distinción es vital para comprender la química de la materia.
El estudio del catión sodio (Na+) nos ha ilustrado la importancia de estos iones no solo en la industria, sino de manera crucial en la biología, donde el sodio es un electrolito esencial para procesos como la transmisión nerviosa y el equilibrio de fluidos corporales. Entender los iones nos permite no solo analizar y comprender el mundo que nos rodea, sino también apreciar los delicados equilibrios químicos que sustentan la vida misma.
Si quieres conocer otros artículos parecidos a Descifrando Cationes y Aniones: Guía Completa puedes visitar la categoría Química.

