02/03/2026
Calcular la concentración de una sustancia en una disolución es una habilidad fundamental en química, crucial tanto en laboratorios de investigación como en procesos industriales y en la vida cotidiana. El cloruro de sodio (NaCl), comúnmente conocido como sal de mesa, es un ejemplo omnipresente de una sustancia cuya concentración a menudo necesitamos determinar o ajustar. Comprender cómo realizar estos cálculos te permitirá preparar soluciones con la precisión requerida, ya sea para un experimento científico, un proceso de fabricación o incluso para usos domésticos.
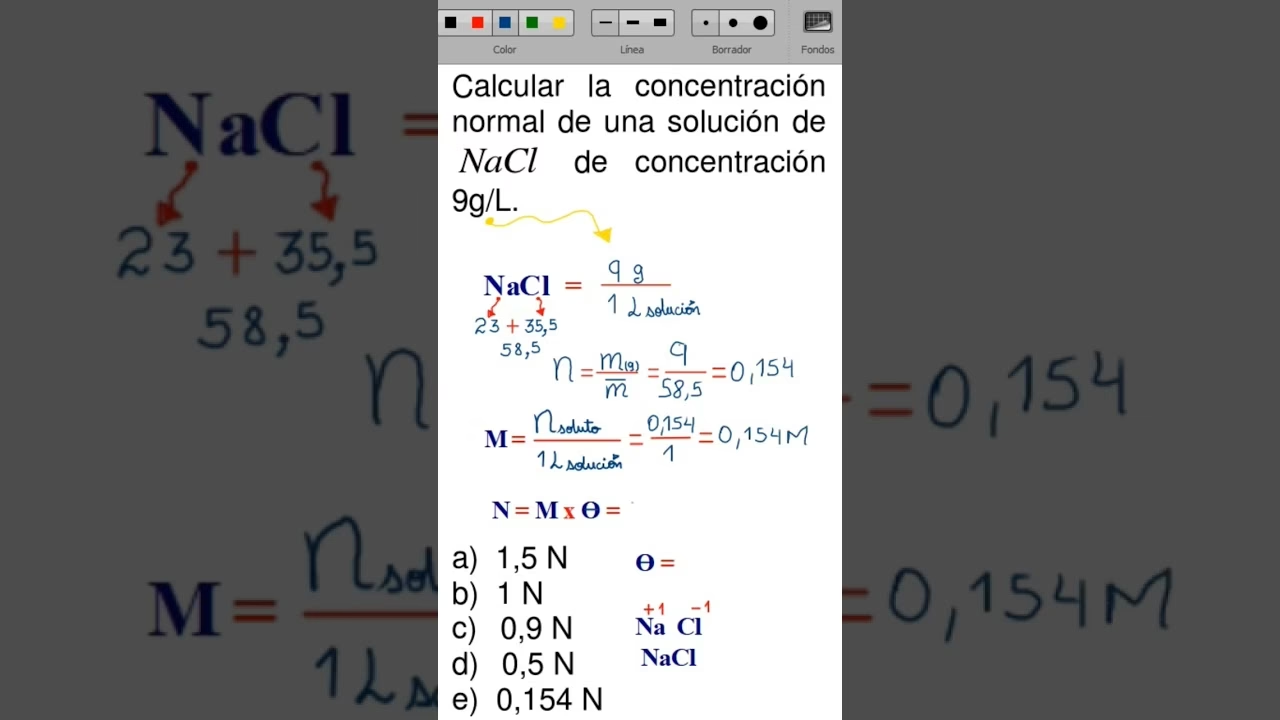
En este artículo, desglosaremos paso a paso el proceso para calcular la concentración de NaCl, centrándonos en la unidad de medida más utilizada en química: la molaridad. También exploraremos otras formas de expresar la concentración y abordaremos preguntas frecuentes para asegurarnos de que comprendas a fondo este concepto esencial. Prepárate para sumergirte en el fascinante mundo de las disoluciones y sus cálculos.
- ¿Qué es la Concentración Química y Por Qué es Importante?
- Entendiendo la Molaridad: La Unidad Reina de la Concentración
- Fórmulas Clave para Calcular la Concentración de NaCl
- Ejemplo Práctico: ¿Cómo Calcular la Masa de NaCl para una Solución Específica?
- La Importancia de las Unidades y las Conversiones
- Más Allá de la Molaridad: Otras Formas de Expresar la Concentración
- Tabla Comparativa de Unidades de Concentración
- Consejos Prácticos para la Preparación de Soluciones en el Laboratorio
- Preguntas Frecuentes (FAQs) sobre la Concentración de NaCl
- 1. ¿Qué es el NaCl y por qué es tan común en los ejemplos de concentración?
- 2. ¿Es lo mismo una solución de 10% de NaCl que una de 10 M de NaCl?
- 3. ¿Cómo puedo calcular la concentración de NaCl si ya tengo una masa y un volumen dados?
- 4. ¿Por qué se usa dm³ en lugar de cm³ o litros en la molaridad?
- 5. ¿Qué sucede si la temperatura de la disolución cambia? ¿Afecta la concentración?
- Conclusión
¿Qué es la Concentración Química y Por Qué es Importante?
La concentración de una disolución es una medida de la cantidad de soluto disuelto en una cantidad dada de solvente o de disolución total. Imagina que tienes un vaso de agua con sal: si añades solo una pizca, la concentración de sal será baja; si añades media taza, la concentración será mucho mayor. Esta simple idea es la base de todos los cálculos de concentración.
La importancia de la concentración radica en que las propiedades de una disolución y su reactividad química dependen directamente de ella. En medicina, la concentración de un medicamento es vital para su dosificación; en la industria alimentaria, la concentración de sal afecta el sabor y la conservación; en el laboratorio, la precisión en la concentración es crítica para obtener resultados reproducibles en experimentos. Una ligera variación puede alterar drásticamente el resultado final de un proceso.
Entendiendo la Molaridad: La Unidad Reina de la Concentración
En el ámbito de la química, la forma más común y útil de expresar la concentración es la Molaridad (M), también conocida como concentración molar. La molaridad se define como el número de moles de soluto por litro de disolución.
- Mol: El mol es una unidad fundamental en química que representa una cantidad específica de partículas (átomos, moléculas, iones, etc.). Un mol de cualquier sustancia contiene aproximadamente 6.022 x 1023 partículas (el número de Avogadro). Es una forma de contar partículas por 'paquetes'.
- Litro (L) o Decímetro Cúbico (dm³): Estas son unidades de volumen equivalentes (1 L = 1 dm³). En el contexto de la molaridad, nos referimos al volumen total de la disolución, no solo al volumen del solvente.
Por lo tanto, una disolución 1 M de NaCl significa que hay 1 mol de NaCl disuelto en 1 litro de disolución. La molaridad nos permite relacionar directamente la cantidad de sustancia (en moles) con el volumen de la disolución, lo cual es muy conveniente para cálculos estequiométricos.
La Masa Molar: Tu Clave para Convertir Gramos a Moles
Para trabajar con moles, necesitamos conocer la Masa Molar (M) de la sustancia. La masa molar es la masa de un mol de una sustancia, expresada en gramos por mol (g/mol). Se calcula sumando las masas atómicas de todos los átomos presentes en la fórmula química de la sustancia.
Para el NaCl:
- Masa atómica del Sodio (Na): aproximadamente 22.99 g/mol
- Masa atómica del Cloro (Cl): aproximadamente 35.45 g/mol
Por lo tanto, la masa molar del NaCl (MNaCl) es:
MNaCl = Masa atómica (Na) + Masa atómica (Cl)
MNaCl = 22.99 g/mol + 35.45 g/mol = 58.44 g/mol
Este valor, 58.44 g/mol, es crucial. Significa que 1 mol de NaCl tiene una masa de 58.44 gramos.
Fórmulas Clave para Calcular la Concentración de NaCl
Para calcular la concentración, o para determinar la cantidad de soluto necesaria para una concentración específica, utilizaremos dos fórmulas fundamentales:
Fórmula de Concentración Molar (Molaridad):
c = n / Vc: Concentración molar (Molaridad), expresada en mol/dm³ o mol/L.n: Número de moles del soluto (NaCl, en este caso), expresado en moles.V: Volumen de la disolución, expresado en dm³ o litros.
Esta fórmula te permite calcular la concentración si conoces los moles de soluto y el volumen de la disolución.
Fórmula para Calcular Moles a partir de la Masa:
n = m / Mn: Número de moles del soluto (NaCl).m: Masa del soluto (NaCl), expresada en gramos.M: Masa molar del soluto (NaCl), expresada en g/mol.
Esta fórmula te permite convertir una masa dada de sustancia a su equivalente en moles, y viceversa.
Ejemplo Práctico: ¿Cómo Calcular la Masa de NaCl para una Solución Específica?
Vamos a aplicar estas fórmulas a un problema común: ¿Cuántos gramos de NaCl se necesitan para preparar 100 cm³ de una disolución con una concentración de 0.500 mol/dm³?
Paso 1: Identificar los datos conocidos y la incógnita.
- Concentración deseada (c) = 0.500 mol/dm³
- Volumen de la disolución (V) = 100 cm³
- Masa molar del NaCl (M) = 58.44 g/mol (calculado previamente)
- Incógnita: Masa de NaCl necesaria (m)
Paso 2: Convertir el volumen a unidades de dm³ (litros).
La molaridad se expresa en mol/dm³, por lo que el volumen debe estar en dm³. Sabemos que 1 dm³ = 1000 cm³.
V = 100 cm³ * (1 dm³ / 1000 cm³) = 0.1 dm³
Paso 3: Calcular el número de moles (n) de NaCl necesarios.
Usaremos la fórmula de concentración molar: c = n / V. Despejando n, obtenemos: n = c * V
n = (0.500 mol/dm³) * (0.1 dm³)
n = 0.05 moles de NaCl
Esto significa que se requieren 0.05 moles de NaCl para preparar la disolución de 0.500 mol/dm³.
Paso 4: Calcular la masa (m) de NaCl necesaria.
Ahora que conocemos el número de moles y la masa molar del NaCl, podemos calcular la masa en gramos usando la fórmula: n = m / M. Despejando m, obtenemos: m = n * M
m = (0.05 moles) * (58.44 g/mol)
m = 2.922 gramos de NaCl
Conclusión del ejemplo: Para preparar 100 cm³ de una disolución de 0.500 mol/dm³ de NaCl, se necesitan 2.922 gramos de NaCl. Este es el proceso exacto que se sigue en un laboratorio para preparar una disolución con una concentración específica.
La Importancia de las Unidades y las Conversiones
Como pudiste observar en el ejemplo anterior, la correcta conversión de unidades es fundamental para obtener resultados precisos. Un error común es no convertir el volumen de centímetros cúbicos (cm³) a decímetros cúbicos (dm³) o litros (L) cuando se trabaja con molaridad.
Aquí tienes una tabla de conversiones de volumen útiles:
| Unidad | Equivalencia en Litros (L) | Equivalencia en cm³ |
|---|---|---|
| 1 Litro (L) | 1 L | 1000 cm³ |
| 1 Decímetro Cúbico (dm³) | 1 L | 1000 cm³ |
| 1 Mililitro (mL) | 0.001 L | 1 cm³ |
| 1 Centímetro Cúbico (cm³) | 0.001 L | 1 mL |
Siempre verifica que las unidades se cancelen correctamente en tus cálculos para asegurar que el resultado final tenga las unidades deseadas.
Más Allá de la Molaridad: Otras Formas de Expresar la Concentración
Aunque la molaridad es muy común, existen otras formas de expresar la concentración de una disolución, cada una útil en diferentes contextos. Una de las preguntas iniciales que recibimos fue: "¿Cómo calcular el 10% de NaCl?". Esta pregunta se refiere a una forma diferente de expresar la concentración: el porcentaje en masa.
1. Porcentaje en Masa (% m/m)
El porcentaje en masa (% m/m) es una de las maneras más sencillas de expresar la concentración y es muy común en la industria y en productos de consumo. Se define como la masa de soluto dividida por la masa total de la disolución, multiplicada por 100.

% m/m = (masa de soluto / masa total de disolución) * 100%
Si alguien te pide una disolución de "10% de NaCl", generalmente se refiere a un 10% en masa. Esto significa que por cada 100 gramos de disolución, habrá 10 gramos de NaCl. Los 90 gramos restantes serían del solvente (comúnmente agua).
Ejemplo: Para preparar 500 g de una disolución de NaCl al 10% (m/m):
- Masa de NaCl = 10% de 500 g = (10/100) * 500 g = 50 gramos de NaCl.
- Masa de agua = 500 g (disolución total) - 50 g (NaCl) = 450 gramos de agua.
Es importante notar que el porcentaje en masa no se relaciona directamente con el volumen de la disolución a menos que conozcas la densidad de la misma.
2. Porcentaje en Volumen (% v/v)
Usado principalmente para disoluciones de líquido en líquido, el porcentaje en volumen se define como el volumen de soluto dividido por el volumen total de la disolución, multiplicado por 100.
% v/v = (volumen de soluto / volumen total de disolución) * 100%
Por ejemplo, el alcohol etílico en bebidas alcohólicas se expresa en % v/v.
3. Porcentaje Masa/Volumen (% m/v)
Este porcentaje es una mezcla de los anteriores y es común en farmacia. Se define como la masa de soluto (en gramos) por cada 100 mL de disolución.
% m/v = (masa de soluto (g) / volumen de disolución (mL)) * 100%
4. Molalidad (m)
Aunque se parece a la molaridad, la molalidad es diferente. Se define como el número de moles de soluto por kilogramo de solvente (no de disolución). Es útil en experimentos que involucran cambios de temperatura, ya que la masa no varía con la temperatura, a diferencia del volumen.
m = moles de soluto / kilogramos de solvente
5. Fracción Molar (X)
La fracción molar es la relación de los moles de un componente (soluto o solvente) con respecto al número total de moles de todos los componentes en la disolución. Es una unidad adimensional (sin unidades).
Xsoluto = moles de soluto / (moles de soluto + moles de solvente)
Tabla Comparativa de Unidades de Concentración
| Unidad de Concentración | Definición | Unidades | Contexto de Uso Común |
|---|---|---|---|
| Molaridad (M) | Moles de soluto por litro de disolución | mol/L o mol/dm³ | Reacciones químicas, cálculos estequiométricos |
| Porcentaje en Masa (% m/m) | (Masa de soluto / Masa total de disolución) * 100 | % | Productos comerciales, formulaciones alimentarias |
| Porcentaje en Volumen (% v/v) | (Volumen de soluto / Volumen total de disolución) * 100 | % | Mezclas de líquidos (ej. alcohol en agua) |
| Porcentaje Masa/Volumen (% m/v) | (Masa de soluto (g) / Volumen de disolución (mL)) * 100 | g/100 mL | Farmacia, soluciones intravenosas |
| Molalidad (m) | Moles de soluto por kilogramo de solvente | mol/kg | Propiedades coligativas (punto de ebullición, congelación) |
| Fracción Molar (X) | Moles de un componente / Moles totales de la disolución | Adimensional | Cálculos de presión de vapor, equilibrio de fases |
Consejos Prácticos para la Preparación de Soluciones en el Laboratorio
La teoría es importante, pero la práctica requiere atención al detalle. Aquí hay algunos consejos para asegurar la precisión al preparar soluciones de NaCl (o cualquier otra sustancia):
- Usa una balanza analítica: Para masas pequeñas como 2.922 g, una balanza de laboratorio de alta precisión (con al menos tres o cuatro decimales) es indispensable.
- Disuelve completamente el soluto: Asegúrate de que todo el NaCl se disuelva antes de aforar. Puedes agitar la mezcla o usar un agitador magnético.
- Afora correctamente: Para preparar una disolución de volumen exacto (como 100 cm³ o 0.1 dm³), debes usar un matraz aforado (o matraz volumétrico). Añade el solvente hasta que el menisco inferior del líquido coincida exactamente con la línea de aforo del matraz.
- Considera la temperatura: El volumen de los líquidos puede variar ligeramente con la temperatura. Las mediciones volumétricas suelen estar calibradas a una temperatura específica (comúnmente 20°C).
- Seguridad: Siempre usa equipo de protección personal adecuado (gafas de seguridad, guantes) cuando manipules productos químicos en el laboratorio.
Preguntas Frecuentes (FAQs) sobre la Concentración de NaCl
1. ¿Qué es el NaCl y por qué es tan común en los ejemplos de concentración?
El NaCl es el cloruro de sodio, la sal de mesa común. Es un compuesto iónico que se disuelve fácilmente en agua, formando iones Na⁺ y Cl⁻. Es extremadamente común en química porque es un electrolito fuerte, esencial para la vida, y se utiliza en una vasta gama de aplicaciones, desde la conservación de alimentos hasta la producción industrial y la medicina (suero fisiológico).
2. ¿Es lo mismo una solución de 10% de NaCl que una de 10 M de NaCl?
No, definitivamente no son lo mismo. Una solución de 10% de NaCl (m/m) significa 10 gramos de NaCl por cada 100 gramos de disolución. Para convertir esto a molaridad, necesitarías conocer la densidad de la disolución, lo cual es un paso adicional. Una solución de 10 M de NaCl significa 10 moles de NaCl por litro de disolución. Dado que 1 mol de NaCl es 58.44 g, 10 M de NaCl significaría 584.4 gramos de NaCl por litro, lo cual es una concentración extremadamente alta y mucho mayor que un 10% en masa. Son unidades fundamentalmente diferentes y no intercambiables sin cálculos y datos adicionales.
3. ¿Cómo puedo calcular la concentración de NaCl si ya tengo una masa y un volumen dados?
Si ya tienes la masa de NaCl (en gramos) y el volumen de la disolución (en litros o dm³), puedes calcular la concentración molar invirtiendo los pasos del ejemplo:
- Primero, convierte la masa de NaCl a moles usando su masa molar:
n = masa / Masa Molar. - Luego, divide el número de moles por el volumen de la disolución (asegúrate de que esté en litros o dm³):
c = n / volumen.
Así obtendrás la concentración molar de tu disolución.
4. ¿Por qué se usa dm³ en lugar de cm³ o litros en la molaridad?
El decímetro cúbico (dm³) es exactamente equivalente a un litro (1 dm³ = 1 L). La razón por la que a veces se prefiere dm³ en lugar de L en las definiciones formales o en algunos campos de la química es por su relación directa con las unidades de longitud del Sistema Internacional (SI), donde el metro es la unidad base. Como 1 dm = 0.1 m, entonces 1 dm³ = (0.1 m)³ = 0.001 m³. Esto lo vincula más directamente con las unidades cúbicas del SI. Sin embargo, en la práctica, 'litro' es la unidad más comúnmente utilizada y aceptada para la molaridad.
5. ¿Qué sucede si la temperatura de la disolución cambia? ¿Afecta la concentración?
La molaridad (moles/volumen) puede verse ligeramente afectada por cambios de temperatura porque el volumen de la disolución puede expandirse o contraerse con la temperatura. Si el volumen cambia, la concentración molar también cambiará. Sin embargo, el número de moles de soluto y la masa del soluto no cambian con la temperatura. Por esta razón, la molalidad (moles/masa de solvente) es una unidad de concentración preferida en experimentos donde la temperatura varía significativamente, ya que es independiente de la temperatura.
Conclusión
Dominar el cálculo de la concentración de sustancias como el NaCl es una habilidad indispensable para cualquier persona que trabaje o estudie en el campo de la química. Hemos explorado la definición de concentración, la importancia de la molaridad como unidad principal, y las fórmulas clave que te permitirán determinar la cantidad de soluto necesaria para preparar una disolución con una concentración específica. A través de un ejemplo detallado, hemos visto cómo aplicar estas fórmulas paso a paso.
Además, hemos diferenciado la molaridad de otras formas de expresar la concentración, como el porcentaje en masa, y hemos proporcionado una tabla comparativa útil. Recordar la importancia de las unidades y las conversiones, junto con seguir buenas prácticas de laboratorio, te garantizará resultados precisos en tus preparaciones.
Con esta guía completa, esperamos que te sientas más seguro y competente al enfrentarte a cálculos de concentración de NaCl y de otras sustancias. La precisión en estos cálculos es el pilar para el éxito en innumerables aplicaciones científicas e industriales.
Si quieres conocer otros artículos parecidos a Calculando la Concentración de NaCl: Guía Completa puedes visitar la categoría Química.
