04/11/2022
En el vasto universo de la química, cada sustancia tiene una identidad única definida por su composición atómica. Para los gases, esta identidad es crucial, ya que sus propiedades y comportamientos están intrínsecamente ligados a los átomos que los conforman y cómo se agrupan. Entender cómo calcular la fórmula molecular de un gas no es solo un ejercicio académico, sino una habilidad fundamental que permite a científicos e ingenieros comprender, predecir y manipular estas sustancias volátiles. Desde el aire que respiramos hasta los compuestos industriales más complejos, la fórmula molecular es la clave para desvelar su verdadera naturaleza.
A menudo, en el laboratorio o en la industria, nos encontramos con un gas cuya composición elemental conocemos (su porcentaje de carbono, hidrógeno, oxígeno, etc.), pero no su estructura atómica exacta. Aquí es donde la determinación de la fórmula molecular se vuelve indispensable. Este proceso no solo nos dice qué elementos están presentes, sino también el número exacto de átomos de cada elemento en una molécula individual. Acompáñanos en este recorrido para dominar el cálculo de la fórmula molecular de cualquier gas, transformando datos brutos en conocimiento químico preciso.
¿Qué es la Fórmula Molecular? ¿Y la Fórmula Empírica?
Antes de sumergirnos en los cálculos, es vital comprender la diferencia entre la fórmula empírica y la fórmula molecular, ya que ambas son componentes esenciales de nuestro proceso.
La fórmula empírica representa la relación más simple de números enteros entre los átomos de cada elemento en un compuesto. Es como la "receta" más reducida de los ingredientes atómicos. Por ejemplo, si un compuesto tiene dos átomos de carbono y cuatro de hidrógeno, su fórmula empírica sería CH₂ (dividiendo los subíndices por su máximo común divisor, que es 2).
Por otro lado, la fórmula molecular nos da el número exacto de átomos de cada elemento presentes en una molécula del compuesto. Es la "receta" real y completa. Siguiendo el ejemplo anterior, si el compuesto real es C₂H₄ (eteno), su fórmula molecular es C₂H₄, mientras que su fórmula empírica es CH₂. La fórmula molecular es siempre un múltiplo entero (n) de la fórmula empírica. Es decir:
Fórmula Molecular = n × (Fórmula Empírica)
Donde 'n' es un número entero positivo (1, 2, 3, etc.). Si 'n' es igual a 1, la fórmula molecular es idéntica a la empírica.
Consideremos algunos ejemplos ilustrativos para afianzar este concepto:
| Nombre del Compuesto | Fórmula Molecular | Fórmula Empírica | Valor de 'n' |
|---|---|---|---|
| Metano | CH₄ | CH₄ | 1 |
| Ácido Acético | C₂H₄O₂ | CH₂O | 2 |
| Glucosa | C₆H₁₂O₆ | CH₂O | 6 |
Como se observa en la tabla, el metano tiene su fórmula molecular y empírica idénticas, lo que significa que 'n' es 1. Sin embargo, el ácido acético y la glucosa, a pesar de ser compuestos muy diferentes, comparten la misma fórmula empírica (CH₂O), pero sus fórmulas moleculares son distintas, reflejando diferentes valores de 'n' y, por lo tanto, diferentes masas moleculares y estructuras.
La Clave: Masa Molar del Gas
Para pasar de la fórmula empírica a la fórmula molecular, necesitamos un dato crucial: la masa molar del compuesto. La masa molar (MM) es la masa de un mol de una sustancia, expresada en gramos por mol (g/mol). Nos proporciona la "masa real" de la molécula, que es fundamental para determinar cuántas "unidades empíricas" caben en una molécula completa.
En un laboratorio, la masa molar de un compuesto, especialmente de un gas, se puede determinar experimentalmente utilizando diversas técnicas. Una de las más precisas es la espectrometría de masas, un instrumento que ioniza las moléculas y las separa según su relación masa/carga, permitiendo una determinación muy exacta de su masa molecular.
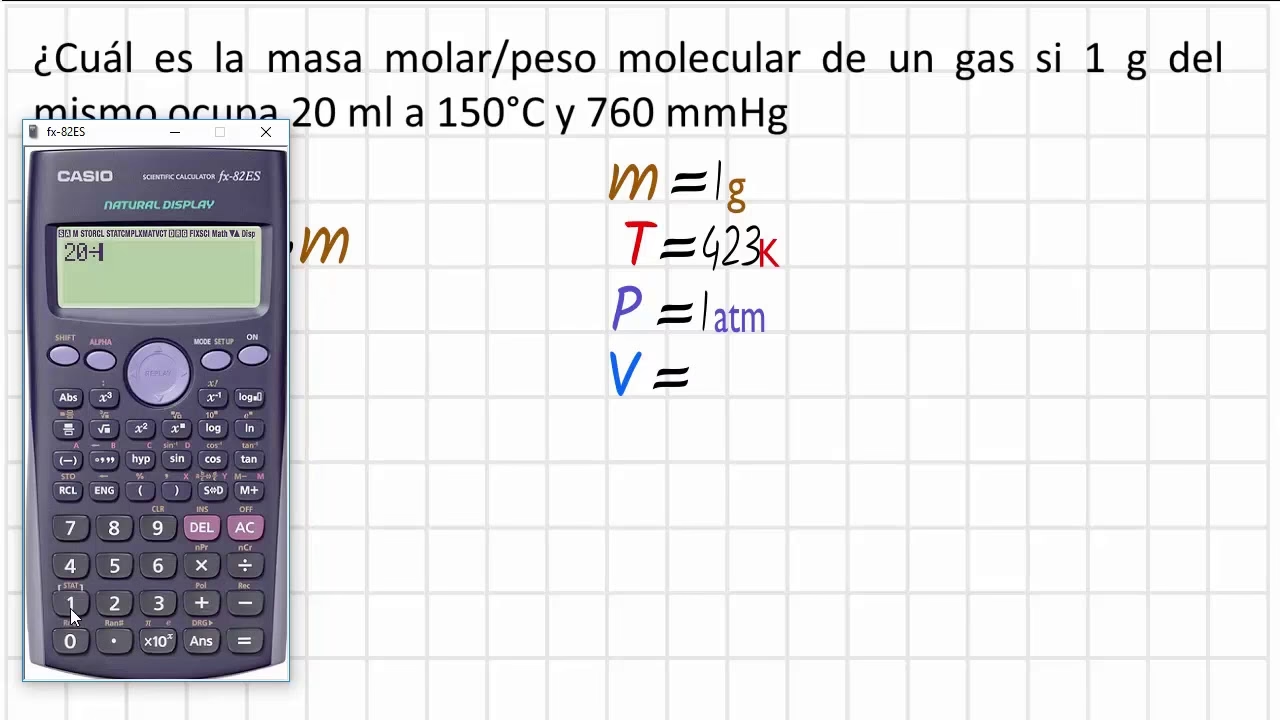
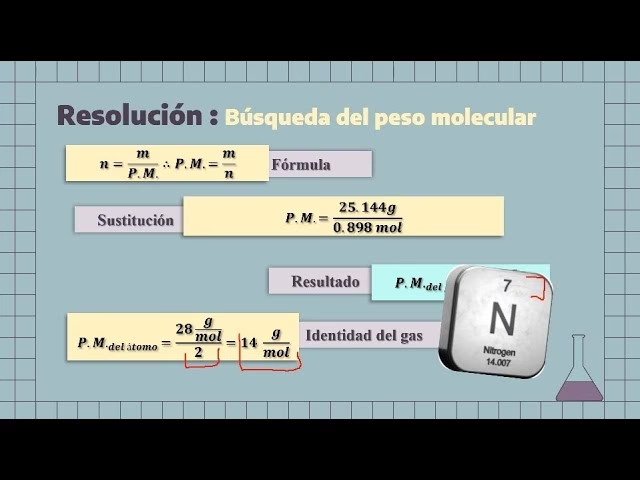
Para los gases, existe otro método muy común y accesible que se basa en la Ley de los Gases Ideales. Si tenemos una muestra de gas a una presión (P), volumen (V) y temperatura (T) conocidos, podemos calcular el número de moles (n) del gas utilizando la ecuación: PV = nRT, donde R es la constante de los gases ideales. Una vez que conocemos los moles (n) y la masa (m) de la muestra de gas, la masa molar (MM) se calcula simplemente como: MM = m / n. Este enfoque es particularmente útil para el cálculo de la fórmula molecular de gases, ya que nos permite obtener la masa molar necesaria directamente de experimentos con gases.
La relación entre la masa molar (MM) y la masa de la fórmula empírica (MFE) es lo que nos permite calcular el factor 'n':
n = MM (masa molar) / MFE (masa de la fórmula empírica)
Pasos para Calcular la Fórmula Molecular de un Gas
El proceso para determinar la fórmula molecular de un gas es sistemático y se puede dividir en los siguientes pasos:
Paso 1: Determinar la Fórmula Empírica del Gas
Este es el punto de partida. La fórmula empírica generalmente se obtiene a partir de la composición porcentual de los elementos en el gas. Si te proporcionan directamente la fórmula empírica, este paso ya está cubierto. Si no, necesitarás convertir los porcentajes de cada elemento a gramos (asumiendo una muestra de 100 g), luego a moles de cada elemento, y finalmente encontrar la relación de números enteros más simple dividiendo por el menor número de moles.
Paso 2: Obtener la Masa Molar del Gas (MM)
Como se mencionó anteriormente, este valor es crucial. Se obtiene experimentalmente, ya sea a través de técnicas avanzadas como la espectrometría de masas, o para gases, a menudo mediante mediciones de presión, volumen, temperatura y masa de una muestra de gas, aplicando la Ley de los Gases Ideales.
Paso 3: Calcular la Masa de la Fórmula Empírica (MFE)
Una vez que tienes la fórmula empírica, calcula su masa sumando las masas atómicas de todos los átomos presentes en ella. Por ejemplo, si la fórmula empírica es CH₂O, la MFE sería: (1 × masa atómica de C) + (2 × masa atómica de H) + (1 × masa atómica de O).
Paso 4: Calcular el Factor Multiplicador 'n'
Divide la masa molar (MM) del gas (obtenida en el Paso 2) entre la masa de la fórmula empírica (MFE) (calculada en el Paso 3). El resultado debe ser un número entero o muy cercano a un número entero. Si obtienes un valor como 1.98 o 2.01, redondéalo al número entero más cercano (2 en este caso).
n = Masa Molar (MM) / Masa de la Fórmula Empírica (MFE)
Paso 5: Obtener la Fórmula Molecular Final
Multiplica los subíndices de cada elemento en la fórmula empírica por el factor 'n' (calculado en el Paso 4). El resultado es la fórmula molecular del gas.
Fórmula Molecular = (Fórmula Empírica)n
Ejemplo Práctico Detallado: Desvelando la Fórmula Molecular
Vamos a aplicar estos pasos a un ejemplo concreto para solidificar la comprensión.
Problema: La fórmula empírica de un compuesto de boro e hidrógeno es BH₃. Su masa molar experimentalmente determinada es aproximadamente 27.7 g/mol. Determine la fórmula molecular de este gas.
Solución:
- Datos Proporcionados:
- Fórmula Empírica (FE) = BH₃
- Masa Molar (MM) = 27.7 g/mol
- Objetivo: Encontrar la Fórmula Molecular (FM) = ?
Paso 1: Determinar la Fórmula Empírica del Gas.
En este caso, la fórmula empírica (BH₃) ya nos ha sido proporcionada directamente en el enunciado del problema. Esto nos ahorra el primer paso de cálculo a partir de la composición porcentual.
Paso 2: Obtener la Masa Molar del Gas (MM).
La masa molar del compuesto, 27.7 g/mol, también se nos proporciona como un dato experimental. Este valor es fundamental y es el que nos permite escalar de la fórmula empírica a la molecular.
Paso 3: Calcular la Masa de la Fórmula Empírica (MFE).
Para la fórmula empírica BH₃, necesitamos las masas atómicas del Boro (B) y del Hidrógeno (H).
- Masa atómica de B (Boro) ≈ 10.81 g/mol
- Masa atómica de H (Hidrógeno) ≈ 1.008 g/mol
Ahora, calculamos la MFE:
MFE = (1 átomo de B × 10.81 g/mol) + (3 átomos de H × 1.008 g/mol)
MFE = 10.81 g/mol + 3.024 g/mol
MFE = 13.834 g/mol
Por lo tanto, la masa de la fórmula empírica BH₃ es de aproximadamente 13.834 g/mol.
Paso 4: Calcular el Factor Multiplicador 'n'.
Utilizamos la fórmula: n = MM / MFE
n = 27.7 g/mol / 13.834 g/mol
n ≈ 2.002
Este valor es extremadamente cercano a 2. Por lo tanto, redondeamos 'n' a 2. Esto significa que la molécula real del gas es el doble de grande que la unidad de la fórmula empírica.
Paso 5: Obtener la Fórmula Molecular Final.
Multiplicamos los subíndices de la fórmula empírica (BH₃) por el factor 'n' que acabamos de calcular (n=2).
Fórmula Molecular = (BH₃)₂
Fórmula Molecular = B₁ₓ₂H₃ₓ₂
Fórmula Molecular = B₂H₆
Así, la fórmula molecular del compuesto de boro e hidrógeno es B₂H₆, conocido como diborano. Este es un gas incoloro, altamente inflamable y tóxico, con un olor dulce distintivo. Su determinación precisa es vital para su manejo y estudio.
Preguntas Frecuentes (FAQs)
¿Cuál es la diferencia fundamental entre fórmula empírica y molecular?
La fórmula empírica muestra la proporción más simple de átomos en un compuesto, mientras que la fórmula molecular indica el número exacto de cada tipo de átomo en una sola molécula. La fórmula molecular es siempre un múltiplo entero de la fórmula empírica.
¿Por qué es crucial conocer la masa molar para este cálculo?
La masa molar es esencial porque nos da la "masa real" de la molécula completa. Sin ella, solo tendríamos la proporción más simple de los átomos (fórmula empírica), pero no sabríamos cuántas de esas "unidades empíricas" conforman una molécula individual. Es el puente entre la proporción y la cantidad exacta.
¿Siempre será 'n' un número entero? ¿Qué hago si no lo es?
Sí, teóricamente, 'n' siempre debe ser un número entero (1, 2, 3, etc.). Si al calcular 'n' obtienes un valor como 1.98, 2.03, 2.99, etc., es debido a pequeñas inexactitudes en las masas atómicas o en la determinación experimental de la masa molar. En estos casos, debes redondear al número entero más cercano. Si el valor está lejos de un número entero (por ejemplo, 1.5, 2.7), esto podría indicar un error significativo en tus cálculos o en los datos experimentales.
¿Cómo se obtiene la composición porcentual de un gas?
La composición porcentual de los elementos en un gas se determina experimentalmente, a menudo mediante técnicas de análisis elemental. Para compuestos orgánicos (que contienen carbono, hidrógeno y a veces oxígeno), esto se logra comúnmente mediante análisis de combustión, donde una muestra del gas se quema y se mide la cantidad de CO₂ y H₂O producida.
¿Este método solo aplica a gases?
No, el método para calcular la fórmula molecular a partir de la fórmula empírica y la masa molar es universal y se aplica a cualquier tipo de compuesto, ya sea un gas, un líquido o un sólido. La única diferencia al tratar con gases es que la determinación experimental de su masa molar a menudo se facilita mediante la aplicación de la Ley de los Gases Ideales, además de otras técnicas más generales como la espectrometría de masas.
Conclusión
La capacidad de determinar la fórmula molecular de un gas es una herramienta poderosa en la química. Nos permite ir más allá de la simple identificación de los elementos presentes para comprender la estructura precisa de las moléculas. Ya sea para identificar un gas desconocido en un proceso industrial, para investigar nuevos compuestos o para comprender mejor los ciclos atmosféricos, el dominio de este cálculo es fundamental. Con los pasos claros y un ejemplo práctico, esperamos haber desmitificado este proceso, haciéndolo accesible para cualquier entusiasta de la química. Recuerda que la precisión en los datos de la masa molar y la correcta determinación de la fórmula empírica son los pilares para un resultado exacto.
Si quieres conocer otros artículos parecidos a Cálculo de la Fórmula Molecular de Gases puedes visitar la categoría Química.