10/11/2023
La química es una ciencia de transformaciones, donde las sustancias se combinan y se alteran para formar otras nuevas. Sin embargo, muy pocas de estas transformaciones son absolutas; la mayoría son dinámicas, alcanzando un estado donde la creación de productos y la reformación de reactivos ocurren simultáneamente a velocidades iguales. Este estado, fundamental para comprender cómo funcionan las reacciones en la naturaleza y la industria, se conoce como equilibrio químico. En el centro de este concepto se encuentra una herramienta matemática poderosa: la constante de equilibrio. Esta cifra no solo nos ayuda a predecir la dirección de una reacción, sino que también nos ofrece una visión profunda de su composición en el punto de equilibrio. Acompáñenos en este viaje para desentrañar el propósito y la importancia de la constante de equilibrio y su papel crucial en la comprensión del universo molecular.

- ¿Qué es el Equilibrio Químico y Por Qué es Tan Importante?
- La Constante de Equilibrio (K): El Corazón del Equilibrio Químico
- Factores que Afectan el Equilibrio Químico: El Principio de Le Chatelier
- La Importancia de las Constantes en la Química Experimental
- Equilibrios Múltiples y Complejidad
- Preguntas Frecuentes (FAQ) sobre la Constante de Equilibrio
- Conclusión
¿Qué es el Equilibrio Químico y Por Qué es Tan Importante?
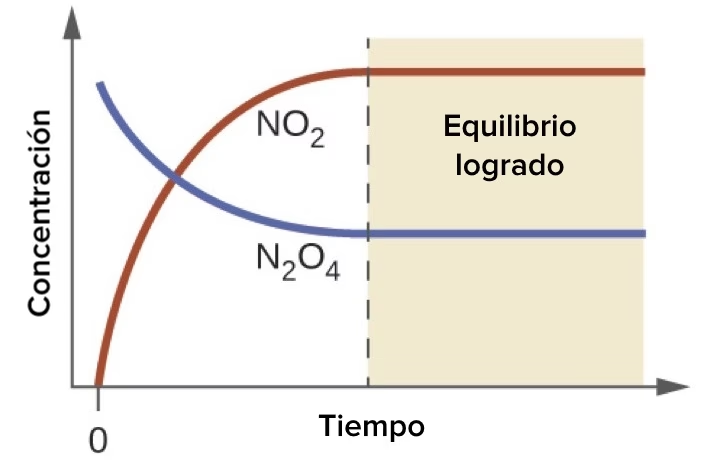
En el vasto mundo de las reacciones químicas, la conversión completa de los reactivos en productos es un fenómeno raro. La gran mayoría de las reacciones, incluidas aquellas que sustentan la vida en nuestro organismo, son inherentemente reacciones reversibles. Esto significa que, a medida que los reactivos se transforman en productos, los productos también pueden reaccionar para reformar los reactivos originales. Cuando las velocidades de la reacción directa (reactivos a productos) y la reacción inversa (productos a reactivos) se igualan, el sistema alcanza un estado de equilibrio químico.
Este estado es de suma importancia porque representa la condición más estable y energéticamente favorable para un sistema de reacción dado bajo ciertas condiciones. El conocimiento de los principios que rigen el equilibrio químico, como el famoso Principio de Le Chatelier, permite a los científicos y a los ingenieros predecir el resultado de muchas reacciones, optimizar procesos tecnológicos y comprender fenómenos naturales. Sin este entendimiento, la química sería una ciencia mucho menos predecible y controlable.
Reacciones Reversibles vs. Irreversibles: Una Distinción Crucial
Para entender el equilibrio, primero debemos diferenciar entre dos tipos de reacciones:
- Reacciones Irreversibles: En estas reacciones, los reactivos se transforman en productos, y la transformación inversa (productos a reactivos) es insignificante o inexistente en la práctica. Se representan con una sola flecha (→) que apunta hacia los productos. Ejemplos comunes incluyen aquellas en las que se forman precipitados insolubles o donde uno de los productos escapa del sistema (como un gas en un recipiente abierto).
- Reacciones Reversibles: Son aquellas en las que los productos se forman a partir de los reactivos, y al mismo tiempo, los productos reaccionan para reconstituir los reactivos. Se representan con dos flechas en direcciones opuestas (⇌). Estas reacciones suelen ocurrir en sistemas cerrados, donde las moléculas de reactivos y productos no pueden escapar y pueden colisionar libremente, lo que permite la interconversión continua. Un ejemplo clásico es la formación de yoduro de hidrógeno a partir de yodo e hidrógeno.
Es importante recordar que la clasificación de una reacción como "irreversible" a menudo se basa en la prevalencia del efecto final bajo condiciones típicas. Teóricamente, pocas reacciones son 100% irreversibles.
A continuación, una tabla comparativa para aclarar estas diferencias:
| Característica | Reacciones Irreversibles | Reacciones Reversibles |
|---|---|---|
| Dirección de la Reacción | Una sola dirección (reactivos a productos) | Ambas direcciones (directa e inversa) |
| Representación | Una flecha (→) | Dos flechas (⇌) |
| Estado Final | Reactivos se consumen casi completamente | Alcanzan un estado de equilibrio dinámico |
| Sistema Típico | Abierto (a menudo con escape de productos) | Cerrado (contiene todos los componentes) |
| Ejemplo | Formación de un precipitado | Formación de yoduro de hidrógeno |
La Constante de Equilibrio (K): El Corazón del Equilibrio Químico
La constante de equilibrio, denotada como K, es un valor numérico que describe la relación entre las concentraciones de productos y reactivos en un sistema en equilibrio. Fue formulada en 1864 como la llamada ley de acción de masas. Para una reacción general:
aA + bB ⇌ cC + dD
Donde A y B son los reactivos, C y D son los productos, y a, b, c, y d son sus respectivos coeficientes estequiométricos, la expresión de la constante de equilibrio (Kc, para concentraciones molares) es:
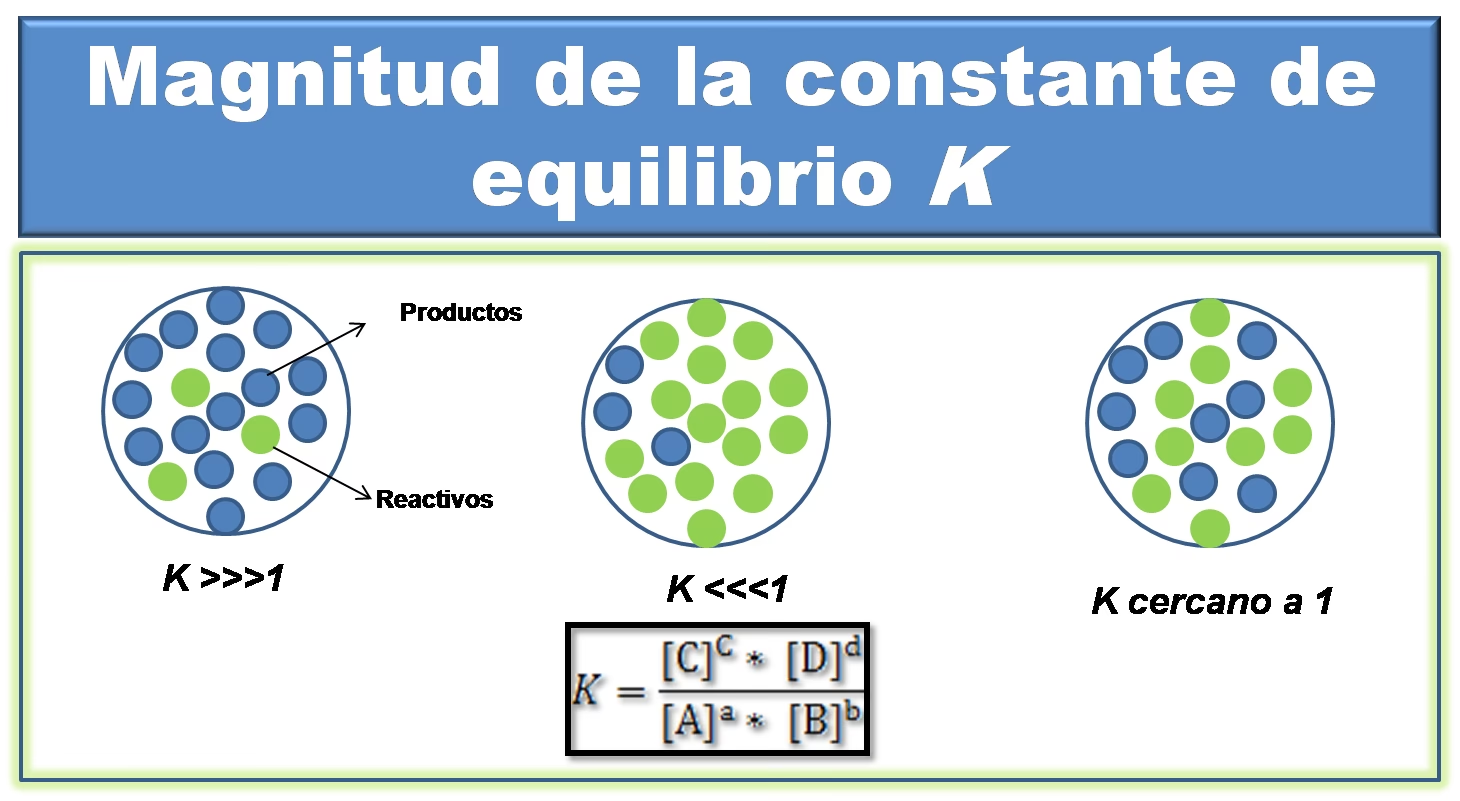
Kc = ([C]c[D]d) / ([A]a[B]b)
En esta expresión, los corchetes [ ] denotan las concentraciones molares de las especies en equilibrio.

¿Qué Nos Dice el Valor de K?
El valor de la constante de equilibrio es un indicador poderoso de la extensión de una reacción en el equilibrio:
- K > 1: Si K es mucho mayor que 1, significa que las concentraciones de los productos en el equilibrio son significativamente más altas que las de los reactivos. La reacción "tiende" a favorecer la formación de productos.
- K < 1: Si K es mucho menor que 1, indica que las concentraciones de los reactivos en el equilibrio son considerablemente más altas que las de los productos. La reacción "tiende" a favorecer a los reactivos.
- K ≈ 1: Si K está cerca de 1, las concentraciones de productos y reactivos son comparables en el equilibrio.
Es fundamental recordar que K es un valor característico para una reacción particular a una temperatura específica. Su valor solo cambia con la temperatura.
Manejo de Sustancias Puras y Disolventes en la Expresión de K
Un aspecto importante en la escritura de las expresiones de la constante de equilibrio es cómo se tratan las sustancias puras (líquidos o sólidos) y los disolventes:
- Sustancias Puras (Sólidos y Líquidos): Sus actividades (o concentraciones efectivas) se consideran unitarias (igual a 1) porque sus concentraciones no cambian significativamente durante la reacción. Por lo tanto, no aparecen en la expresión de K. Un ejemplo es la reacción de Boudouard: 2 CO(g) ⇌ CO2(g) + C(s). La expresión de Kc sería Kc = [CO2] / [CO]2, donde el carbono sólido (C) no se incluye.
- Disolventes (en Soluciones Diluidas): De manera similar, si el agua actúa como disolvente en una solución diluida, su actividad se considera unitaria. Por ejemplo, en la autoionización del agua, 2 H2O(l) ⇌ H3O+(aq) + OH-(aq), la constante de ionización del agua (Kw) se define como Kw = [H3O+][OH-], omitiendo el agua líquida.
Esta simplificación es clave para que la constante de equilibrio sea una herramienta práctica y útil.
Factores que Afectan el Equilibrio Químico: El Principio de Le Chatelier
Aunque el equilibrio químico representa un estado estable, no es inmutable. Diversos factores externos pueden perturbar este equilibrio, haciendo que el sistema se reajuste para alcanzar un nuevo estado de equilibrio. Este comportamiento se describe por el Principio de Le Chatelier (también conocido como la Ley del Equilibrio), que establece que "si se aplica una perturbación a un sistema en equilibrio, el sistema se desplazará en la dirección que minimice o contrarreste esa perturbación".
Impacto de la Concentración de Reactivos
La adición o eliminación de reactivos o productos alterará el equilibrio. Si se añade un reactivo, el sistema se desplazará para consumir ese reactivo adicional, produciendo más productos. Si se añade un producto, el sistema se desplazará para consumir ese producto, reformando los reactivos. Esto es fundamental en procesos industriales para maximizar el rendimiento de un producto deseado.
Efecto de la Temperatura
La temperatura es el único factor que cambia el valor numérico de la constante de equilibrio (K). Su efecto depende de si la reacción es exotérmica (libera calor, ΔH < 0) o endotérmica (absorbe calor, ΔH > 0):
- Reacciones Endotérmicas: Un aumento de la temperatura favorece la reacción directa (hacia los productos), ya que el sistema absorbe el calor añadido para contrarrestar la perturbación. Por lo tanto, K aumenta.
- Reacciones Exotérmicas: Un aumento de la temperatura favorece la reacción inversa (hacia los reactivos), ya que el sistema disipa el calor añadido. Por lo tanto, K disminuye.
La relación cuantitativa entre K y la temperatura se describe mediante la ecuación de Van 't Hoff.
Influencia de la Presión y el Volumen
Para reacciones que involucran gases, los cambios en la presión (o volumen del sistema) pueden desplazar el equilibrio. Un aumento de la presión (o disminución del volumen) favorecerá la dirección que reduzca el número total de moles de gas. Una disminución de la presión (o aumento del volumen) favorecerá la dirección que aumente el número total de moles de gas. Si el número de moles de gas es igual en ambos lados de la ecuación, la presión no tendrá efecto sobre el equilibrio.
El Papel de los Catalizadores
Los catalizadores son sustancias que aumentan la velocidad a la que una reacción alcanza el equilibrio, pero no afectan la posición del equilibrio ni el valor de la constante de equilibrio. Aceleran tanto la reacción directa como la inversa en la misma medida, lo que significa que el sistema simplemente llega al equilibrio más rápidamente, pero la composición final en el equilibrio no cambia.
La Importancia de las Constantes en la Química Experimental
Más allá de la constante de equilibrio, el concepto de "constante" es fundamental en toda la ciencia, especialmente en la química experimental. Lo que a menudo se denomina "variable constante" o "variable de control" es un factor que se mantiene inalterado durante un experimento. Estas variables son cruciales para asegurar la validez y la precisión de los resultados, permitiendo a los investigadores aislar y comprender el efecto de las variables independientes.

Por ejemplo, al determinar una constante de equilibrio, es esencial mantener la temperatura constante, ya que sabemos que K depende de ella. Otras variables de control comunes en experimentos químicos incluyen la humedad, la presión, la duración del experimento, el volumen de la muestra, la técnica utilizada y la pureza de los reactivos. Al controlar estas variables, los científicos pueden establecer correlaciones claras entre las variables de interés y obtener resultados reproducibles. Sin el control de estas constantes, sería extremadamente difícil obtener conclusiones válidas y fiables, lo que socavaría todo el propósito de la experimentación científica.
Este rigor experimental es lo que permite a los químicos desarrollar nuevos combustibles, baterías más eficientes y comprender procesos biológicos complejos, basándose en la confianza de que los "constantes" se han mantenido como tales para revelar el verdadero comportamiento de las "variables" estudiadas.
Equilibrios Múltiples y Complejidad
Muchas reacciones químicas, especialmente aquellas en sistemas biológicos o industriales, no son simples equilibrios de un solo paso. En cambio, involucran una serie de equilibrios acoplados. Consideremos, por ejemplo, un ácido diprótico (H2A), que puede disociarse en dos pasos sucesivos:
H2A ⇌ HA- + H+ (con constante K1)
HA- ⇌ A2- + H+ (con constante K2)
Cada uno de estos pasos tiene su propia constante de equilibrio (K1 y K2 son constantes de disociación escalonadas). La constante de equilibrio global para la disociación completa de H2A a A2- se obtiene multiplicando las constantes escalonadas:
Kglobal = K1 * K2
El estudio de estos equilibrios múltiples es esencial para comprender sistemas complejos, como la química de la sangre (amortiguadores), la formación de complejos metálicos o las reacciones en cadenas de polímeros. A menudo, es más conveniente trabajar con constantes de asociación (donde las especies se unen) en lugar de constantes de disociación, dependiendo del contexto.
Preguntas Frecuentes (FAQ) sobre la Constante de Equilibrio
- ¿Para qué sirve la constante de equilibrio?
- La constante de equilibrio (K) sirve para predecir la composición de una mezcla de reacción en el equilibrio. Nos indica si una reacción tenderá a formar más productos o si los reactivos predominarán en el estado de equilibrio. Un valor de K grande indica una alta concentración de productos, mientras que un valor pequeño indica una alta concentración de reactivos.
- ¿Cómo se calcula la constante de equilibrio?
- Para una reacción general aA + bB ⇌ cC + dD, la constante de equilibrio (Kc para concentraciones) se calcula como el cociente de las concentraciones de los productos elevadas a sus coeficientes estequiométricos, dividido por las concentraciones de los reactivos elevadas a sus coeficientes estequiométricos, todo medido en el estado de equilibrio: Kc = ([C]c[D]d) / ([A]a[B]b).
- ¿Qué factores afectan el equilibrio químico?
- Los factores que afectan el equilibrio químico son los cambios en la concentración de reactivos o productos, la temperatura y la presión (para reacciones con gases). El sistema se ajustará para contrarrestar estas perturbaciones, siguiendo el Principio de Le Chatelier.
- ¿Un catalizador afecta la constante de equilibrio?
- No, un catalizador no afecta el valor de la constante de equilibrio ni la posición del equilibrio. Su única función es acelerar la velocidad a la que la reacción alcanza el estado de equilibrio, ya que acelera tanto la reacción directa como la inversa por igual.
- ¿Por qué las sustancias puras (sólidos y líquidos) no aparecen en la expresión de K?
- Las sustancias puras (sólidos y líquidos) y los disolventes en soluciones diluidas tienen una concentración efectiva (actividad) que se considera constante e igual a la unidad (1). Dado que su "concentración" no cambia significativamente durante la reacción, no se incluyen en la expresión de la constante de equilibrio, ya que su inclusión no alteraría el valor numérico de K.
Conclusión
El equilibrio químico y su constante de equilibrio asociada son conceptos pilares en la química. Nos proporcionan la capacidad de comprender, predecir y manipular el resultado de las reacciones químicas, desde los procesos industriales a gran escala hasta los intrincados mecanismos biológicos dentro de las células. La constante de equilibrio no es solo un número; es una ventana a la composición dinámica de un sistema en su estado más estable, revelando la propensión de una reacción a favorecer la formación de productos o la persistencia de los reactivos. Al dominar la comprensión de K y el Principio de Le Chatelier, los químicos pueden diseñar sistemas más eficientes, desarrollar nuevos materiales y profundizar en el conocimiento fundamental de cómo interactúa la materia. Es una constante que nos permite entender el cambio, una herramienta indispensable para cualquier estudio serio de las transformaciones químicas.
Si quieres conocer otros artículos parecidos a La Constante de Equilibrio: Entendiendo las Reacciones Químicas puedes visitar la categoría Química.