08/12/2023
En el vasto y fascinante mundo de la química, las soluciones son omnipresentes. Desde el café que bebes por la mañana hasta los medicamentos que salvan vidas, y los productos de limpieza que usamos a diario, todos son ejemplos de soluciones. Comprender cómo se componen estas mezclas es fundamental, y una de las tareas más comunes es determinar la cantidad de una sustancia disuelta, conocida como soluto. ¿Alguna vez te has preguntado cómo se calcula su peso exacto? Esta guía te llevará paso a paso a través de los conceptos y cálculos necesarios para dominar esta habilidad esencial.
Calcular el peso del soluto no solo es una habilidad crucial en laboratorios de química y en la industria, sino que también tiene aplicaciones prácticas en nuestra vida cotidiana. Nos permite, por ejemplo, preparar soluciones con la concentración adecuada para experimentos, formulaciones farmacéuticas o incluso para recetas de cocina específicas. La base de este cálculo a menudo reside en el concepto de porcentaje en masa, una medida de concentración que expresa la masa del soluto en relación con la masa total de la solución.
- Entendiendo los Componentes de una Solución
- La Fórmula Clave: Porcentaje en Masa
- Paso a Paso: Calculando la Masa del Soluto
- Ejemplos Prácticos de Cálculo
- Conceptos Relacionados y Unidades de Concentración
- Factores que Afectan la Solubilidad
- La Importancia de la Precisión en la Química
- Preguntas Frecuentes (FAQs)
- ¿Qué diferencia hay entre soluto y solvente?
- ¿Por qué es importante el porcentaje en masa?
- ¿Puedo calcular el peso del soluto si solo tengo el volumen de la solución?
- ¿Qué pasa si el porcentaje en masa es muy bajo (ej. 0.001%) o muy alto (ej. 90%)?
- ¿Cómo se mide la masa total de una solución en el laboratorio?
- ¿Es lo mismo porcentaje en masa que porcentaje en peso?
- ¿La temperatura afecta el porcentaje en masa?
- Conclusión
Entendiendo los Componentes de una Solución
Antes de sumergirnos en las fórmulas, es vital tener claros los términos básicos:
- Soluto: Es la sustancia que se disuelve en otra. Generalmente, es el componente que se encuentra en menor proporción en la solución. Por ejemplo, en una solución de sal en agua, la sal es el soluto.
- Solvente (o Disolvente): Es la sustancia en la que se disuelve el soluto. Es el componente que se encuentra en mayor proporción. En el ejemplo de la sal en agua, el agua es el solvente.
- Solución: Es la mezcla homogénea resultante de la disolución de un soluto en un solvente. Homogénea significa que la composición es uniforme en toda la mezcla; no se pueden distinguir sus componentes a simple vista.
La masa de una solución es simplemente la suma de la masa del soluto y la masa del solvente. Esta relación es fundamental para cualquier cálculo de concentración basado en la masa.
La Fórmula Clave: Porcentaje en Masa
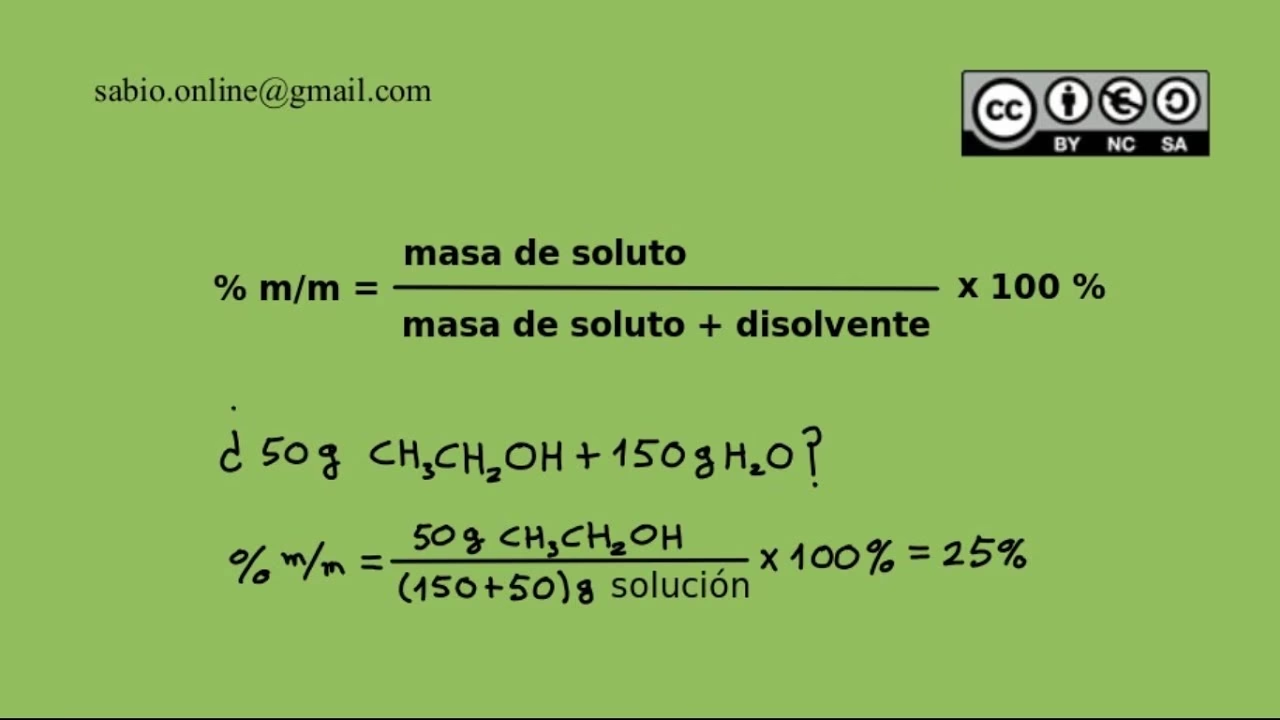
El porcentaje en masa (% m/m) es una de las formas más comunes de expresar la concentración de una solución. Se define como:
Porcentaje en masa (% m/m) = (Masa del soluto / Masa total de la solución) x 100%
Esta fórmula nos dice qué proporción de la masa total de la solución corresponde al soluto. Para calcular el peso del soluto a partir de un porcentaje en masa conocido, necesitamos reorganizar esta fórmula. Si conocemos el porcentaje en masa y la masa total de la solución, podemos despejar la masa del soluto de la siguiente manera:
Masa del soluto = (Porcentaje en masa / 100%) x Masa total de la solución
Esta es la ecuación central que utilizaremos. Es importante recordar que el porcentaje en masa debe dividirse por 100 para convertirlo a una fracción decimal antes de multiplicarlo por la masa total de la solución.
Paso a Paso: Calculando la Masa del Soluto
Para garantizar la precisión en tus cálculos, sigue estos sencillos pasos:
- Identifica los datos conocidos: Asegúrate de tener el porcentaje en masa de la solución y la masa total de la solución. Si te dan el volumen de la solución en lugar de la masa, necesitarás conocer la densidad de la solución para convertir el volumen a masa (Masa = Densidad x Volumen).
- Convierte el porcentaje a decimal: Divide el valor del porcentaje en masa por 100. Por ejemplo, si tienes un 15% en masa, divídelo por 100 para obtener 0.15.
- Aplica la fórmula: Multiplica el valor decimal del porcentaje por la masa total de la solución.
- Verifica las unidades: La masa del soluto resultante tendrá las mismas unidades que la masa total de la solución (por ejemplo, gramos, kilogramos).
Ejemplos Prácticos de Cálculo
Ejemplo 1: Cálculo Directo
Problema: Se tiene una solución acuosa de cloruro de sodio (NaCl) al 12% en masa, y la masa total de la solución es de 250 gramos. ¿Cuál es la masa de NaCl disuelto?
- Datos conocidos:
- Porcentaje en masa = 12%
- Masa total de la solución = 250 g
- Paso 1: Convertir porcentaje a decimal:
- 12% / 100% = 0.12
- Paso 2: Aplicar la fórmula:
- Masa del soluto = 0.12 x 250 g
- Masa del soluto = 30 g de NaCl
Por lo tanto, hay 30 gramos de cloruro de sodio en la solución.
Ejemplo 2: Preparación de una Solución
Problema: Necesitas preparar 500 mL de una solución de glucosa al 5% (m/m) para un experimento. Si la densidad de la solución es aproximadamente 1.02 g/mL, ¿cuántos gramos de glucosa necesitas pesar?
- Datos conocidos:
- Volumen de la solución = 500 mL
- Densidad de la solución = 1.02 g/mL
- Porcentaje en masa = 5%
- Paso 1: Calcular la masa total de la solución (usando la densidad):
- Masa total de la solución = Densidad x Volumen
- Masa total de la solución = 1.02 g/mL x 500 mL
- Masa total de la solución = 510 g
- Paso 2: Convertir porcentaje a decimal:
- 5% / 100% = 0.05
- Paso 3: Aplicar la fórmula para la masa del soluto:
- Masa del soluto = 0.05 x 510 g
- Masa del soluto = 25.5 g de glucosa
Necesitarías pesar 25.5 gramos de glucosa para preparar esta solución.
Conceptos Relacionados y Unidades de Concentración
Aunque el porcentaje en masa es muy útil, existen otras formas de expresar la concentración de una solución, cada una con sus propias aplicaciones. Comprenderlas te dará una visión más completa de la química de las soluciones.
Otras Unidades de Concentración Comunes:
- Molaridad (M): Se define como el número de moles de soluto por litro de solución (moles/L). Es muy utilizada en química por su relación directa con el número de partículas.
- Molalidad (m): Se define como el número de moles de soluto por kilogramo de solvente (moles/kg). Es útil cuando la temperatura de la solución puede variar, ya que la masa no cambia con la temperatura.
- Partes por millón (ppm) / Partes por billón (ppb): Se utilizan para soluciones muy diluidas, donde la cantidad de soluto es extremadamente pequeña. Por ejemplo, la concentración de contaminantes en el agua o el aire.
- Porcentaje en volumen (% v/v): Similar al porcentaje en masa, pero expresado en volumen de soluto por volumen total de solución. Común para mezclas de líquidos.
Tabla Comparativa de Unidades de Concentración
| Unidad | Definición | Fórmula | Uso Común |
|---|---|---|---|
| Porcentaje en Masa (% m/m) | Masa de soluto por 100 unidades de masa de solución. | (Masa soluto / Masa solución) x 100% | Preparación de soluciones, análisis gravimétrico, productos comerciales. |
| Molaridad (M) | Moles de soluto por litro de solución. | Moles soluto / Litros solución | Reacciones químicas, estequiometría, titulaciones. |
| Molalidad (m) | Moles de soluto por kilogramo de solvente. | Moles soluto / Kg solvente | Estudios de propiedades coligativas (punto de ebullición, congelación). |
| Porcentaje en Volumen (% v/v) | Volumen de soluto por 100 unidades de volumen de solución. | (Volumen soluto / Volumen solución) x 100% | Mezclas de líquidos (ej. alcohol en agua), bebidas. |
| Partes por Millón (ppm) | Masa de soluto por millón de unidades de masa de solución. | (Masa soluto / Masa solución) x 10^6 | Contaminantes, trazas de sustancias, control de calidad del agua. |
Factores que Afectan la Solubilidad
Aunque el cálculo del peso del soluto es directo una vez que se conoce el porcentaje y la masa total, es importante recordar que no siempre es posible disolver una cantidad ilimitada de soluto en un solvente. La solubilidad, que es la cantidad máxima de soluto que se puede disolver en una cantidad dada de solvente a una temperatura específica, está influenciada por varios factores:
- Naturaleza del Soluto y del Solvente: La regla general es 'lo semejante disuelve a lo semejante'. Las sustancias polares tienden a disolverse en solventes polares, y las no polares en solventes no polares. Por ejemplo, el azúcar (polar) se disuelve bien en agua (polar), mientras que el aceite (no polar) no lo hace.
- Temperatura: Para la mayoría de los sólidos, la solubilidad aumenta con la temperatura. Para los gases, la solubilidad disminuye a medida que la temperatura aumenta.
- Presión: La presión tiene un efecto significativo en la solubilidad de los gases en líquidos. A mayor presión, mayor solubilidad de un gas. Este es el principio detrás de las bebidas carbonatadas.
Entender estos factores es clave para preparar soluciones de manera efectiva y para interpretar los resultados de los cálculos de concentración.
La Importancia de la Precisión en la Química
La capacidad de calcular con exactitud el peso del soluto es más que un simple ejercicio matemático; es una habilidad crítica que subyace en la química analítica, la química preparativa y numerosas aplicaciones industriales. Una pequeña desviación en la cantidad de soluto puede tener consecuencias significativas:
- En Farmacia: Una dosis incorrecta de un medicamento, debido a una concentración mal calculada, podría ser ineficaz o incluso tóxica.
- En la Industria Alimentaria: La concentración de aditivos, saborizantes o conservantes debe ser precisa para garantizar la seguridad y calidad del producto.
- En Investigación: Los resultados experimentales dependen de la preparación exacta de las soluciones. Errores aquí pueden llevar a conclusiones erróneas.
- En el Control de Calidad: Muchas industrias utilizan la concentración para verificar la calidad de las materias primas y los productos finales.
Por lo tanto, no solo es importante saber cómo calcular, sino también cómo realizar mediciones de masa y volumen con la mayor precisión posible utilizando balanzas analíticas y material volumétrico adecuado.
Preguntas Frecuentes (FAQs)
¿Qué diferencia hay entre soluto y solvente?
El soluto es la sustancia que se disuelve y se encuentra en menor cantidad. El solvente es la sustancia que disuelve al soluto y generalmente se encuentra en mayor cantidad. Por ejemplo, en el agua azucarada, el azúcar es el soluto y el agua es el solvente.
¿Por qué es importante el porcentaje en masa?
El porcentaje en masa es una forma sencilla y práctica de expresar la concentración, especialmente útil en la industria y en aplicaciones donde la masa es una medida conveniente. Permite una fácil preparación de soluciones por pesada directa y es independiente de la temperatura, a diferencia de las unidades basadas en volumen.
¿Puedo calcular el peso del soluto si solo tengo el volumen de la solución?
Sí, pero necesitarás conocer la densidad de la solución. La densidad (masa/volumen) te permitirá convertir el volumen de la solución a su masa total. Una vez que tengas la masa total de la solución, puedes aplicar la fórmula del porcentaje en masa para encontrar el peso del soluto.
¿Qué pasa si el porcentaje en masa es muy bajo (ej. 0.001%) o muy alto (ej. 90%)?
Si el porcentaje es muy bajo, se suelen usar unidades como partes por millón (ppm) o partes por billón (ppb) para evitar números decimales muy pequeños. Un porcentaje muy alto significa que la solución es muy concentrada, con una gran cantidad de soluto. Ambos escenarios son comunes y los cálculos siguen siendo los mismos.
¿Cómo se mide la masa total de una solución en el laboratorio?
La masa total de una solución se mide pesando el recipiente vacío (tara), luego añadiendo el solvente y el soluto y pesando el conjunto. La masa total de la solución se obtiene restando la tara del peso total. Alternativamente, se puede pesar el soluto y el solvente por separado y luego sumarlos.
¿Es lo mismo porcentaje en masa que porcentaje en peso?
Sí, en el contexto de la química y la física, los términos 'masa' y 'peso' a menudo se usan indistintamente, especialmente cuando se habla de la cantidad de una sustancia en condiciones de gravedad estándar. Sin embargo, 'masa' es el término científicamente más preciso, ya que se refiere a la cantidad de materia, mientras que 'peso' es la fuerza de la gravedad sobre esa masa.
¿La temperatura afecta el porcentaje en masa?
No directamente. El porcentaje en masa se basa en las masas del soluto y la solución, y la masa de una sustancia no cambia con la temperatura. Sin embargo, la temperatura sí afecta la solubilidad, lo que significa que la cantidad máxima de soluto que se puede disolver para formar una solución con un cierto porcentaje en masa sí puede depender de la temperatura.
Conclusión
Calcular el peso del soluto a partir del porcentaje en masa es una habilidad fundamental que te abre las puertas a una comprensión más profunda de las soluciones químicas. Con la fórmula simple: Masa del soluto = (Porcentaje en masa / 100%) x Masa total de la solución, y una comprensión clara de los conceptos de soluto, solvente y solución, puedes abordar una amplia gama de problemas de concentración. Recuerda siempre la importancia de la precisión en cada paso y cómo esta habilidad se aplica en numerosos campos, desde el laboratorio hasta la vida cotidiana. Dominar este cálculo te empodera para entender y manipular la composición de las mezclas que nos rodean.
Si quieres conocer otros artículos parecidos a Calculando el Peso del Soluto: Guía Esencial puedes visitar la categoría Química.

