26/01/2022
En el fascinante mundo de la química, las reacciones son el pan de cada día. Sin embargo, para que una reacción ocurra de manera controlada y eficiente, es fundamental comprender las cantidades de las sustancias que interactúan. No siempre se mezclan las cantidades exactas de reactivos que reaccionan por completo, y es aquí donde entran en juego los conceptos de reactivo limitante y reactivo en exceso. Comprender cómo calcular el reactivo en exceso es una habilidad esencial no solo para estudiantes de química, sino también para ingenieros, investigadores y profesionales de la industria, ya que permite optimizar procesos, predecir rendimientos y minimizar el desperdicio de materiales. Este artículo te guiará paso a paso para dominar este cálculo fundamental.
Cuando dos o más sustancias, conocidas como reactivos, se combinan para formar nuevas sustancias, llamadas productos, lo hacen en proporciones estequiométricas fijas. Esto significa que hay una relación ideal entre las cantidades de reactivos que deben mezclarse para que la reacción se complete perfectamente, sin que sobre ninguna de las sustancias iniciales. Sin embargo, en la práctica, es muy común que uno de los reactivos se agote antes que los demás, deteniendo la reacción. A este reactivo que se consume por completo se le conoce como reactivo limitante, porque su cantidad limita la cantidad de producto que se puede formar. Por otro lado, el reactivo o los reactivos que quedan sin reaccionar una vez que el reactivo limitante se ha agotado, se denominan reactivos en exceso. Calcular cuánto de este reactivo en exceso permanece sin reaccionar es crucial para diversas aplicaciones, desde la síntesis de nuevos compuestos hasta la producción industrial a gran escala.
- Fundamentos Químicos para el Cálculo
- Diferenciando el Reactivo Limitante del Reactivo en Exceso
- Paso a Paso: Cómo Calcular el Reactivo en Exceso
- Ejemplo Práctico Detallado
- Importancia y Aplicaciones en la Vida Real
- Errores Comunes a Evitar
- Tabla Comparativa: Reactivo Limitante vs. Reactivo en Exceso
- Preguntas Frecuentes (FAQ)
- Conclusión
Fundamentos Químicos para el Cálculo
Antes de sumergirnos en los cálculos, es vital repasar algunos conceptos clave que son la base de la estequiometría:
- Ecuación Química Balanceada: Toda reacción química debe representarse mediante una ecuación balanceada. Esto significa que el número de átomos de cada elemento debe ser el mismo en ambos lados de la ecuación (reactivos y productos), cumpliendo con la Ley de Conservación de la Masa. Los coeficientes estequiométricos en una ecuación balanceada representan las proporciones molares en las que reaccionan y se forman las sustancias.
- Mol: La unidad fundamental en química para medir la cantidad de sustancia. Un mol de cualquier sustancia contiene aproximadamente 6.022 x 1023 partículas (átomos, moléculas, iones, etc.), conocido como el número de Avogadro. El mol es el puente entre la masa de una sustancia y el número de partículas, y es indispensable para realizar cálculos estequiométricos.
- Masa Molar: La masa de un mol de una sustancia, expresada en gramos por mol (g/mol). Se calcula sumando las masas atómicas de todos los átomos en una molécula.
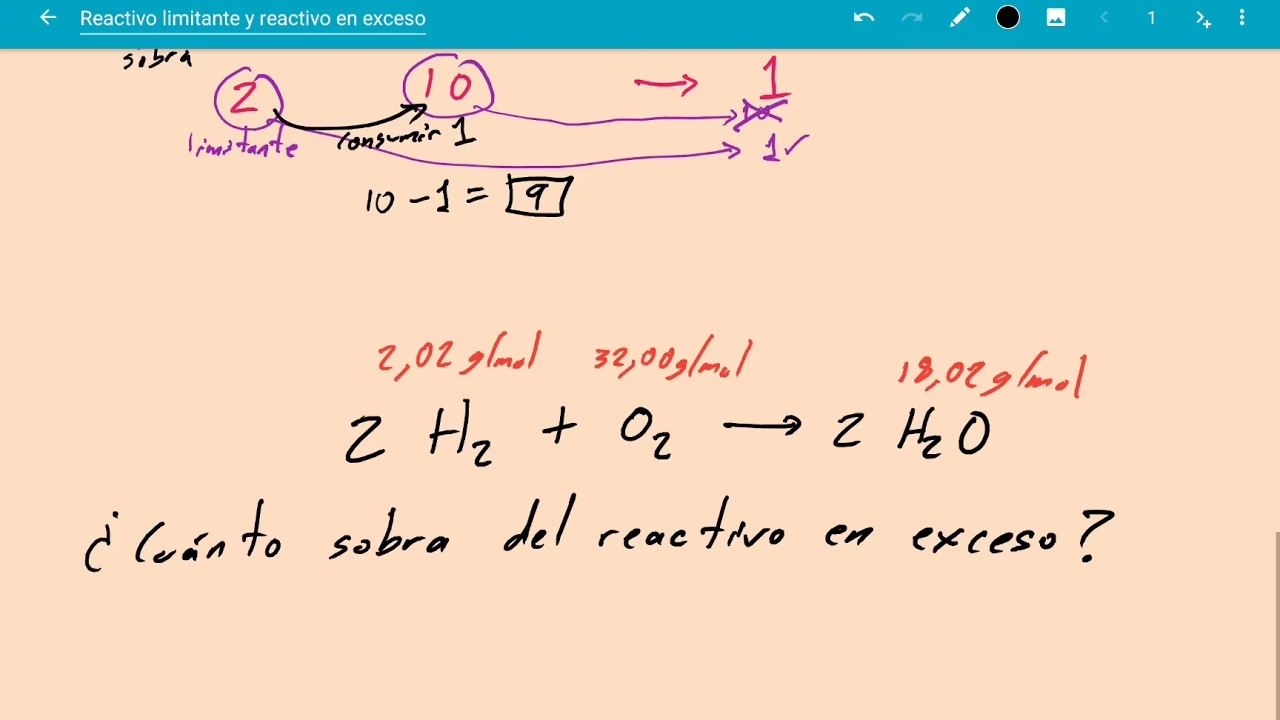
- Relaciones Estequiométricas: Son las proporciones en moles entre los reactivos y los productos, derivadas de los coeficientes de la ecuación balanceada. Por ejemplo, en la reacción 2H2 + O2 → 2H2O, 2 moles de hidrógeno reaccionan con 1 mol de oxígeno para producir 2 moles de agua.
Diferenciando el Reactivo Limitante del Reactivo en Exceso
La clave para calcular el reactivo en exceso es primero identificar el reactivo limitante. Imagina que estás preparando sándwiches de queso y jamón. Si cada sándwich requiere 2 rebanadas de pan, 1 rebanada de queso y 1 rebanada de jamón, y tú tienes 10 rebanadas de pan, 4 de queso y 4 de jamón: ¿Cuántos sándwiches puedes hacer? El pan te permitiría hacer 5 sándwiches (10/2). El queso y el jamón te permitirían hacer 4 sándwiches cada uno. Por lo tanto, el queso y el jamón son los reactivos limitantes, ya que se agotarán primero, y el pan sería el reactivo en exceso, ya que te sobrarán rebanadas. En química, el principio es el mismo: el reactivo limitante es el que se consume por completo y determina la máxima cantidad de producto que se puede formar, mientras que el reactivo en exceso es el que sobra.
Paso a Paso: Cómo Calcular el Reactivo en Exceso
El proceso para calcular el reactivo en exceso sigue una serie de pasos lógicos. Se recomienda llevar un registro claro de cada cálculo para evitar confusiones.
Paso 1: Escribir y Balancear la Ecuación Química
Este es el punto de partida fundamental. Sin una ecuación balanceada, todas las proporciones molares serán incorrectas, y los cálculos posteriores carecerán de validez. Asegúrate de que el número de átomos de cada elemento sea el mismo en ambos lados de la flecha de reacción.
Paso 2: Convertir las Cantidades Dadas de Reactivos a Moles
Las cantidades iniciales de los reactivos suelen darse en unidades de masa (gramos, kilogramos), volumen (litros, mililitros) si son líquidos o gases a condiciones específicas, o concentración (molaridad). Para poder utilizar las relaciones estequiométricas de la ecuación balanceada, es imprescindible convertir estas cantidades a moles. Para masas, se usa la masa molar (moles = masa / masa molar). Para soluciones, se usa la molaridad (moles = molaridad x volumen).
Paso 3: Determinar el Reactivo Limitante
Hay varias maneras de hacer esto. Una de las más comunes y directas es la siguiente:
- Elige uno de los reactivos y calcula cuántos moles del *otro* reactivo serían necesarios para que el primer reactivo reaccione por completo, utilizando las relaciones estequiométricas de la ecuación balanceada.
- Compara la cantidad necesaria del segundo reactivo con la cantidad *realmente disponible* de ese reactivo.
- Si la cantidad necesaria es mayor que la disponible, entonces el segundo reactivo es el limitante. Si la cantidad necesaria es menor que la disponible, entonces el primer reactivo que elegiste es el limitante.
Otra forma es calcular la cantidad de producto que se podría formar con cada uno de los reactivos, asumiendo que el otro es en exceso. El reactivo que produce la menor cantidad de producto es el limitante.
Paso 4: Calcular la Cantidad del Reactivo en Exceso que Realmente Reacciona
Una vez que has identificado el reactivo limitante, puedes usarlo para determinar cuánto del reactivo en exceso se consume realmente durante la reacción. Utiliza la cantidad de moles del reactivo limitante y las relaciones estequiométricas de la ecuación balanceada para calcular cuántos moles del reactivo en exceso son necesarios para reaccionar completamente con el limitante.
Paso 5: Calcular la Cantidad del Reactivo en Exceso que Sobra
Finalmente, para encontrar la cantidad de reactivo en exceso que queda sin reaccionar, simplemente resta la cantidad de reactivo en exceso que se consumió (calculada en el Paso 4) de la cantidad inicial de reactivo en exceso que tenías (calculada en el Paso 2). Si es necesario, puedes convertir esta cantidad de moles de nuevo a gramos u otras unidades, dependiendo de lo que se te pida.
Ejemplo Práctico Detallado
Consideremos la reacción de combustión del propano (C3H8) con oxígeno (O2) para producir dióxido de carbono (CO2) y agua (H2O).
Problema: Si se hacen reaccionar 22.0 g de propano (C3H8) con 64.0 g de oxígeno (O2), ¿cuál es el reactivo limitante y cuántos gramos del reactivo en exceso quedarán sin reaccionar?
Solución:
Paso 1: Escribir y Balancear la Ecuación Química
La ecuación no balanceada es: C3H8 + O2 → CO2 + H2O
Balanceando, obtenemos: C3H8(g) + 5O2(g) → 3CO2(g) + 4H2O(g)
Paso 2: Convertir las Cantidades Dadas de Reactivos a Moles
- Masas molares:
- C3H8: (3 * 12.01) + (8 * 1.008) = 44.096 g/mol
- O2: (2 * 16.00) = 32.00 g/mol
- Moles iniciales:
- Moles de C3H8 = 22.0 g / 44.096 g/mol ≈ 0.4989 mol
- Moles de O2 = 64.0 g / 32.00 g/mol = 2.00 mol
Paso 3: Determinar el Reactivo Limitante
Usemos el método de comparar las cantidades necesarias. Calculemos cuánto O2 se necesita para que reaccionen los 0.4989 mol de C3H8:
- Según la ecuación balanceada: 1 mol de C3H8 reacciona con 5 moles de O2.
- Moles de O2 necesarios = 0.4989 mol C3H8 * (5 mol O2 / 1 mol C3H8) = 2.4945 mol O2
Ahora comparamos: Necesitamos 2.4945 mol de O2, pero solo tenemos 2.00 mol de O2. Dado que la cantidad disponible de O2 (2.00 mol) es menor que la cantidad necesaria (2.4945 mol), el O2 es el reactivo limitante. Esto significa que el C3H8 es el reactivo en exceso.
Paso 4: Calcular la Cantidad del Reactivo en Exceso (C3H8) que Realmente Reacciona
Usamos la cantidad del reactivo limitante (O2) para calcular cuánto C3H8 se consume:
- Moles de C3H8 consumidos = 2.00 mol O2 * (1 mol C3H8 / 5 mol O2) = 0.400 mol C3H8
Paso 5: Calcular la Cantidad del Reactivo en Exceso (C3H8) que Sobra
- Moles iniciales de C3H8 = 0.4989 mol
- Moles de C3H8 consumidos = 0.400 mol
- Moles de C3H8 en exceso = 0.4989 mol - 0.400 mol = 0.0989 mol
Finalmente, convertimos estos moles en exceso a gramos:
- Gramos de C3H8 en exceso = 0.0989 mol * 44.096 g/mol ≈ 4.36 g de C3H8
Por lo tanto, el oxígeno es el reactivo limitante, y quedarán aproximadamente 4.36 gramos de propano sin reaccionar.
Importancia y Aplicaciones en la Vida Real
El cálculo del reactivo en exceso no es solo un ejercicio académico; tiene implicaciones significativas en la industria y la investigación. Aquí algunas razones por las que es tan importante:
- Optimización del Rendimiento: Al identificar el reactivo limitante, los químicos e ingenieros pueden predecir la cantidad máxima de producto que se puede obtener (rendimiento teórico). A menudo, se usa un reactivo en exceso para asegurar que el reactivo limitante, que puede ser más costoso o difícil de purificar, reaccione completamente, maximizando así la conversión y el rendimiento del producto deseado.
- Control de Subproductos y Pureza: En algunas reacciones, la presencia de un reactivo en exceso puede influir en la formación de subproductos indeseados. En otros casos, un exceso de un reactivo puede favorecer la reacción principal y mejorar la pureza del producto final.
- Minimización de Residuos y Costos: Un exceso no controlado de reactivos puede llevar a un desperdicio significativo de materiales, un aumento en los costos de producción y la generación de más residuos que requieren tratamiento o eliminación. Calcular el exceso permite usar la cantidad óptima para el proceso.
- Seguridad: Ciertas reacciones son altamente exotérmicas (liberan calor) o peligrosas. Controlar la cantidad de reactivos, incluyendo el exceso, es crucial para mantener la reacción bajo control y asegurar la seguridad operativa.
- Investigación y Desarrollo: En el laboratorio, los investigadores utilizan el concepto de reactivo en exceso para diseñar experimentos, estudiar la cinética de las reacciones (cómo de rápido ocurren) y determinar los mecanismos de reacción.
Errores Comunes a Evitar
Aunque el proceso es lógico, es fácil cometer errores. Aquí algunos de los más frecuentes:
- No Balancear la Ecuación: Es el error más crítico. Sin una ecuación balanceada, las relaciones molares son incorrectas y todos los cálculos posteriores serán erróneos.
- Errores en la Conversión a Moles: Usar masas molares incorrectas o aplicar fórmulas de conversión erróneas (por ejemplo, confundir gramos con moles).
- Confundir Limitante con Exceso: No identificar correctamente cuál es el reactivo limitante. Esto lleva a calcular el exceso del reactivo que en realidad se agota.
- Errores en las Proporciones Estequiométricas: No aplicar correctamente los coeficientes de la ecuación balanceada al calcular las moles necesarias o consumidas.
- No Distinguir entre Cantidad Inicial y Cantidad Consumida: Es fundamental recordar que el exceso se calcula restando la cantidad consumida de la cantidad inicial, no de la cantidad necesaria para una reacción ideal.
- Unidades Incorrectas: Mezclar unidades o no convertir a las unidades deseadas al final del cálculo (por ejemplo, dejar la respuesta en moles cuando se pide en gramos).
Tabla Comparativa: Reactivo Limitante vs. Reactivo en Exceso
| Característica | Reactivo Limitante | Reactivo en Exceso |
|---|---|---|
| Definición | Se consume completamente en la reacción. | Parte de él queda sin reaccionar. |
| Determinante de Producto | Sí, determina la cantidad máxima de producto formado. | No, no determina la cantidad de producto. |
| Disponibilidad | Es la cantidad más pequeña en relación con la estequiometría. | Es la cantidad más grande en relación con la estequiometría. |
| Función en la Reacción | Detiene la reacción una vez agotado. | Parte de él permanece al final de la reacción. |
| Impacto en el Rendimiento | Directamente relacionado con el rendimiento teórico. | Puede usarse para asegurar la conversión completa del limitante. |
| Recuperación/Reutilización | No se puede recuperar, ya que se agotó. | Potencialmente recuperable o reciclable. |
Preguntas Frecuentes (FAQ)
¿Por qué es importante calcular el reactivo en exceso?
Es crucial para la optimización de procesos químicos. Permite asegurar que el reactivo más costoso o valioso (el limitante) se consuma por completo, maximizando el rendimiento del producto. También ayuda a minimizar el desperdicio, reducir costos y controlar las condiciones de la reacción, como la temperatura o la presión, al conocer las cantidades exactas de los reactivos.
¿Qué sucede si no se usa un reactivo en exceso en una reacción?
Si se mezclan los reactivos en proporciones estequiométricas exactas, idealmente no habría reactivo en exceso. Sin embargo, en la práctica, esto es muy difícil de lograr debido a impurezas, errores de medición o reacciones secundarias. Usar un ligero exceso de un reactivo barato o fácilmente removible asegura que el reactivo limitante, y por ende la reacción principal, proceda hasta su máxima conversión.
¿Siempre hay un reactivo en exceso en una reacción?
En la práctica, la mayoría de las veces sí. Es muy raro que las cantidades exactas de reactivos se mezclen y reaccionen completamente sin que nada sobre. Incluso si se busca una relación estequiométrica perfecta, pequeñas variaciones en la medición o pureza harán que uno de los reactivos se convierta en limitante y el otro en exceso.
¿Cómo afecta la pureza de los reactivos al cálculo del exceso?
La pureza es un factor crítico. Los cálculos estequiométricos asumen que los reactivos son 100% puros. Si un reactivo tiene una pureza del 90%, por ejemplo, solo el 90% de su masa contribuirá a la reacción. Esto debe tenerse en cuenta al convertir las masas dadas a moles. Si se ignora la pureza, los cálculos de reactivo limitante y en exceso serán incorrectos, llevando a predicciones erróneas del rendimiento y del sobrante.
¿El reactivo en exceso es siempre el más abundante en masa?
No necesariamente. El concepto de reactivo en exceso se basa en las proporciones molares estequiométricas, no solo en las masas iniciales. Un reactivo puede tener una masa inicial mayor pero, debido a su masa molar o a su coeficiente estequiométrico en la ecuación balanceada, puede terminar siendo el limitante. Siempre se debe convertir a moles y usar las relaciones estequiométricas para una determinación correcta.
Conclusión
El cálculo del reactivo en exceso es una habilidad fundamental en química que va más allá de un simple ejercicio de clase. Es una herramienta poderosa para comprender y controlar las reacciones químicas, optimizando procesos industriales, minimizando residuos y asegurando la seguridad en el laboratorio y la planta de producción. Al dominar los pasos de balancear la ecuación, convertir a moles, identificar el limitante y calcular el sobrante, estarás equipado para abordar una amplia gama de problemas químicos con confianza y precisión. La estequiometría es la base de la química cuantitativa, y el reactivo en exceso es una pieza clave de este rompecabezas, permitiéndonos no solo predecir lo que sucederá en una reacción, sino también cómo optimizarla para obtener los mejores resultados.
Si quieres conocer otros artículos parecidos a Calculando el Reactivo en Exceso: Guía Completa puedes visitar la categoría Química.