03/08/2024
Durante años, la imagen de un sólido oscuro y cristalino transformándose directamente en un vapor púrpura vibrante ha fascinado a estudiantes y educadores por igual. El yodo, conocido por su aparente sublimación a presión atmosférica, ha sido el protagonista de innumerables demostraciones en laboratorios de química. Sin embargo, ¿qué pasaría si le dijera que esta creencia popular, extendida y repetida por generaciones, es en realidad una profunda concepción errónea? Prepárese para descubrir la sorprendente verdad detrás del comportamiento del yodo y cómo un simple experimento puede desvelar un mundo de fases y estados que desafían nuestras percepciones más arraigadas.

¿Qué es un Punto Triple? La Armonía de las Fases
Antes de sumergirnos en las particularidades del yodo, es esencial comprender el concepto de punto triple. En termodinámica, el punto triple de una sustancia pura es una combinación única y específica de temperatura y presión en la que sus tres estados de la materia —sólido, líquido y gaseoso— pueden coexistir en equilibrio termodinámico. Esto significa que las fases no solo están presentes simultáneamente, sino que también están en un estado de equilibrio dinámico, donde las tasas de transformación entre ellas son iguales.
El ejemplo más conocido de punto triple es el del agua. A 0.0098 °C y una presión de 611.73 Pascales (aproximadamente 0.006 atmósferas), el agua puede existir como hielo, agua líquida y vapor de agua al mismo tiempo. Es un fenómeno que choca con nuestra experiencia cotidiana, donde el agua hierve a 100 °C y se congela a 0 °C a presión atmosférica normal. La clave para alcanzar este punto es la manipulación precisa de la presión. Al reducir drásticamente la presión, la temperatura de ebullición del agua disminuye hasta igualar su temperatura de fusión, permitiendo la coexistencia de las tres fases.
El Punto Triple del Yodo: Desafiando la Convención
El yodo, al igual que el agua, posee su propio punto triple. Según los datos más aceptados y fiables, el punto triple del yodo se encuentra a una temperatura de 113.5 °C y una presión de 12.1 kPa. Esta información es crucial para entender su comportamiento y desmentir el mito de la sublimación universal a presión atmosférica normal.
La creencia errónea de que el yodo sólido se sublima directamente a presión atmosférica (aproximadamente 101.3 kPa) ha sido persistente. Cuando el yodo se calienta en un recipiente abierto en un laboratorio, el denso vapor púrpura que emana es inconfundible y visible incluso en pequeñas concentraciones. Esto ha llevado a muchos a concluir que el yodo pasa directamente de sólido a gas, equiparándolo con el hielo seco (dióxido de carbono sólido), que sí se sublima a presión atmosférica. Sin embargo, este es un error de interpretación basado en las condiciones de un experimento de demostración.
La Revelación del Líquido: Un Experimento Simple
La verdad sobre el comportamiento del yodo fue descubierta por el educador Mike Jansen, quien, al preparar una lección, se topó con el diagrama de fases del yodo y notó que contradecía su experiencia en el laboratorio. Decidido a comprobarlo, realizó una demostración simple. Calentó cristales de yodo en un vaso de precipitados y, al observar los familiares humos púrpuras, rápidamente vertió el contenido sobre una hoja de papel blanco. La sorpresa fue mayúscula: el yodo formó un patrón de salpicadura, una clara evidencia de que había estado presente en estado líquido. El yodo se había fundido antes de evaporarse por completo.
Este experimento empírico es la prueba definitiva de que, a presión atmosférica estándar, el yodo sólido se funde a 113.7 °C y luego hierve a 184.3 °C. La intensa coloración del vapor de yodo a bajas concentraciones y la naturaleza abierta de los experimentos de demostración son los factores que contribuyen a la confusión. En un sistema abierto, el vapor de yodo escapa, y el sólido parece desaparecer, dando la impresión de sublimación directa, cuando en realidad, si la temperatura es lo suficientemente alta, también se forma líquido.
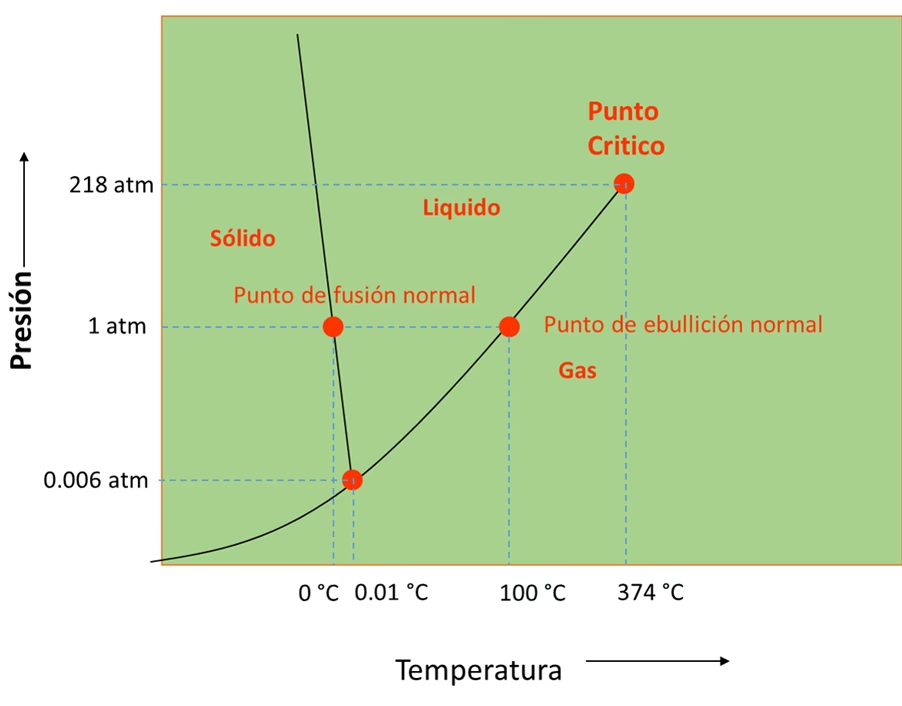
Entendiendo el Diagrama de Fases del Yodo
Un diagrama de fases es una herramienta indispensable para comprender el comportamiento de una sustancia bajo diferentes condiciones de presión y temperatura. Para el yodo, este diagrama nos revela:
- Regiones de Fase: El diagrama se divide en tres regiones principales: sólido (a bajas temperaturas y altas presiones), líquido (a temperaturas intermedias y presiones moderadas) y gas (a altas temperaturas y bajas presiones).
- Líneas de Equilibrio: Las líneas que separan estas regiones representan las condiciones de presión y temperatura en las que dos fases coexisten en equilibrio.
- La línea sólido-líquido (curva de fusión) indica el punto de fusión/congelación.
- La línea líquido-gas (curva de vaporización) indica el punto de ebullición/condensación.
- La línea sólido-gas (curva de sublimación) indica el punto de sublimación/deposición.
- Punto Triple: Es el punto donde las tres líneas se encuentran, representando la única combinación de temperatura y presión donde las tres fases coexisten. Para el yodo, este punto es crucial porque su presión (12.1 kPa) es significativamente menor que la presión atmosférica normal (101.3 kPa). Esto significa que, a presión atmosférica normal, el yodo siempre pasará por la fase líquida al calentarse.
- Punto Crítico: Es el punto más allá del cual las fases líquida y gaseosa se vuelven indistinguibles, formando un fluido supercrítico. Para el yodo, el punto crítico se encuentra a 546 °C y 11,700 kPa.
Una observación interesante en el diagrama de fases del yodo es la pendiente de la línea sólido-líquido. A diferencia del agua, donde esta línea tiene una pendiente negativa (lo que explica por qué el hielo flota y por qué el hielo se funde bajo presión), la línea sólido-líquido del yodo tiene una pendiente positiva. Esto indica que el yodo sólido es más denso que el yodo líquido, un comportamiento típico para la mayoría de las sustancias y consistente con el principio de Le Châtelier: un aumento de presión favorecerá la fase de menor volumen, que en este caso es el sólido.
Condiciones Ideales vs. Realidad Experimental
La confusión sobre la sublimación del yodo también radica en la diferencia entre las condiciones ideales descritas por un diagrama de fases y las condiciones de un experimento de laboratorio real. Un diagrama de fases es válido para una sustancia química pura, en un sistema cerrado y bajo condiciones de equilibrio con temperatura y presión uniformes en todo el sistema.
Sin embargo, el experimento de calentar yodo en un vaso de precipitados abierto no cumple estas condiciones:
- Sistema Abierto: El vaso de precipitados no está sellado, lo que permite que el yodo vaporizado escape y que el aire ambiente interactúe con el sistema.
- No Es una Sustancia Única: El sistema contiene yodo y aire (nitrógeno, oxígeno, argón, etc.), lo que lo convierte en una mezcla de componentes, no una sustancia pura aislada.
- No Está en Equilibrio: La temperatura no es uniforme en todo el vaso. La parte inferior, en contacto con la fuente de calor, estará más caliente que la superior, y la evaporación constante del yodo impide un equilibrio estable.
En un sistema abierto como este, incluso si la temperatura es inferior al punto de fusión, el yodo sólido puede evaporarse lentamente porque su vapor puede difundirse en el aire. Es similar a cómo un cubito de hielo se "evapora" lentamente en un congelador (se sublima) a temperaturas por debajo de su punto de fusión, debido a que su vapor de agua se difunde en el aire más seco del congelador. La alta intensidad del color del vapor de yodo hace que este proceso sea muy visible, lo que contribuye a la confusión.
Importancia del Punto Triple en la Ciencia y la Metrología
Más allá de las curiosidades del yodo, el concepto de punto triple tiene una profunda importancia científica y práctica, especialmente en el campo de la metrología, la ciencia de la medición. Debido a que el punto triple es un punto fijo y altamente reproducible para una sustancia pura, se utiliza como un estándar fundamental para la calibración de termómetros de alta precisión.
La Escala Internacional de Temperatura de 1990 (ITS-90) define varios de sus puntos fijos basándose en los puntos triples de sustancias puras como el hidrógeno, el neón, el oxígeno, el argón, el mercurio y el agua. Las "celdas de punto triple" son dispositivos especialmente diseñados que contienen una sustancia de altísima pureza (a menudo 99.9999% pura) y se utilizan para crear un entorno donde la sustancia se mantiene precisamente en su punto triple. Esto proporciona una temperatura de referencia extremadamente estable y precisa para calibrar instrumentos de medición de temperatura, garantizando la uniformidad y exactitud de las mediciones en todo el mundo.
Tabla 1: Puntos Triples Seleccionados
| Sustancia | Temperatura (°C) | Presión (kPa) |
|---|---|---|
| Yodo (I₂) | 113.5 | 12.1 |
| Agua (H₂O) | 0.0098 | 0.61173 |
| Dióxido de Carbono (CO₂) | -56.6 | 517 |
| Argón (Ar) | -189.34 | 68.9 |
Tabla 2: Presión de Vapor del Yodo Sólido (Ejemplo)
Aunque el yodo no se sublima completamente a presión atmosférica, su presión de vapor es lo suficientemente alta como para que el vapor sea visible a temperaturas relativamente bajas, lo que contribuye a la confusión sobre su sublimación.

| Temperatura (°C) | Presión de Vapor (kPa) |
|---|---|
| 20 | 0.027 |
| 40 | 0.14 |
| 60 | 0.57 |
| 80 | 2.0 |
| 100 | 6.1 |
| 114.15 (cerca del p. triple) | 12.0 |
Preguntas Frecuentes sobre el Yodo y sus Fases
Aclaramos algunas de las dudas más comunes sobre el comportamiento del yodo y el concepto de punto triple.
¿El yodo se sublima siempre?
No, el yodo no se sublima siempre. Si bien es cierto que el yodo sólido tiene una presión de vapor apreciable a temperatura ambiente y puede parecer que se sublima en un sistema abierto (debido a que su vapor se difunde en el aire), a presión atmosférica normal (101.3 kPa), el yodo se funde antes de hervir. Su punto de fusión a 1 atm es de 113.7 °C, y su punto de ebullición es de 184.3 °C. La sublimación directa significativa, donde la fase líquida no aparece en absoluto, solo ocurre a presiones por debajo de su punto triple (12.1 kPa).
¿Por qué es importante el punto triple en la ciencia?
El punto triple es de vital importancia en la ciencia, especialmente en la metrología y la termometría. Debido a que el punto triple es una condición de temperatura y presión única y reproducible para una sustancia pura, se utiliza como un punto de referencia fijo para la calibración de termómetros de alta precisión. La escala de temperatura internacional (ITS-90) define varios de sus puntos fijos utilizando celdas de punto triple de diversas sustancias, lo que garantiza mediciones de temperatura precisas y consistentes a nivel global.
¿Cómo se logra el punto triple en el laboratorio?
Lograr el punto triple de una sustancia en el laboratorio requiere un control extremadamente preciso de la temperatura y la presión, así como una alta pureza de la sustancia. Se utilizan dispositivos especiales llamados "celdas de punto triple", que son recipientes sellados que contienen la sustancia pura. Se manipulan cuidadosamente las condiciones para que las tres fases coexistan en equilibrio. Para el agua, por ejemplo, se logra a 0.0098 °C y 611.73 Pa, condiciones que requieren un vacío considerable y un aislamiento térmico meticuloso para mantener la estabilidad.
¿Es el yodo líquido a temperatura ambiente?
No, el yodo no es líquido a temperatura ambiente. A 20 °C y presión atmosférica, el yodo se encuentra en estado sólido. Para que el yodo sea líquido, la temperatura debe estar entre su punto de fusión (113.7 °C a 1 atm) y su punto de ebullición (184.3 °C a 1 atm), y la presión debe ser superior a su punto triple (12.1 kPa).
Conclusión: La Ciencia en Constante Reevaluación
La historia del yodo y su aparente sublimación es un poderoso recordatorio de la importancia de la observación crítica y la reevaluación constante en la ciencia. Lo que parece obvio a primera vista puede ocultar una complejidad fascinante que solo se revela con un análisis más profundo y la comprensión de los principios fundamentales de la termodinámica. El yodo no solo nos enseña sobre los estados de la materia y los diagramas de fases, sino también sobre la humildad científica y la disposición a corregir nuestras propias concepciones erróneas. La próxima vez que vea yodo en el laboratorio, recuerde que hay más de lo que el ojo puede ver, y que el líquido púrpura es tan real como el vapor que lo acompaña.
Si quieres conocer otros artículos parecidos a El Punto Triple del Yodo: Desvelando un Misterio puedes visitar la categoría Química.

