28/05/2023
En el vasto universo de la química, la forma en que los átomos se unen para formar moléculas es un campo de estudio fascinante y fundamental. Más allá de la simple conexión, la distribución de la carga eléctrica dentro de estas uniones determina muchas de las propiedades físicas y químicas de las sustancias que nos rodean. Aquí es donde entra en juego un concepto crucial: el momento dipolar. Comprender cómo se calcula y qué factores lo influyen no solo es esencial para estudiantes y profesionales, sino que también nos permite apreciar la complejidad y elegancia del mundo molecular.
- Comprendiendo la Polaridad Molecular: La Clave del Momento Dipolar
- El Cálculo del Momento Dipolar: Una Guía Detallada
- La Relación Directa: Momento Dipolar y Electronegatividad
- Observando el Momento Dipolar en Acción
- Preguntas Frecuentes sobre el Momento Dipolar
- Tabla Comparativa: Ejemplos de Moléculas y su Polaridad
Comprendiendo la Polaridad Molecular: La Clave del Momento Dipolar
¿Qué es un Momento Dipolar?
Un momento dipolar es una medida de la polaridad de una molécula. Surge cuando hay una separación de cargas eléctricas, es decir, cuando un extremo de la molécula posee una carga parcial positiva (δ+) y el otro una carga parcial negativa (δ-). Esta separación de carga puede ocurrir tanto en enlaces iónicos como en enlaces covalentes, aunque es más notable y relevante para la polaridad molecular en los enlaces covalentes polares.
Imagina dos cargas eléctricas, de signo opuesto y magnitud igual, separadas por una distancia. Esta configuración establece lo que se conoce como un dipolo eléctrico. El tamaño de este dipolo se cuantifica mediante su momento dipolar (μ). En los enlaces químicos, esta separación de carga se debe a la distribución desigual de los electrones compartidos entre los átomos. Cuando los electrones no se comparten por igual, el átomo más electronegativo atrae con mayor fuerza los electrones hacia sí, generando una densidad electrónica mayor a su alrededor y, por ende, una carga parcial negativa. El átomo menos electronegativo, por su parte, adquiere una carga parcial positiva.
Electronegatividad: El Motor de la Polaridad
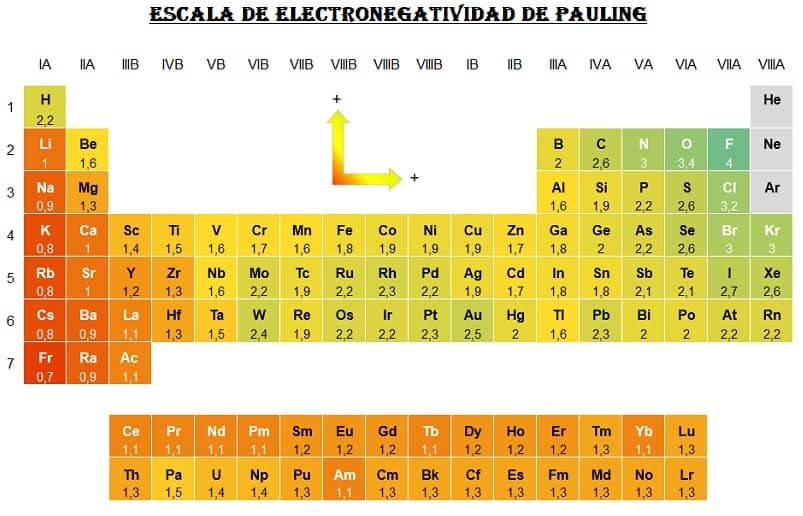
El concepto de electronegatividad es fundamental para entender por qué se forman los momentos dipolares. La electronegatividad es la capacidad de un átomo en una molécula para atraer hacia sí los electrones de un enlace químico. En 1936, Linus Pauling propuso una escala que permite estimar la electronegatividad de los átomos, la cual sigue siendo la base de nuestra comprensión actual.
La diferencia en la electronegatividad entre dos átomos unidos es el factor principal que determina la polaridad de un enlace:
- Enlaces covalentes puros: Ocurren cuando la diferencia de electronegatividad es nula o muy pequeña (generalmente entre 0 y 0.4). Los electrones se comparten por igual. Un ejemplo clásico son las moléculas homonucleares como H₂ o Cl₂.
- Enlaces covalentes polares: Se forman cuando hay una diferencia significativa de electronegatividad (generalmente entre 0.4 y 1.7). Los electrones se comparten de forma desigual, creando cargas parciales (δ+ y δ-). El agua (H₂O) o el cloruro de hidrógeno (HCl) son ejemplos.
- Enlaces iónicos: Surgen de una gran diferencia de electronegatividad (mayor a 1.7), donde hay una transferencia casi completa de electrones de un átomo a otro, formando iones. El fluoruro de potasio (KF) es un ejemplo de un enlace casi puramente iónico.
La mayoría de los enlaces químicos en la naturaleza no son puramente covalentes ni puramente iónicos; son enlaces covalentes polares con un carácter parcial iónico y parcial covalente. Cuanto mayor sea la diferencia de electronegatividad, mayor será el momento dipolar del enlace y, por lo tanto, mayor será su carácter iónico.
El Cálculo del Momento Dipolar: Una Guía Detallada
La Fórmula Fundamental del Momento Dipolar
El momento dipolar (μ) de un sistema de dos cargas separadas se calcula mediante una fórmula relativamente sencilla:
μ = Q × r
Donde:
- Q es la magnitud de la carga (en Coulombs, C). En el caso de los enlaces, representa la magnitud de las cargas parciales.
- r es la distancia de separación entre las cargas (en metros, m). Para un enlace, esta es la longitud del enlace.
El momento dipolar es una magnitud vectorial, lo que significa que tiene tanto magnitud como dirección. Por convención en química, el vector del momento dipolar apunta desde la carga parcial positiva (δ+) hacia la carga parcial negativa (δ-).
Unidades del Momento Dipolar
La unidad del momento dipolar en el Sistema Internacional (SI) es el Coulomb-metro (C·m). Sin embargo, en química, es mucho más común expresar el momento dipolar en unidades de Debye (D), en honor al físico y químico Peter Debye. La equivalencia entre estas unidades es:
1 Debye (D) = 3.336 × 10-30 C·m
Ejemplos Prácticos de Cálculo
Consideremos un sistema simple de un solo electrón y un protón separados por una distancia fija. La carga elemental de un protón (o electrón) es 1.60 × 10-19 C.
Ejemplo 1: Protón y electrón separados por 100 pm
Si la distancia (r) es de 100 pm (picómetros), lo que equivale a 1.00 × 10-10 m:
μ = (1.60 × 10-19 C) × (1.00 × 10-10 m)
μ = 1.60 × 10-29 C·m
Para convertir esto a Debye:
μ = (1.60 × 10-29 C·m) × (1 D / 3.336 × 10-30 C·m)
μ ≈ 4.80 D
Este valor de 4.80 D es una referencia clave, ya que representa el momento dipolar de una carga pura de +1 y -1 separada por 100 pm.
Ejemplo 2: Variación del momento dipolar con la distancia
El momento dipolar aumenta linealmente con la distancia de separación de las cargas:
- Si el protón y el electrón están separados por 120 pm: μ = (120/100) × 4.80 D = 5.76 D
- Si el protón y el electrón están separados por 150 pm: μ = (150/100) × 4.80 D = 7.20 D
- Si el protón y el electrón están separados por 200 pm: μ = (200/100) × 4.80 D = 9.60 D
Estos ejemplos ilustran cómo la distancia de enlace también es un factor determinante en la magnitud del momento dipolar.
Momento Dipolar Molecular: Más Allá de un Solo Enlace
En moléculas con más de dos átomos, el momento dipolar total de la molécula (momento dipolar molecular neto) es la suma vectorial de los momentos dipolares individuales de cada enlace. Aquí es donde la geometría molecular juega un papel crucial.
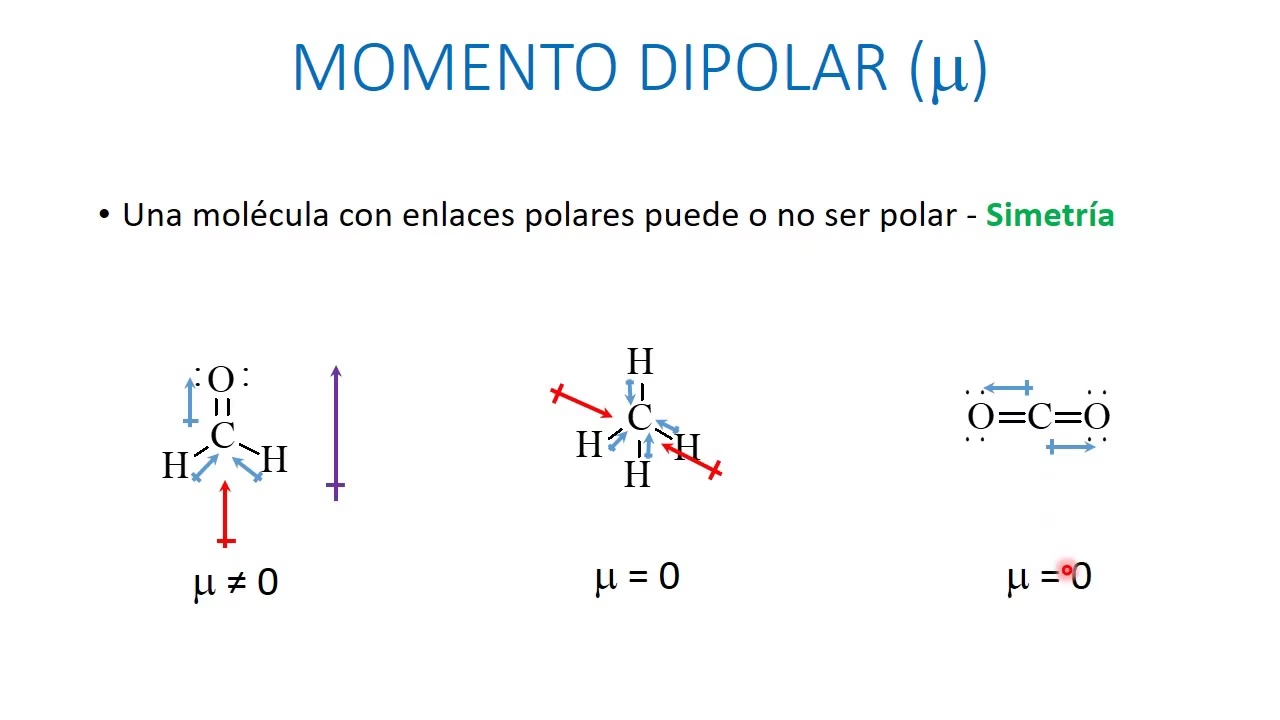
Una molécula puede tener enlaces polares, pero no ser polar en su conjunto si los momentos dipolares de los enlaces se cancelan debido a la simetría de la molécula. Consideremos dos ejemplos comunes:
- Agua (H₂O): El oxígeno es más electronegativo que el hidrógeno, creando dos momentos dipolares de enlace O-H que apuntan hacia el oxígeno. Debido a la presencia de pares de electrones no enlazantes en el oxígeno, la geometría del agua es angular (en forma de V). Esta geometría asimétrica hace que los vectores de los momentos dipolares de los enlaces no se cancelen, resultando en un momento dipolar molecular neto significativo, lo que convierte al agua en una molécula altamente polar.
- Dióxido de Carbono (CO₂): El oxígeno es más electronegativo que el carbono, creando dos momentos dipolares de enlace C=O que apuntan hacia los átomos de oxígeno. Sin embargo, la molécula de CO₂ tiene una geometría lineal. Los dos momentos dipolares de enlace son de igual magnitud pero apuntan en direcciones opuestas, cancelándose mutuamente. Por lo tanto, el CO₂ es una molécula no polar, a pesar de tener enlaces polares.
- Tetracloruro de Carbono (CCl₄): Similar al CO₂, los enlaces C-Cl son polares, con el cloro siendo más electronegativo. Pero la geometría tetraédrica de la molécula de CCl₄ es perfectamente simétrica. Los cuatro momentos dipolares de enlace se cancelan vectorialmente, haciendo que el CCl₄ sea una molécula no polar.
La dirección del vector del momento dipolar molecular neto, al igual que los dipolos de enlace individuales, se representa con una flecha que va desde el centro de carga positiva hacia el centro de carga negativa.
La Relación Directa: Momento Dipolar y Electronegatividad
¿Es el Momento Dipolar Proporcional a la Electronegatividad?
Sí, el momento dipolar es directamente proporcional a la diferencia de electronegatividad entre los átomos que forman un enlace, siempre y cuando la distancia de enlace se mantenga relativamente constante. Cuanto mayor sea la diferencia de electronegatividad, mayor será la magnitud de las cargas parciales (Q) y, en consecuencia, mayor será el momento dipolar del enlace.
Esta relación es fundamental porque la diferencia de electronegatividad nos proporciona una forma de cuantificar el grado de polaridad de un enlace y, por extensión (considerando la geometría), el grado de polaridad de una molécula. Un momento dipolar grande indica una mayor separación de carga, lo que implica un mayor carácter iónico en el enlace.
Impacto en las Propiedades de las Moléculas
La polaridad de una molécula, determinada por su momento dipolar, influye significativamente en sus propiedades físicas y químicas:
- Puntos de Fusión y Ebullición: Las moléculas polares tienen fuerzas intermoleculares más fuertes (como las interacciones dipolo-dipolo y los puentes de hidrógeno), lo que requiere más energía para separarlas y, por lo tanto, tienen puntos de fusión y ebullición más altos que las moléculas no polares de masa molecular similar.
- Solubilidad: La regla general es "lo similar disuelve lo similar". Las sustancias polares tienden a disolverse en solventes polares (como el agua), mientras que las sustancias no polares se disuelven mejor en solventes no polares.
- Interacciones Biológicas: La polaridad es crucial para muchas funciones biológicas, como la estructura de las proteínas, la función de las membranas celulares y la capacidad de las enzimas para interactuar con sus sustratos.
Observando el Momento Dipolar en Acción
¿Cómo se Mide el Momento Dipolar?
La presencia y magnitud de un momento dipolar molecular pueden medirse experimentalmente. Un método común implica colocar la sustancia entre placas cargadas de un capacitor. Las moléculas polares tienden a alinearse con el campo eléctrico, lo que aumenta la capacidad de almacenamiento de carga de las placas (capacitancia del sistema). A partir de este cambio en la capacitancia, se puede determinar el momento dipolar.
En general, las moléculas polares exhiben una clara tendencia a alinearse en presencia de un campo eléctrico. Además, se alinean unas con otras y con iones, lo que explica muchas de sus propiedades en soluciones y estados condensados.
La Importancia de la Polaridad en la Vida Cotidiana
El agua es el ejemplo más elocuente de la importancia del momento dipolar. Su alta polaridad es responsable de su capacidad como solvente universal, su elevada tensión superficial y su calor específico, propiedades que son vitales para la vida en la Tierra. Sin la polaridad del agua, muchos de los procesos biológicos y químicos que conocemos simplemente no serían posibles.
Preguntas Frecuentes sobre el Momento Dipolar
¿Qué significa un momento dipolar alto?
Un momento dipolar alto indica una gran separación de carga dentro de la molécula, lo que significa que es altamente polar. Esto se traduce en fuerzas intermoleculares más fuertes, como mayores puntos de ebullición y una mayor solubilidad en solventes polares.
¿Puede una molécula tener enlaces polares pero ser no polar en general?
Sí, absolutamente. Esto ocurre cuando la geometría molecular de la molécula es simétrica, lo que hace que los momentos dipolares de los enlaces individuales se cancelen vectorialmente. Ejemplos clásicos son el dióxido de carbono (CO₂) y el tetracloruro de carbono (CCl₄).
¿Cuál es la unidad del momento dipolar?
La unidad más común para el momento dipolar en química es el Debye (D). En el Sistema Internacional (SI), la unidad es el Coulomb-metro (C·m).
¿Cómo afecta la geometría molecular al momento dipolar?
La geometría molecular es crucial porque determina cómo se suman los momentos dipolares de los enlaces individuales. Una molécula puede tener enlaces muy polares, pero si su geometría es simétrica (como lineal, trigonal plana o tetraédrica sin sustituyentes diferentes), los momentos dipolares pueden cancelarse, resultando en una molécula no polar. Por el contrario, una geometría asimétrica (como angular o piramidal) generalmente resultará en una molécula polar si los enlaces son polares.
Tabla Comparativa: Ejemplos de Moléculas y su Polaridad
Para ilustrar mejor cómo la geometría y la polaridad de los enlaces influyen en el momento dipolar molecular, observemos algunos ejemplos comunes:
| Molécula | Fórmula | Geometría Molecular | Polaridad de Enlaces | Momento Dipolar Molecular (D) | Comentarios |
|---|---|---|---|---|---|
| Agua | H₂O | Angular | Polar (O-H) | 1.85 | Los dipolos de enlace no se cancelan debido a la geometría. |
| Dióxido de Carbono | CO₂ | Lineal | Polar (C=O) | 0 | Los dipolos de enlace se cancelan por simetría. |
| Cloruro de Hidrógeno | HCl | Lineal | Polar (H-Cl) | 1.11 | Molécula diatómica, por ende, su polaridad de enlace es su polaridad molecular. |
| Tetracloruro de Carbono | CCl₄ | Tetraédrica | Polar (C-Cl) | 0 | Los dipolos de enlace se cancelan por simetría. |
| Amoníaco | NH₃ | Piramidal trigonal | Polar (N-H) | 1.47 | La presencia del par solitario y la geometría causan un momento dipolar neto. |
En resumen, el momento dipolar es una herramienta poderosa que nos permite cuantificar la polaridad de los enlaces y moléculas. Su cálculo, aunque sencillo en su forma básica (Q × r), se vuelve más complejo al considerar la geometría molecular y la suma vectorial de los dipolos de enlace. La electronegatividad es el pilar de este concepto, dictando la distribución desigual de los electrones y, por ende, la formación de cargas parciales. Comprender el momento dipolar no solo es esencial para la química teórica, sino que también nos proporciona una visión profunda de las propiedades de las sustancias que son vitales para la vida y la tecnología moderna.
Si quieres conocer otros artículos parecidos a ¿Cómo se Calcula el Momento Dipolar? puedes visitar la categoría Química.