21/03/2023
En el vasto y fascinante mundo de la química, las soluciones juegan un papel protagónico. Desde la preparación de medicamentos hasta los procesos industriales más complejos, entender cómo se componen y se cuantifican las soluciones es fundamental. Una solución es una mezcla homogénea de dos o más sustancias, donde la sustancia en menor proporción se denomina soluto y la que está en mayor proporción es el solvente. Pero, ¿cómo cuantificamos la cantidad de soluto en una solución? Y, ¿cómo preparamos soluciones con una concentración conocida y precisa? Este artículo se adentrará en las metodologías y cálculos necesarios para determinar la masa de una solución y para preparar soluciones estándar, herramientas indispensables para cualquier químico.

La capacidad de calcular con precisión la masa de una solución y de preparar soluciones con una concentración específica no es solo una habilidad técnica, sino una base crucial para la reproducibilidad y fiabilidad de los experimentos y análisis químicos. Sin esta base, los resultados podrían ser erróneos, llevando a conclusiones incorrectas y potencialmente peligrosas. Por ello, es imperativo comprender los conceptos subyacentes y aplicar las fórmulas correctas con una meticulosidad inquebrantable.
- Entendiendo la Masa de una Solución y el Porcentaje en Masa
- ¿Qué son las Soluciones Estándar y por qué son Cruciales?
- Cálculos Fundamentales para Soluciones Estándar
- Tabla Comparativa de Métodos de Preparación
- Consejos para una Preparación de Soluciones Estándar Precisa y Exacta
- Preguntas Frecuentes sobre el Cálculo de Masas y Soluciones
- ¿Cuál es la diferencia entre soluto y solvente?
- ¿Por qué es importante usar gramos para el cálculo del porcentaje en masa?
- ¿Qué es un estándar primario y por qué es tan importante?
- ¿Se puede usar cualquier sustancia para hacer una solución estándar?
- ¿Cuál es la diferencia entre exactitud y precisión?
- Conclusión
Entendiendo la Masa de una Solución y el Porcentaje en Masa
Antes de sumergirnos en los cálculos, es vital comprender que la masa total de una solución es simplemente la suma de las masas de sus componentes: el soluto y el solvente. Esta es una aplicación directa de la ley de conservación de la masa. Por lo tanto, si conocemos la masa del soluto y la masa del solvente, la masa de la solución se calcula mediante la siguiente relación sencilla:
Masa de la Solución = Masa del Soluto + Masa del Solvente
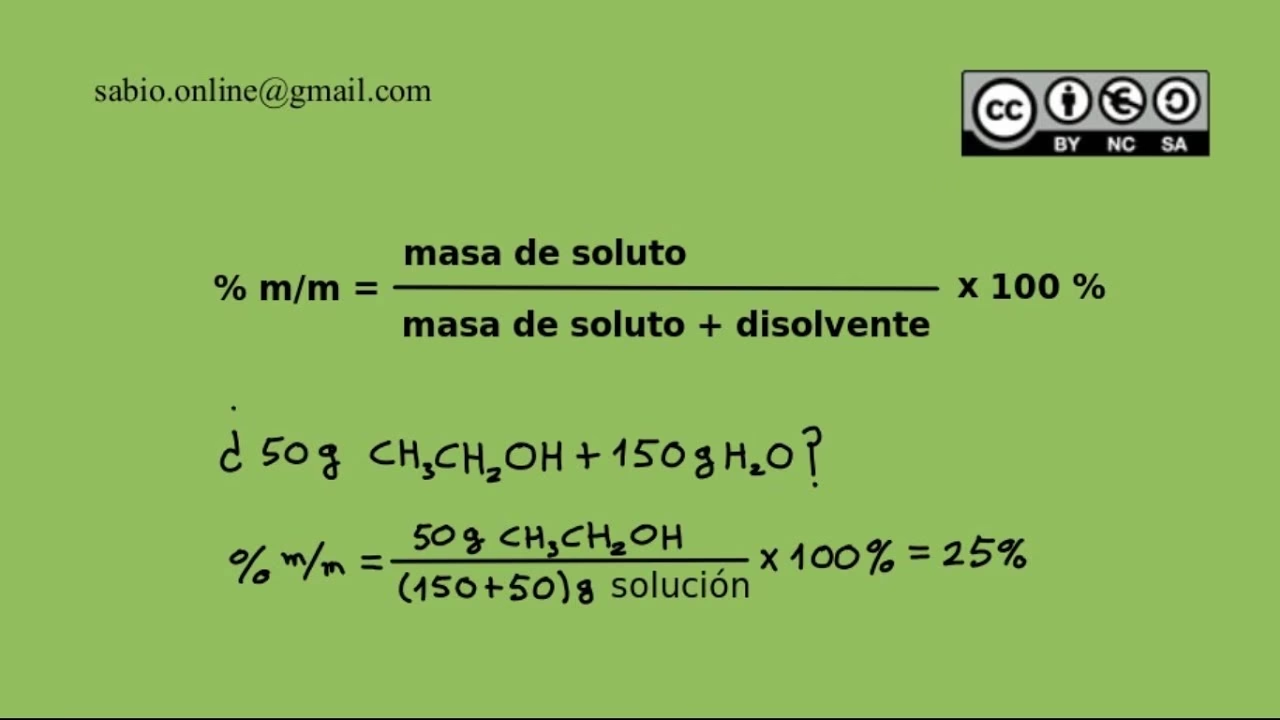
Sin embargo, en química, a menudo necesitamos expresar la cantidad de soluto en relación con la masa total de la solución. Aquí es donde entra en juego el concepto de porcentaje en masa (% m/m), una de las formas más comunes de expresar la concentración de una solución, especialmente útil para soluciones en fase sólida y líquida. El porcentaje en masa se define como la relación entre la masa del soluto y la masa total de la solución, multiplicada por 100 para expresarla como un porcentaje.
Porcentaje en Masa (% m/m) = (Masa del Soluto / Masa de la Solución) × 100
Alternativamente, si se conoce la masa del soluto y la masa del solvente, la fórmula puede expresarse como:
Porcentaje en Masa (% m/m) = (Masa del Soluto / (Masa del Soluto + Masa del Solvente)) × 100
Consideraciones Importantes para el Cálculo del Porcentaje en Masa
Para asegurar la precisión en estos cálculos, todas las masas deben expresarse en la misma unidad, preferiblemente gramos (g). Si las cantidades se proporcionan en otras unidades (miligramos, kilogramos, etc.), es crucial convertirlas a gramos antes de aplicar las fórmulas. Durante el cálculo, las unidades de masa se cancelan, dejando el resultado como un porcentaje. Para diferenciar el porcentaje en masa de otras concentraciones porcentuales (como el porcentaje en volumen), se utiliza la unidad "% m/m". Además, la fórmula química del soluto se suele escribir como una unidad secundaria para mayor claridad, por ejemplo, "% m/m LiC2H3O2".
Es importante recordar que los porcentajes en masa no son cantidades exactas y, por lo tanto, sus valores deben reportarse utilizando el número correcto de cifras significativas. El factor "100" en la fórmula es un número exacto y no afecta la cantidad de cifras significativas del resultado final.
Ejemplo Práctico de Cálculo de Porcentaje en Masa
Consideremos un ejemplo: Calcular el porcentaje en masa de una solución de 235 gramos que se prepara disolviendo 96 gramos de acetato de litio (LiC2H3O2) en agua.
Primero, identificamos el soluto y el solvente. El acetato de litio es el soluto (la sustancia que se disuelve) y el agua es el solvente. La masa total de la solución ya nos es dada (235 g).
Aplicamos la primera fórmula de porcentaje en masa:
Porcentaje en Masa = (Masa del Soluto / Masa de la Solución) × 100
Porcentaje en Masa = (96 g LiC2H3O2 / 235 g solución) × 100
Porcentaje en Masa = 0.408516... × 100
Porcentaje en Masa = 40.8516... % m/m LiC2H3O2
Ajustando a las cifras significativas correctas (96 g tiene dos, 235 g tiene tres, por lo que el resultado debe tener dos o tres, dependiendo de la interpretación estricta de la división, pero comúnmente se redondea a la menor cantidad de cifras significativas del numerador si la división es la operación final que domina las cifras significativas):
Porcentaje en Masa ≈ 41 % m/m LiC2H3O2
¿Qué son las Soluciones Estándar y por qué son Cruciales?
Más allá de simplemente conocer la concentración en masa, en química analítica es frecuente la necesidad de trabajar con soluciones de concentración extremadamente precisa y conocida. Estas son las soluciones estándar. Una solución estándar se prepara a partir de una sustancia de referencia (un estándar primario) con una pureza muy alta, disolviéndola en un volumen específico de solvente para lograr una concentración deseada y exacta. Son el pilar de muchos métodos analíticos, como las titulaciones, donde se utilizan para determinar la cantidad de una sustancia en una solución de concentración desconocida.
La concentración de una solución estándar se expresa típicamente en moles por litro (mol/L), también conocida como molaridad (M). Otras unidades, como moles por decímetro cúbico o kilomoles por metro cúbico, también pueden ser utilizadas. La elección de la unidad depende a menudo de la escala del trabajo, desde pequeños volúmenes de laboratorio hasta grandes procesos de fabricación química.
Las soluciones estándar no solo sirven como herramientas de comparación, sino también como reactivos y soluciones tampón. Se preparan a partir de estándares primarios, que son sustancias con características muy específicas: alta pureza, estabilidad, no higroscópicas (no absorben humedad del aire) y un alto peso molecular. No todas las sustancias pueden calificarse como un estándar primario, lo que subraya la importancia de seleccionarlos cuidadosamente.
Cálculos Fundamentales para Soluciones Estándar
La preparación de una solución estándar implica cálculos basados en la proporcionalidad de las concentraciones. El parámetro principal a calcular es la concentración del soluto en proporción al solvente, generalmente expresada en molaridad (M). La molaridad es la relación entre el número de moles de un soluto y el volumen de la solución en litros.
Molaridad (M) = Moles de Soluto / Volumen de Solución (L)
Para calcular la masa necesaria de un soluto para preparar una solución estándar, primero necesitamos conocer su masa molar. La masa molar de una sustancia se calcula sumando los pesos atómicos de todos los átomos presentes en su fórmula química, valores que se encuentran en la tabla periódica. Por ejemplo, para el sacarosa (C12H22O11):
- Carbono (C): 12 átomos × 12.01 g/mol = 144.12 g/mol
- Hidrógeno (H): 22 átomos × 1.01 g/mol = 22.22 g/mol
- Oxígeno (O): 11 átomos × 16.00 g/mol = 176.00 g/mol
Masa Molar de Sacarosa = 144.12 + 22.22 + 176.00 = 342.34 g/mol
Si quisiéramos preparar 1 litro de una solución 0.5 M de sacarosa, necesitaríamos disolver 0.5 moles de sacarosa. Dado que 1 mol de sacarosa son 342.34 gramos, 0.5 moles serían:
Masa de Sacarosa = 0.5 mol × 342.34 g/mol = 171.17 g
Así, 171.17 gramos de sacarosa disueltos en agua hasta un volumen total de 1 litro nos darían una solución 0.5 M.
Métodos de Preparación de Soluciones Estándar
Existen dos métodos principales para preparar soluciones estándar, cada uno con sus propias aplicaciones y consideraciones:
- El método de dilución.
- El método de pesaje.
Ambos métodos requieren cálculos precisos y una manipulación cuidadosa para asegurar la exactitud de la concentración final.
Método de Dilución de Soluciones Estándar
El método de dilución se utiliza cuando se tiene una solución concentrada (solución madre o stock) de la que se desea obtener una solución menos concentrada (diluida). Este método se basa en el principio de que la cantidad de soluto permanece constante antes y después de la dilución. La fórmula clave para la dilución es:
M1V1 = M2V2
Donde:
M1: Molaridad deseada de la solución diluida.V1: Volumen deseado de la solución diluida.M2: Molaridad de la solución concentrada (stock).V2: Volumen de la solución concentrada que se necesita tomar.
Proceso del Método de Dilución:
- Establecer la concentración molar deseada (M1) y el volumen deseado (V1) de la solución diluida.
- Calcular el volumen de la solución madre (V2) necesario utilizando la fórmula
M1V1 = M2V2. - Medir cuidadosamente el volumen calculado de la solución madre, preferiblemente con una pipeta volumétrica para mayor precisión.
- Transferir el volumen medido a un matraz aforado (o de volumen conocido) y añadir el solvente (generalmente agua destilada) hasta la marca de aforo, asegurándose de mezclar bien la solución.
Ejemplo de Dilución de Ácido:
Supongamos que queremos preparar 50 mL de una solución de ácido sulfúrico (H2SO4) 1.0 M a partir de una solución concentrada de 2.0 M.
Aplicando la fórmula:
M1V1 = M2V2
(1.0 M)(50 mL) = (2.0 M)V2
Despejando V2:
V2 = (1.0 M × 50 mL) / 2.0 M
V2 = 50 mL M / 2.0 M
V2 = 25 mL de solución madre
Esto significa que se deben tomar 25 mL de la solución de ácido sulfúrico 2.0 M y diluirlos con agua hasta un volumen final de 50 mL para obtener la solución deseada de 1.0 M.
Método de Preparación por Pesaje
El método de pesaje es el más directo para preparar soluciones estándar, especialmente cuando se parte de un sólido puro. Implica pesar con precisión una cantidad específica del soluto y disolverlo en un volumen conocido de solvente. Este método es fundamental para la preparación de soluciones a partir de estándares primarios.
Proceso del Método de Pesaje:
- Establecer la molaridad deseada de la solución a preparar y el volumen final.
- Determinar la masa molar del soluto en gramos/mol a partir de su fórmula química y los pesos atómicos.
- Calcular la masa exacta del soluto necesaria para alcanzar la concentración y volumen deseados.
- Pesar con precisión esa cantidad de sustancia pura utilizando una balanza analítica.
- Disolver la sustancia pesada en una cantidad menor de solvente (agua destilada, por ejemplo) en un vaso de precipitados.
- Transferir la solución cuantitativamente a un matraz aforado del volumen deseado.
- Enjuagar el vaso de precipitados varias veces con pequeñas porciones de solvente y añadir los enjuagues al matraz aforado para asegurar que todo el soluto se transfiera.
- Añadir solvente adicional al matraz aforado hasta la marca de aforo, asegurándose de que el menisco coincida con la marca. Tapar y mezclar bien invirtiendo el matraz varias veces.
Ejemplo de Solución Base:
Para preparar una solución 1 M de hidróxido de sodio (NaOH), necesitamos calcular su masa molar:
- Sodio (Na): 22.99 g/mol
- Oxígeno (O): 16.00 g/mol
- Hidrógeno (H): 1.01 g/mol
Masa Molar de NaOH = 22.99 + 16.00 + 1.01 = 40.00 g/mol
Si queremos preparar 1 litro de una solución 1 M de NaOH, necesitaríamos disolver 40.00 gramos de NaOH en agua hasta un volumen total de 1 litro.
Tabla Comparativa de Métodos de Preparación
Para facilitar la comprensión, presentamos una tabla comparativa entre los dos métodos principales:
| Característica | Método de Dilución | Método de Pesaje |
|---|---|---|
| Punto de partida | Solución concentrada (stock) | Sustancia pura (sólido o líquido) |
| Principio | Conservación de moles (M1V1=M2V2) | Disolución de una masa conocida en un volumen conocido |
| Uso principal | Preparar soluciones de menor concentración a partir de una más concentrada | Preparar soluciones estándar primarias |
| Equipamiento clave | Pipetas volumétricas, matraces aforados | Balanza analítica, matraces aforados |
| Complejidad | Relativamente simple una vez dominada la fórmula | Requiere pesaje muy preciso y cuidado en la transferencia |
Consejos para una Preparación de Soluciones Estándar Precisa y Exacta
La precisión y la exactitud son pilares en la química analítica. La exactitud se refiere a cuán cerca está una medición del valor real, mientras que la precisión se refiere a la reproducibilidad de las mediciones. Para garantizar resultados confiables en la preparación de soluciones:
- Calibración de Instrumentos: Asegúrate de que todas las balanzas (analíticas) y el material volumétrico (pipetas, matraces aforados) estén correctamente calibrados. La verificación regular con pesos de referencia es crucial.
- Material de Vidrio Limpio: La presencia de impurezas o residuos en el material de vidrio puede alterar significativamente la concentración de la solución. Lava y enjuaga a fondo todo el material con agua destilada o desionizada antes de usarlo.
- Uso Correcto de Material Volumétrico: Los matraces aforados están diseñados para contener un volumen exacto a una temperatura específica. Asegúrate de que el menisco esté alineado con la marca de aforo. Las pipetas volumétricas ofrecen la mayor precisión para transferir volúmenes.
- Control de Temperatura: La densidad de las soluciones y el volumen del material de vidrio pueden variar con la temperatura. Prepara las soluciones a una temperatura ambiente constante y cercana a la de calibración del material.
- Evitar Contaminación: Utiliza siempre reactivos de alta pureza. Evita el contacto de los reactivos con las manos o superficies no limpias. Cierra los recipientes inmediatamente después de usarlos.
- Disolución Completa: Asegúrate de que el soluto esté completamente disuelto antes de aforar la solución. Agita suavemente o usa un agitador magnético si es necesario.
- Cifras Significativas: Reporta siempre tus resultados con el número correcto de cifras significativas, reflejando la precisión de tus mediciones.
Equipamiento Esencial
Para la preparación de soluciones estándar, el equipamiento básico incluye:
- Balanza analítica: Para pesar masas con alta precisión (hasta 0.0001 g).
- Matraces aforados: Para preparar soluciones con un volumen exacto y preciso. Vienen en diferentes volúmenes (e.g., 25 mL, 50 mL, 100 mL, 250 mL, 500 mL, 1000 mL).
- Pipetas volumétricas: Para transferir volúmenes exactos de líquidos, especialmente en el método de dilución.
- Vasos de precipitados o Erlenmeyers: Para disolver el soluto inicialmente antes de transferirlo al matraz aforado.
- Frascos lavadores: Con agua destilada o desionizada para enjuagar el material y aforar.
Preguntas Frecuentes sobre el Cálculo de Masas y Soluciones
¿Cuál es la diferencia entre soluto y solvente?
El soluto es la sustancia que se disuelve en otra, y está presente en menor cantidad. El solvente es la sustancia que disuelve al soluto y está presente en mayor cantidad. Por ejemplo, en una solución de sal en agua, la sal es el soluto y el agua es el solvente.
¿Por qué es importante usar gramos para el cálculo del porcentaje en masa?
Si bien se puede usar cualquier unidad de masa siempre que sea consistente (la misma unidad para el soluto y la solución), el gramo es la unidad estándar en química y facilita la comparación de resultados y la interoperabilidad con otras fórmulas y datos químicos.
¿Qué es un estándar primario y por qué es tan importante?
Un estándar primario es una sustancia química de alta pureza, estabilidad, no higroscópica y con un peso molecular elevado, utilizada para preparar soluciones estándar con una concentración conocida de forma extremadamente precisa. Su importancia radica en que su pureza y estabilidad permiten una preparación directa y fiable de soluciones de referencia, que a su vez se utilizan para estandarizar otras soluciones de menor pureza.
¿Se puede usar cualquier sustancia para hacer una solución estándar?
No. Para que una solución sea considerada "estándar" y utilizada en análisis de alta precisión, la sustancia de la que se parte debe ser un estándar primario o debe ser estandarizada frente a un estándar primario. Las sustancias que no cumplen con los criterios de un estándar primario (por ejemplo, son higroscópicas o inestables) no son adecuadas para la preparación directa de soluciones estándar.
¿Cuál es la diferencia entre exactitud y precisión?
Exactitud se refiere a cuán cerca está una medición del valor verdadero o aceptado. Precisión se refiere a cuán cerca están entre sí una serie de mediciones repetidas, independientemente de si están cerca del valor verdadero.
Conclusión
El cálculo de la masa de una solución y la preparación de soluciones estándar son habilidades fundamentales en el laboratorio de química. Ya sea que estemos determinando el porcentaje en masa de un componente o preparando una solución con una molaridad exacta para una titulación, la meticulosidad y el entendimiento de los principios subyacentes son clave. La aplicación correcta de fórmulas, el uso adecuado del material de laboratorio y el control de las condiciones experimentales no solo garantizan la validez de los resultados, sino que también fortalecen la base para futuras exploraciones y descubrimientos en el campo de la química. Dominar estas técnicas es un paso esencial para convertirse en un químico competente y confiable.
Si quieres conocer otros artículos parecidos a Dominando el Cálculo de Masas y Soluciones puedes visitar la categoría Química.

