04/09/2022
En el vasto universo de la química, cada elemento posee una identidad única, definida no solo por el número de protones en su núcleo, sino también por una característica fundamental que influye en todas sus reacciones y propiedades: su masa atómica. Sin embargo, a diferencia de lo que podríamos pensar intuitivamente, la masa de un átomo de un elemento no es siempre un número entero simple. Esto se debe a la existencia de variedades de un mismo elemento, conocidas como isótopos, que difieren en su número de neutrones y, por lo tanto, en su masa. Para abordar esta complejidad, los químicos utilizan un concepto crucial: la masa atómica relativa. Este valor no representa la masa de un solo átomo, sino un promedio ponderado que considera la contribución de cada isótopo en una muestra natural. Comprender cómo se calcula esta masa es fundamental para cualquier persona que desee adentrarse en el fascinante mundo de la química, desde cálculos estequiométricos hasta la interpretación de fenómenos naturales.

- ¿Qué es la Masa Atómica Relativa?
- Isótopos: La Clave de la Variedad Atómica
- La Abundancia Natural: Un Factor Crucial
- Paso a Paso: Cómo Calcular la Masa Atómica Relativa
- ¿Por qué es un Promedio Ponderado?
- Aplicaciones de la Masa Atómica Relativa
- Herramientas para la Determinación: Espectrometría de Masas
- Preguntas Frecuentes (FAQs)
- ¿Es la masa atómica relativa siempre un número entero?
- ¿Cuál es la diferencia entre masa atómica y masa atómica relativa?
- ¿Por qué se usa el carbono-12 como referencia para la unidad de masa atómica?
- ¿Pueden cambiar las abundancias naturales de los isótopos?
- ¿Por qué es importante conocer la masa atómica relativa?
- Conclusión
¿Qué es la Masa Atómica Relativa?
La masa atómica relativa, también conocida como peso atómico, es el promedio ponderado de las masas de los isótopos de un elemento, tal como se encuentran en la naturaleza. Se expresa en unidades de masa atómica (uma o u), que se define como 1/12 de la masa de un átomo de carbono-12. Es importante destacar que es una masa relativa porque se compara con un estándar, no es una masa absoluta en gramos. Este promedio es vital porque la mayoría de los elementos existen en la naturaleza como una mezcla de dos o más isótopos, cada uno con una masa ligeramente diferente y una cierta proporción de presencia.
Imagínese que tiene una bolsa llena de canicas de diferentes tamaños, pero todas son del mismo 'tipo' de canica. Si quiere saber el 'peso promedio' de una canica de esa bolsa, no solo sumaría los pesos de todas y dividiría por el número total, sino que también consideraría cuántas canicas de cada tamaño hay. Si las canicas más grandes son mucho más abundantes, el promedio se inclinará hacia el peso de esas canicas más grandes. De manera similar, la masa atómica relativa refleja las proporciones en que cada isótopo contribuye al peso total del elemento.
Isótopos: La Clave de la Variedad Atómica
Antes de sumergirnos en el cálculo, es esencial comprender qué son los isótopos. Los isótopos son átomos del mismo elemento (es decir, tienen el mismo número de protones) pero con un número diferente de neutrones en su núcleo. Esta diferencia en el número de neutrones implica una diferencia en su masa atómica. Por ejemplo, el elemento hidrógeno tiene tres isótopos principales:
- Protio (Hidrógeno-1): 1 protón, 0 neutrones (masa ≈ 1 u)
- Deuterio (Hidrógeno-2): 1 protón, 1 neutrón (masa ≈ 2 u)
- Tritio (Hidrógeno-3): 1 protón, 2 neutrones (masa ≈ 3 u)
Aunque químicamente se comportan de manera muy similar debido a que tienen el mismo número de electrones y, por ende, la misma configuración electrónica, sus masas son distintas. La existencia de estos isótopos es la razón principal por la que la masa atómica relativa de un elemento rara vez es un número entero, ya que es un promedio de las masas de estas diferentes 'versiones' del átomo.
La Abundancia Natural: Un Factor Crucial
Para calcular la masa atómica relativa, no solo necesitamos conocer las masas de cada isótopo, sino también su abundancia natural. La abundancia natural de un isótopo es el porcentaje de ese isótopo que se encuentra en una muestra típica y natural del elemento. Por ejemplo, el cloro tiene dos isótopos estables significativos: cloro-35 y cloro-37. En la naturaleza, aproximadamente el 75.77% del cloro es cloro-35, mientras que el 24.23% restante es cloro-37.
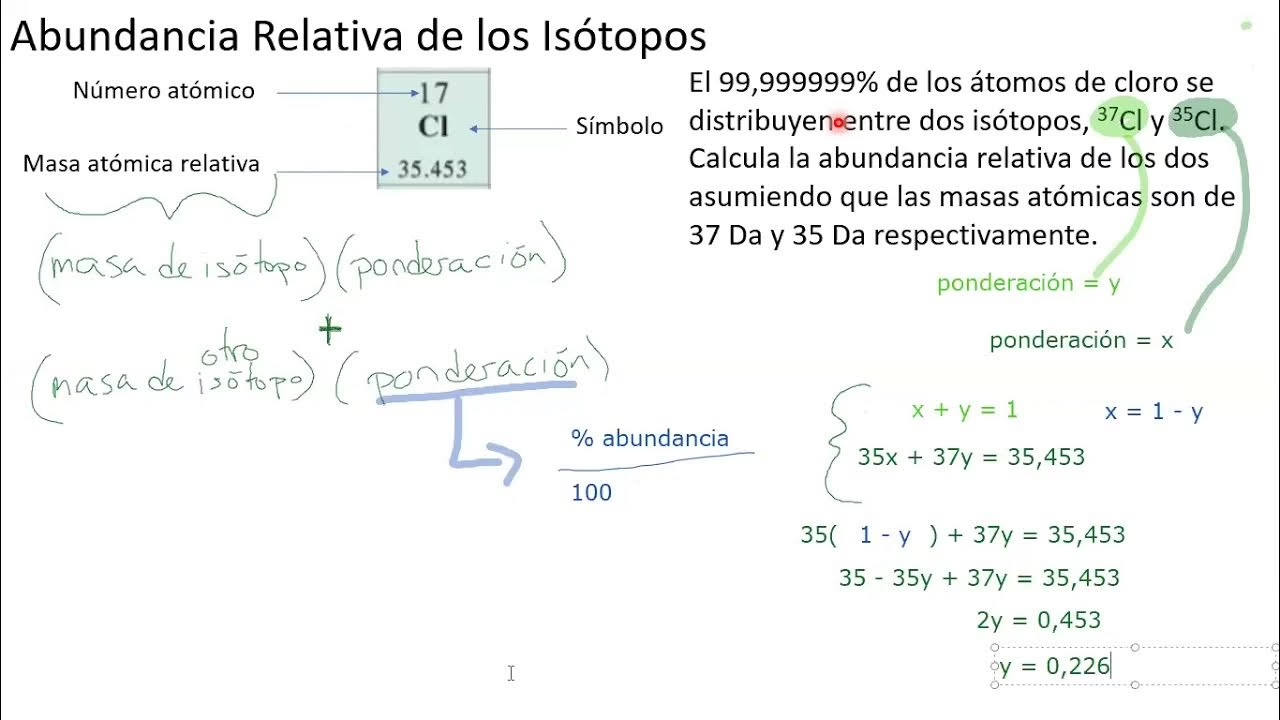
Estas abundancias se determinan experimentalmente utilizando técnicas avanzadas como la espectrometría de masas. Son valores empíricos que reflejan la composición isotópica de los elementos tal como se encuentran en la Tierra. Sin la información de la abundancia natural, simplemente promediar las masas de los isótopos daría un resultado incorrecto, ya que no consideraría el hecho de que algunos isótopos son mucho más comunes que otros.
Paso a Paso: Cómo Calcular la Masa Atómica Relativa
El cálculo de la masa atómica relativa es un proceso sistemático que implica cuatro pasos clave:
- Identificar los isótopos y sus masas: Para el elemento en cuestión, se deben conocer las masas atómicas exactas de cada uno de sus isótopos relevantes. Estas masas suelen proporcionarse en unidades de masa atómica (u).
- Determinar la abundancia natural de cada isótopo: Se necesita el porcentaje de cada isótopo presente en una muestra natural. Es crucial convertir estos porcentajes a su forma decimal dividiéndolos por 100 (por ejemplo, 75.77% se convierte en 0.7577).
- Multiplicar la masa de cada isótopo por su abundancia natural: Para cada isótopo, se multiplica su masa atómica por su abundancia expresada como un decimal. Este producto representa la contribución de ese isótopo a la masa atómica relativa total.
- Sumar los resultados: La suma de todas las contribuciones individuales de cada isótopo dará como resultado la masa atómica relativa del elemento.
Ejemplo Práctico: El Cloro
Vamos a aplicar estos pasos al elemento cloro, que tiene dos isótopos principales:
- Cloro-35: Masa atómica = 34.96885 u; Abundancia natural = 75.77%
- Cloro-37: Masa atómica = 36.96590 u; Abundancia natural = 24.23%
Cálculo:
Paso 1 y 2: Tenemos las masas y las abundancias (convertidas a decimales: 0.7577 y 0.2423).
Paso 3: Calcular la contribución de cada isótopo:
- Contribución de Cloro-35 = 34.96885 u * 0.7577 = 26.495 u
- Contribución de Cloro-37 = 36.96590 u * 0.2423 = 8.956 u
Paso 4: Sumar las contribuciones:
- Masa Atómica Relativa del Cloro = 26.495 u + 8.956 u = 35.451 u
Este resultado, 35.451 u, es el valor que encontramos en la tabla periódica para la masa atómica del cloro. Es un promedio, lo que explica por qué no es exactamente 35 ni 37.
Tabla Comparativa de Contribuciones
Para visualizar mejor el proceso, podemos organizar los datos en una tabla:
| Isótopo | Masa Isotópica (u) | Abundancia Natural (%) | Abundancia (decimal) | Contribución al Total (Masa x Abundancia) |
|---|---|---|---|---|
| Cloro-35 | 34.96885 | 75.77 | 0.7577 | 26.495 |
| Cloro-37 | 36.96590 | 24.23 | 0.2423 | 8.956 |
| Masa Atómica Relativa Total | 35.451 u | |||
¿Por qué es un Promedio Ponderado?
La clave para entender la masa atómica relativa reside en el término "promedio ponderado". Un promedio simple (sumar todos los valores y dividir por el número de valores) sería engañoso porque no todos los isótopos son igual de comunes. Si el cloro-35 y el cloro-37 fueran igualmente abundantes (50% cada uno), entonces la masa atómica relativa sería simplemente el promedio de sus masas (aproximadamente 36 u). Sin embargo, dado que el cloro-35 es mucho más abundante, su contribución al promedio es significativamente mayor, 'tirando' el promedio hacia su propia masa.

Piense en un curso universitario donde la calificación final se calcula a partir de exámenes y tareas. Si los exámenes valen el 70% de la nota final y las tareas el 30%, su calificación en los exámenes 'pesa' más en el promedio final. De manera similar, la abundancia natural de un isótopo actúa como su 'peso' o 'ponderación' en el cálculo de la masa atómica relativa. Este enfoque asegura que el valor resultante represente con precisión la masa de un átomo promedio del elemento tal como lo encontraríamos en la naturaleza.
Aplicaciones de la Masa Atómica Relativa
La masa atómica relativa no es solo un concepto teórico; tiene numerosas aplicaciones prácticas en la química y más allá:
- Estequiometría: Es fundamental para realizar cálculos de estequiometría, que implican las relaciones cuantitativas entre reactivos y productos en reacciones químicas. Permite convertir entre masa y moles de una sustancia.
- Determinación de Fórmulas Moleculares: Al conocer las masas atómicas relativas de los elementos, se pueden determinar las fórmulas empíricas y moleculares de compuestos.
- Análisis Químico: En laboratorios, se utiliza para calibrar instrumentos y para el análisis cuantitativo de muestras, por ejemplo, en la determinación de la pureza de sustancias o la composición de mezclas.
- Industria: Es crucial en procesos industriales donde la precisión de la masa de los reactivos es vital, como en la fabricación de productos farmacéuticos, materiales y alimentos.
- Investigación Científica: Permite a los científicos comprender mejor la composición de materiales, desde minerales hasta muestras biológicas, y estudiar fenómenos como el fraccionamiento isotópico.
Herramientas para la Determinación: Espectrometría de Masas
La información sobre las masas isotópicas y sus abundancias naturales no se obtiene con una simple balanza. La técnica analítica principal utilizada para determinar estos valores es la espectrometría de masas. Este método separa los iones de diferentes masas (o más precisamente, diferentes relaciones masa-carga) y los detecta. Al analizar el patrón de iones y sus intensidades, un espectrómetro de masas puede:
- Identificar los diferentes isótopos de un elemento.
- Determinar la masa precisa de cada isótopo.
- Medir la abundancia relativa de cada isótopo en la muestra.
La espectrometría de masas es una herramienta increíblemente poderosa y sensible, capaz de proporcionar datos con una precisión asombrosa, lo que es esencial para los cálculos de la masa atómica relativa que vemos en las tablas periódicas.
Preguntas Frecuentes (FAQs)
¿Es la masa atómica relativa siempre un número entero?
No, la masa atómica relativa rara vez es un número entero. Esto se debe a que es un promedio ponderado de las masas de los isótopos de un elemento, y las masas de los isótopos individuales (aunque cercanas a números enteros) no suelen ser exactas, y sus abundancias naturales varían. La única excepción es el carbono-12, que por definición tiene una masa atómica de exactamente 12 u, y es el estándar de referencia.
¿Cuál es la diferencia entre masa atómica y masa atómica relativa?
La 'masa atómica' (o masa isotópica) se refiere a la masa de un átomo individual de un isótopo específico (por ejemplo, la masa de un átomo de Cloro-35). La 'masa atómica relativa' (o peso atómico) es el promedio ponderado de las masas de todos los isótopos naturales de un elemento, considerando sus abundancias.

¿Por qué se usa el carbono-12 como referencia para la unidad de masa atómica?
El carbono-12 se eligió como estándar de referencia en la década de 1960 por varias razones. Es un isótopo muy común y estable, y su uso permitió una mayor precisión y coherencia en las mediciones de masa atómica en comparación con los estándares anteriores (como el oxígeno o el hidrógeno). Definir 1 u como 1/12 de la masa de un átomo de carbono-12 proporciona una escala de masa universalmente aceptada.
¿Pueden cambiar las abundancias naturales de los isótopos?
Para la mayoría de los propósitos químicos generales, se considera que las abundancias naturales de los isótopos son constantes y universales. Sin embargo, en un análisis muy detallado (como en la geoquímica isotópica o el análisis de materiales extraterrestres), pueden observarse variaciones ligeras en las proporciones isotópicas debido a procesos nucleares, geológicos o biológicos específicos que pueden fraccionar los isótopos.
¿Por qué es importante conocer la masa atómica relativa?
Es crucial para realizar cálculos precisos en química. Sin ella, no podríamos determinar la cantidad de sustancia (moles) a partir de una masa dada, lo que es fundamental para predecir rendimientos de reacción, formular soluciones con concentraciones específicas, y en general, para cualquier aplicación cuantitativa de la química.
Conclusión
La masa atómica relativa es un concepto fundamental que cierra la brecha entre el mundo microscópico de los átomos individuales y el mundo macroscópico de las cantidades que podemos medir en el laboratorio. Al comprender la existencia de los isótopos y el papel crítico de su abundancia natural, podemos calcular con precisión el 'peso promedio' de un elemento. Este valor no solo es una pieza de información vital que encontramos en cada tabla periódica, sino que es la base para una infinidad de cálculos y aplicaciones en la química, la física, la biología y la industria. Dominar este concepto es dar un paso significativo hacia una comprensión más profunda y precisa de la materia que nos rodea y las transformaciones que experimenta.
Si quieres conocer otros artículos parecidos a Calculando la Masa Atómica Relativa: Guía Completa puedes visitar la categoría Química.
