18/11/2023
Desde los albores de la filosofía, la humanidad se ha preguntado de qué está hecha la materia. Demócrito, un pensador griego antiguo, propuso que todo estaba compuesto por partículas indivisibles a las que llamó átomos, del griego 'átomon', que significa 'indivisible'. Aunque su intuición fue asombrosa, hoy sabemos que los átomos no son tan indivisibles como creía. De hecho, están formados por partículas aún más pequeñas: los protones, neutrones y electrones. Comprender la disposición de estas partículas subatómicas es clave para desentrañar los misterios de la materia y sus propiedades. Este artículo te guiará a través de la compleja, pero fascinante, estructura atómica, desde sus componentes básicos hasta cómo calcularlos y los modelos que han moldeado nuestra comprensión a lo largo de la historia.
- La Estructura Básica del Átomo: Protones, Neutrones y Electrones
- Calculando la Estructura Atómica: El Número Atómico y el Número Másico
- Ejemplos Prácticos de Estructuras Atómicas
- Iones e Isótopos: Variaciones del Átomo
- La Masa Atómica Relativa: Un Promedio Ponderado
- La Distribución de los Electrones en el Átomo
- Cómo Dibujar la Estructura Atómica Paso a Paso
- Propiedades Fundamentales del Átomo
- La Evolución de los Modelos Atómicos: Un Viaje Histórico
- Modelo de Dalton (1803): Las Esferas Indivisibles
- Modelo de Thomson (1897): El Pudín de Pasas
- Modelo de Nagaoka (1904): El Átomo Planetario
- Modelo de Rutherford (1911): El Núcleo Central
- Modelo de Bohr (1913): Las Órbitas Cuantizadas
- Modelo de Sommerfeld (1916): Órbitas Elípticas y Relatividad
- Modelo de Schrödinger (1926): La Nube de Probabilidad
- Modelo de Dirac (1928) y Modelos Posteriores
- Preguntas Frecuentes (FAQ)
La Estructura Básica del Átomo: Protones, Neutrones y Electrones
Todo átomo se compone de una estructura fundamental: un núcleo denso en el centro y una región de capas que orbitan alrededor de este. Dentro de esta estructura, encontramos tres tipos principales de partículas subatómicas, cada una con características únicas que definen el comportamiento del átomo.
Protones: Los Determinantes de la Identidad
Los protones son partículas con carga positiva ubicadas en el núcleo del átomo. Son, sin duda, los más importantes para la identidad de un elemento. El número de protones en un átomo determina su número atómico (Z) y, por ende, a qué elemento pertenece y su posición en la tabla periódica. Aunque diminutos, con una masa real de aproximadamente 1.67 x 10-27 kg, su masa relativa en la escala de carbono-12 se considera 1. Son una parte crucial del núcleo atómico.
Neutrones: Los Estabilizadores Silenciosos
Los neutrones son partículas sin carga eléctrica, es decir, neutras, que también residen en el núcleo junto a los protones. Su número puede variar entre átomos del mismo elemento sin alterar sus propiedades químicas, lo que da origen a los isótopos. Al igual que los protones, tienen una masa relativa de aproximadamente 1 en la escala de carbono-12. Juntos, los protones y neutrones forman lo que se conoce como nucleones, concentrando más del 99.94% de la masa total del átomo en su minúsculo núcleo.
Electrones: Los Orbitadores Energéticos
A diferencia de protones y neutrones, los electrones son partículas con carga negativa que no se encuentran en el núcleo, sino que orbitan alrededor de él en niveles de energía específicos, también conocidos como capas. El número de electrones en un átomo neutro es igual al número de protones, lo que equilibra las cargas y hace que el átomo sea eléctricamente neutro. Los electrones determinan las propiedades químicas y la reactividad de un átomo. Son increíblemente pequeños, con una masa real de 9.11 x 10-31 kg, o una masa relativa de apenas 1/1840 en la escala de carbono-12, lo que los hace casi despreciables en el cálculo de la masa atómica.
La siguiente tabla resume las características clave de estas partículas subatómicas:
| Partícula | Masa Relativa (u) | Carga Relativa | Ubicación en el Átomo |
|---|---|---|---|
| Protón | 1 | +1 | Dentro del núcleo |
| Neutrón | 1 | 0 | Dentro del núcleo |
| Electrón | 1/1840 (o ≈ 0) | -1 | En las capas orbitando el núcleo |
Calculando la Estructura Atómica: El Número Atómico y el Número Másico
Para conocer la estructura atómica de un elemento y el número exacto de cada partícula subatómica, recurrimos a dos valores fundamentales que se encuentran en la tabla periódica: el número atómico y el número másico.
- Número Atómico (Z): Este número representa la cantidad de protones en el núcleo de un átomo. Es el “DNI” del elemento, ya que cada elemento tiene un número atómico único. En un átomo eléctricamente neutro, el número de electrones es igual al número de protones, lo que significa que el número atómico (Z) también nos indica el número de electrones.
- Número Másico (A): Este número es la suma total de protones y neutrones en el núcleo del átomo. Representa la masa total del átomo, ya que la masa de los electrones es insignificante en comparación.
Con estos dos números, podemos calcular fácilmente el número de cada partícula:
- Número de Protones: Igual al número atómico (Z).
- Número de Electrones: Igual al número atómico (Z) en un átomo neutro.
- Número de Neutrones: Se calcula restando el número atómico (Z) del número másico (A). Es decir, Neutrones = A - Z.
Ejemplos Prácticos de Estructuras Atómicas
Veamos cómo aplicar estos principios con algunos ejemplos reales de elementos:
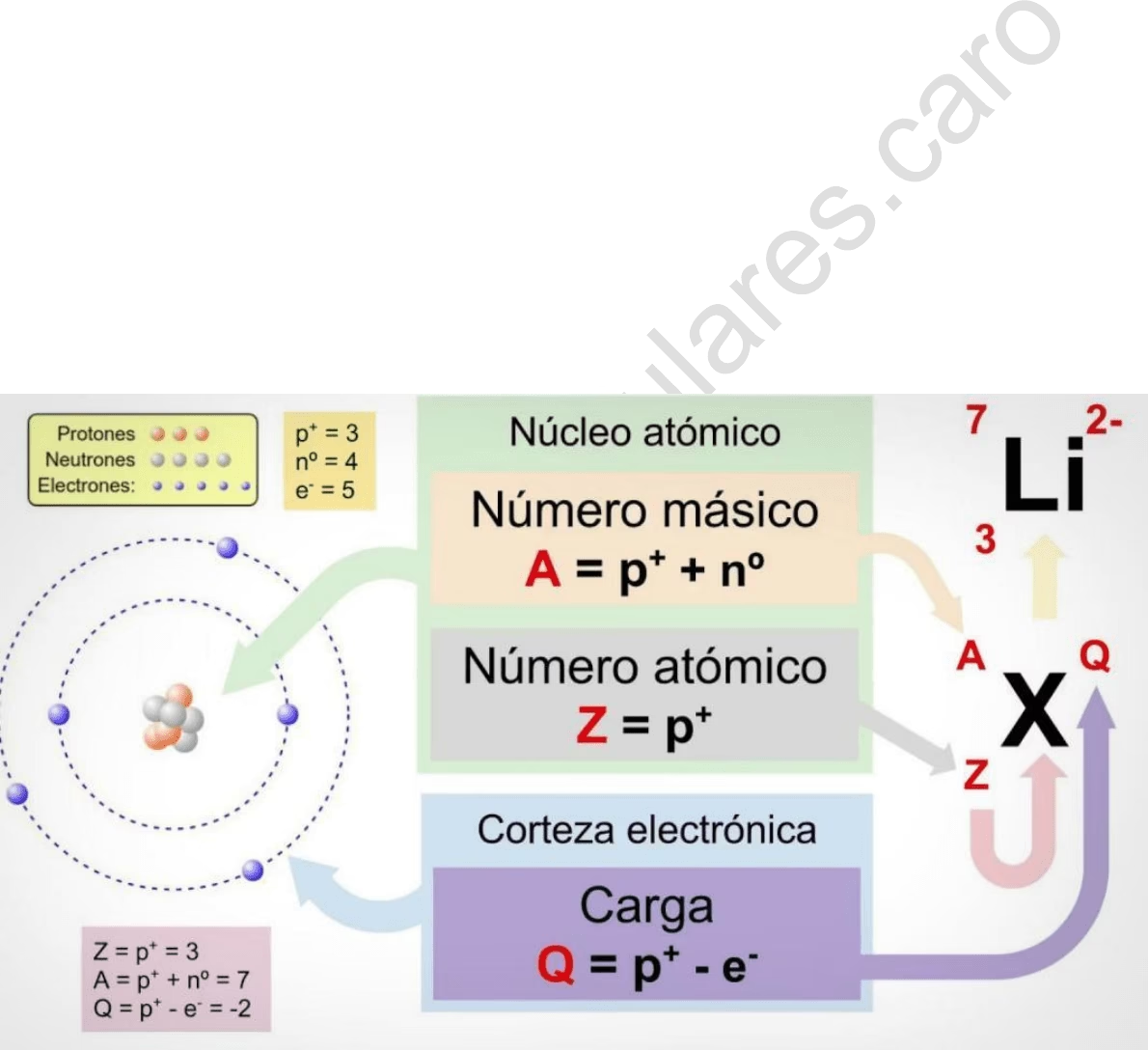
Estructura Atómica del Litio (Li)
El litio (Li) tiene un número atómico (Z) de 3 y un número másico (A) de 7.
- Protones: Z = 3
- Electrones: Z = 3 (para un átomo neutro)
- Neutrones: A - Z = 7 - 3 = 4
Por lo tanto, un átomo neutro de litio tiene 3 protones, 4 neutrones y 3 electrones.
Estructura Atómica del Oxígeno (O)
El oxígeno (O) tiene un número atómico (Z) de 8 y un número másico (A) de 16.
- Protones: Z = 8
- Electrones: Z = 8 (para un átomo neutro)
- Neutrones: A - Z = 16 - 8 = 8
Así, un átomo neutro de oxígeno posee 8 protones, 8 neutrones y 8 electrones.

Estructura Atómica del Carbono (C)
El carbono (C) tiene un número atómico (Z) de 6 y un número másico (A) de 12.
- Protones: Z = 6
- Electrones: Z = 6 (para un átomo neutro)
- Neutrones: A - Z = 12 - 6 = 6
Un átomo neutro de carbono-12 está compuesto por 6 protones, 6 neutrones y 6 electrones.
Iones e Isótopos: Variaciones del Átomo
Aunque hemos hablado de átomos neutros, los átomos pueden sufrir modificaciones que cambian sus propiedades o su masa. Estas variaciones nos llevan a los conceptos de iones e isótopos.
Iones: Átomos con Carga Eléctrica
Un ion es un átomo que ha ganado o perdido electrones, adquiriendo así una carga eléctrica neta. Si un átomo neutro pierde uno o más electrones (partículas negativas), se convierte en un ion con carga positiva, llamado catión. Si, por el contrario, gana uno o más electrones, se convierte en un ion con carga negativa, llamado anión. Los iones tienen propiedades químicas diferentes a las de sus átomos neutros, debido a sus distintas configuraciones electrónicas.
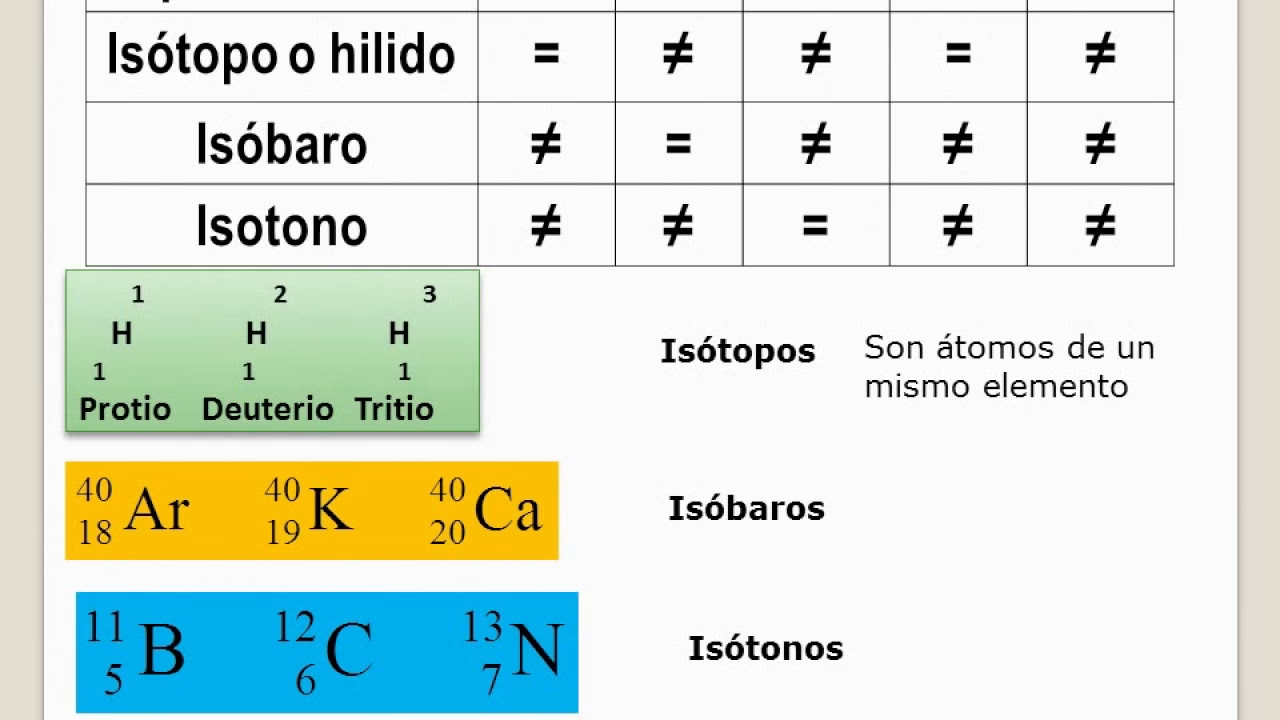
Isótopos: Variaciones en el Número de Neutrones
Los isótopos son átomos del mismo elemento (es decir, con el mismo número de protones y, por tanto, el mismo número atómico) pero con un número diferente de neutrones. Esta diferencia en el número de neutrones implica que tienen una masa diferente. Por ejemplo, el carbono-12 tiene 6 neutrones, mientras que el carbono-14 tiene 8 neutrones, pero ambos son átomos de carbono (con 6 protones). Dado que sus configuraciones electrónicas son las mismas, los isótopos de un elemento tienen propiedades químicas muy similares, aunque sus propiedades nucleares pueden variar significativamente (por ejemplo, algunos isótopos son radiactivos).
La Masa Atómica Relativa: Un Promedio Ponderado
Si observas la tabla periódica, notarás que la masa atómica de muchos elementos no es un número entero. Esto se debe a que la masa atómica que se muestra es en realidad la masa atómica relativa, un promedio ponderado de las masas de todos los isótopos naturales de un elemento, considerando su abundancia en la naturaleza. Se compara con la doceava parte de la masa de un átomo de carbono-12.
Por ejemplo, el cloro tiene dos isótopos principales: cloro-35 (aproximadamente 75% de abundancia) y cloro-37 (aproximadamente 25% de abundancia). Para calcular la masa atómica relativa del cloro, se realiza el siguiente cálculo:
(0.75 * 35 u) + (0.25 * 37 u) = 26.25 u + 9.25 u = 35.5 u
De ahí que la masa atómica relativa del cloro sea 35.5 u. Para medir estas masas con precisión, se utiliza una técnica llamada espectrometría de masas.
La Distribución de los Electrones en el Átomo
Los electrones no orbitan el núcleo de forma aleatoria, sino que se organizan en niveles de energía discretos, conocidos como capas, subcapas y orbitales. Esta organización, o configuración electrónica, es la que determina las propiedades químicas de cada elemento y cómo interactúa con otros átomos.
Los electrones siempre buscarán ocupar los niveles de energía más bajos posibles para alcanzar un estado de mayor estabilidad. Dentro de cada capa, existen subcapas (s, p, d, f), y dentro de cada subcapa, hay orbitales. Cada orbital puede albergar un máximo de dos electrones. Las reglas de llenado, aunque pueden parecer complejas al principio, siguen una lógica precisa para predecir la configuración electrónica.

| Subcapa | Número de Orbitales | Número Máximo de Electrones |
|---|---|---|
| s | 1 | 2 |
| p | 3 | 6 |
| d | 5 | 10 |
| f | 7 | 14 |
Cómo Dibujar la Estructura Atómica Paso a Paso
Visualizar la estructura atómica puede ser de gran ayuda para comprenderla. Aunque es un modelo simplificado, ayuda a entender la disposición de las partículas:
- Encuentra el Número Atómico (Z) y el Número Másico (A): Busca estos valores para el elemento deseado en la tabla periódica.
- Determina el Número de Protones, Neutrones y Electrones:
- Protones = Z
- Electrones = Z (para un átomo neutro)
- Neutrones = A - Z
- Dibuja el Núcleo: Representa el núcleo con un círculo en el centro. Dentro de él, escribe el símbolo del elemento y el número de protones y neutrones (por ejemplo, 'Li: 3p+, 4n').
- Dibuja las Capas Electrónicas: Dibuja círculos concéntricos alrededor del núcleo. Estas representan los niveles de energía o capas de los electrones.
- Llena las Capas de Electrones: Distribuye los electrones comenzando por la capa más interna y avanzando hacia afuera. Recuerda la regla de 2n² para el número máximo de electrones por capa (2 en la primera, 8 en la segunda, 18 en la tercera, etc.), y las subcapas (s, p, d, f) para una distribución más precisa si se requiere.
Propiedades Fundamentales del Átomo
Más allá de su composición, los átomos poseen propiedades físicas que son cruciales para entender su comportamiento en el universo.
Masa Atómica: El Peso de la Materia
Como ya se mencionó, la mayor parte de la masa de un átomo proviene de sus protones y neutrones en el núcleo. La unidad de masa atómica (u) es la escala estándar para medir estas masas, definida como la doceava parte de la masa de un átomo neutro de carbono-12. Un protón y un neutrón libres tienen una masa de aproximadamente 1 u. Esto significa que la masa de un átomo es casi igual a su número másico (A) expresado en unidades de masa atómica. El átomo estable más pesado conocido es el plomo-208, con una masa de 207.98 u. En química, también se utiliza el concepto de mol, donde un mol de átomos de cualquier elemento contiene el mismo número de átomos (6.022 x 1023, el número de Avogadro), y su masa en gramos es numéricamente igual a la masa atómica del elemento en u.
Tamaño Atómico: Un Mundo Microscópico
Los átomos son increíblemente pequeños, con diámetros típicos alrededor de 100 picómetros (10-10 metros). No tienen límites definidos, por lo que su tamaño se estima a través de su 'nube electrónica'. Los métodos para medir el radio atómico (la distancia del núcleo a la capa más externa de electrones) arrojan valores entre 0.5 y 5 Å (ángstroms). Dentro de la tabla periódica, el tamaño de los átomos tiende a disminuir a lo largo de un período (fila) y aumenta drásticamente al comienzo de un nuevo período, a medida que los electrones ocupan niveles de energía más altos.
Niveles de Energía: La Clave de la Reactividad
Los electrones en un átomo ocupan niveles de energía discretos. Un electrón ligado al átomo posee una energía potencial que aumenta con su distancia al núcleo. El nivel con la energía más baja se llama estado fundamental, mientras que los demás son estados excitados. Cuando un electrón se mueve entre estos niveles, absorbe o emite fotones (partículas de luz) con una energía igual a la diferencia entre los niveles. Estas transiciones son la base de los espectros de líneas característicos de cada elemento, que actúan como su 'huella dactilar' atómica. La espectroscopia, que analiza estas líneas, permite determinar la composición de las sustancias. Fenómenos como el efecto fotoeléctrico o el láser se basan en estas interacciones energéticas de los electrones.
La Evolución de los Modelos Atómicos: Un Viaje Histórico
Nuestra comprensión del átomo no surgió de la noche a la mañana, sino que es el resultado de siglos de investigación y el desarrollo de diversos modelos que han intentado explicar su naturaleza.
Modelo de Dalton (1803): Las Esferas Indivisibles
John Dalton propuso el primer modelo atómico con base científica. Imaginó los átomos como diminutas esferas indivisibles e indestructibles. Postuló que los átomos de un mismo elemento eran idénticos en masa y propiedades, pero diferentes de los átomos de otros elementos. También explicó que los compuestos químicos se forman por la combinación de átomos de diferentes elementos en proporciones simples. Aunque revolucionario para su época, este modelo no podía explicar fenómenos como los rayos catódicos o la existencia de partículas subatómicas.
Modelo de Thomson (1897): El Pudín de Pasas
Tras el descubrimiento del electrón por J.J. Thomson, se hizo evidente que el átomo no era indivisible. Thomson propuso un modelo en el que el átomo era una esfera de carga positiva uniformemente distribuida, con electrones negativos incrustados en ella, como pasas en un pudín. Este modelo explicaba la neutralidad del átomo y la formación de iones, pero fallaba en explicar cómo las cargas positivas y negativas permanecían estables sin colapsar.
Modelo de Nagaoka (1904): El Átomo Planetario
Hantarō Nagaoka, disconforme con el modelo de Thomson, propuso un modelo similar a Saturno, con un núcleo central masivo y cargado positivamente, rodeado por electrones que orbitaban como los anillos del planeta. Aunque más cercano a la realidad que el de Thomson, este modelo aún no resolvía el problema de la estabilidad de los electrones en órbita, que según las leyes del electromagnetismo deberían irradiar energía y colapsar.
Modelo de Rutherford (1911): El Núcleo Central
Ernest Rutherford, a través de su famoso experimento de la lámina de oro, descubrió que la mayor parte de la masa del átomo se concentra en un núcleo central muy pequeño y cargado positivamente, mientras que los electrones orbitan a su alrededor en un vasto espacio vacío. Este modelo fue un gran avance, pero, al igual que el de Nagaoka, no podía explicar por qué los electrones no colapsaban sobre el núcleo ni el origen de los espectros atómicos discretos.

Modelo de Bohr (1913): Las Órbitas Cuantizadas
Niels Bohr propuso un modelo que abordaba las deficiencias del modelo de Rutherford, especialmente para el átomo de hidrógeno. Postuló que los electrones solo podían orbitar en ciertas capas o niveles de energía permitidos, sin emitir energía mientras permanecieran en ellas. Los electrones podían saltar entre estas órbitas, absorbiendo o emitiendo cantidades discretas de energía (cuantos o fotones). Este modelo explicó con éxito los espectros de emisión del hidrógeno, pero no funcionaba para átomos más complejos y no justificaba la cuantificación de las órbitas.
Modelo de Sommerfeld (1916): Órbitas Elípticas y Relatividad
Arnold Sommerfeld refinó el modelo de Bohr, introduciendo la idea de que los electrones también podían tener órbitas elípticas, además de las circulares. Esto explicaba la existencia de subniveles energéticos dentro de un mismo nivel principal, observados en los espectros más finos. También incorporó correcciones relativistas para electrones de alta velocidad, acercando el modelo a una descripción más precisa de la realidad, aunque aún no era completo.
Modelo de Schrödinger (1926): La Nube de Probabilidad
Con el advenimiento de la mecánica cuántica, Erwin Schrödinger desarrolló un modelo mucho más sofisticado. Abandonó la idea de órbitas definidas y propuso que los electrones se describen mediante una función de onda. El cuadrado de esta función representa la probabilidad de encontrar un electrón en una región particular del espacio alrededor del núcleo, conocida como orbital. Este modelo es la base de nuestra comprensión actual de la distribución electrónica y es fundamental para la química.
Modelo de Dirac (1928) y Modelos Posteriores
Paul Dirac desarrolló una ecuación relativista para el electrón, que naturalmente incorporaba el concepto de espín del electrón y predijo la existencia de la antimateria. Los modelos posteriores, especialmente a partir de los años 60 y 70, se centraron en la física de partículas, descubriendo que protones y neutrones no son elementales, sino que están formados por partículas aún más pequeñas llamadas quarks, unidas por gluones a través de la fuerza nuclear fuerte. Aunque la complejidad del núcleo atómico es inmensa, los modelos actuales explican satisfactoriamente las propiedades químicas de la materia, que dependen principalmente de la estructura electrónica del átomo.
Preguntas Frecuentes (FAQ)
¿Por qué el número atómico es tan importante?
El número atómico (Z) es crucial porque define la identidad de un elemento. Cada elemento químico tiene un número único de protones, y este número es lo que lo diferencia de cualquier otro elemento. También determina el número de electrones en un átomo neutro, lo que a su vez influye en sus propiedades químicas y cómo reacciona.
¿Pueden cambiar las partículas de un átomo?
Sí, las partículas de un átomo pueden cambiar bajo ciertas condiciones. El número de electrones puede variar, formando iones. El número de neutrones puede cambiar, dando lugar a diferentes isótopos del mismo elemento. El número de protones solo puede cambiar a través de reacciones nucleares (como la desintegración radiactiva o la fisión/fusión nuclear), lo que resulta en la transmutación de un elemento a otro.
¿Qué es la escala de carbono-12?
La escala de carbono-12 es un estándar de referencia para medir las masas atómicas y moleculares relativas. Se define que un átomo de carbono-12 (con 6 protones y 6 neutrones) tiene una masa de exactamente 12 unidades de masa atómica (u). Las masas de todas las demás partículas y átomos se expresan en relación con esta referencia, lo que permite trabajar con números más manejables que las masas reales en kilogramos.
¿Cómo sabemos que los átomos están mayormente vacíos?
El experimento de la lámina de oro de Rutherford fue clave para demostrar esto. Al disparar partículas alfa (núcleos de helio) a una delgada lámina de oro, la mayoría de las partículas pasaron directamente sin desviarse. Solo un pequeño porcentaje se desvió o rebotó. Esto indicaba que la masa y la carga positiva del átomo estaban concentradas en un núcleo minúsculo, dejando la mayor parte del átomo como espacio vacío por donde las partículas alfa podían pasar.
La comprensión de la estructura atómica es un pilar fundamental de la ciencia moderna. Desde la antigua idea de Demócrito hasta los complejos modelos cuánticos actuales, cada avance ha desvelado nuevas capas de complejidad y maravilla en la unidad más básica de la materia. Conocer cómo se organizan los protones, neutrones y electrones, cómo se calculan y cómo estas variaciones dan lugar a iones e isótopos, nos permite comprender no solo la composición de todo lo que nos rodea, sino también predecir su comportamiento y sus interacciones. El átomo, lejos de ser indivisible, es un universo en miniatura que sigue revelando sus secretos a medida que profundizamos en su estudio.
Si quieres conocer otros artículos parecidos a Explorando el Átomo: Su Estructura y Cálculo puedes visitar la categoría Química.