18/03/2023
Las mezclas de líquidos son omnipresentes en la industria y la investigación, pero algunas presentan un comportamiento peculiar: hierven a una temperatura constante y su composición de vapor es idéntica a la del líquido. Estas son las mezclas azeotrópicas, o azeótropos, y su existencia complica los procesos de separación convencionales, como la destilación simple. Comprender y calcular la composición de un azeótropo es fundamental para el diseño de procesos químicos eficientes y para la investigación de propiedades termodinámicas de las soluciones.
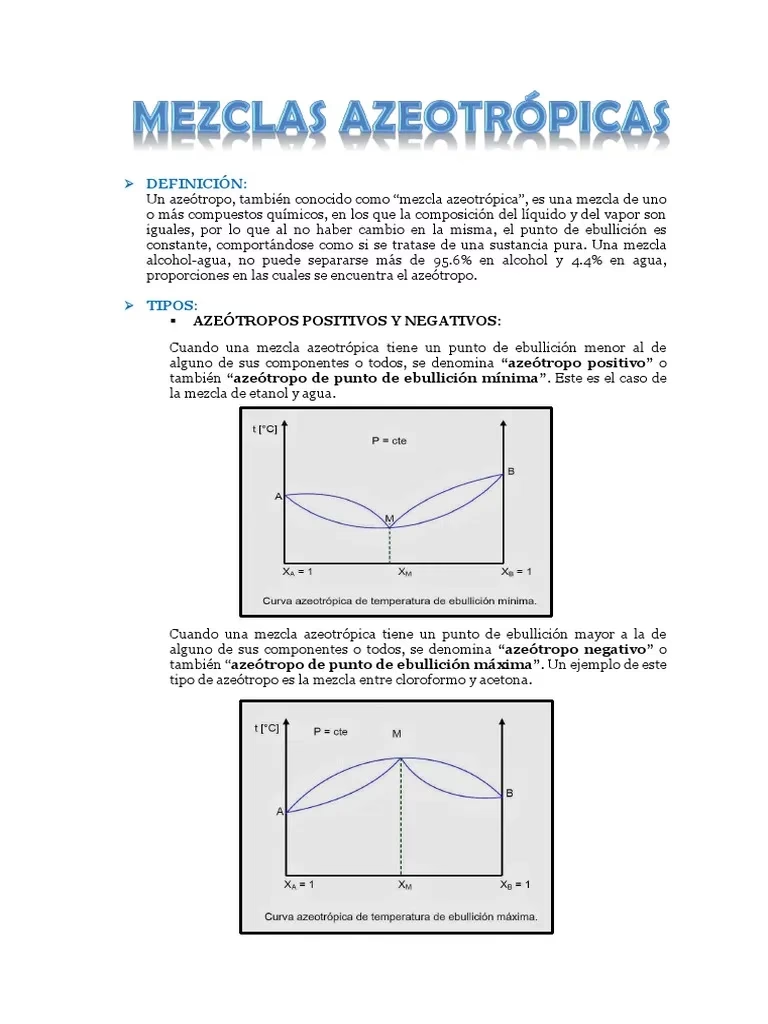
El término azeótropo, que proviene del griego y significa “hervir sin cambio”, describe perfectamente la naturaleza de estas mezclas únicas. A una temperatura y presión dadas, la composición de equilibrio vapor-líquido es idéntica, lo que significa que no es posible separarlos completamente mediante destilación fraccionada.
- ¿Cómo Saber Si en una Mezcla Hay un Azeótropo?
- La Base Termodinámica: La Energía Libre de Gibbs de Mezclado
- Determinación Experimental de la Composición del Azeótropo
- 1. Preparación de Soluciones y Determinación de Fracciones Molares Líquidas (\(\chi_i\))
- 2. Análisis por Cromatografía de Gases (GC)
- 3. Curvas Estándar y Fracciones Molares en Fase Gaseosa (\(y_i\))
- 4. Leyes de Raoult y Dalton: Calculando los Coeficientes de Actividad (\(\gamma_i\))
- 5. Cálculo de la Energía Libre de Gibbs de Mezclado y Propiedades Adicionales
- 6. Identificación de la Composición Azeotrópica
- ¿Por Qué las Mezclas Azeotrópicas No Pueden Separarse por Destilación Simple?
- Destilación Azeotrópica: Una Solución para Separar Azeótropos
- Preguntas Frecuentes (FAQs)
¿Cómo Saber Si en una Mezcla Hay un Azeótropo?
La condición fundamental para la existencia de un azeótropo, ya sea homogéneo o heterogéneo, es que la composición del vapor debe ser igual a la del líquido. Para los azeótropos homogéneos, esto se refiere a la composición de una única fase líquida en equilibrio con su vapor. En el caso de los azeótropos heterogéneos, donde existen dos fases líquidas inmiscibles en equilibrio, la composición global del líquido (considerando ambas fases) es la que coincide con la del vapor.
La Base Termodinámica: La Energía Libre de Gibbs de Mezclado
El corazón del cálculo de la composición de un azeótropo reside en la energía libre de Gibbs de mezclado (∆Gmix). Para una solución binaria, la composición con la mínima energía libre de Gibbs de mezclado es la que corresponde al azeótropo. Esta propiedad termodinámica nos permite entender por qué ciertas mezclas forman azeótropos y dónde se encuentra su punto de equilibrio.
La ecuación general para la energía libre de Gibbs molar de mezclado (∆Gmix) para una solución binaria es:
\[\Delta G_{mix} = RT (\chi_1 \ln a_1 + \chi_2 \ln a_2)\]
Donde R es la constante de los gases ideales, T es la temperatura absoluta, \(\chi_i\) es la fracción molar del componente i-ésimo, \(a_i\) es su actividad, y \(\gamma_i\) es su coeficiente de actividad. Reemplazando la actividad por el producto del coeficiente de actividad y la fracción molar (\(a_i = \gamma_i \chi_i\)), obtenemos:
\[\Delta G_{mix} = RT (\chi_1 \ln \gamma_1 \chi_1 + \chi_2 \ln \gamma_2 \chi_2)\]
Esta ecuación se puede descomponer en dos partes fundamentales:
\[\Delta G_{mix} = RT (\chi_1 \ln \gamma_1 + \chi_2 \ln \gamma_2) + RT (\chi_1 \ln \chi_1 + \chi_2 \ln \chi_2)\]
Aquí, el término \(RT (\chi_1 \ln \chi_1 + \chi_2 \ln \chi_2)\) representa la energía libre de Gibbs molar de mezclado ideal (\(∆G_{mix}^{ideal}\)), que describe el mezclado de componentes sin interacciones específicas. El otro término, \(RT (\chi_1 \ln \gamma_1 + \chi_2 \ln \gamma_2)\), se conoce como la energía libre de Gibbs molar de exceso (\(∆G_{mix}^{excess}\)). Esta parte es crucial, ya que cuantifica las desviaciones del comportamiento ideal y es directamente responsable de la formación de azeótropos.
Además, podemos relacionar la energía libre de Gibbs de mezclado con la entalpía de mezclado (\(∆H_{mix}\)) y la entropía de mezclado (\(∆S_{mix}\)) a través de la ecuación fundamental:
\[\Delta G_{mix} = \Delta H_{mix} - T \Delta S_{mix}\]
Si asumimos que la entropía de mezclado es ideal (válida para moléculas pequeñas de tamaño similar, como en el modelo de solución regular), entonces \(∆S_{mix} = - R (\chi_1 \ln \chi_1 + \chi_2 \ln \chi_2)\). Esto implica que la entalpía de mezclado para una solución real es igual a la energía libre de Gibbs de exceso:
\[\Delta H_{mix} = RT (\chi_1 \ln \gamma_1 + \chi_2 \ln \gamma_2) = \Delta G_{mix}^{excess}\]
Por lo tanto, la ∆Gmix es la propiedad clave que, al ser minimizada respecto a la composición, nos revela la composición del azeótropo.
Determinación Experimental de la Composición del Azeótropo
Para aplicar estos principios termodinámicos en la práctica, necesitamos datos experimentales. Un método común implica el uso de cromatografía de gases (GC) para analizar la composición de fases líquidas y de vapor. Consideremos un ejemplo práctico con soluciones binarias de ciclohexano y etanol:
1. Preparación de Soluciones y Determinación de Fracciones Molares Líquidas (\(\chi_i\))
Se preparan una serie de soluciones binarias con diferentes proporciones de los componentes. Las fracciones molares líquidas (\(\chi_i\)) se calculan a partir de los volúmenes de los componentes, sus densidades y sus masas molares. Es crucial considerar la incertidumbre asociada a cada medición (volumen, densidad, masa molar) y propagar estos errores para obtener una estimación precisa de la incertidumbre en las fracciones molares.
2. Análisis por Cromatografía de Gases (GC)
Las soluciones preparadas se analizan con un cromatógrafo de gases para determinar la altura de los picos (\(h_i\)) de cada componente. A partir de estas alturas, se calculan las funciones de altura de pico (\(H_i\)) para la fase líquida:
\[H_i = \dfrac{h_i}{h_i + h_j}\]
Posteriormente, las soluciones se hierven y los destilados se recogen y se analizan también con el GC bajo las mismas condiciones para obtener las alturas de pico del destilado (\(h'_i\)) y las funciones de altura de pico para el destilado (\(H'_i\)).
3. Curvas Estándar y Fracciones Molares en Fase Gaseosa (\(y_i\))
Para determinar las fracciones molares en la fase gaseosa (\(y_i\)), se construyen curvas estándar. Estas curvas son ajustes polinómicos (por ejemplo, de tercer orden) de las fracciones molares líquidas (\(\chi_i\)) en función de las funciones de altura de pico de la fase líquida (\(H_i\)). Una vez obtenidas estas funciones, se utilizan las funciones de altura de pico de los destilados (\(H'_i\)) como variables independientes para calcular las fracciones molares en el destilado (\(y_i\)), asumiendo que representan la composición de la fase de vapor.
4. Leyes de Raoult y Dalton: Calculando los Coeficientes de Actividad (\(\gamma_i\))
Los coeficientes de actividad (\(\gamma_i\)) son esenciales para caracterizar las desviaciones del comportamiento ideal de una solución. Se pueden derivar de un análisis de la composición del destilado utilizando las leyes de Raoult y Dalton.
- La ley de Raoult modificada para soluciones reales establece que la presión de vapor del componente i-ésimo sobre la solución binaria (\(P_i\)) es: \[P_i = a_i P^o_i = \gamma_i \chi_i P^o_i\] Donde \(P^o_i\) es la presión de vapor del componente puro i-ésimo.
- Si la fase de vapor se asume ideal, la ley de Dalton establece que: \[P_i = y_i P_{total}\] Donde \(y_i\) es la fracción molar del componente i-ésimo en la fase de vapor y \(P_{total}\) es la presión total.
Igualando estas dos expresiones, podemos calcular los coeficientes de actividad:
\[y_i P_{total} = \gamma_i \chi_i P^o_i \implies \gamma_i = \dfrac{y_i P_{total}}{\chi_i P^o_i}\]
Para ello, necesitamos la presión total (\(P_{total}\), que es la presión barométrica corregida) y las presiones de vapor de los componentes puros (\(P^o_i\)) a la temperatura de ebullición de la solución binaria. Las presiones de vapor puras se estiman utilizando la ecuación de Antoine (\(\ln P = A + \dfrac{B}{T}\)) con parámetros A y B conocidos para cada componente.
5. Cálculo de la Energía Libre de Gibbs de Mezclado y Propiedades Adicionales
Con \(\chi_i\), \(y_i\), y \(\gamma_i\) (y sus incertidumbres) ya calculados, se procede a determinar la energía libre de Gibbs de mezclado (\(∆G_{mix}\)) para cada solución utilizando la Ecuación 1. Es crucial propagar las incertidumbres de todas las mediciones para obtener un valor de \(∆G_{mix}\) con su incertidumbre asociada.
Además de \(∆G_{mix}\), se calculan otros términos termodinámicos como \(∆G_{mix}^{ideal}\), \(∆G_{mix}^{excess}\), \(∆S_{mix}\) y \(∆H_{mix}\), junto con sus respectivas incertidumbres.

6. Identificación de la Composición Azeotrópica
Finalmente, se grafica \(∆G_{mix}\) en función de la fracción molar de uno de los componentes (por ejemplo, \(\chi_{ciclohexano}\)). Se ajusta un polinomio (típicamente de tercer orden) a los datos. La composición del azeótropo se encuentra determinando el valor de \(\chi_i\) en el mínimo de esta curva de \(∆G_{mix}\). Matemáticamente, esto implica derivar la función polinómica respecto a \(\chi_i\) e igualar la derivada a cero para encontrar el punto crítico.
Una vez obtenida la composición azeotrópica, se puede estimar la temperatura de ebullición del azeótropo mediante interpolación a partir de los datos experimentales de temperatura de ebullición de las soluciones.
¿Por Qué las Mezclas Azeotrópicas No Pueden Separarse por Destilación Simple?
La razón principal por la que los azeótropos no pueden separarse por destilación simple es que, al hervir, los vapores generados tienen la misma proporción de los componentes que la mezcla líquida sin hervir. Esto significa que la destilación no altera la composición de la mezcla, impidiendo su separación efectiva.
Destilación Azeotrópica: Una Solución para Separar Azeótropos
Dado el desafío que presentan los azeótropos, se han desarrollado técnicas especializadas para su separación. La destilación azeotrópica es uno de los métodos más comunes y efectivos. Se define como el proceso de separar los componentes de una mezcla azeotrópica mediante destilación.
El método más frecuente para romper un azeótropo implica la adición de un agente de separación de material, también conocido como arrastrador o agente de arrastre. Este agente tiene la capacidad de cambiar las interacciones moleculares entre los componentes de la mezcla, alterando los coeficientes de actividad de los componentes y, por ende, la volatilidad relativa de la mezcla en su conjunto. Esto permite que la destilación separe los componentes.
Un ejemplo clásico es la separación de la mezcla de etanol y agua, que forma un azeótropo. Históricamente, el benceno fue un arrastrador común, pero debido a su naturaleza carcinógena, ha sido reemplazado por alternativas como el tolueno, ciclohexano, isooctano y heptano. Estos agentes forman un nuevo azeótropo con uno de los componentes originales (o con ambos), permitiendo la separación del otro componente.
Tabla Comparativa: Destilación Simple vs. Destilación Azeotrópica
| Característica | Destilación Simple | Destilación Azeotrópica |
|---|---|---|
| Principio de Separación | Diferencia en los puntos de ebullición (volatilidades) | Alteración de la volatilidad relativa mediante un agente de arrastre |
| Capacidad para Separar Azeótropos | No puede separar azeótropos | Diseñada específicamente para separar azeótropos |
| Necesidad de Agente Externo | No requiere la adición de un agente externo | Requiere la adición de un agente de arrastre (entrainer) |
| Complejidad del Proceso | Relativamente simple | Más compleja, requiere recuperación del agente de arrastre |
| Aplicaciones Típicas | Separación de mezclas ideales o con grandes diferencias de P.E. | Separación de mezclas azeotrópicas (ej. etanol-agua) |
Preguntas Frecuentes (FAQs)
¿Cuál es la principal diferencia entre destilación extractiva y destilación azeotrópica?
La principal diferencia radica en el proceso de separación. En la destilación extractiva, se utiliza un solvente de separación específico que no forma un azeótropo con la mezcla y que modifica las volatilidades relativas de los componentes. En la destilación azeotrópica, el agente de separación sí forma un azeótropo con uno o más componentes, lo que permite su separación. La destilación extractiva puede ser un método más sencillo en algunos casos, ya que el solvente no destila con los componentes principales.
¿Por qué las mezclas azeotrópicas no pueden separarse por destilación simple?
No pueden separarse por destilación simple porque, al hervir, el vapor tiene la misma composición que la mezcla líquida. Esto significa que la separación por cambios de fase no altera las proporciones de los constituyentes, impidiendo una purificación efectiva.
¿Por qué se utiliza la destilación azeotrópica?
La destilación azeotrópica se utiliza para mejorar la separación de mezclas que forman azeótropos. Al añadir ciertos componentes (agentes de arrastre) a la mezcla, se puede aumentar la volatilidad relativa de los químicos, permitiendo que la destilación sea efectiva donde la destilación simple falla.
¿Qué significa azeótropo en química?
En química, un azeótropo es una mezcla de líquidos con un punto de ebullición constante debido a que la composición del vapor es idéntica a la de la mezcla líquida. El punto de ebullición de una mezcla azeotrópica puede ser mayor o menor que el de cualquiera de sus constituyentes puros.
¿Qué ocurre durante la destilación al vacío?
La destilación al vacío implica reducir la presión en la columna por encima del solvente a un valor menor que la presión de vapor de la mezcla. Esto genera un vacío, lo que permite que los elementos con presiones de vapor más bajas se evaporen a temperaturas más reducidas. Es útil para compuestos sensibles al calor o con puntos de ebullición muy altos, pero no resuelve el problema de la composición constante de los azeótropos.
En resumen, el cálculo de la composición de un azeótropo es un proceso que combina principios termodinámicos rigurosos con técnicas experimentales precisas. La minimización de la energía libre de Gibbs de mezclado, junto con el análisis detallado de las fases líquida y de vapor mediante cromatografía de gases y la aplicación de las leyes de Raoult y Dalton, nos permite caracterizar estas mezclas singulares. Comprender su comportamiento y las estrategias para su separación, como la destilación azeotrópica, es esencial para numerosos procesos industriales y de investigación en química e ingeniería química.
Si quieres conocer otros artículos parecidos a ¿Cómo Calcular la Composición de un Azeótropo? puedes visitar la categoría Química.
