26/02/2023
En el vasto y fascinante universo de la química, existen conceptos fundamentales que actúan como pilares para comprender cómo interactúan los elementos y cómo se transforman las sustancias. Uno de esos conceptos cruciales es el estado de oxidación, también conocido como número de oxidación. Este valor, que a menudo genera confusión, es en realidad una herramienta poderosa que nos permite rastrear el flujo de electrones en las reacciones químicas, desvelando si un átomo gana o pierde cargas, y por ende, si se oxida o se reduce. Comprender cómo calcularlo y qué significa su variación es esencial para cualquier estudiante o entusiasta de la química, abriendo las puertas a un entendimiento más profundo de las reacciones redox, la electroquímica y la estabilidad de los compuestos.
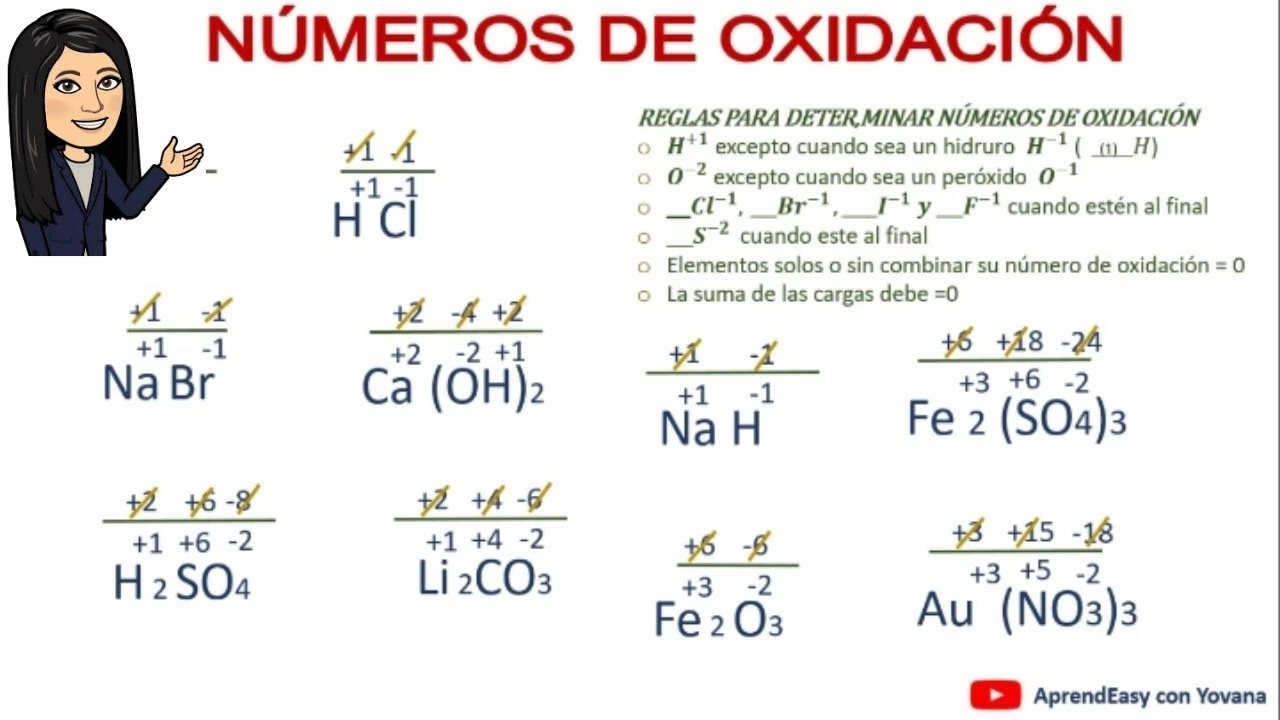
Acompáñanos en este recorrido detallado donde desglosaremos el significado del número de oxidación, las reglas para asignarlo, y lo aplicaremos a ejemplos concretos, como el intrigante caso del cloro en el ión ClO2-. Prepárate para desmitificar este concepto y potenciar tu comprensión de la química.
¿Qué es el Número de Oxidación?
El número de oxidación (N.O.) o estado de oxidación de un átomo en un compuesto es un número que representa la carga hipotética que tendría ese átomo si todos los enlaces con otros átomos fueran completamente iónicos. En otras palabras, es una medida de la capacidad de un átomo para ganar, perder o compartir electrones con otros átomos en un compuesto. Se asigna asumiendo que los electrones compartidos en un enlace covalente son atraídos completamente por el átomo más electronegativo.
Es importante no confundir el número de oxidación con la valencia. Mientras que la valencia indica el número de enlaces que un átomo puede formar, el número de oxidación es un valor con signo (positivo, negativo o cero) que refleja la distribución de electrones y es fundamental para balancear ecuaciones de reacciones redox.
Reglas Fundamentales para Asignar Números de Oxidación
Para calcular correctamente el número de oxidación de un elemento en un compuesto o ión, es indispensable seguir una serie de reglas establecidas. Estas reglas se basan en la electronegatividad de los elementos y en la carga total de la especie química:
- Elementos en estado elemental: Cualquier elemento que se encuentre en su forma libre, sin combinarse con otros elementos (ya sea como átomo individual o como molécula diatómica/poliatómica), tiene un número de oxidación de cero. Ejemplos: Na (0), Fe (0), O2 (0), S8 (0).
- Iones monoatómicos: Para un ión formado por un solo átomo, el número de oxidación es igual a la carga del ión. Ejemplos: Cl- (-1), Na+ (+1), Al3+ (+3), O2- (-2).
- Hidrógeno (H): En la mayoría de los compuestos, el hidrógeno tiene un número de oxidación de +1. Sin embargo, en hidruros metálicos (compuestos con metales del Grupo 1 y 2), su número de oxidación es -1. Ejemplos: H2O (+1), HCl (+1), NaH (-1), CaH2 (-1).
- Oxígeno (O): El oxígeno casi siempre tiene un número de oxidación de -2. Las excepciones notables incluyen los peróxidos (donde tiene -1, como en H2O2), los superóxidos (donde tiene -1/2, como en KO2), y cuando se combina con flúor (el elemento más electronegativo), donde puede tener +2 (como en OF2).
- Metales Alcalinos (Grupo 1) y Alcalinotérreos (Grupo 2): Los metales alcalinos (Li, Na, K, Rb, Cs, Fr) siempre tienen un número de oxidación de +1 en sus compuestos. Los metales alcalinotérreos (Be, Mg, Ca, Sr, Ba, Ra) siempre tienen un número de oxidación de +2 en sus compuestos.
- Flúor (F): El flúor es el elemento más electronegativo y siempre tiene un número de oxidación de -1 en sus compuestos.
- Compuestos neutros: La suma algebraica de los números de oxidación de todos los átomos en un compuesto neutro debe ser igual a cero.
- Iones poliatómicos: La suma algebraica de los números de oxidación de todos los átomos en un ión poliatómico debe ser igual a la carga neta del ión.
Cálculo del Número de Oxidación del Cloro en ClO2-
Ahora, apliquemos estas reglas para determinar el número de oxidación del cloro en el ión diclorito, ClO2-. Este es un excelente ejemplo para practicar con iones poliatómicos.
Para ello, seguiremos los siguientes pasos:
- Identificar la carga total del ión: El ión ClO2- tiene una carga neta de -1. Esto significa que la suma de los números de oxidación de todos los átomos que lo componen debe ser igual a -1.
- Asignar el número de oxidación conocido: Sabemos que el oxígeno (O) casi siempre tiene un número de oxidación de -2. En este caso, no hay razones para que sea una excepción (no es un peróxido ni está con flúor).
- Establecer la ecuación: Sea 'x' el número de oxidación desconocido del cloro (Cl). Tenemos dos átomos de oxígeno, cada uno con -2. La ecuación sería: (Número de N.O. de Cl) + (Número de átomos de O × N.O. de O) = Carga total del ión.
Sustituyendo los valores conocidos:
x + (2 × -2) = -1
x + (-4) = -1
x - 4 = -1
Para despejar 'x', sumamos 4 a ambos lados de la ecuación:
x = -1 + 4
x = +3
Por lo tanto, el número de oxidación del cloro en el ión ClO2- es +3.
Tabla Comparativa: Números de Oxidación del Cloro en Diferentes Compuestos
El cloro es un elemento fascinante que puede presentar una amplia gama de números de oxidación, desde -1 hasta +7, lo que lo hace muy versátil en reacciones químicas. A continuación, se muestra una tabla con algunos ejemplos:
| Compuesto/Ión | Número de Oxidación del Cloro | Notas |
|---|---|---|
| Cl- (ión cloruro) | -1 | Ión monoatómico, su carga es su N.O. |
| Cl2 (cloro elemental) | 0 | Elemento en su estado libre. |
| HCl (ácido clorhídrico) | -1 | H es +1, por lo tanto Cl es -1. |
| ClO- (ión hipoclorito) | +1 | O es -2, carga total -1, entonces Cl es +1. |
| ClO2- (ión clorito) | +3 | O es -2, carga total -1, entonces Cl es +3. |
| ClO3- (ión clorato) | +5 | O es -2, carga total -1, entonces Cl es +5. |
| ClO4- (ión perclorato) | +7 | O es -2, carga total -1, entonces Cl es +7. |
Oxidación y Reducción: El Baile de los Electrones
Los números de oxidación son la clave para entender las reacciones redox (reducción-oxidación), que son procesos químicos fundamentales donde hay una transferencia de electrones entre especies. Estos procesos son omnipresentes, desde la combustión de combustibles hasta la respiración celular y la corrosión de metales.
Definición Electrónica de Oxidación y Reducción:
- Oxidación: Es un proceso en el que un átomo o ión pierde electrones. Cuando un átomo se oxida, su número de oxidación aumenta (se vuelve más positivo o menos negativo). Los electrones perdidos suelen aparecer en el lado derecho de la semirreacción de oxidación.
- Reducción: Es un proceso en el que un átomo o ión gana electrones. Cuando un átomo se reduce, su número de oxidación disminuye (se vuelve menos positivo o más negativo). Los electrones ganados suelen aparecer en el lado izquierdo de la semirreacción de reducción.
Es crucial recordar que la oxidación y la reducción siempre ocurren simultáneamente; no puede haber una sin la otra. La sustancia que se oxida (pierde electrones) es el agente reductor, ya que provoca la reducción de otra sustancia. Por otro lado, la sustancia que se reduce (gana electrones) es el agente oxidante, ya que provoca la oxidación de otra sustancia.

Analizando Cambios en Números de Oxidación
La variación en el número de oxidación nos indica la magnitud de la transferencia de electrones y si un proceso es de oxidación o reducción. Veamos cómo aplicar esto con los ejemplos que se mencionaron previamente:
- Variación del Cloro: Si el número de oxidación del cloro en el ión ClO2- es +3 y pasa a -1 (por ejemplo, en un ión Cl-), su variación es de -4 unidades (de +3 a -1). Esto significa que el átomo de cloro ha ganado 4 electrones, por lo que ha experimentado una reducción.
- Variación del Azufre: Si el azufre (S) pasa de tener un número de oxidación de 0 (en S elemental) a +6 (en el ión SO42-, por ejemplo), su variación es de +6 unidades (de 0 a +6). Esto indica que el átomo de azufre ha perdido 6 electrones, lo que corresponde a una oxidación.
- Variación del Hierro: Si el hierro (Fe) pasa de un número de oxidación de +2 (en Fe2+) a +3 (en Fe3+), su variación es de +1 unidad (de +2 a +3). Esto significa que el átomo de hierro ha perdido 1 electrón, lo que también es un proceso de oxidación.
Estos ejemplos ilustran cómo el cambio en el número de oxidación no solo nos dice si un elemento se oxida o se reduce, sino también cuántos electrones están involucrados en ese cambio.
Preguntas Frecuentes (FAQ) sobre Números de Oxidación
¿Por qué es tan importante el número de oxidación en química?
El número de oxidación es fundamental por varias razones. Primero, nos permite identificar qué elementos se oxidan y cuáles se reducen en una reacción química, lo cual es crucial para comprender las reacciones redox. Segundo, es una herramienta indispensable para balancear ecuaciones redox, ya sea por el método del ión-electrón o por el método del cambio en el número de oxidación. Tercero, nos ayuda a predecir la reactividad de los compuestos y su estabilidad, ya que un elemento en su número de oxidación más alto o más bajo suele ser más reactivo. Finalmente, es clave para la nomenclatura de muchos compuestos inorgánicos, especialmente aquellos con metales de transición que pueden tener múltiples estados de oxidación.
¿Puede un elemento tener múltiples números de oxidación?
¡Absolutamente! De hecho, muchos elementos, especialmente los metales de transición (como el hierro, cobre, cromo, etc.) y los no metales (como el azufre, nitrógeno, cloro, etc.), pueden exhibir múltiples números de oxidación en diferentes compuestos. Esto se debe a su capacidad para perder, ganar o compartir electrones de diversas maneras, formando enlaces con diferentes tipos de átomos. Por ejemplo, el hierro puede tener +2 (en FeO) o +3 (en Fe2O3), y el nitrógeno puede ir desde -3 (en NH3) hasta +5 (en HNO3).
¿Cuál es la diferencia entre número de oxidación y valencia?
Aunque a veces se usan indistintamente, son conceptos distintos. La valencia se refiere al número de enlaces que un átomo puede formar, y es siempre un número entero positivo. Representa la capacidad de combinación de un átomo. Por ejemplo, el carbono tiene una valencia de 4. El número de oxidación, por otro lado, es una carga hipotética asignada a un átomo en un compuesto y puede ser positivo, negativo, cero o incluso fraccionario. Indica el grado de oxidación o reducción de un átomo y es clave para las reacciones redox. Por ejemplo, en el metano (CH4), el carbono tiene una valencia de 4, pero un número de oxidación de -4.
¿Es siempre el oxígeno -2 y el hidrógeno +1?
En la gran mayoría de los compuestos, sí. Estas son las reglas generales y más comunes. Sin embargo, existen excepciones importantes que es crucial recordar. Para el oxígeno, las excepciones incluyen los peróxidos (como H2O2), donde es -1, y cuando se combina con flúor (como en OF2), donde es +2. Para el hidrógeno, la excepción principal son los hidruros metálicos (como NaH), donde es -1. Conocer estas excepciones es vital para evitar errores en los cálculos.
¿Qué es una reacción de dismutación?
Una reacción de dismutación (o desproporción) es un tipo especial de reacción redox en la que un mismo elemento se oxida y se reduce simultáneamente. Es decir, un átomo de ese elemento en un estado de oxidación intermedio se transforma en dos o más productos donde el mismo elemento tiene números de oxidación diferentes: uno más alto (oxidado) y otro más bajo (reducido). Un ejemplo clásico es la descomposición del peróxido de hidrógeno (H2O2) en agua (H2O) y oxígeno (O2), donde el oxígeno pasa de -1 a -2 y a 0.
Conclusión
El número de oxidación es mucho más que un simple valor numérico; es una ventana a la dinámica de las reacciones químicas. Dominar su cálculo y comprender su significado es indispensable para cualquiera que desee adentrarse en el estudio de la química, desde la estequiometría hasta la electroquímica. Hemos visto cómo una herramienta tan simple nos permite desentrañar procesos complejos como la oxidación y la reducción, y cómo un elemento como el cloro puede adoptar múltiples identidades dependiendo de su entorno químico. Al comprender estos principios, no solo resolvemos ejercicios, sino que desarrollamos una visión más profunda y apreciación por la intrincada belleza de las transformaciones de la materia.
Si quieres conocer otros artículos parecidos a Dominando el Número de Oxidación: Guía Completa puedes visitar la categoría Química.

