22/01/2022
En el vasto universo de la química, la capacidad de cuantificar y manipular las sustancias es fundamental. Dos conceptos que se entrelazan de manera indispensable en este proceso son la molaridad y la dilución. Comprender su relación y cómo aplicarlos correctamente no solo es crucial para el éxito en cualquier experimento de laboratorio, sino también para innumerables aplicaciones industriales y cotidianas. Desde la preparación de un reactivo para una titulación hasta la formulación precisa de un medicamento, la precisión en la concentración es la clave. Este artículo explorará en profundidad qué son la molaridad y la dilución, cómo se interrelacionan y por qué dominarlas te abrirá las puertas a un entendimiento más profundo de la química.

- La Molaridad: El Lenguaje de la Concentración Química
- La Dilución: Reduciendo la Concentración con Precisión
- La Interconexión Vital: Molaridad y Dilución Juntas
- Importancia Fundamental en el Laboratorio y la Industria
- Consideraciones Clave y Errores Comunes al Trabajar con Diluciones
- Tabla Comparativa: Soluciones Concentradas vs. Diluidas
- Preguntas Frecuentes (FAQs) sobre Molaridad y Dilución
La Molaridad: El Lenguaje de la Concentración Química
La molaridad es una de las unidades de concentración más utilizadas en química, especialmente en disoluciones. Proporciona una medida precisa de la cantidad de soluto disuelto en un volumen específico de disolvente, formando una disolución. A diferencia de otras unidades como el porcentaje en masa o el porcentaje en volumen, la molaridad se basa en la cantidad de sustancia (moles), lo que la hace particularmente útil para cálculos estequiométricos en reacciones químicas.
Una disolución se compone de un soluto (la sustancia que se disuelve) y un disolvente (la sustancia que disuelve al soluto, generalmente en mayor cantidad). La molaridad nos dice cuántos moles de soluto hay por cada litro de disolución total (soluto + disolvente). Esta es la razón por la que es tan valiosa: nos permite saber exactamente cuántas partículas de soluto están disponibles para reaccionar en un volumen dado.
¿Cómo se Calcula la Molaridad?
El cálculo de la molaridad es directo y se basa en una fórmula sencilla. Para determinar la concentración molar de una disolución, solo necesitas conocer la cantidad de soluto en moles y el volumen total de la disolución en litros.
Molaridad (M) = Moles de soluto (n) / Volumen de la disolución (V en Litros)Donde:
- M es la molaridad, expresada en moles por litro (mol/L) o simplemente 'M'.
- n es el número de moles del soluto. Si tienes la masa del soluto, puedes convertirla a moles utilizando su masa molar (n = masa / masa molar).
- V es el volumen total de la disolución, expresado en litros. Es crucial recordar que debe ser el volumen de la disolución completa, no solo del disolvente.
Ejemplo Práctico de Cálculo de Molaridad
Imagina que has disuelto 58.44 gramos de cloruro de sodio (NaCl) en agua para formar un volumen total de 500 mL de disolución. ¿Cuál es la molaridad de esta disolución?
- Paso 1: Calcular los moles de soluto (NaCl).
La masa molar del NaCl es aproximadamente 58.44 g/mol (22.99 g/mol para Na + 35.45 g/mol para Cl).
Moles de NaCl (n) = Masa de NaCl / Masa molar de NaCl = 58.44 g / 58.44 g/mol = 1 mol. - Paso 2: Convertir el volumen de la disolución a litros.
El volumen dado es 500 mL. Sabemos que 1 Litro = 1000 mL.
Volumen (V) = 500 mL / 1000 mL/L = 0.5 L. - Paso 3: Calcular la molaridad.
Molaridad (M) = n / V = 1 mol / 0.5 L = 2 M.
Por lo tanto, la molaridad de la disolución de cloruro de sodio es de 2 M.
La Dilución: Reduciendo la Concentración con Precisión
La dilución es el proceso de disminuir la concentración de una disolución añadiendo más disolvente. Es una práctica común en el laboratorio y la industria cuando se necesita una disolución menos concentrada a partir de una disolución madre o de stock que es más concentrada. Durante la dilución, la cantidad de soluto permanece constante; lo que cambia es el volumen total de la disolución, lo que a su vez reduce la molaridad.
Piensa en un jugo concentrado al que le añades agua. El sabor se vuelve menos intenso porque la cantidad de sustancia que da sabor (el soluto) se distribuye en un volumen mayor de líquido. En química, la dilución se realiza de manera controlada para obtener una concentración específica que sea adecuada para un determinado experimento o aplicación.
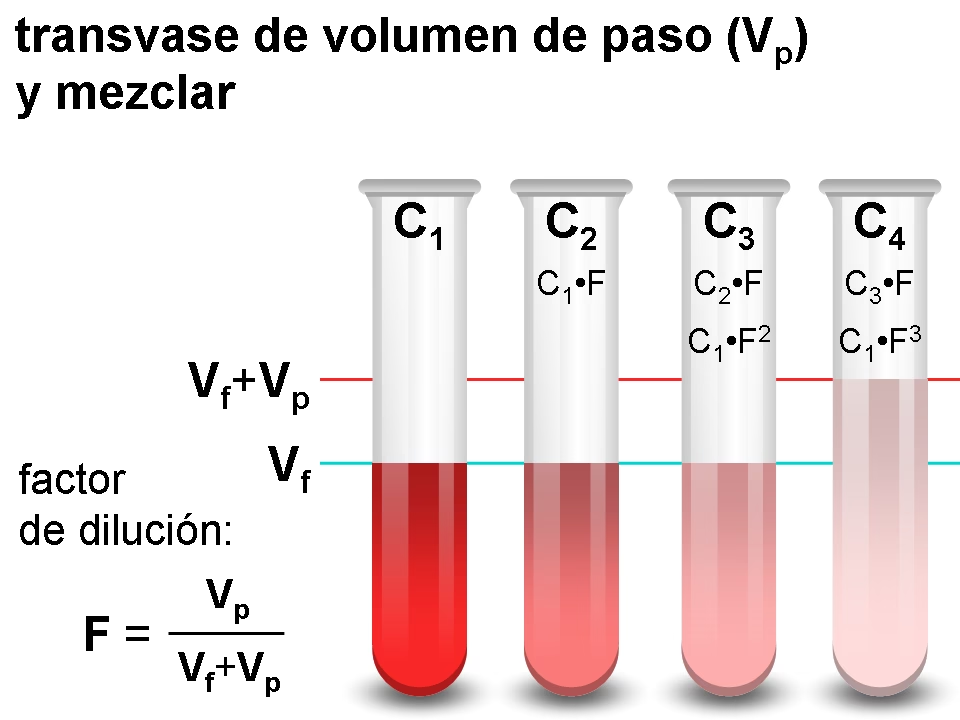
La Ecuación Clave de la Dilución: M1V1 = M2V2
La relación fundamental que rige la dilución es una de las fórmulas más útiles en la química de disoluciones. Se basa en el principio de que la cantidad de soluto (en moles) antes y después de la dilución permanece constante. Si la cantidad de moles de soluto es la misma, entonces el producto de la molaridad por el volumen debe ser igual antes y después de la dilución.
M1V1 = M2V2Donde:
- M1 es la molaridad inicial de la disolución concentrada.
- V1 es el volumen inicial de la disolución concentrada que se toma para diluir.
- M2 es la molaridad final de la disolución diluida que se desea obtener.
- V2 es el volumen final total de la disolución diluida.
Esta fórmula es increíblemente potente porque, conociendo tres de las cuatro variables, puedes calcular la cuarta. Por ejemplo, si tienes una disolución madre de cierta molaridad (M1) y quieres preparar un volumen específico (V2) de una disolución menos concentrada (M2), puedes calcular qué volumen de la disolución madre (V1) necesitas tomar.
Ejemplo Práctico de Cálculo de Dilución
Supongamos que tienes una disolución madre de ácido clorhídrico (HCl) 12 M y necesitas preparar 250 mL de una disolución de HCl 0.5 M para un experimento. ¿Qué volumen de la disolución 12 M debes tomar?
- Paso 1: Identificar las variables conocidas y la incógnita.
M1 = 12 M (molaridad de la disolución madre)
V1 = ? (volumen a tomar de la disolución madre)
M2 = 0.5 M (molaridad deseada de la disolución diluida)
V2 = 250 mL = 0.250 L (volumen final deseado de la disolución diluida) - Paso 2: Aplicar la fórmula de dilución y despejar V1.
M1V1 = M2V2
V1 = (M2 * V2) / M1 - Paso 3: Sustituir los valores y calcular.
V1 = (0.5 M * 0.250 L) / 12 M
V1 = 0.125 / 12 L
V1 = 0.010416 L - Paso 4: Convertir el volumen a mL (si es más conveniente).
V1 = 0.010416 L * 1000 mL/L = 10.42 mL (aproximadamente)
Así, necesitarías tomar aproximadamente 10.42 mL de la disolución madre de HCl 12 M y añadirle suficiente agua hasta que el volumen total de la disolución alcance los 250 mL.
La Interconexión Vital: Molaridad y Dilución Juntas
La relación entre molaridad y dilución es intrínseca y fundamental. La dilución es, en esencia, la manipulación directa de la molaridad de una disolución. Cuando diluimos una disolución, estamos reduciendo su molaridad al aumentar el volumen del disolvente mientras la cantidad de soluto permanece constante. Este principio es la base de cómo los químicos preparan disoluciones de trabajo a partir de disoluciones de stock más concentradas, ahorrando tiempo, espacio y recursos.
¿Por Qué Diluimos Soluciones?
Existen múltiples razones para diluir una disolución:
- Preparación de Reactivos: Muchas veces, los reactivos se compran o se preparan en forma concentrada (disoluciones madre) para su almacenamiento y estabilidad. Antes de usarlos en un experimento, se diluyen a la concentración de trabajo necesaria.
- Seguridad: Ciertos ácidos o bases concentrados son muy corrosivos y peligrosos. Diluirlos los hace más seguros de manejar y usar en el laboratorio.
- Precisión en la Reacción: Para muchas reacciones químicas, se requiere una concentración muy específica para asegurar que los reactivos reaccionen en las proporciones estequiométricas correctas, o para estudiar la cinética de la reacción.
- Calibración de Instrumentos: En química analítica, se preparan series de disoluciones con concentraciones conocidas (curvas de calibración) para calibrar equipos como espectrofotómetros. Estas disoluciones a menudo se preparan por dilución en serie.
- Reducción de Costos: Comprar o preparar disoluciones muy concentradas y luego diluirlas puede ser más económico que adquirir grandes volúmenes de disoluciones ya diluidas.
Importancia Fundamental en el Laboratorio y la Industria
La comprensión y aplicación correcta de la molaridad y la dilución no son meros ejercicios teóricos; son habilidades prácticas esenciales que impactan directamente la seguridad, la precisión y la eficiencia en una amplia gama de campos científicos y tecnológicos. En cualquier laboratorio de química, ya sea educativo, de investigación o industrial, estas dos propiedades son el pan de cada día.
Aplicaciones en Diversos Campos
- Investigación Científica: Desde la síntesis de nuevos materiales hasta el estudio de mecanismos de reacción complejos, la capacidad de preparar disoluciones con concentraciones exactas es vital para obtener resultados reproducibles y significativos.
- Farmacéutica y Medicina: La dosificación precisa de medicamentos es crítica para la eficacia y seguridad del paciente. Los farmacéuticos y los fabricantes de medicamentos utilizan la molaridad y la dilución para formular inyecciones, jarabes y otras preparaciones con la concentración exacta de principio activo.
- Análisis Ambiental: Para monitorear contaminantes en agua, aire o suelo, los químicos ambientales deben preparar estándares de calibración y diluir muestras a rangos detectables por los instrumentos.
- Industria Alimentaria: En la producción de alimentos y bebidas, la concentración de aditivos, saborizantes o conservantes debe controlarse rigurosamente. La dilución se utiliza para ajustar los niveles de estos componentes según las especificaciones del producto.
- Biología y Bioquímica: En la preparación de medios de cultivo, soluciones tampón y reactivos para experimentos con enzimas o ADN, la molaridad y la dilución son herramientas indispensables para mantener las condiciones óptimas.
Consideraciones Clave y Errores Comunes al Trabajar con Diluciones
Aunque la dilución parece un proceso sencillo, la precisión es primordial. Pequeños errores pueden llevar a grandes desviaciones en la concentración final, invalidando los resultados de un experimento o comprometiendo la calidad de un producto. Aquí hay algunas consideraciones importantes:
- Precisión del Material Volumétrico: Utiliza siempre material volumétrico calibrado (matraces aforados, pipetas volumétricas) para mediciones de volumen precisas, especialmente para la disolución final. Las probetas graduadas son menos precisas para este fin.
- Temperatura: El volumen de las disoluciones puede variar ligeramente con la temperatura. Asegúrate de que tanto la disolución madre como el disolvente estén a una temperatura similar y de que el volumen final se ajuste a la temperatura de calibración del material volumétrico (generalmente 20°C).
- Seguridad: Al diluir ácidos o bases fuertes, siempre añade el ácido/base concentrado lentamente al agua (nunca al revés) y con agitación constante. Esto ayuda a disipar el calor generado por la disolución y previene salpicaduras peligrosas. Siempre usa equipo de protección personal (gafas de seguridad, guantes, bata de laboratorio).
- Mezcla Homogénea: Después de añadir el disolvente, asegúrate de mezclar la disolución a fondo para garantizar una concentración uniforme en todo el volumen. En un matraz aforado, esto se logra invirtiendo el matraz varias veces.
- Solutos Volátiles o Sensibles: Al diluir solutos volátiles o sensibles al aire/luz, toma precauciones adicionales como trabajar en una campana de extracción o en condiciones de baja luz.
Tabla Comparativa: Soluciones Concentradas vs. Diluidas
Para visualizar mejor las diferencias y usos de las soluciones concentradas y diluidas, la siguiente tabla resume sus características principales:
| Característica | Solución Concentrada | Solución Diluida |
|---|---|---|
| Cantidad de Soluto | Mayor por unidad de volumen | Menor por unidad de volumen |
| Volumen de Solvente | Menor en proporción al soluto | Mayor en proporción al soluto |
| Valor de Molaridad | Alto | Bajo |
| Usos Típicos | Almacenamiento, soluciones madre, reacciones que requieren alta concentración | Preparación de reactivos de trabajo, análisis, dosificación, seguridad |
| Color/Intensidad | Generalmente más intenso (si aplica) | Generalmente menos intenso (si aplica) |
| Reactividad | Potencialmente más reactiva o corrosiva | Generalmente menos reactiva o corrosiva |
Preguntas Frecuentes (FAQs) sobre Molaridad y Dilución
- ¿Por qué la molaridad es la unidad de concentración preferida en muchos laboratorios?
- La molaridad se basa en moles de soluto, que es una medida de la cantidad de partículas. Esto la hace ideal para cálculos estequiométricos en reacciones químicas, donde las proporciones molares entre reactivos y productos son fundamentales. Además, el volumen de la disolución es fácil de medir con precisión en el laboratorio.
- ¿Cómo afecta la temperatura a la molaridad?
- La molaridad se define por el volumen de la disolución, y el volumen de un líquido puede cambiar ligeramente con la temperatura (expansión o contracción). Por lo tanto, una disolución preparada a una temperatura específica tendrá una molaridad ligeramente diferente si su temperatura cambia significativamente. Sin embargo, para la mayoría de las aplicaciones de laboratorio, la variación es mínima y se considera despreciable, a menos que se requiera una precisión extrema o se trabaje con grandes cambios de temperatura.
- ¿La dilución cambia la cantidad total de soluto en la solución?
- No, la dilución no cambia la cantidad total de soluto (en moles o gramos) en la disolución. Lo que cambia es la concentración de ese soluto porque se le añade más disolvente, lo que aumenta el volumen total de la disolución. Los moles de soluto permanecen constantes, lo cual es el principio fundamental detrás de la fórmula M1V1 = M2V2.
- ¿Cuál es la diferencia entre disolver y diluir?
- Disolver es el proceso de mezclar un soluto con un disolvente para formar una disolución. Por ejemplo, disolver azúcar en agua. Diluir es el proceso de reducir la concentración de una disolución ya existente añadiendo más disolvente. Es decir, primero se disuelve algo y luego, si la concentración es demasiado alta, se diluye.
- ¿Qué precauciones de seguridad debo tomar al diluir ácidos o bases fuertes?
- Siempre debes añadir el ácido o la base concentrada lentamente al agua, nunca el agua al ácido/base. Esta regla se conoce como 'siempre el ácido sobre el agua'. Esto es porque la disolución de ácidos y bases fuertes en agua es a menudo una reacción exotérmica (libera calor). Si añades agua al ácido concentrado, el agua puede hervir violentamente y salpicar, lo que es muy peligroso. Al añadir el ácido al agua, el mayor volumen de agua puede absorber el calor de forma más segura. Usa siempre gafas de seguridad, guantes y una bata de laboratorio, y trabaja en una campana de extracción para evitar la inhalación de vapores.
En conclusión, la molaridad y la dilución son dos conceptos inseparables y esenciales en la química. La molaridad nos permite cuantificar con precisión la concentración de una disolución, mientras que la dilución nos brinda la herramienta para ajustar esa concentración a nuestras necesidades. Dominar la fórmula M1V1 = M2V2 y comprender los principios subyacentes no solo te capacitará para realizar cálculos con confianza, sino que también te permitirá abordar con seguridad y eficacia una multitud de tareas en el laboratorio y en diversas aplicaciones industriales. Estos pilares de la química cuantitativa son la base para el éxito en cualquier esfuerzo que involucre la manipulación de sustancias químicas.
Si quieres conocer otros artículos parecidos a Molaridad y Dilución: Pilares de la Química Cuantitativa puedes visitar la categoría Química.
