29/05/2023
En el vasto y fascinante mundo de la química, comprender las cantidades de sustancias que interactúan en una reacción es fundamental. No podemos simplemente mezclarlas al azar y esperar los resultados deseados; necesitamos precisión. Es aquí donde el concepto de mol y el análisis de reactivos limitantes y en exceso se vuelven indispensables. Estos pilares de la estequiometría nos permiten predecir con exactitud cuánto producto se formará y qué sustancias quedarán sin reaccionar, optimizando procesos y evitando desperdicios. Prepárate para sumergirte en los cálculos que rigen las transformaciones químicas.
El Concepto de Mol y Su Cálculo: La Base de la Cantidad Química
Antes de sumergirnos en las complejidades de las reacciones, es crucial entender la unidad fundamental de cantidad de sustancia en química: el mol. El mol no es solo una medida de peso o volumen; es una forma de contar partículas, ya sean átomos, moléculas, iones o cualquier otra entidad microscópica. Imagina que es como una 'docena' gigantesca, pero para el mundo subatómico.
¿Qué es un Mol?
Un mol se define como la cantidad de sustancia que contiene un número de partículas igual al número de átomos en 12 gramos del isótopo carbono-12. Este número es el famoso número de Avogadro, que aproximadamente es 6.022 x 1023 partículas por mol. Así, 1 mol de agua contiene 6.022 x 1023 moléculas de agua, y 1 mol de hierro contiene 6.022 x 1023 átomos de hierro.
La importancia del mol radica en que nos permite relacionar la masa macroscópica (que podemos medir con una balanza) con el número de partículas microscópicas, facilitando los cálculos en el laboratorio.
Fórmula para Calcular Moles a partir de la Masa
La forma más común de calcular el número de moles (n) de una sustancia es a partir de su masa (m) y su masa molar (M). La masa molar es la masa de un mol de una sustancia y se expresa en gramos por mol (g/mol). Para elementos, la masa molar es numéricamente igual a su masa atómica expresada en gramos. Para compuestos, es la suma de las masas atómicas de todos los átomos en su fórmula química.
La fórmula es la siguiente:
n = m / M
Donde:
n= número de moles (mol)m= masa de la sustancia (gramos)M= masa molar de la sustancia (g/mol)
Ejemplo 1: Cálculo de Moles de Agua
Supongamos que queremos saber cuántos moles hay en 25.0 gramos de agua (H2O).
Primero, necesitamos la masa molar del agua:
- Masa atómica de H ≈ 1.0 g/mol
- Masa atómica de O ≈ 16.0 g/mol
- Masa molar de H2O = (2 × 1.0 g/mol) + (1 × 16.0 g/mol) = 2.0 g/mol + 16.0 g/mol = 18.0 g/mol
Ahora aplicamos la fórmula:
n = 25.0 g / 18.0 g/mol = 1.39 mol de H2O
Fórmula para Calcular Moles a partir del Número de Partículas
Si conocemos el número de partículas (N) de una sustancia, también podemos calcular el número de moles utilizando el número de Avogadro (NA):
n = N / NA
Donde:
n= número de moles (mol)N= número de partículas (átomos, moléculas, etc.)NA= número de Avogadro (6.022 x 1023 partículas/mol)
Ejemplo 2: Cálculo de Moles a partir de Moléculas de H2SO4
¿Cuántos moles hay en 3.4 x 1023 moléculas de H2SO4?
Aplicamos la fórmula:
n = 3.4 x 1023 moléculas / 6.022 x 1023 moléculas/mol = 0.56 mol de H2SO4
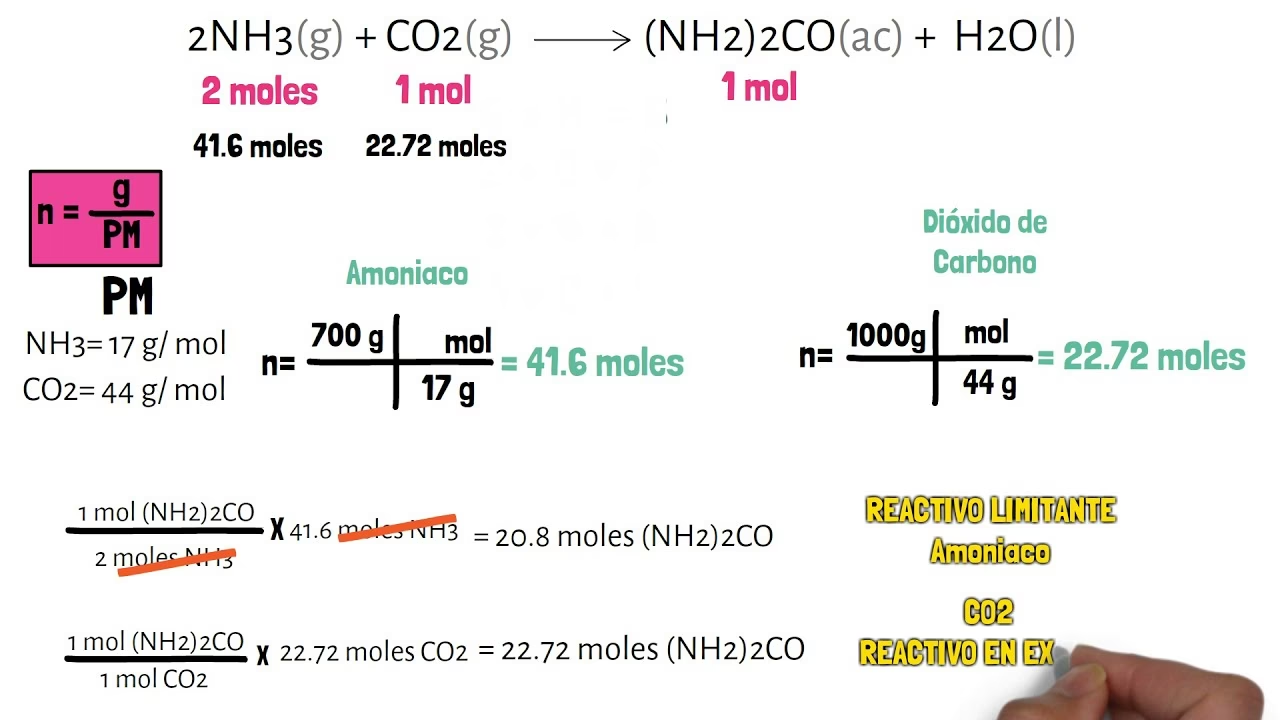
Reactivo Limitante y Reactivo en Exceso: La Clave de las Reacciones Químicas
En una reacción química, las sustancias rara vez se mezclan en las proporciones estequiométricas exactas. Esto significa que uno de los reactivos se consumirá por completo antes que los demás, deteniendo la reacción y limitando la cantidad de producto que se puede formar. Este es el concepto de reactivo limitante y reactivo en exceso.
La Analogía del Sándwich de Queso
Imagina que quieres hacer sándwiches de queso. La "receta" dice:
1 rebanada de queso + 2 rebanadas de pan → 1 sándwich
Si tienes 28 rebanadas de pan y 11 rebanadas de queso, ¿cuántos sándwiches puedes hacer?
- Con 11 rebanadas de queso, puedes hacer 11 sándwiches (usando 22 rebanadas de pan).
- Con 28 rebanadas de pan, puedes hacer 14 sándwiches (usando 14 rebanadas de queso).
El queso es el "ingrediente" que se agotará primero, limitando la producción a 11 sándwiches. Por lo tanto, el queso es el reactivo limitante. Te sobrarán 6 rebanadas de pan (28 - 22), lo que convierte al pan en el reactivo en exceso.
Identificación del Reactivo Limitante
En química, el principio es el mismo. Para identificar el reactivo limitante, debemos:
- Escribir y balancear la ecuación química.
- Convertir las cantidades dadas de los reactivos a moles.
- Calcular la cantidad de producto que se formaría si cada reactivo se consumiera completamente, utilizando las relaciones estequiométricas de la ecuación balanceada.
- El reactivo que produce la menor cantidad de producto es el reactivo limitante.
Ejemplo de Identificación: Reacción de Hidrógeno y Cloro
Consideremos la reacción de hidrógeno con cloro para producir cloruro de hidrógeno:
H2(g) + Cl2(g) → 2HCl(g)
La ecuación balanceada muestra que el hidrógeno y el cloro reaccionan en una proporción estequiométrica 1:1. Si combinamos 6 moles de H2 y 4 moles de Cl2, ¿cuál es el reactivo limitante?
Calculemos cuánto HCl se produciría con cada reactivo:
- Si todo el H2 reaccionara:
- Si todo el Cl2 reaccionara:
6 mol H2 × (2 mol HCl / 1 mol H2) = 12 mol HCl
4 mol Cl2 × (2 mol HCl / 1 mol Cl2) = 8 mol HCl
Dado que el cloro (Cl2) produciría la menor cantidad de HCl (8 moles), el Cl2 es el reactivo limitante. El hidrógeno (H2) es el reactivo en exceso.
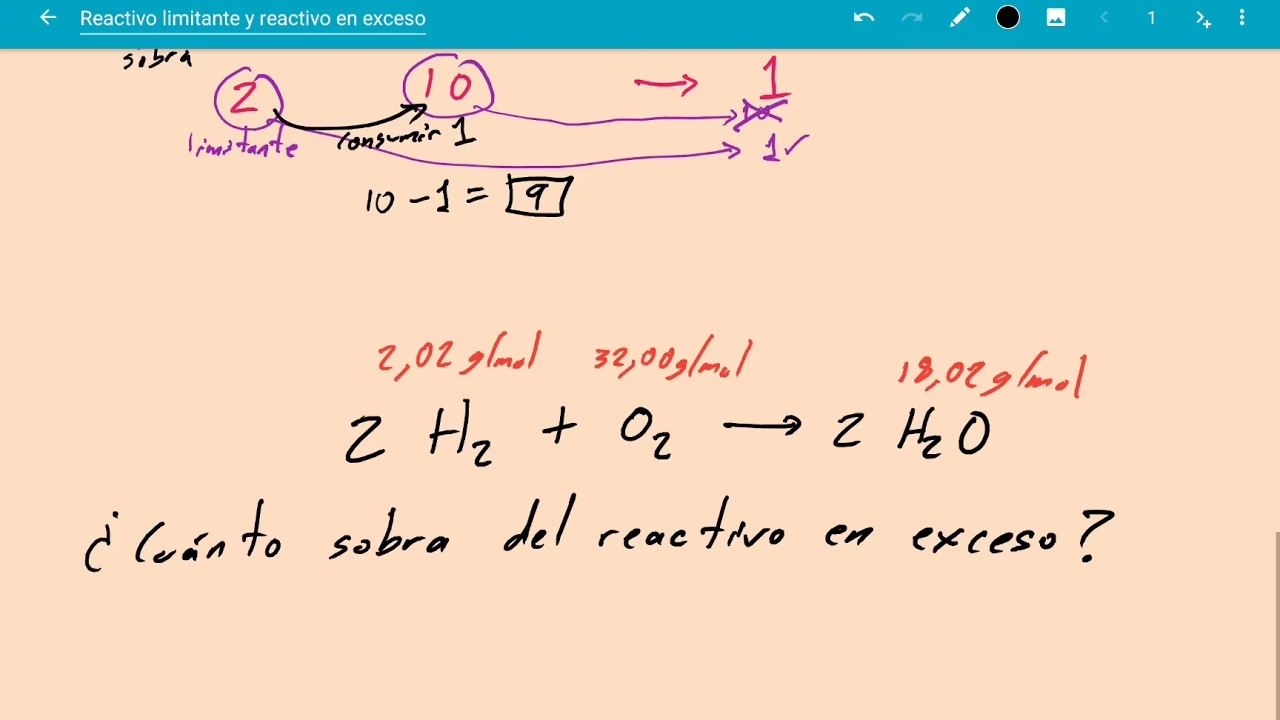
Cálculo del Reactivo en Exceso No Consumido
Una vez que hemos identificado el reactivo limitante, podemos determinar cuánto del reactivo en exceso queda sin reaccionar. Esto es crucial para entender la eficiencia de una reacción y para futuras purificaciones.

Pasos para Calcular el Exceso Remanente
- Identifica el reactivo limitante (como se explicó anteriormente).
- Calcula la cantidad de reactivo en exceso que *reaccionó* utilizando la cantidad del reactivo limitante y la estequiometría de la ecuación.
- Resta la cantidad de reactivo en exceso que reaccionó de la cantidad inicial de reactivo en exceso para encontrar la cantidad que queda sin reaccionar.
Continuando el Ejemplo de H2 y Cl2
Sabemos que el Cl2 es el reactivo limitante y que se produjeron 8 moles de HCl. Ahora, calculemos cuánto H2 reaccionó para producir esos 8 moles de HCl:
8 mol HCl × (1 mol H2 / 2 mol HCl) = 4 mol H2 reaccionaron
Inicialmente teníamos 6 moles de H2. La cantidad de H2 en exceso que queda sin reaccionar es:
Moles de H2 en exceso = 6 mol H2 inicial - 4 mol H2 consumido = 2 mol H2 en exceso
Ejemplo Detallado: Reacción de Rubidio y Cloruro de Magnesio
Consideremos la siguiente reacción química:
2 Rb (s) + MgCl2 (s) → Mg (s) + 2 RbCl (s)
Se combinan 5.00 g de Rb con 3.44 g de MgCl2. Queremos saber qué masa de Mg se forma y qué masa de qué reactivo queda sin reaccionar.
Paso 1: Identificar la información dada y lo que se busca.
- Dados: 5.00 g Rb, 3.44 g MgCl2
- Buscar: Masa de Mg formada (rendimiento teórico); identificar reactivo en exceso y su masa remanente.
Paso 2: Listar otras cantidades conocidas (masas molares).
- 1 mol Rb = 85.47 g Rb
- 1 mol MgCl2 = 95.21 g MgCl2
- 1 mol Mg = 24.31 g Mg
- Relaciones estequiométricas de la ecuación: 2 mol Rb: 1 mol Mg; 1 mol MgCl2: 1 mol Mg
Paso 3: Calcular el rendimiento teórico para cada reactivo.
Convertimos los gramos de cada reactivo a moles, luego a moles de producto (Mg), y finalmente a gramos de producto.
Cálculo con Rubidio (Rb):
5.00 g Rb × (1 mol Rb / 85.47 g Rb) × (1 mol Mg / 2 mol Rb) × (24.31 g Mg / 1 mol Mg) = 0.711 g Mg
Cálculo con Cloruro de Magnesio (MgCl2):
3.44 g MgCl2 × (1 mol MgCl2 / 95.21 g MgCl2) × (1 mol Mg / 1 mol MgCl2) × (24.31 g Mg / 1 mol Mg) = 0.878 g Mg
Paso 4: Identificar el reactivo limitante y el rendimiento teórico.
El reactivo limitante es el Rubidio (Rb) porque produce la menor cantidad de producto (0.711 g de Mg). Por lo tanto, el rendimiento teórico de Mg es 0.711 g.
El reactivo en exceso es el MgCl2, ya que con su cantidad inicial se podría haber producido más Mg (0.878 g) de lo que el Rb permite.
Paso 5: Calcular la masa de reactivo en exceso que reacciona.
Usamos la cantidad de producto formada (0.711 g Mg) para calcular cuánto MgCl2 se consumió:
0.711 g Mg × (1 mol Mg / 24.31 g Mg) × (1 mol MgCl2 / 1 mol Mg) × (95.21 g MgCl2 / 1 mol MgCl2) = 2.78 g MgCl2 reaccionaron
Paso 6: Calcular la masa de reactivo en exceso que queda.
Restamos la masa de MgCl2 que reaccionó de la masa inicial:
Masa inicial de MgCl2 - Masa de MgCl2 reaccionada = Masa de MgCl2 remanente
3.44 g MgCl2 inicial - 2.78 g MgCl2 reaccionaron = 0.66 g MgCl2 remanente
En resumen, se formarán 0.711 g de Mg, y quedarán 0.66 g de MgCl2 sin reaccionar.

Preguntas Frecuentes (FAQ)
¿Cuál es la fórmula para calcular moles?
Existen dos fórmulas principales, dependiendo de la información que tengas:
- Si tienes la masa (
m) de la sustancia y conoces su masa molar (M):n = m / M - Si tienes el número de partículas (
N) de la sustancia y usas el número de Avogadro (NA= 6.022 x 1023 partículas/mol):n = N / NA
¿Cómo se define el mol?
El mol es la unidad del Sistema Internacional de Unidades (SI) para la cantidad de sustancia. Se define como la cantidad de sustancia que contiene 6.022 x 1023 entidades elementales (como átomos, moléculas, iones, etc.). Este número es conocido como el número de Avogadro.
¿Por qué es importante identificar el reactivo limitante?
Es importante identificar el reactivo limitante porque este determina la cantidad máxima de producto que puede formarse en una reacción química. Sin esta identificación, no se puede predecir con precisión el rendimiento teórico de la reacción, lo que es crucial para la eficiencia en procesos industriales y de laboratorio, así como para la comprensión fundamental de las reacciones.
¿Cómo calcular el reactivo en exceso que queda sin reaccionar?
Para calcular la cantidad de reactivo en exceso que queda sin reaccionar, sigue estos pasos:
- Identifica el reactivo limitante.
- Calcula cuánto del reactivo en exceso se consumió en la reacción, utilizando la cantidad del reactivo limitante y las proporciones estequiométricas de la ecuación balanceada.
- Resta la cantidad del reactivo en exceso consumida de la cantidad inicial de este reactivo que tenías al principio. El resultado será la cantidad de reactivo en exceso que queda sin reaccionar.
¿Cómo hallar los moles de una solución?
Para hallar los moles de una sustancia disuelta en una solución, generalmente se utiliza el concepto de concentración molar o molaridad (M), que se define como los moles de soluto por litro de solución (M = n / V). Si conoces la molaridad de una solución y su volumen (en litros), puedes calcular los moles de soluto (n = M × V). Este artículo se centró en los cálculos de moles a partir de masa o número de partículas y la estequiometría de reacciones, pero la molaridad es la clave para trabajar con moles en soluciones.
Conclusión
El dominio del concepto de mol y la habilidad para identificar y calcular las cantidades de reactivos limitantes y en exceso son habilidades fundamentales en química. Estas herramientas nos permiten no solo predecir los resultados de las reacciones, sino también optimizar los procesos, reducir los residuos y comprender profundamente cómo interactúan las sustancias a nivel molecular. Con la práctica y los pasos detallados proporcionados, estarás bien equipado para abordar los desafíos estequiométricos y desentrañar los misterios de las transformaciones químicas.
Si quieres conocer otros artículos parecidos a Calculando Moles y Reactivos en Reacciones Químicas puedes visitar la categoría Química.
