13/08/2025
En el fascinante mundo de la química, comprender cómo interactúan las sustancias y en qué proporciones lo hacen es fundamental. Aquí es donde entra en juego la estequiometría, una rama de la química que nos permite cuantificar con precisión las relaciones entre reactivos y productos en una reacción química. Si alguna vez te has preguntado cuánto producto se formará a partir de una cantidad específica de reactivo, o cuánto reactivo necesitas para obtener una cantidad deseada de producto, entonces este artículo es para ti. Nos adentraremos en los principios esenciales para determinar el número de moles en una reacción, una habilidad indispensable para cualquier químico o entusiasta de la ciencia.
La estequiometría es, en esencia, el cálculo de las cantidades de reactivos que se consumen y de productos que se forman en una reacción química. Es la herramienta que nos permite traducir una ecuación química abstracta en información cuantitativa y práctica, esencial tanto en laboratorios de investigación como en grandes plantas industriales. Sin ella, sería imposible predecir rendimientos, optimizar procesos o incluso comprender la eficiencia de una reacción.
La Ecuación Química Ajustada: La Clave Fundamental
El punto de partida de cualquier cálculo estequiométrico es una ecuación química correctamente ajustada, también conocida como ecuación balanceada. ¿Por qué es tan crucial? Porque los coeficientes numéricos que preceden a cada molécula o átomo en una ecuación ajustada no son arbitrarios; representan proporciones fundamentales. Estos coeficientes nos indican:
- El número relativo de moléculas (o átomos) que participan en la reacción.
- El número relativo de moles que intervienen en dicha reacción.
Consideremos, por ejemplo, la reacción de formación de agua a partir de hidrógeno y oxígeno:
2 H₂ (g) + O₂ (g) → 2 H₂O (l)
En esta ecuación ajustada, los coeficientes nos dicen que dos moléculas de hidrógeno reaccionan con una molécula de oxígeno para producir dos moléculas de agua. Pero, lo que es aún más importante para nuestros cálculos, es que también nos indica que dos moles de H₂ reaccionan con un mol de O₂ para producir dos moles de H₂O. Estas proporciones son las "relaciones estequiométricas" y son la base de todos los cálculos de moles y masas en química. Son equivalencias que nos permiten pasar de una sustancia a otra dentro de la misma reacción.
Ejemplo Práctico de Relaciones Estequiométricas
Imaginemos que tenemos 1.57 moles de O₂ y queremos saber cuántas moles de H₂O se producirán, asumiendo que el hidrógeno está en exceso (es decir, tenemos más que suficiente H₂ disponible). Gracias a la ecuación ajustada, sabemos que la relación estequiométrica entre H₂O y O₂ es 2 moles de H₂O por cada 1 mol de O₂. Podemos usar esta relación como un factor de conversión:
Moles de H₂O = 1.57 moles de O₂ × (2 moles de H₂O / 1 mol de O₂)
Moles de H₂O = 3.14 moles de H₂O
Este simple ejemplo ilustra cómo los coeficientes de una ecuación balanceada se convierten en herramientas poderosas para predecir cantidades.
Las Etapas Esenciales para Cálculos Estequiométricos
Independientemente de si estamos calculando moles o masas, hay una serie de pasos sistemáticos que debemos seguir para asegurar la precisión de nuestros resultados. Estas son las etapas fundamentales:
- Ajustar la ecuación química: Este es el primer y más crítico paso. Una ecuación no ajustada llevará a resultados incorrectos.
- Calcular el peso molecular o fórmula de cada compuesto: Necesitarás esta información para convertir entre moles y gramos.
- Convertir las masas a moles: Generalmente, medimos las sustancias en gramos en el laboratorio, pero las reacciones ocurren en proporciones molares.
- Usar la ecuación química ajustada para obtener los datos necesarios: Aquí es donde aplicamos las relaciones estequiométricas (factores de conversión molar) derivadas de los coeficientes.
- Reconvertir las moles a masas si se requiere: Si la pregunta final pide una cantidad en gramos, deberás realizar el paso inverso al tercero.
Tipos de Cálculos Estequiométricos
Los cálculos estequiométricos se pueden clasificar en diferentes tipos según las unidades iniciales y finales que manejemos. A continuación, exploraremos los más comunes:
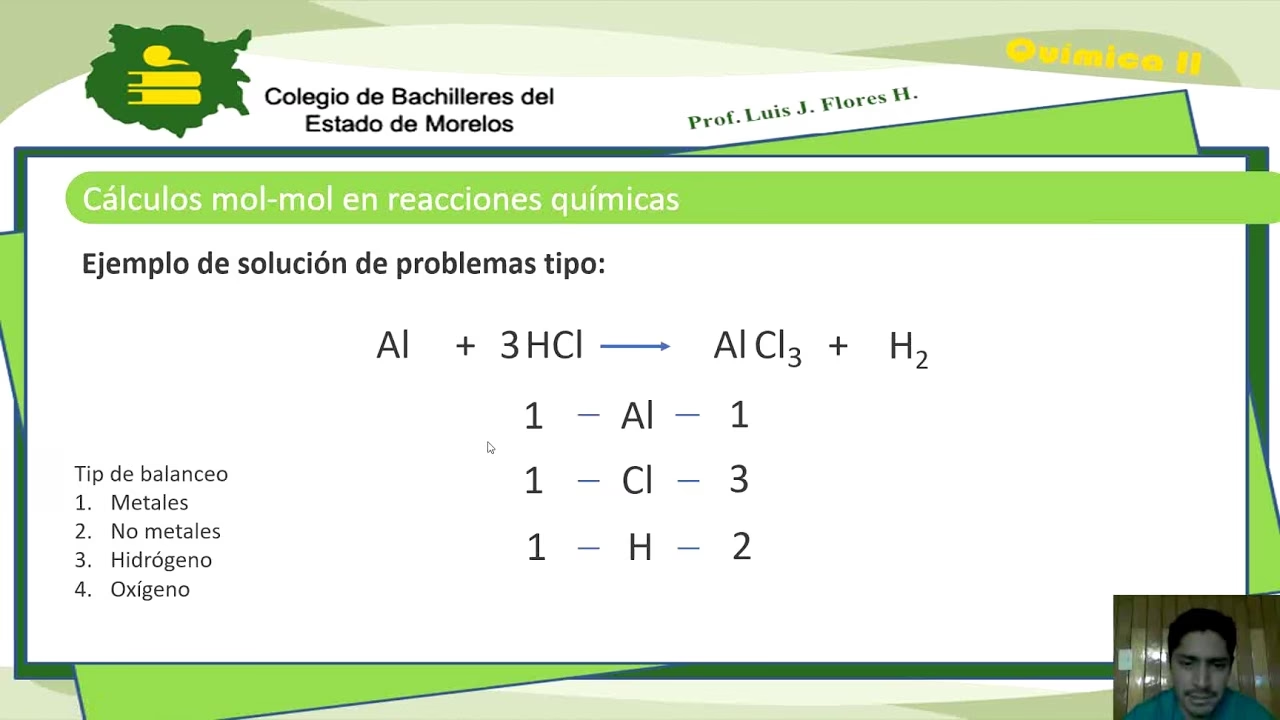
1. Cálculos de Moles a Moles
Este es el tipo de cálculo más directo y se basa puramente en las proporciones molares indicadas por la ecuación ajustada. Si conocemos las moles de una sustancia, podemos encontrar las moles de cualquier otra sustancia en la reacción.
La fórmula general para calcular moles de un reactivo o producto (X) a partir de moles de otra sustancia (Y) es:
Moles de X = Moles de Y × (Coeficiente de X en la ecuación ajustada / Coeficiente de Y en la ecuación ajustada)
Ejemplo: Para la producción de amoníaco (NH₃) según la ecuación:
N₂ (g) + 3 H₂ (g) → 2 NH₃ (g)
¿Cuántas moles de hidrógeno (H₂) son necesarias para producir 6 moles de NH₃?
La relación estequiométrica entre H₂ y NH₃ es 3 moles de H₂ por cada 2 moles de NH₃. Por lo tanto:
Moles de H₂ = 6 moles de NH₃ × (3 moles de H₂ / 2 moles de NH₃)
Moles de H₂ = 9 moles de H₂
2. Cálculos de Moles a Masa
Cuando necesitamos saber la masa de un producto a partir de una cantidad conocida de moles de reactivo (o viceversa), introducimos el concepto de peso molecular. El peso molecular (o masa molar) de una sustancia nos dice cuántos gramos hay en un mol de esa sustancia.
Conversión de Moles a Gramos:
Masa (gramos) = Moles × Peso Molecular (g/mol)
Ejemplo: ¿Cuál es la masa de oxígeno (O₂) producida a partir de 0.25 moles de KClO₃ según la siguiente ecuación?
2 KClO₃ (s) → 2 KCl (s) + 3 O₂ (g)
(Pesos Atómicos: K = 39.1 g/mol, Cl = 35.45 g/mol, O = 16.00 g/mol)
Primero, calculamos las moles de O₂ producidas:
Moles de O₂ = 0.25 moles de KClO₃ × (3 moles de O₂ / 2 moles de KClO₃)
Moles de O₂ = 0.375 moles de O₂
Ahora, convertimos las moles de O₂ a gramos. El peso molecular del O₂ es 2 × 16.00 g/mol = 32.00 g/mol.

Masa de O₂ = 0.375 moles de O₂ × 32.00 g/mol
Masa de O₂ = 12.00 gramos de O₂
3. Cálculos de Masa a Masa
Este es el tipo de cálculo estequiométrico más completo y común en el laboratorio, ya que las sustancias se miden típicamente en gramos. Implica la conversión de masa a moles, luego el uso de la relación estequiométrica y finalmente la reconversión de moles a masa.
Los pasos son:
- Convertir la masa conocida a moles (usando el peso molecular).
- Usar los coeficientes de la ecuación ajustada para determinar las moles de la sustancia deseada.
- Reconvertir las moles de la sustancia deseada a masa (usando su peso molecular).
Ejemplo: ¿Qué masa de H₂ reacciona con un exceso de O₂ para producir 11.91 g de H₂O?
2 H₂ (g) + O₂ (g) → 2 H₂O (l)
(Pesos Atómicos: H = 1.008 g/mol, O = 16.00 g/mol)
- Convertir la masa de H₂O a moles:
Peso molecular de H₂O = (2 × 1.008) + 16.00 = 18.016 g/molMoles de H₂O = 11.91 g / 18.016 g/mol = 0.6611 moles de H₂O
- Calcular las moles de H₂ necesarias:
Según la ecuación, 2 moles de H₂ producen 2 moles de H₂O. La relación es 1:1.Moles de H₂ = 0.6611 moles de H₂O × (2 moles de H₂ / 2 moles de H₂O) = 0.6611 moles de H₂
- Convertir las moles de H₂ a masa:
Peso molecular de H₂ = 2 × 1.008 = 2.016 g/molMasa de H₂ = 0.6611 moles de H₂ × 2.016 g/mol = 1.333 gramos de H₂
Tabla Resumen de Conversiones Estequiométricas
Para facilitar la comprensión, la siguiente tabla resume los diferentes tipos de cálculos y las conversiones clave:
| Tipo de Cálculo | Punto de Partida | Conversión Intermedia | Punto Final |
|---|---|---|---|
| Moles-Moles | Moles de Sustancia A | Relación Estequiométrica (de la ecuación ajustada) | Moles de Sustancia B |
| Moles-Masa | Moles de Sustancia A | Relación Estequiométrica (para obtener moles de B) | Masa de Sustancia B (usando Peso Molecular de B) |
| Masa-Moles | Masa de Sustancia A (usando Peso Molecular de A) | Relación Estequiométrica (para obtener moles de B) | Moles de Sustancia B |
| Masa-Masa | Masa de Sustancia A (usando Peso Molecular de A) | Relación Estequiométrica (para obtener moles de B) | Masa de Sustancia B (usando Peso Molecular de B) |
Preguntas Frecuentes (FAQ) sobre Estequiometría y Moles
Aquí respondemos algunas de las preguntas más comunes relacionadas con los cálculos de moles en reacciones químicas:
¿Qué es exactamente un mol?
Un mol es una unidad de cantidad de sustancia en el Sistema Internacional de Unidades (SI). Representa la cantidad de sustancia que contiene exactamente 6.02214076 × 10²³ entidades elementales (como átomos, moléculas o iones). Este número se conoce como el número de Avogadro. El mol es crucial porque permite relacionar la masa de una sustancia (medida en gramos) con el número de partículas que contiene, y por ende, con las proporciones de una reacción química.
¿Por qué es tan importante balancear una ecuación química antes de hacer cálculos?
Balancear una ecuación química asegura que se cumpla la Ley de Conservación de la Masa, que establece que la materia no se crea ni se destruye en una reacción química. Si la ecuación no está balanceada, los coeficientes no representarán las proporciones reales de moles, lo que llevará a cálculos estequiométricos incorrectos y, por lo tanto, a predicciones erróneas de las cantidades de reactivos o productos.
¿Cómo sé cuándo usar el peso molecular para convertir?
El peso molecular (o masa molar) es la clave para convertir entre gramos y moles. Lo usarás siempre que necesites pasar de una unidad de masa (gramos, kilogramos, etc.) a una unidad de cantidad de sustancia (moles), o viceversa. Si la pregunta te da una masa y te pide moles, o te da moles y te pide una masa, el peso molecular será tu factor de conversión.
¿Qué significa que un reactivo esté en "exceso"?
Cuando se dice que un reactivo está en "exceso", significa que hay más cantidad de ese reactivo de la que se necesita para reaccionar completamente con el otro reactivo (el reactivo limitante). En los cálculos estequiométricos, si un reactivo está en exceso, no lo consideramos para determinar la cantidad de producto, ya que el producto se formará en función del reactivo limitante.
Conclusión
Dominar el cálculo de moles en reacciones químicas es una habilidad fundamental que te abrirá las puertas a una comprensión más profunda de la química. Desde la predicción de rendimientos en el laboratorio hasta la optimización de procesos industriales, la estequiometría es una herramienta indispensable. Al seguir los pasos sistemáticos, comprender el papel crucial de la ecuación ajustada y utilizar correctamente los pesos moleculares, podrás determinar con precisión las cantidades de cualquier sustancia involucrada en una reacción. Recuerda, la práctica hace al maestro, así que no dudes en aplicar estos conceptos a diversos problemas para consolidar tu conocimiento.
Si quieres conocer otros artículos parecidos a Descifrando Moles: Guía de Estequiometría Química puedes visitar la categoría Química.

