13/12/2025
Desde el aire que respiramos hasta los metales que construyen nuestras ciudades, todo en el universo se compone de unidades fundamentales conocidas como elementos químicos. Estas sustancias puras son los bloques de construcción esenciales de la materia, cada uno con propiedades únicas que lo distinguen. Pero, ¿cómo se definen, cómo se obtienen y, lo más importante, cómo podemos determinar qué es un elemento químico? Acompáñanos en este recorrido para desvelar los misterios detrás de la composición fundamental de nuestro mundo.
¿Qué son los Elementos Químicos?
Los elementos químicos son sustancias puras, lo que significa que la materia que los compone está constituida por un mismo tipo de átomo. Es decir, un elemento es un tipo específico de materia, formado enteramente por átomos de la misma clase, y cuyas propiedades intrínsecas lo diferencian de cualquier otro elemento. Por ejemplo, el oxígeno (O) posee características y comportamientos distintos a los del oro (Au), a pesar de que ambos son elementos fundamentales. En esencia, los elementos son la base a partir de la cual, mediante diversas reacciones, procesos y períodos de tiempo, se combinan para dar lugar a toda la diversidad de materia que conocemos. Ya sea que se encuentren de forma natural o sean obtenidos artificialmente, sus usos y aplicaciones varían ampliamente según sus propiedades específicas.
¿Cómo se Obtienen y Encuentran los Elementos Químicos?
La mayoría de los elementos químicos se obtienen de la naturaleza, ya sea de manera espontánea en su forma pura o, más comúnmente, formando compuestos con otros elementos. Son sustancias atómicamente puras que no pueden ser descompuestas en otras más simples mediante reacciones químicas ordinarias. Sin embargo, no todos los elementos son de origen natural. De los 118 elementos actualmente reconocidos en la Tabla Periódica, 26 han sido obtenidos artificialmente en laboratorios. Esto significa que no existen de forma natural en la Tierra, sino que han sido creados por el ser humano a través de procesos como la aceleración de partículas o en reactores atómicos. Estos elementos sintéticos suelen ser inestables y existen solo por milésimas de segundo.
A lo largo de la historia del universo, la variedad de elementos químicos ha ido generándose a partir de procesos de nucleosíntesis, fundamentalmente en el interior de las estrellas. Las estrellas actúan como verdaderas fábricas de elementos, fusionando átomos más ligeros para formar otros más pesados, hasta que, al final de su vida, explotan y dispersan estos elementos por el cosmos.
Es crucial diferenciar entre un elemento químico y una sustancia simple. Un elemento (como el oxígeno, O) es un tipo de átomo. Una sustancia simple, en cambio, es una forma molecular de un elemento. Por ejemplo, el ozono (O₃) y el dioxígeno (O₂) son dos sustancias simples distintas, cada una con propiedades diferentes, pero ambas están compuestas por el mismo elemento químico: el oxígeno (O).
¿Cómo Determinar un Elemento Químico? El Rol del Número Atómico
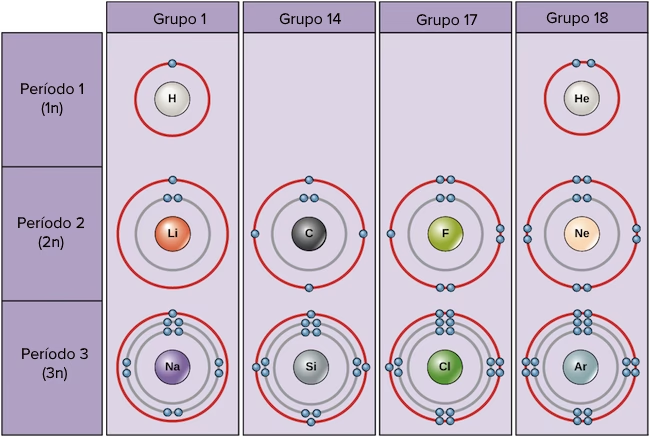
La clave para determinar y diferenciar un elemento químico reside en su Número Atómico. Este número, representado por la letra 'Z', corresponde a la cantidad de protones que posee el núcleo de un átomo. Cada elemento tiene un número de protones único y característico. Por ejemplo, todos los átomos de hidrógeno tienen 1 protón, todos los de helio tienen 2 protones, y así sucesivamente. Esta es la propiedad fundamental que define la identidad de un elemento.
Aunque los átomos de un mismo elemento siempre tienen el mismo número de protones, pueden variar en el número de neutrones. Cuando átomos de un mismo elemento poseen un número de masa distinto (debido a una variación en el número de neutrones), se les conoce como isótopos. A pesar de esta diferencia en masa, siguen siendo el mismo elemento porque su número de protones es idéntico.
La organización de los elementos en la Tabla Periódica se basa precisamente en este número atómico creciente, lo que permite clasificar y predecir sus propiedades químicas y físicas de manera sistemática.

La Tabla Periódica: Un Mapa de los Elementos
La Tabla Periódica de los Elementos, creada por el químico ruso Dimitri Mendeléyev en 1869, es el sistema de clasificación más importante en química. Organiza los elementos de forma visual y lógica basándose en sus propiedades y características. Actualmente, la tabla cuenta con 118 elementos conocidos, ordenados por su número atómico creciente. Esta organización permite agrupar los elementos en categorías principales que comparten propiedades similares.
La denominación de los elementos procede de diversas fuentes: nombres en griego, latín, inglés, o incluso llevan el nombre de su descubridor o la ciudad donde fueron descubiertos. Históricamente, el descubrimiento de elementos ha sido un proceso continuo, desde los 13 elementos conocidos antes del año 1500, hasta los más recientes obtenidos por fusión nuclear en el siglo XXI.
Principales Tipos de Elementos Químicos
La clasificación más fundamental de los elementos en la tabla periódica los divide en tres grandes grupos: metales, no metales y gases nobles, aunque también existen los metaloides, que exhiben propiedades intermedias. Esta clasificación, aunque con algunas excepciones, es muy útil para entender el comportamiento químico de los elementos.
Metales
Los Metales constituyen la mayor parte de los elementos de la tabla periódica. Se caracterizan por ser, en su mayoría, excelentes conductores de la electricidad y del calor. A temperatura ambiente, suelen ser sólidos (con la notable excepción del mercurio, que es líquido), opacos, poseen una estructura cristalina en estado sólido y adquieren un brillo característico cuando se pulen. Son maleables (pueden ser golpeados para formar láminas delgadas) y dúctiles (pueden estirarse para formar alambres).
Los metales tienden a tener energías de ionización bajas, lo que significa que pierden electrones con relativa facilidad en las reacciones químicas, es decir, se oxidan. Muchos metales reaccionan con sustancias comunes como el oxígeno (O₂) y los ácidos.
Se utilizan ampliamente con fines estructurales, en la fabricación de recipientes, y para la conducción de calor y electricidad. Además, muchos iones metálicos son vitales para funciones biológicas en los seres vivos.
Algunos ejemplos comunes de metales incluyen:
- Aluminio (Al): Muy ligero, no ferromagnético, resistente a la corrosión. Valorado en la industria.
- Plata (Ag): Metal precioso, el mejor conductor de calor y electricidad conocido.
- Oro (Au): Metal precioso, blando, brillante, inerte a la mayoría de las sustancias químicas.
- Cobre (Cu): Excelente conductor de electricidad y calor, muy utilizado en cableado.
- Calcio (Ca): Indispensable para huesos y dientes, presente en muchos minerales.
- Mercurio (Hg): El único metal líquido a temperatura ambiente, utilizado en termómetros.
- Magnesio (Mg): Abundante, indispensable para la vida, utilizado en aleaciones.
- Hierro (Fe): Abundante en la corteza terrestre, ferromagnético, base del acero.
- Níquel (Ni): Dúctil, maleable, buen conductor, ferromagnético.
- Zinc (Zn): Utilizado en galvanización para proteger otros metales de la corrosión.
- Plomo (Pb): Muy denso, barrera contra la radiación, flexible.
- Estaño (Sn): Empleado en aleaciones para resistencia a la corrosión.
- Sodio (Na): Metal alcalino blando, muy reactivo, esencial para organismos vivos.
No Metales
Los No Metales varían considerablemente en apariencia y propiedades. A diferencia de los metales, no poseen lustre metálico y por lo general son malos conductores del calor y la electricidad. Sus puntos de fusión son más bajos que los de los metales (con la notable excepción del diamante, una forma de carbono). Muchos no metales existen en condiciones ordinarias como moléculas diatómicas (como H₂, N₂, O₂, F₂, Cl₂). Algunos son gases (oxígeno), líquidos (bromo) o sólidos (carbono, azufre) a temperatura ambiente. Los sólidos no metálicos suelen ser quebradizos y no pueden estirarse en hilos ni en láminas.
Los no metales tienen una alta capacidad de ionización y una alta tendencia a ganar electrones en las reacciones químicas, es decir, se reducen. La mayor parte de sus óxidos son sustancias moleculares que forman soluciones ácidas. Son vitales para la vida, ya que muchos se encuentran en todos los seres vivos en cantidades importantes (carbono, hidrógeno, oxígeno, nitrógeno, fósforo, azufre, cloro) o como oligoelementos (flúor, bromo, yodo, selenio).

Algunos de los no metales más comunes son:
- Carbono (C): Base de la vida, presente en todas las moléculas orgánicas.
- Oxígeno (O): Esencial para la respiración y la combustión.
- Hidrógeno (H): El elemento más abundante en el universo, componente del agua.
- Flúor (F): Muy reactivo, presente en pastas dentales.
- Fósforo (P): Esencial para el ADN y la energía celular.
- Yodo (I): Importante para la función tiroidea.
- Bromo (Br): El único no metal líquido a temperatura ambiente.
- Azufre (S): Presente en aminoácidos y proteínas.
Gases Nobles
Los Gases Nobles (Helio, Neón, Argón, Kriptón, Xenón, Radón) presentan una característica distintiva: su inercia química. Son sumamente estables y no tienden a reaccionar químicamente con otros elementos. Su estado natural es el gaseoso a temperatura ambiente y suelen presentarse como moléculas monoatómicas o diatómicas de muy baja reactividad. Debido a su estabilidad, son conocidos también como gases inertes. Esta propiedad los hace útiles en aplicaciones donde se requiere una atmósfera no reactiva, como en iluminación (neón) o en procesos de soldadura (argón).
Comparación de Metales y No Metales
Para una mejor comprensión, la siguiente tabla resume las principales diferencias entre metales y no metales:
| Característica | Metales | No Metales |
|---|---|---|
| Lustre | Brillante (colores diversos, muchos plateados) | No tienen lustre (colores diversos) |
| Estado Físico (sol.) | Sólidos (excepto mercurio) | Sólidos (quebradizos), líquidos o gases |
| Conductividad | Buenos conductores de calor y electricidad | Malos conductores de calor y electricidad |
| Maleabilidad/Ductilidad | Maleables y dúctiles | Quebradizos (no se pueden estirar) |
| Óxidos | Óxidos metálicos suelen ser sólidos iónicos básicos | Óxidos no metálicos son moleculares y forman soluciones ácidas |
| Formación de Iones | Tienden a formar cationes (pierden electrones) | Tienden a formar aniones u oxianiones (ganan electrones) |
| Electrones capa externa | Pocos electrones (habitualmente tres o menos) | Cuatro o más electrones (excepto H y He) |
| Localización en Tabla Periódica | Izquierda y centro (Grupos 1-12 y parte de los siguientes) | Derecha de la línea quebrada |
Preguntas Frecuentes (FAQ)
¿Qué es el número atómico y por qué es tan importante para los elementos?
El Número Atómico (Z) es el número de protones en el núcleo de un átomo. Es la característica más importante porque define la identidad única de un elemento. Cada elemento tiene un número atómico diferente, lo que lo distingue de todos los demás. Sin el concepto de número atómico, la clasificación y el estudio sistemático de los elementos serían imposibles.
¿Todos los elementos químicos se encuentran de forma natural en la Tierra?
No. De los 118 elementos conocidos, la mayoría se encuentran en la naturaleza, ya sea en su forma pura o formando compuestos. Sin embargo, un número significativo (actualmente 26) son elementos sintéticos o artificiales, creados en laboratorios mediante procesos nucleares. Estos últimos no existen de forma natural y suelen ser muy inestables.
¿Por qué algunos elementos son inestables y solo existen por milésimas de segundo?
Los elementos más pesados, especialmente los creados artificialmente en aceleradores de partículas o reactores atómicos, suelen ser inestables. Esto se debe a que sus núcleos atómicos contienen una cantidad muy grande de protones y neutrones, lo que los hace inherentemente inestables. Para alcanzar una configuración más estable, estos núcleos se desintegran rápidamente, transformándose en otros elementos, y su vida media puede ser extremadamente corta, a veces de solo milisegundos.
¿Cuál es la diferencia entre un elemento químico y una sustancia simple?
Un elemento químico se refiere al tipo de átomo, definido por su número de protones (por ejemplo, el elemento oxígeno, O). Una sustancia simple es una forma en la que un elemento puede existir en la naturaleza o en el laboratorio, donde las moléculas están compuestas únicamente por átomos de ese mismo elemento. Por ejemplo, el elemento oxígeno puede formar dos sustancias simples diferentes: el dioxígeno (O₂), que es el gas que respiramos, y el ozono (O₃), que es una molécula con tres átomos de oxígeno. Ambas son sustancias simples del elemento oxígeno, pero tienen propiedades físicas y químicas muy distintas.
¿Por qué el mercurio es un metal si es líquido a temperatura ambiente?
El mercurio (Hg) es clasificado como un metal porque posee la mayoría de las propiedades características de los metales: es un buen conductor de la electricidad y el calor, tiene un brillo metálico (aunque sea líquido) y forma aleaciones con otros metales. Su estado líquido a temperatura ambiente es una excepción a la regla general de que los metales son sólidos, pero no invalida sus otras propiedades metálicas fundamentales.
Conclusión
Los elementos químicos son la base de todo lo que existe en el universo. Comprender qué son, cómo se obtienen, cómo se determinan por su Número Atómico y cómo se clasifican en la Tabla Periódica es fundamental para cualquier estudio de la materia. Desde los robustos Metales hasta los vitales No Metales y los inertes Gases Nobles, cada elemento contribuye a la asombrosa diversidad y complejidad del mundo que nos rodea. Explorar sus propiedades y usos nos permite no solo entender la naturaleza a nivel fundamental, sino también aplicar este conocimiento para innovar y mejorar nuestra calidad de vida.
Si quieres conocer otros artículos parecidos a Desentrañando los Elementos Químicos: La Esencia de la Materia puedes visitar la categoría Química.

