28/01/2025
El agua, esa sustancia omnipresente y vital, es mucho más que una simple combinación de hidrógeno y oxígeno. Para comprenderla a fondo, especialmente en campos como la química, la biología o la ingeniería, es fundamental entender cómo se mide su cantidad a nivel molecular. Aquí es donde entran en juego conceptos como la masa molar y los moles. Aunque puedan sonar complejos, son herramientas esenciales que nos permiten cuantificar la materia de una manera precisa y consistente. En este artículo, desglosaremos paso a paso cómo calcular la masa molar de una molécula de agua, exploraremos el caso de compuestos relacionados como el H2O3, y aprenderemos a convertir esa masa en moles, desmitificando así la química detrás de una de las moléculas más importantes de nuestro planeta.

- ¿Qué es la Masa Molar y por qué es Importante?
- Elementos Esenciales: La Tabla Periódica y las Masas Atómicas
- Paso a Paso: Cálculo de la Masa Molar del Agua (H2O)
- ¿Y el H2O3? Un Caso Menos Común pero Interesante
- De la Masa a los Moles: ¿Cómo Calcular los Moles del H2O?
- Aplicaciones Prácticas de los Cálculos de Masa Molar y Moles
- Errores Comunes al Calcular la Masa Molar y los Moles
- Preguntas Frecuentes (FAQ)
¿Qué es la Masa Molar y por qué es Importante?
Antes de sumergirnos en los cálculos, es crucial entender qué es la masa molar y por qué es un concepto tan fundamental en química. La masa molar (M) de una sustancia es la masa de un mol de esa sustancia. Se expresa generalmente en gramos por mol (g/mol). Pero, ¿qué es un mol? Un mol es una unidad de medida en el Sistema Internacional de Unidades (SI) que representa una cantidad de sustancia. Específicamente, un mol de cualquier sustancia contiene aproximadamente 6.022 x 1023 unidades elementales (átomos, moléculas, iones, etc.). Este número es conocido como el Número de Avogadro.
La importancia de la masa molar radica en que nos permite relacionar la masa macroscópica de una sustancia (lo que podemos pesar en una balanza) con el número microscópico de partículas que la componen. Es el puente entre el mundo de los gramos y el mundo de los átomos y moléculas. Sin la masa molar, sería increíblemente difícil realizar cálculos estequiométricos, es decir, predecir las cantidades de reactivos y productos en una reacción química, o determinar la concentración de una solución.
Elementos Esenciales: La Tabla Periódica y las Masas Atómicas
Para calcular la masa molar de cualquier compuesto, necesitamos conocer las masas atómicas de cada uno de los elementos que lo componen. Estas masas se encuentran en la Tabla Periódica de los Elementos. La masa atómica de un elemento es la masa promedio de los átomos de ese elemento, considerando la abundancia de sus isótopos. Se expresa en unidades de masa atómica (uma) o, para propósitos de masa molar, directamente en gramos por mol (g/mol).
Para el agua (H2O), los elementos involucrados son el hidrógeno (H) y el oxígeno (O). Busquemos sus masas atómicas aproximadas en la Tabla Periódica:
- Hidrógeno (H): Aproximadamente 1.008 uma o 1.008 g/mol
- Oxígeno (O): Aproximadamente 15.999 uma o 15.999 g/mol
Para simplificar los cálculos y para la mayoría de los propósitos educativos, a menudo se redondean estas masas a valores más convenientes, como 1.01 g/mol para el H y 16.00 g/mol para el O. Utilizaremos estos valores redondeados para nuestros ejemplos.
Tabla 1: Masas Atómicas de los Elementos en el Agua
| Elemento | Símbolo | Masa Atómica (g/mol) (Aprox.) |
|---|---|---|
| Hidrógeno | H | 1.01 |
| Oxígeno | O | 16.00 |
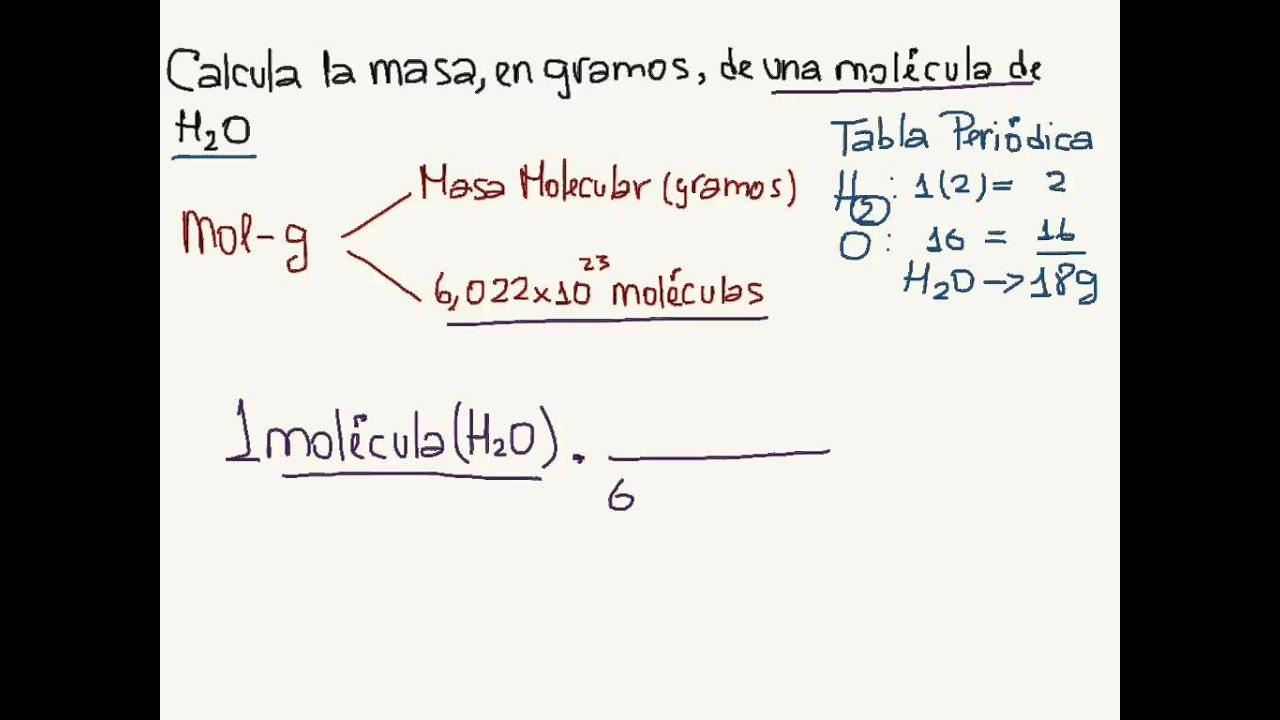
Paso a Paso: Cálculo de la Masa Molar del Agua (H2O)
Ahora que tenemos las masas atómicas, el cálculo de la masa molar del agua es sencillo. La fórmula química del agua es H2O, lo que significa que cada molécula de agua está compuesta por dos átomos de hidrógeno y un átomo de oxígeno.
- Identificar los elementos y sus cantidades:
- Hidrógeno (H): 2 átomos
- Oxígeno (O): 1 átomo
- Multiplicar la cantidad de cada átomo por su masa atómica:
- Para el Hidrógeno: 2 átomos × 1.01 g/mol/átomo = 2.02 g/mol
- Para el Oxígeno: 1 átomo × 16.00 g/mol/átomo = 16.00 g/mol
- Sumar los resultados:
- Masa molar de H2O = (Masa de H) + (Masa de O)
- Masa molar de H2O = 2.02 g/mol + 16.00 g/mol = 18.02 g/mol
Por lo tanto, la masa molar de una molécula de agua (H2O) es aproximadamente 18.02 g/mol. Esto significa que un mol de agua tiene una masa de 18.02 gramos.
¿Y el H2O3? Un Caso Menos Común pero Interesante
La pregunta sobre el H2O3 es pertinente, aunque el H2O3 (trioxidano o peróxido de hidrógeno cíclico) es una molécula mucho menos estable y común que el H2O (agua) o el H2O2 (peróxido de hidrógeno). Sin embargo, el principio para calcular su masa molar es exactamente el mismo. Solo necesitamos ajustar el número de átomos de oxígeno.
Para la molécula de H2O3, tenemos:
- Hidrógeno (H): 2 átomos
- Oxígeno (O): 3 átomos
Siguiendo los mismos pasos:
- Multiplicar la cantidad de cada átomo por su masa atómica:
- Para el Hidrógeno: 2 átomos × 1.01 g/mol/átomo = 2.02 g/mol
- Para el Oxígeno: 3 átomos × 16.00 g/mol/átomo = 48.00 g/mol
- Sumar los resultados:
- Masa molar de H2O3 = (Masa de H) + (Masa de O)
- Masa molar de H2O3 = 2.02 g/mol + 48.00 g/mol = 50.02 g/mol
Así, la masa molecular (o molar) del H2O3 es aproximadamente 50.02 g/mol. Esto demuestra que, sin importar la complejidad de la molécula, el método para calcular la masa molar es universal y se basa en la suma de las masas atómicas de sus componentes.
Tabla 2: Resumen de Cálculos de Masa Molar
| Compuesto | Átomos de H | Masa de H (g/mol) | Átomos de O | Masa de O (g/mol) | Masa Molar Total (g/mol) |
|---|---|---|---|---|---|
| H2O | 2 | 2 × 1.01 = 2.02 | 1 | 1 × 16.00 = 16.00 | 18.02 |
| H2O3 | 2 | 2 × 1.01 = 2.02 | 3 | 3 × 16.00 = 48.00 | 50.02 |
De la Masa a los Moles: ¿Cómo Calcular los Moles del H2O?
Una vez que conocemos la masa molar de una sustancia, podemos usarla para convertir una masa dada (en gramos) a moles, y viceversa. Esta conversión es una de las habilidades más utilizadas en química. La relación es la siguiente:
Moles (n) = Masa (m) / Masa Molar (M)
Donde:
nes el número de moles (en mol)mes la masa de la sustancia (en gramos)Mes la masa molar de la sustancia (en g/mol)
Ejemplo: Calcular los moles de H2O en 36.04 gramos de agua
Sabemos que la masa molar del H2O es 18.02 g/mol.

Si tenemos 36.04 gramos de agua, el cálculo sería:
Moles de H2O = 36.04 g / 18.02 g/mol
Moles de H2O = 2.00 mol
Esto significa que en 36.04 gramos de agua hay exactamente 2.00 moles de moléculas de agua. Si quisiéramos saber cuántas moléculas son, multiplicaríamos 2.00 mol por el Número de Avogadro (6.022 x 1023 moléculas/mol), lo que nos daría aproximadamente 1.2044 x 1024 moléculas de H2O.
Ejemplo: Calcular la masa de 0.5 moles de H2O
Podemos reorganizar la fórmula para calcular la masa si conocemos los moles:
Masa (m) = Moles (n) × Masa Molar (M)
Si tenemos 0.5 moles de agua:
Masa de H2O = 0.5 mol × 18.02 g/mol
Masa de H2O = 9.01 g
Así, 0.5 moles de agua tienen una masa de 9.01 gramos.
Aplicaciones Prácticas de los Cálculos de Masa Molar y Moles
La capacidad de calcular la masa molar y convertir entre masa y moles es fundamental en una amplia gama de campos y aplicaciones:
- Química Analítica: Para determinar la cantidad de una sustancia en una muestra, calcular concentraciones de soluciones o realizar titulaciones.
- Estequiometría: Para predecir las cantidades de reactivos necesarios y productos formados en reacciones químicas, asegurando que las reacciones sean eficientes y sin desperdicio.
- Farmacología: En la dosificación de medicamentos, donde la cantidad precisa de un compuesto activo es crucial para la eficacia y seguridad del tratamiento.
- Bioquímica: Para estudiar las reacciones metabólicas en los organismos vivos, donde las cantidades de moléculas biológicas son esenciales.
- Ingeniería Química: En el diseño de procesos industriales, para optimizar la producción y minimizar costos.
- Nutrición: Para entender la composición de los alimentos y la cantidad de nutrientes en términos de moles para reacciones metabólicas.
Estos cálculos son la base para entender cómo las sustancias interactúan a nivel molecular, permitiendo a científicos e ingenieros manipular la materia de manera controlada y predecible.
Errores Comunes al Calcular la Masa Molar y los Moles
Aunque los cálculos de masa molar y moles son relativamente sencillos, existen errores comunes que se deben evitar:
- No usar la masa atómica correcta: Siempre consulta una tabla periódica actualizada. Redondear demasiado las masas atómicas puede llevar a errores significativos en cálculos más complejos o sensibles.
- Olvidar multiplicar por el subíndice: En una fórmula como H2O, es fácil olvidar que hay dos átomos de hidrógeno. Asegúrate de multiplicar la masa atómica de cada elemento por el número de veces que aparece en la fórmula.
- Confundir masa atómica con masa molecular o molar: La masa atómica se refiere a un solo átomo, mientras que la masa molecular es la suma de las masas atómicas en una molécula individual (en uma), y la masa molar es la masa de un mol de moléculas (en g/mol). Aunque los valores numéricos son los mismos, las unidades y el concepto detrás son distintos.
- Errores en las unidades: Siempre presta atención a las unidades (gramos, moles, g/mol). Un error común es intentar dividir gramos por gramos en lugar de gramos por g/mol. Las unidades deben cancelarse correctamente para obtener el resultado deseado (por ejemplo, gramos / (gramos/mol) = mol).
- Error de cálculo aritmético: Aunque parezca obvio, un simple error de suma o multiplicación puede invalidar todo el cálculo. Siempre verifica tus operaciones.
Preguntas Frecuentes (FAQ)
¿Qué diferencia hay entre masa molecular y masa molar?
Numéricamente, son iguales, pero conceptualmente son diferentes. La masa molecular se refiere a la masa de una sola molécula y se expresa en unidades de masa atómica (uma). Por ejemplo, la masa molecular del H2O es 18.02 uma. La masa molar, en cambio, es la masa de un mol de esa sustancia y se expresa en gramos por mol (g/mol). Así, la masa molar del H2O es 18.02 g/mol. La masa molar es la que se utiliza para cálculos con cantidades macroscópicas de sustancias.
¿Por qué se usa el mol en química?
El mol es una unidad fundamental porque nos permite trabajar con cantidades de sustancias que son medibles en el laboratorio (gramos, litros) y relacionarlas directamente con el número de átomos o moléculas, que son demasiado pequeños para contarlos individualmente. El mol actúa como un 'puente' entre el mundo macroscópico y el mundo microscópico, simplificando la estequiometría y los cálculos de reacciones químicas.
¿Cuál es la masa de un solo átomo de hidrógeno?
La masa de un solo átomo de hidrógeno es aproximadamente 1.008 uma (unidades de masa atómica). Para obtener su masa en gramos, se necesitaría dividir 1.008 g/mol por el Número de Avogadro (6.022 x 1023 átomos/mol), lo que resultaría en un valor extremadamente pequeño, del orden de 1.67 x 10-24 gramos.
¿Se puede calcular la masa molar de cualquier compuesto?
Sí, la masa molar se puede calcular para cualquier compuesto cuya fórmula química sea conocida. El procedimiento es siempre el mismo: sumar las masas atómicas de todos los átomos presentes en la fórmula, multiplicando cada masa atómica por el número de veces que ese elemento aparece en la molécula. Esto aplica tanto para moléculas simples como el agua, como para polímeros complejos o compuestos iónicos.
¿Es importante la precisión de las masas atómicas?
Para la mayoría de los ejercicios educativos y cálculos introductorios, redondear las masas atómicas a dos decimales es suficiente. Sin embargo, en aplicaciones de investigación, industria o cuando se necesitan resultados de alta precisión, se utilizan masas atómicas con más decimales, o incluso masas isotópicas específicas, para obtener la mayor exactitud posible.
Comprender cómo calcular la masa molar y los moles es una habilidad fundamental en el estudio de la química. Estos conceptos no solo son esenciales para resolver problemas en el aula, sino que también son la base para muchas aplicaciones prácticas en la ciencia y la industria. Al dominar estos cálculos, se abre una puerta para entender mejor el comportamiento de la materia y cómo interactúan las sustancias a nivel molecular.
Si quieres conocer otros artículos parecidos a Calculando Masa Molar y Moles: La Química del Agua puedes visitar la categoría Química.