10/02/2022
El ácido sulfúrico, con su fórmula química H2SO4, es una de las sustancias más fundamentales y versátiles en la industria y la investigación científica. Conocido como el 'aceite de vitriolo' en la antigüedad, su importancia radica en su amplio uso, desde la fabricación de fertilizantes hasta el procesamiento de metales. Pero más allá de sus aplicaciones, la molécula de H2SO4 encierra un fascinante misterio en su estructura: la naturaleza de sus enlaces químicos. Comprender si es un compuesto iónico, covalente, o una combinación de ambos, requiere una inmersión profunda en el concepto de la electronegatividad, esa propiedad fundamental que define cómo los átomos comparten o transfieren electrones.
A menudo surge la pregunta: ¿Cuál es la diferencia de electronegatividad del H2SO4? Es crucial entender que la diferencia de electronegatividad se calcula entre *dos átomos específicos* que forman un enlace, no para una molécula completa. Sin embargo, al analizar las diferencias de electronegatividad entre los átomos que componen el ácido sulfúrico (hidrógeno, azufre y oxígeno), podemos desentrañar la naturaleza de cada enlace individual y, por extensión, comprender el comportamiento general de esta potente sustancia. Este artículo explorará la compleja red de enlaces en el H2SO4, clarificando la presencia de enlaces covalentes y el peculiar 'carácter iónico' que exhibe en ciertas condiciones, para ofrecer una visión completa de su enigmática composición.
- La Electronegatividad: Una Clave para Entender los Enlaces
- La Estructura Molecular del Ácido Sulfúrico (H2SO4)
- Análisis de los Enlaces Covalentes en el H2SO4: S-O y O-H
- ¿Existen Enlaces Iónicos en el H2SO4? Desmitificando la Afirmación
- H2SO4: Un Compuesto con Carácter Dual
- Preguntas Frecuentes sobre la Electronegatividad y el H2SO4
La Electronegatividad: Una Clave para Entender los Enlaces
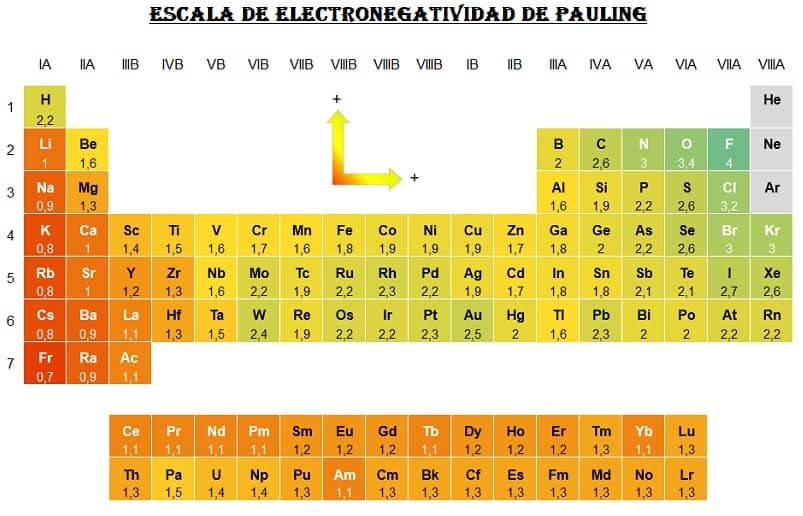
Antes de sumergirnos en el ácido sulfúrico, es fundamental comprender qué es la electronegatividad. La electronegatividad es la capacidad de un átomo en una molécula para atraer hacia sí los electrones de un enlace químico. Esta propiedad, medida comúnmente en la escala de Pauling, es crucial para predecir el tipo de enlace que se formará entre dos átomos. Una diferencia significativa en la electronegatividad entre dos átomos indica un enlace con mayor carácter iónico, mientras que una diferencia pequeña o nula apunta a un enlace covalente.
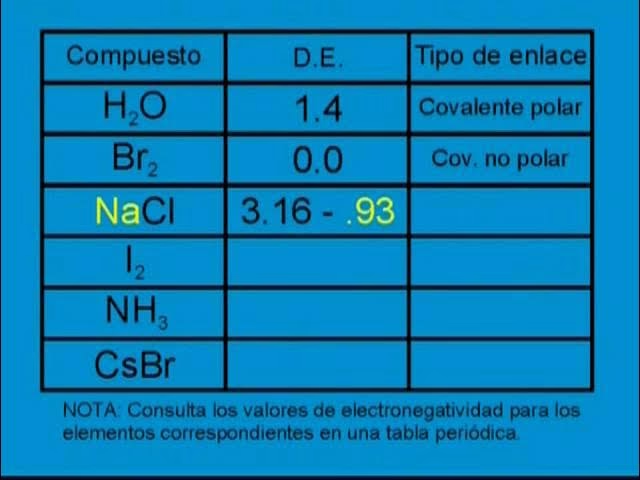
- Enlace Covalente No Polar: La diferencia de electronegatividad es muy pequeña (generalmente < 0.4). Los electrones se comparten de manera equitativa. Ejemplo: H-H (0.0).
- Enlace Covalente Polar: La diferencia de electronegatividad es moderada (generalmente entre 0.4 y 1.7). Los electrones se comparten de manera desigual, creando una carga parcial positiva (δ+) y una carga parcial negativa (δ-) en los átomos. Ejemplo: H-Cl (0.96).
- Enlace Iónico: La diferencia de electronegatividad es grande (generalmente > 1.7). Un átomo 'roba' electrones al otro, formando iones con cargas completas (positiva y negativa), que se atraen electrostáticamente. Ejemplo: Na-Cl (2.23).
Los valores de electronegatividad de los elementos más relevantes para el H2SO4 son:
| Elemento | Símbolo | Electronegatividad (Pauling) |
|---|---|---|
| Hidrógeno | H | 2.20 |
| Oxígeno | O | 3.44 |
| Azufre | S | 2.58 |
La Estructura Molecular del Ácido Sulfúrico (H2SO4)
Para analizar los enlaces en el H2SO4, primero debemos visualizar su estructura. El ácido sulfúrico tiene una estructura tetraédrica alrededor del átomo de azufre central. El azufre (S) está unido a cuatro átomos de oxígeno (O). A su vez, dos de estos oxígenos están unidos a átomos de hidrógeno (H), mientras que los otros dos oxígenos están unidos solo al azufre. Esto significa que en la molécula existen dos tipos principales de enlaces a considerar: enlaces azufre-oxígeno (S-O) y enlaces oxígeno-hidrógeno (O-H).
La representación de Lewis del H2SO4 muestra que el azufre central forma dos enlaces simples con dos átomos de oxígeno (que a su vez están unidos a hidrógeno) y dos enlaces dobles con los otros dos átomos de oxígeno. Esta representación es una simplificación, ya que en realidad, los enlaces S-O tienen un carácter intermedio debido a la resonancia, donde los electrones se deslocalizan entre los oxígenos y el azufre.
Análisis de los Enlaces Covalentes en el H2SO4: S-O y O-H
Considerando los valores de electronegatividad, podemos calcular las diferencias para cada tipo de enlace:
Enlaces Oxígeno-Hidrógeno (O-H)
- Electronegatividad de O: 3.44
- Electronegatividad de H: 2.20
- Diferencia: |3.44 - 2.20| = 1.24
Una diferencia de 1.24 se encuentra en el rango de un enlace covalente polar. Esto significa que los electrones compartidos en el enlace O-H son atraídos con más fuerza por el átomo de oxígeno, que es más electronegativo. Como resultado, el oxígeno adquiere una carga parcial negativa (δ-) y el hidrógeno una carga parcial positiva (δ+). Esta polaridad es crucial para la naturaleza ácida del H2SO4, ya que facilita la disociación del protón (H+) cuando el ácido se disuelve en agua.
Enlaces Azufre-Oxígeno (S-O)
- Electronegatividad de O: 3.44
- Electronegatividad de S: 2.58
- Diferencia: |3.44 - 2.58| = 0.86
Una diferencia de 0.86 también indica un enlace covalente polar. En este caso, el oxígeno es más electronegativo que el azufre, por lo que los electrones compartidos en el enlace S-O son atraídos hacia el oxígeno. Esto contribuye a la distribución de carga en la molécula y a la estabilidad del ion sulfato.
Es importante destacar que, a pesar de la polaridad, tanto los enlaces O-H como los enlaces S-O son fundamentalmente covalentes dentro de la molécula intacta de H2SO4. La compartición de electrones es el mecanismo principal de unión, aunque desigual.
¿Existen Enlaces Iónicos en el H2SO4? Desmitificando la Afirmación
El texto inicial menciona que "los enlaces iónicos se forman entre los iones hidrógeno y el ion sulfato". Esta afirmación, aunque puede generar confusión, se refiere más precisamente al comportamiento del ácido sulfúrico cuando se disuelve en un solvente polar como el agua, y no a los enlaces internos de la molécula neutra H2SO4. Dentro de la molécula de H2SO4 tal como existe en su estado puro, los enlaces son, como hemos visto, principalmente covalentes polares.
Cuando el H2SO4 se disuelve en agua, ocurre un proceso conocido como disociación o ionización. El agua, al ser una molécula polar, interactúa fuertemente con los enlaces O-H altamente polares del ácido sulfúrico. El átomo de hidrógeno, al tener una carga parcial positiva significativa, es atraído por las moléculas de agua y se transfiere a ellas, formando iones hidronio (H3O+) y el ion sulfato (SO4^2-). Es en este contexto de disociación que se forman iones: iones H+ (o H3O+) y el ion sulfato (SO4^2-).
Una vez que estos iones se han formado en solución, las fuerzas que los mantienen unidos o que interactúan con otras especies en la solución son de naturaleza iónica (atracciones electrostáticas entre cargas opuestas). Por lo tanto, el H2SO4 no contiene enlaces iónicos *dentro de su propia estructura molecular intacta*, sino que *se comporta como un compuesto iónico* al ionizarse en solución, liberando iones que luego pueden formar enlaces iónicos con otros iones en el entorno o con metales en compuestos como el sulfato de sodio (Na2SO4).
H2SO4: Un Compuesto con Carácter Dual
La combinación de enlaces covalentes polares y su capacidad para disociarse en iones le otorga al H2SO4 un carácter dual. Internamente, la molécula es predominantemente covalente, con una distribución de carga significativa debido a la alta electronegatividad del oxígeno. Externamente, y en presencia de solventes adecuados, se comporta como un compuesto que forma iones, lo que explica su naturaleza de ácido fuerte y su capacidad para conducir la electricidad en solución acuosa.
Esta dualidad es la clave de muchas de sus propiedades. La fuerte polaridad de sus enlaces contribuye a su alta solubilidad en agua y a su capacidad para actuar como agente deshidratante. La facilidad con la que los protones H+ se separan de la molécula, impulsada por la alta polaridad del enlace O-H y la estabilidad del ion sulfato resultante (gracias a la resonancia y la distribución de carga), es lo que lo clasifica como un ácido fuerte.
Resumen de los Enlaces en H2SO4
| Tipo de Enlace | Átomos Involucrados | Diferencia de Electronegatividad | Naturaleza del Enlace | Implicaciones |
|---|---|---|---|---|
| O-H | Oxígeno - Hidrógeno | 1.24 | Covalente Polar | Facilita la disociación del H+; responsable de la acidez. |
| S-O | Azufre - Oxígeno | 0.86 | Covalente Polar | Contribuye a la estabilidad del ion sulfato y la distribución de carga. |
| Interacción H+-SO4^2- | Iones Hidrógeno - Ion Sulfato | N/A (no es un enlace intramolecular) | Interacción Iónica (en solución) | Resultado de la disociación en solventes polares, confiere carácter iónico al comportamiento. |
Preguntas Frecuentes sobre la Electronegatividad y el H2SO4
¿Es el H2SO4 un compuesto iónico o covalente?
El H2SO4 es fundamentalmente un compuesto con enlaces covalentes polares dentro de su estructura molecular. Sin embargo, debido a su capacidad para ionizarse completamente en agua, liberando iones H+ y SO4^2-, exhibe un comportamiento característico de un compuesto iónico en solución. Por lo tanto, se puede decir que tiene un carácter dual, siendo covalente en su forma molecular y exhibiendo propiedades iónicas al disociarse.
¿Por qué el H2SO4 es un ácido fuerte?
La fuerza del H2SO4 como ácido se debe principalmente a la alta polaridad de los enlaces O-H, resultado de la gran diferencia de electronegatividad entre el oxígeno y el hidrógeno. Esta polaridad debilita el enlace O-H, permitiendo que el protón (H+) se separe fácilmente en presencia de un solvente como el agua. Además, el ion sulfato (SO4^2-) resultante es muy estable debido a la resonancia, lo que también favorece la disociación.
¿Cómo afecta la electronegatividad a la reactividad del H2SO4?
La electronegatividad influye directamente en la reactividad del H2SO4. La alta electronegatividad del oxígeno crea centros de carga parcial negativa en los oxígenos y centros de carga parcial positiva en los hidrógenos y el azufre. Esto hace que la molécula sea muy susceptible a ataques nucleofílicos (en los centros positivos) y electrófilos (en los centros negativos), lo que contribuye a su naturaleza corrosiva y a su capacidad para reaccionar con una amplia variedad de sustancias, actuando como agente oxidante o deshidratante.
¿Se puede calcular la electronegatividad de una molécula entera?
No, la electronegatividad es una propiedad de los átomos dentro de un enlace. No se calcula una 'electronegatividad' para una molécula entera. Lo que se analiza es la electronegatividad de los átomos individuales y las diferencias entre ellos para determinar la polaridad de cada enlace y la polaridad general de la molécula (momento dipolar), así como su tipo de enlace predominante.
¿Qué papel juega el azufre en los enlaces del H2SO4?
El azufre actúa como el átomo central en la molécula de H2SO4. Su electronegatividad intermedia entre el oxígeno y el hidrógeno permite la formación de enlaces covalentes polares con el oxígeno. Además, el azufre puede expandir su octeto, lo que le permite formar cuatro enlaces con los oxígenos y contribuir a la estabilidad del ion sulfato a través de la resonancia.
En resumen, el ácido sulfúrico es un ejemplo fascinante de cómo la electronegatividad y la estructura molecular se combinan para definir las propiedades de una sustancia. Aunque sus enlaces internos son claramente covalentes polares, su comportamiento en solución, marcado por una disociación casi completa en iones, le confiere un carácter iónico superficial pero crucial. Esta dualidad es lo que lo convierte en un compuesto tan potente y versátil, un pilar indispensable en la química moderna y la industria.
Si quieres conocer otros artículos parecidos a H2SO4: Enlaces, Electronegatividad y Carácter Dual puedes visitar la categoría Química.