30/08/2022
La neutralización es una de las reacciones químicas más fundamentales, presente tanto en la naturaleza como en innumerables procesos industriales. Cuando un ácido y una base reaccionan, no solo se produce una sal y agua, sino que también se libera o absorbe energía en forma de calor. Este cambio energético es lo que conocemos como entalpía de neutralización, una magnitud crucial para comprender la termodinámica de las reacciones ácido-base. Medir y calcular esta entalpía nos permite no solo predecir el comportamiento energético de estas reacciones, sino también diseñar procesos más eficientes y seguros. En este artículo, exploraremos en detalle cómo se calcula la entalpía de neutralización, los factores que la influyen y las teorías que sustentan su comportamiento.
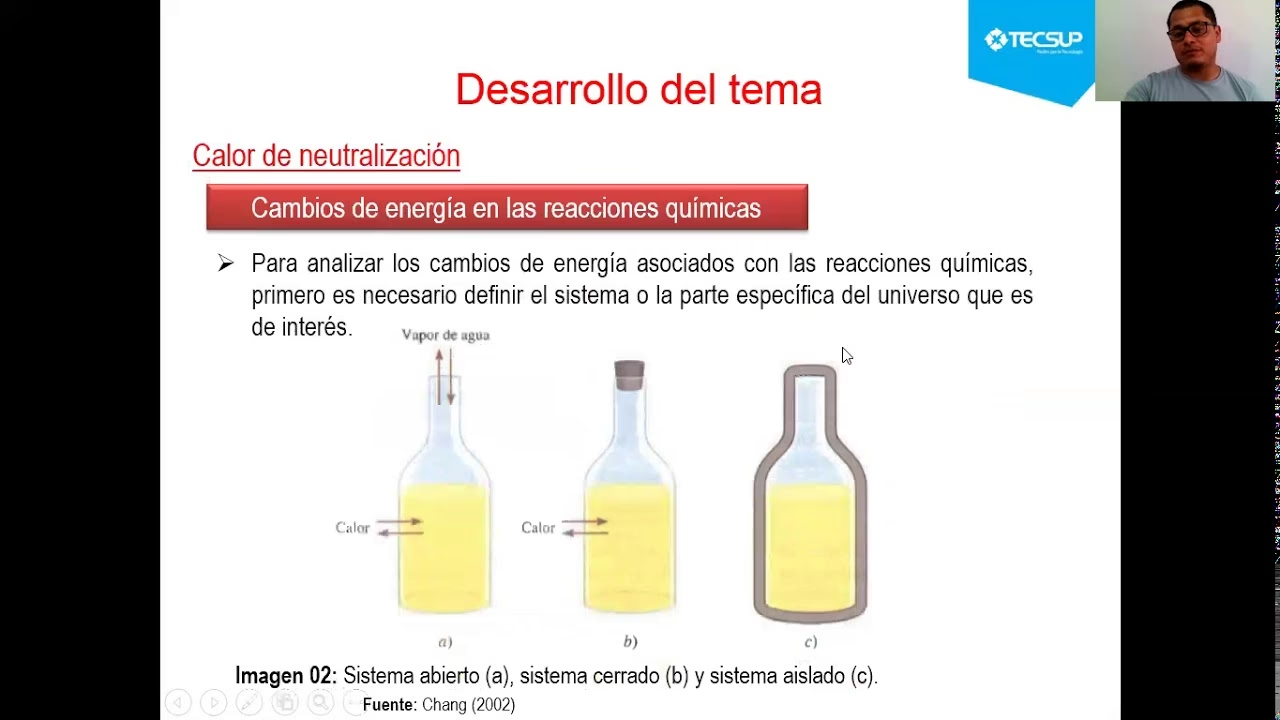
La entalpía de neutralización (ΔH) representa el cambio de calor que ocurre cuando un equivalente de ácido reacciona con un equivalente de base para formar un mol de agua. De manera general, el cambio de entalpía para cualquier reacción puede calcularse como la diferencia entre la suma de las entalpías de los productos y la suma de las entalpías de los reactivos:
ΔH = Σ entalpías de productos – Σ entalpías de reactivos
En el contexto de una reacción de neutralización llevada a cabo a presión atmosférica, este cambio de energía se manifiesta comúnmente como un aumento de temperatura en el sistema. Es precisamente este cambio de temperatura, medido con un termómetro, el que nos proporciona la información clave para determinar la cantidad de calor liberado o absorbido durante el proceso.
- Factores que Influyen en la Entalpía de Neutralización
- Fundamentos Teóricos: Las Teorías de Ácidos y Bases
- Factores Determinantes de la Fuerza de un Ácido
- Cálculo de la Entalpía Molar de Neutralización: Un Enfoque Práctico
- Diseño Experimental para la Determinación de ΔHneut
- Preguntas Frecuentes sobre la Entalpía de Neutralización
- ¿Qué es exactamente la entalpía de neutralización?
- ¿Por qué la entalpía de neutralización varía entre ácidos/bases fuertes y débiles?
- ¿Qué es un reactivo limitante en una reacción de neutralización y por qué es importante?
- ¿Cómo se relaciona la calorimetría con el cálculo de la entalpía de neutralización?
- ¿Cuál es el valor típico de la entalpía de neutralización para ácidos y bases fuertes?
- Conclusión
Factores que Influyen en la Entalpía de Neutralización
El valor de la entalpía de neutralización no es constante para todas las reacciones ácido-base. Depende fundamentalmente de la fuerza de los ácidos y bases que participan en la reacción. Esta relación es crucial para entender por qué algunas neutralizaciones liberan más calor que otras.
Fuerza de Ácidos y Bases: Un Impacto Directo en la Energía
Cuando los reactivos son ácidos y bases fuertes, se produce una disociación completa de sus moléculas en solución acuosa. Por ejemplo, en la reacción entre el ácido clorhídrico (HCl, un ácido fuerte) y el hidróxido de sodio (NaOH, una base fuerte), ambos se disocian completamente en iones H+, Cl-, Na+ y OH-. La reacción neta de neutralización es esencialmente la combinación de iones hidrógeno e iones hidroxilo para formar agua: H+(aq) + OH-(aq) → H2O(l). Esta reacción es altamente exotérmica y libera una cantidad de calor considerable y bastante consistente, alrededor de -57.3 kJ/mol, independientemente del ácido fuerte o la base fuerte utilizados.
Sin embargo, en el caso de un ácido débil o una base débil, la situación es diferente. La disociación de estas sustancias en solución no es completa. Una parte de la energía liberada durante la neutralización se utiliza para romper los enlaces moleculares de estos reactivos y permitir su disociación antes de que puedan reaccionar completamente. Este consumo de energía para la disociación interna significa que la cantidad de calor neto liberado al entorno es menor. Por lo tanto, el valor absoluto de la entalpía de neutralización disminuye a medida que la fuerza de los ácidos y las bases disminuye.
La siguiente tabla ilustra cómo el calor de neutralización varía con la fuerza de los ácidos y las bases:
| Ácido | Álcali | Calor de Neutralización (kJ/mol) |
|---|---|---|
| HNO3 | NaOH | 57.3 |
| 1/2 H2SO4 | NaOH | 57.3 |
| HCl | KOH | 57.3 |
| HNO3 | KOH | 57.3 |
| HNO3 | 1/2 Ca(OH)2 | 57.3 |
| H2S | NaOH | 16.0 |
| HCN | NaOH | 12.0 |
| HCl | NH3 | 51.5 |
| CH3COOH | NaOH | 55.0 |
Como se puede observar, las combinaciones de ácidos y bases fuertes (como HNO3/NaOH, HCl/KOH) muestran un calor de neutralización muy similar y elevado. Sin embargo, cuando intervienen ácidos débiles (H2S, HCN, CH3COOH) o bases débiles (NH3), los valores son significativamente menores, lo que confirma que parte de la energía se consume en la disociación.
Fundamentos Teóricos: Las Teorías de Ácidos y Bases
Para comprender a fondo la disociación de ácidos y bases y su impacto en la entalpía de neutralización, es fundamental revisar las principales teorías que definen estas sustancias. Cada una ofrece una perspectiva valiosa sobre su comportamiento en solución.
Teoría de Arrhenius: La Base de la Disociación Iónica
La teoría de Svante Arrhenius, propuesta a finales del siglo XIX, establece que los ácidos son sustancias que se disocian en agua para producir iones hidrógeno (H+), mientras que las bases son aquellas que se disocian para producir iones hidroxilo (OH-). Esta teoría es particularmente útil para entender la disociación de compuestos iónicos en medios acuosos. Por ejemplo, ácidos como el ácido clorhídrico (HCl), el ácido perclórico (HClO4), el ácido bromhídrico (HBr), el ácido nítrico (HNO3) y el ácido sulfúrico (H2SO4) se consideran ácidos fuertes porque se disocian completamente en sus iones constituyentes en un medio acuoso. De manera similar, bases fuertes como el hidróxido de calcio (Ca(OH)2), el hidróxido de litio (LiOH), el hidróxido de potasio (KOH) y el hidróxido de sodio (NaOH) se disocian completamente en una solución acuosa para liberar iones hidroxilo.
Sin embargo, la teoría de Arrhenius tiene limitaciones. Está restringida a soluciones acuosas y no explica la basicidad de sustancias como el amoníaco (NH3), que no poseen un grupo hidroxilo pero actúan como bases.
Teoría de Brönsted-Lowry: El Intercambio de Protones
Johannes Brönsted y Thomas Lowry propusieron una definición más amplia y general de ácidos y bases. Según su teoría, un ácido es una sustancia que dona iones hidrógeno (H+) o protones, y una base es una sustancia que acepta iones hidrógeno (H+) o protones. En otras palabras, los ácidos son donadores de protones, y las bases son aceptores de protones. Esta teoría es crucial para entender las reacciones en las que no interviene necesariamente el agua como disolvente o en las que se involucran sustancias que no cumplen la definición de Arrhenius.
Un concepto clave en esta teoría son los pares ácido-base conjugados, que son pares de sustancias que difieren en un solo protón. Si un ácido de Brönsted es fuerte, su base conjugada será débil y viceversa. Por ejemplo, ácidos fuertes como HClO4, HCl, HNO3 y HBr tienen bases conjugadas débiles (ClO4-, Cl-, NO3- y Br-). Por otro lado, ácidos débiles como el ácido nitroso (HNO2), el ácido fluorhídrico (HF) y el ácido acético (CH3COOH) tienen bases conjugadas fuertes (NO2-, F- y CH3COO-) que son muy buenos aceptores de protones.
Teoría de Lewis: La Aceptación y Donación de Pares de Electrones
Gilbert N. Lewis introdujo una teoría aún más general, definiendo un ácido como una especie que acepta un par de electrones (aceptor de electrones) y una base como una especie que dona un par de electrones (donador de electrones). Esta teoría amplía el concepto de ácido-base más allá de la transferencia de protones. Por ejemplo, si el trifluoruro de boro (BF3) reacciona con el amoníaco (NH3), el BF3 actúa como ácido aunque no tenga un protón para donar, porque acepta un par de electrones del NH3:
BF3 + :NH3 → BF3:NH3
Especies deficientes en electrones, como AlCl3, cationes metálicos (CO3+, Mg2+) y moléculas con orbitales vacíos, pueden actuar como ácidos de Lewis. Por el contrario, especies que pueden donar pares de electrones, como H2O, NH3 y OH-, actúan como bases de Lewis. Esta teoría es fundamental en la química orgánica y en la comprensión de las interacciones en complejos metálicos.
Factores Determinantes de la Fuerza de un Ácido
La fuerza de un ácido, es decir, el grado en que se disocia en iones H+, depende de varios factores intrínsecos a su estructura. Estos factores influyen directamente en la facilidad con la que un ácido libera su protón, lo que a su vez impacta en el calor liberado durante la neutralización.
Fuerza y Polaridad del Enlace HA
La extensión de la disociación ácida depende principalmente de la fuerza y la polaridad del enlace entre el hidrógeno y el átomo al que está unido (enlace H-A). Cuando la fuerza del enlace H-A disminuye, la energía requerida para romper ese enlace también disminuye. En consecuencia, el ácido H-A se vuelve más fuerte porque libera su protón con mayor facilidad. Por ejemplo, en los haluros de hidrógeno (HX), la fuerza del enlace disminuye a medida que bajamos en el grupo de los halógenos, lo que explica el aumento de la acidez de HF a HI.

Además, cuando el enlace H-A se vuelve más polar, es decir, cuando la diferencia de electronegatividad entre los átomos H y A aumenta, se produce una clara separación de carga (Hδ+-Aδ-). Esta polaridad facilita la ruptura heterolítica del enlace y, por lo tanto, la liberación del protón H+, haciendo que el ácido sea más fuerte.
Tamaño del Átomo A
En un grupo de la tabla periódica, a medida que el tamaño de los elementos aumenta, la fuerza del ácido también tiende a aumentar. Esto se debe a que un átomo más grande puede distribuir mejor la carga negativa del anión conjugado (A-) resultante después de la pérdida del protón, haciéndolo más estable. Por ejemplo, la fuerza ácida de los hidrácidos de halógenos aumenta significativamente a medida que el tamaño del halógeno aumenta:
Tamaño aumenta: HF << HCl << HBr << HI, fuerza ácida aumenta.
Electronegatividad del Átomo A
En un período de la tabla periódica, a medida que la electronegatividad del átomo A aumenta, la fuerza del ácido también se incrementa. Un átomo más electronegativo atrae más fuertemente los electrones del enlace H-A, haciendo que el hidrógeno sea más positivo y, por lo tanto, más fácil de liberar como protón. Esto se observa claramente en los hidruros de los elementos del segundo período:
Electronegatividad de A aumenta: CH4 < NH3 < H2O < HF, fuerza ácida aumenta.
Cálculo de la Entalpía Molar de Neutralización: Un Enfoque Práctico
La entalpía molar de neutralización, denotada como ΔHneut, es una medida más específica y estandarizada. Representa el flujo de calor asociado con la reacción de un mol de H+ con un mol de OH-. ΔHneut se determina generalmente midiendo el flujo de calor total (qneut) para la reacción de neutralización y dividiendo este valor por el número de moles (n) del reactivo limitante (H+ o OH-).
ΔHneut = qneut / nreactivo_limitante
En un experimento típico, una solución acuosa de ácido clorhídrico (HCl) se añade a una solución acuosa de hidróxido de sodio (NaOH). La reacción de neutralización ocurre hasta que el H+ o el OH- se consume por completo. El reactivo que se consume primero es el reactivo limitante, ya que determina la cantidad máxima de producto que se puede formar y, por lo tanto, la cantidad total de calor liberado para una cantidad dada de sustancias.
Es importante destacar que las grandes concentraciones de iones hidrógeno e iones hidroxilo no pueden coexistir en solución, ya que la reacción de neutralización (mostrada a continuación) favorece fuertemente la formación de agua:
H+(aq) + OH-(aq) → H2O(l)
La Calorimetría en Acción: Midiendo el Flujo de Calor
El objetivo principal de un experimento para determinar la entalpía molar de neutralización es utilizar la calorimetría. Un calorímetro es un dispositivo diseñado para medir el calor liberado o absorbido en una reacción química o un cambio físico. Para un calorímetro ideal, que sea perfectamente aislante y no permita que el calor entre o salga del sistema (es decir, del calorímetro y la solución), el principio de conservación de la energía establece que la suma de todos los flujos de calor dentro del sistema es cero:
0 = qcal + qaq + qneut
Donde:
qcales el calor absorbido o liberado por el calorímetro mismo.qaqes el calor absorbido o liberado por la solución acuosa combinada (HCl y NaOH mezclados).qneutes el calor liberado o absorbido por la reacción de neutralización.
Los valores de qcal y qaq se pueden determinar conociendo las capacidades caloríficas del calorímetro y de la solución, y el cambio de temperatura del sistema. Una vez que se conocen qcal y qaq, se puede calcular qneut, que es el calor generado directamente por la reacción. Es crucial recordar que si la reacción es exotérmica (libera calor), qneut será negativo, y este calor será absorbido por la solución (qaq > 0) y el calorímetro (qcal > 0).
Diseño Experimental para la Determinación de ΔHneut
Un montaje experimental típico para determinar la entalpía molar de neutralización consiste en un calorímetro que contiene una solución de hidróxido de sodio (NaOH) de concentración conocida (por ejemplo, 1.00 M) y un recipiente o bureta que contiene una solución de ácido clorhídrico (HCl) de concentración también conocida (por ejemplo, 2.00 M). El procedimiento se lleva a cabo de la siguiente manera:
- Se introduce un volumen específico de la solución de NaOH (por ejemplo, entre 80 y 200 mL) en el calorímetro.
- Se introduce un volumen específico de la solución de HCl (por ejemplo, entre 20 y 100 mL) en el recipiente auxiliar o bureta.
- Se registra la temperatura inicial (Ti) del sistema. Es importante que el calorímetro, la solución de NaOH y la solución de HCl estén inicialmente a la misma temperatura para asegurar un punto de partida uniforme.
- Se inicia la mezcla. La solución de HCl se drena o se añade cuidadosamente al calorímetro que contiene la solución de NaOH. A medida que las soluciones se mezclan, se produce la reacción de neutralización.
- Se monitorea la temperatura de la solución de reacción. Después de que se ha alcanzado el equilibrio térmico (es decir, la temperatura deja de cambiar), se registra la temperatura final (Tf).
- Con los datos de temperatura (ΔT = Tf - Ti), los volúmenes y las capacidades caloríficas de las soluciones y el calorímetro, se calcula el calor total transferido (qcal y qaq). A partir de esto, se determina qneut.
- Finalmente, se identifica cuál de los reactivos, HCl o NaOH, es el reactivo limitante. Se calcula el número de moles de H+ y OH- que reaccionaron y se utiliza el número de moles del reactivo limitante para calcular la entalpía molar de neutralización (ΔHneut), expresándola en unidades de kJ mol-1.
Es fundamental repetir el experimento varias veces con diferentes volúmenes o concentraciones, si es posible, para asegurar la reproducibilidad de los resultados y para obtener un valor promedio de ΔHneut dentro del error experimental aceptable.
Preguntas Frecuentes sobre la Entalpía de Neutralización
¿Qué es exactamente la entalpía de neutralización?
Es el cambio de entalpía (calor) que ocurre cuando un ácido y una base reaccionan para formar una sal y agua. Específicamente, para ácidos y bases fuertes, se refiere al calor liberado cuando un mol de iones H+ reacciona con un mol de iones OH- para formar un mol de agua líquida.
¿Por qué la entalpía de neutralización varía entre ácidos/bases fuertes y débiles?
Para ácidos y bases fuertes, la disociación es completa, y el calor liberado es casi constante porque la reacción fundamental es siempre H+ + OH- → H2O. Para ácidos o bases débiles, parte de la energía liberada en la formación de agua se consume para disociar las moléculas no ionizadas del ácido o base débil, lo que resulta en un valor absoluto de entalpía de neutralización menor.
¿Qué es un reactivo limitante en una reacción de neutralización y por qué es importante?
El reactivo limitante es el ácido o la base que se consume completamente primero en la reacción. Es importante porque la cantidad de calor total liberado (qneut) y, por lo tanto, el cálculo de la entalpía molar de neutralización (ΔHneut), se basa en los moles del reactivo limitante, ya que este determina la extensión máxima de la reacción.
¿Cómo se relaciona la calorimetría con el cálculo de la entalpía de neutralización?
La calorimetría es la técnica experimental utilizada para medir el calor liberado o absorbido durante una reacción. Al medir el cambio de temperatura del sistema (solución y calorímetro), y conociendo sus capacidades caloríficas, se puede calcular el calor total transferido, lo que a su vez permite determinar el calor específico de la reacción de neutralización.
¿Cuál es el valor típico de la entalpía de neutralización para ácidos y bases fuertes?
Para la neutralización de un ácido fuerte con una base fuerte en solución acuosa, el valor de la entalpía de neutralización es aproximadamente -57.3 kJ/mol (el signo negativo indica que es una reacción exotérmica, es decir, libera calor).
Conclusión
La entalpía de neutralización es un concepto termoquímico fundamental que nos permite cuantificar la energía liberada o absorbida durante las reacciones ácido-base. Hemos visto cómo su valor depende intrínsecamente del grado de disociación de los ácidos y las bases que participan en la mezcla de reacción, lo cual, a su vez, está directamente relacionado con su fuerza. Las teorías de Arrhenius, Brönsted-Lowry y Lewis nos proporcionan el marco conceptual necesario para comprender esta disociación, desde la formación de iones en soluciones acuosas hasta la transferencia de protones y la donación/aceptación de pares de electrones.
Además, hemos explorado cómo factores estructurales como la fuerza y polaridad del enlace, el tamaño y la electronegatividad del átomo central influyen en la fuerza de un ácido y, por ende, en la eficiencia de su neutralización. Finalmente, la calorimetría se revela como la herramienta experimental indispensable para la determinación práctica de la entalpía molar de neutralización, permitiéndonos medir con precisión el calor liberado y relacionarlo con el número de moles del reactivo limitante. Comprender estos principios no solo es esencial para la química básica, sino que tiene implicaciones significativas en campos que van desde la bioquímica hasta la ingeniería química, donde el control de la energía es clave para el éxito de los procesos.
Si quieres conocer otros artículos parecidos a Entalpía de Neutralización: Cálculo y Factores Clave puedes visitar la categoría Química.
