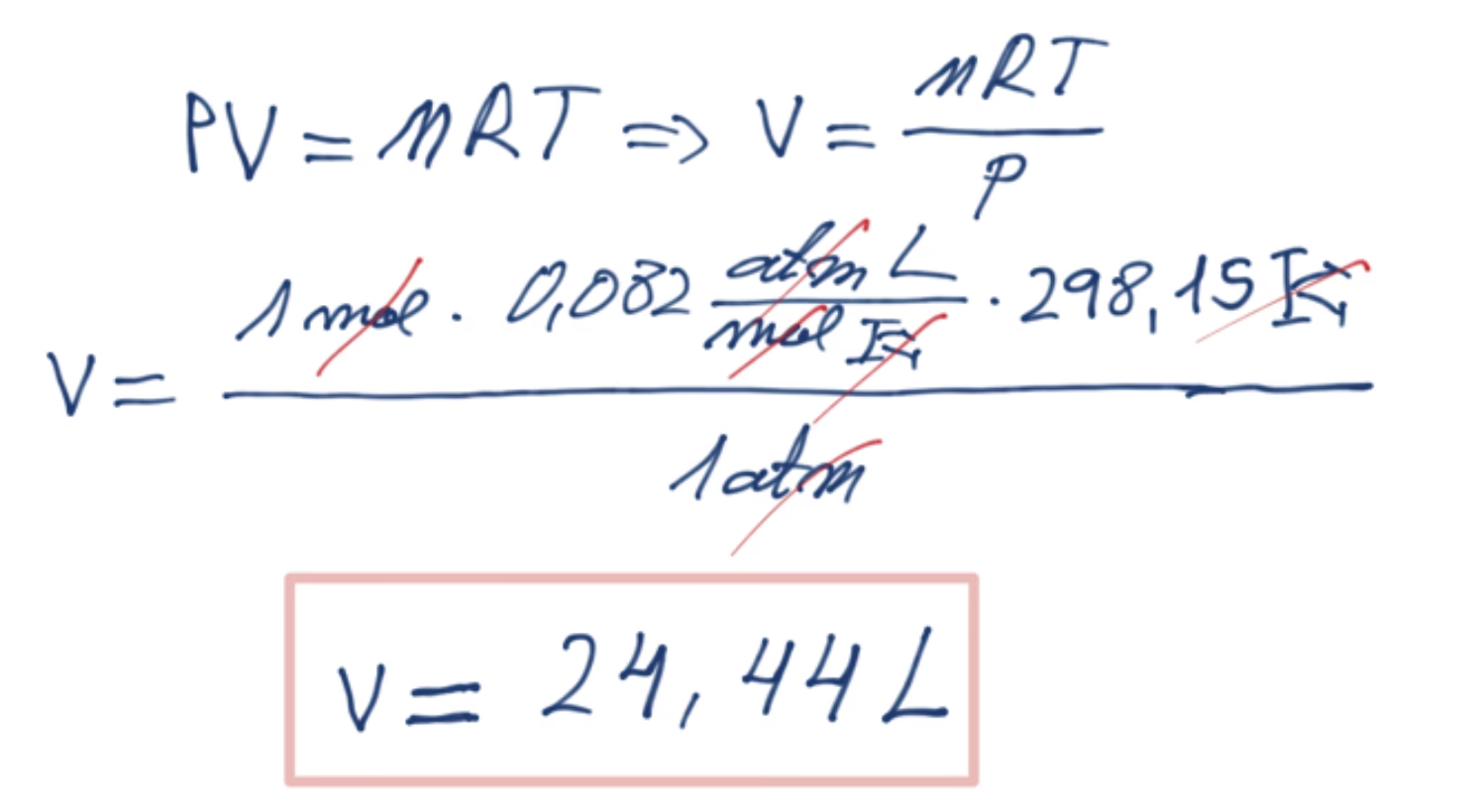08/11/2022
La química de los gases es un campo fascinante que nos permite entender cómo se comportan estas sustancias volátiles bajo diferentes condiciones. Uno de los conceptos más fundamentales y a menudo malinterpretados es el de las Condiciones Normales de Presión y Temperatura, universalmente conocidas como STP (Standard Temperature and Pressure). Comprender qué son las STP y cómo afectan el volumen de los gases es crucial para cualquier estudiante o profesional de la química. Pero, ¿sabes realmente cómo calcular los moles de un gas en estas condiciones o, incluso más importante, cómo se relaciona el volumen molar con la famosa constante de 22.4 litros por mol? Este artículo desglosará cada aspecto, ofreciéndote una guía completa para dominar los cálculos de gases, tanto en condiciones normales como en escenarios más complejos.
A menudo, la clave para resolver problemas de química de gases radica en saber cuándo aplicar la fórmula simplificada de STP y cuándo es imperativo recurrir a la poderosa Ley de los Gases Ideales. Te guiaremos a través de ejemplos prácticos y te daremos las herramientas para identificar la mejor estrategia en cada situación. Prepárate para desmitificar la relación entre moles, volumen, presión y temperatura, y para descubrir la elegancia de las leyes que rigen el comportamiento de los gases.
- ¿Qué son las Condiciones Normales (STP)?
- El Concepto Crucial: Volumen Molar en STP
- Calculando Moles y Volumen Bajo Condiciones Normales
- Más Allá de STP: La Ley de los Gases Ideales
- Ejemplos Prácticos y Soluciones Detalladas
- Ejemplo 1: Calcular el volumen de un gas a STP a partir de condiciones no estándar.
- Ejemplo 2: Calcular el volumen molar de un gas a STP a partir de condiciones no estándar.
- Ejemplo 3: Calcular el volumen de moles de gas a STP.
- Ejemplo 4: Calcular el volumen de una masa de gas a STP.
- Ejemplo 5: Determinar el volumen molar a una temperatura diferente.
- Ejemplo 6: Determinar la masa molar de un gas a STP.
- Consideraciones Clave para Evitar Errores
- Preguntas Frecuentes (FAQ)
- ¿Cuál es la fórmula para los moles en condiciones normales (STP)?
- ¿Por qué el volumen molar a STP es 22.4 L/mol?
- ¿Puedo usar siempre 22.4 L/mol para calcular el volumen o los moles de un gas?
- ¿Cómo calcular el volumen molar fuera de las condiciones normales?
- ¿Qué es la constante de los gases ideales (R) y qué valor debo usar?
- ¿Qué pasa si tengo una mezcla de gases a STP?
- Conclusión
¿Qué son las Condiciones Normales (STP)?
Las Condiciones Normales de Presión y Temperatura, o STP, son un conjunto de condiciones estándar utilizadas en química y física para facilitar la comparación de volúmenes de gases. Es un punto de referencia esencial que permite a los científicos hablar de manera uniforme sobre el comportamiento de los gases. En el sistema STP, la temperatura y la presión se definen con valores específicos que son universalmente aceptados.
Tradicionalmente, las condiciones STP se definen de la siguiente manera:
- Temperatura (T): 273.15 Kelvin (K), que equivale a 0 grados Celsius (°C). Este valor se elige porque es el punto de congelación del agua.
- Presión (P): 1 atmósfera (atm), que es igual a 760 milímetros de mercurio (mmHg) o 760 torr. También puede expresarse como 101.325 kilopascales (kPa) o 101325 pascales (Pa).
Es importante destacar que, aunque estas son las definiciones más comunes para STP, existen otras definiciones de condiciones estándar (por ejemplo, IUPAC ha propuesto diferentes estándares). Sin embargo, en el contexto de los cálculos de gases en la mayoría de los cursos introductorios y avanzados, se hace referencia a los valores de 273 K y 760 torr/1 atm.
Estas condiciones son fundamentales porque, bajo ellas, un mol de cualquier gas ideal ocupa un volumen específico, lo que simplifica enormemente muchos cálculos. Comprender y recordar estos valores es el primer paso para dominar la química de los gases.
El Concepto Crucial: Volumen Molar en STP
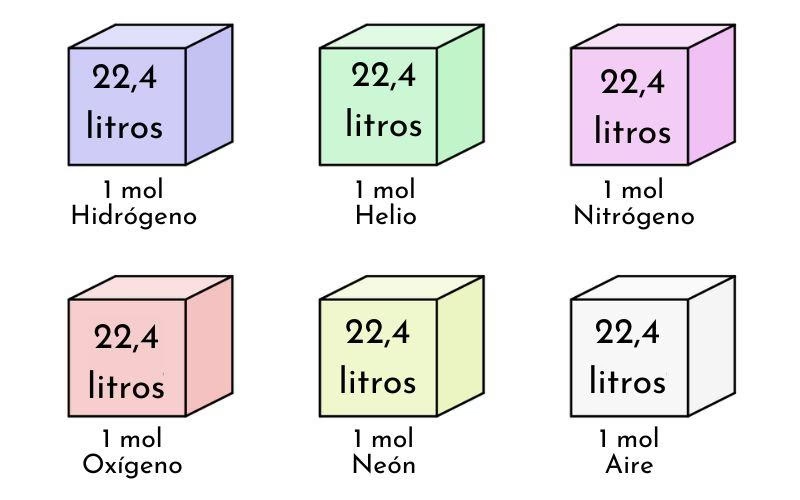
El volumen molar es uno de los conceptos más importantes cuando se trabaja con gases en condiciones STP. Se define como el volumen ocupado por un mol de cualquier gas ideal bajo estas condiciones estándar. Y aquí viene la cifra mágica: un mol de cualquier gas ideal a STP ocupa un volumen de 22.4 litros. Más precisamente, el valor es 22.414 L/mol, aunque 22.4 L/mol es suficiente para la mayoría de los cálculos prácticos.
¿De dónde proviene este valor? No es una constante de la naturaleza como la velocidad de la luz, sino una consecuencia directa de la Ley de los Gases Ideales, PV = nRT, aplicada a las condiciones STP. Vamos a desglosarlo:
La Ley de los Gases Ideales establece la relación entre la presión (P), el volumen (V), el número de moles (n), la constante de los gases ideales (R) y la temperatura (T). La fórmula es:
PV = nRT
Donde:
- P es la presión del gas (en atmósferas).
- V es el volumen del gas (en litros).
- n es el número de moles del gas.
- R es la constante de los gases ideales, cuyo valor es 0.08206 L·atm/(mol·K).
- T es la temperatura del gas (en Kelvin).
Para derivar el volumen molar a STP, configuramos la ecuación para un mol de gas (n=1 mol) a las condiciones STP:
- P = 1 atm
- T = 273.15 K
- n = 1 mol
- R = 0.08206 L·atm/(mol·K)
Sustituyendo estos valores en la Ley de los Gases Ideales y despejando V (el volumen molar):
(1 atm) * V = (1 mol) * (0.08206 L·atm/(mol·K)) * (273.15 K)
V = (1 * 0.08206 * 273.15) L
V ≈ 22.414 L
Así, se confirma que un mol de cualquier gas ideal ocupa aproximadamente 22.4 litros a STP. Este valor simplifica muchos cálculos, ya que no necesitamos la Ley de los Gases Ideales completa si estamos seguros de que las condiciones son STP.
Calculando Moles y Volumen Bajo Condiciones Normales
Ahora que entendemos el volumen molar en STP, veamos cómo aplicarlo para calcular moles o volúmenes en estas condiciones. La simplicidad de usar 22.4 L/mol es su mayor ventaja.
1. Si tienes la cantidad de gas en moles:
Para encontrar el volumen que ocupa un gas a STP, simplemente multiplica el número de moles por 22.4 L/mol.
Volumen (L) = Moles (mol) × 22.4 L/mol
Ejemplo: Si tienes 2 moles de gas nitrógeno (N₂), ¿qué volumen ocupará a STP?
Volumen = 2 mol × 22.4 L/mol = 44.8 L
2. Si tienes la masa del gas:
Si conoces la masa del gas, primero debes convertirla a moles utilizando la masa molar (peso molecular) del gas. Luego, usa la relación de 22.4 L/mol.
Moles (mol) = Masa (g) / Masa Molar (g/mol)
Volumen (L) = Moles (mol) × 22.4 L/mol
Ejemplo: ¿Qué volumen ocuparán 96 gramos de oxígeno (O₂) a STP?
- Primero, calcula los moles de O₂. La masa molar de O₂ es 2 × 16 g/mol = 32 g/mol.
Moles de O₂ = 96 g / 32 g/mol = 3 mol- Luego, calcula el volumen:
Volumen = 3 mol × 22.4 L/mol = 67.2 L
3. Para una mezcla de gases a STP:
Si tienes una mezcla de varios gases, puedes calcular el volumen de cada componente por separado como si estuvieran solos, y luego sumarlos. Esto es posible porque tanto la temperatura como la presión se mantienen constantes en STP, y el volumen total de una mezcla de gases ideales es la suma de los volúmenes de sus componentes (Ley de Dalton de las presiones parciales y Ley de Amagat de los volúmenes parciales).
Volumen Total = Volumen_Gas1 + Volumen_Gas2 + ...
Alternativamente, puedes calcular el número total de moles en la mezcla y luego multiplicarlo por 22.4 L/mol.
Más Allá de STP: La Ley de los Gases Ideales
Aunque el volumen molar a STP es una herramienta poderosa, es fundamental recordar que solo se aplica estrictamente cuando las condiciones son precisamente STP (273.15 K y 1 atm/760 torr). ¿Qué sucede si la temperatura o la presión no son las estándar? Aquí es donde la Ley de los Gases Ideales (PV = nRT) se convierte en tu mejor aliada. Esta ley es mucho más versátil y puede utilizarse para cualquier condición de presión y temperatura, siempre que el gas se comporte como un gas ideal.
La Ley de los Gases Ideales es tu fórmula de referencia para situaciones no estándar. Los componentes de la ecuación son:
- P: Presión. Asegúrate de que las unidades sean consistentes con la constante R que utilices (generalmente atmósferas o pascales).
- V: Volumen. Generalmente en litros (L) o metros cúbicos (m³).
- n: Número de moles.
- R: La constante de los gases ideales. Su valor varía dependiendo de las unidades de presión y volumen que uses. Los valores comunes son:
- 0.08206 L·atm/(mol·K) (cuando P está en atm y V en L)
- 8.314 J/(mol·K) o 8.314 Pa·m³/(mol·K) (cuando P está en Pa y V en m³)
- T: Temperatura absoluta. Siempre debe estar en Kelvin (K). Para convertir de grados Celsius a Kelvin, usa la fórmula:
K = °C + 273.15.
Es vital que todas las unidades de tus variables coincidan con las unidades de la constante R que elijas. La inconsistencia de unidades es una fuente común de errores en los cálculos de gases.
Fórmula para Ajustar Volumen a STP desde Otras Condiciones:
A veces, se te dará el volumen de un gas a ciertas condiciones (P, T) y se te pedirá que calcules su volumen si estuviera a STP (V_STP). Esto se puede hacer combinando la Ley de Boyle (P₁V₁ = P₂V₂) y la Ley de Charles (V₁/T₁ = V₂/T₂), resultando en la Ley Combinada de los Gases:
(P₁V₁)/T₁ = (P₂V₂)/T₂
Donde P₁, V₁, T₁ son las condiciones iniciales y P₂, V₂, T₂ son las condiciones finales (en este caso, STP). Despejando V_STP (V₂):
V_STP = V * (T_STP/T) * (P/P_STP)
Donde:
- V es el volumen inicial.
- T es la temperatura inicial (en K).
- P es la presión inicial (en las mismas unidades que P_STP).
- T_STP = 273 K.
- P_STP = 760 torr (o 1 atm, según la unidad de P).
Ejemplos Prácticos y Soluciones Detalladas
Vamos a aplicar lo aprendido con algunos ejemplos, incluyendo los proporcionados, para solidificar tu comprensión de los cálculos de gases.
Ejemplo 1: Calcular el volumen de un gas a STP a partir de condiciones no estándar.
Problema: El volumen de un gas es de 0.5 L a una presión de 700 torr y una temperatura de 300 K. Calcula el volumen de este gas a STP.
Respuesta:
- Datos iniciales: V = 0.5 L, P = 700 torr, T = 300 K.
- Condiciones STP: P_STP = 760 torr, T_STP = 273 K.
Usamos la fórmula de ajuste de volumen a STP:
V_STP = V * (T_STP/T) * (P/P_STP)
V_STP = 0.5 L * (273 K / 300 K) * (700 torr / 760 torr)
V_STP = 0.5 * 0.91 * 0.92105
V_STP ≈ 0.419 L
Por lo tanto, el volumen del gas a STP sería aproximadamente 0.419 litros.

Ejemplo 2: Calcular el volumen molar de un gas a STP a partir de condiciones no estándar.
Problema: A 1100 torr y 350 K, el volumen de un gas es de 30 L. Calcula el volumen molar de este gas a STP.
Respuesta:
- Datos iniciales: V = 30 L, P = 1100 torr, T = 350 K.
- Condiciones STP: P_STP = 760 torr, T_STP = 273 K.
Usamos la misma fórmula de ajuste de volumen a STP:
V_STP = V * (T_STP/T) * (P/P_STP)
V_STP = 30 L * (273 K / 350 K) * (1100 torr / 760 torr)
V_STP = 30 * 0.78 * 1.447
V_STP ≈ 33.868 L
Este resultado nos da el volumen que ocuparía esa cantidad específica de gas si se llevara a condiciones STP. Para obtener el volumen *molar* a STP, necesitaríamos saber el número de moles de ese gas en los 30 L iniciales, y luego dividir el V_STP calculado por ese número de moles. Sin embargo, el problema pide 'el volumen molar de un gas a STP', que por definición es 22.4 L/mol para un gas ideal. La pregunta parece estar formulada para calcular el volumen *equivalente* a STP para la cantidad de gas dada.
Ejemplo 3: Calcular el volumen de moles de gas a STP.
Problema: Tienes 2.00 moles de H₂ seco a STP. ¿Cuántos litros son?
Respuesta:
Dado que las condiciones son STP, podemos usar directamente el volumen molar:
Volumen = Moles × Volumen Molar a STP
Volumen = 2.00 mol × 22.414 L/mol = 44.828 L ≈ 44.8 L (a tres cifras significativas)
Ejemplo 4: Calcular el volumen de una masa de gas a STP.
Problema: 0.250 moles de HCl ocuparán ¿cuántos litros a STP?
Respuesta:
Similar al ejemplo anterior, las condiciones son STP:
Volumen = 0.250 mol × 22.414 L/mol = 5.6035 L ≈ 5.60 L (a tres cifras significativas)
Ejemplo 5: Determinar el volumen molar a una temperatura diferente.
Problema: ¿Cuál es el volumen molar a 576 K?
Respuesta:
El término 'volumen molar' aquí se refiere al volumen que ocuparía 1 mol de gas a la temperatura especificada, asumiendo una presión de 1 atm (condiciones estándar, pero no *normales* de temperatura). Podemos usar la Ley de Charles (V₁/T₁ = V₂/T₂) o la Ley de los Gases Ideales.
Usando la Ley de Charles, con V₁ = 22.414 L (volumen molar a STP) y T₁ = 273 K:
22.414 L / 273 K = V₂ / 576 K
V₂ = (22.414 L / 273 K) * 576 K
V₂ ≈ 47.2 L (a tres cifras significativas)
Alternativamente, usando PV=nRT para n=1 mol, P=1 atm, T=576 K, R=0.08206 L·atm/(mol·K):
(1 atm) * V = (1 mol) * (0.08206 L·atm/(mol·K)) * (576 K)
V = 0.08206 * 576 = 47.2896 L ≈ 47.3 L
La pequeña diferencia se debe al redondeo de las cifras significativas en el primer método.
Ejemplo 6: Determinar la masa molar de un gas a STP.
Problema: Determina la masa molar de un gas si una muestra de 0.250 g ocupa 0.200 L a STP.
Respuesta:
Primero, podemos calcular los moles de gas presentes usando el volumen molar a STP:
Moles = Volumen / Volumen Molar a STP
Moles = 0.200 L / 22.414 L/mol ≈ 0.008923 mol
Ahora que tenemos la masa (0.250 g) y los moles (0.008923 mol), podemos calcular la masa molar:
Masa Molar = Masa / Moles
Masa Molar = 0.250 g / 0.008923 mol ≈ 28.017 g/mol ≈ 28.0 g/mol
Este es un excelente ejemplo de cómo el conocimiento del volumen molar a STP puede simplificar los cálculos de masa molar.
Consideraciones Clave para Evitar Errores
Para garantizar la precisión en tus cálculos de gases, ten en cuenta las siguientes consideraciones:
- Unidades: La consistencia de las unidades es la clave. Asegúrate de que todas las variables en tus ecuaciones estén en las unidades correctas, especialmente al usar la constante de los gases ideales (R). Si R está en L·atm/(mol·K), tu volumen debe estar en litros, la presión en atmósferas y la temperatura en Kelvin.
- Temperatura en Kelvin: Nunca uses grados Celsius en la Ley de los Gases Ideales o en cualquier cálculo que involucre la temperatura de un gas, a menos que sea para una diferencia de temperatura. ¡Siempre convierte a Kelvin!
- Cuándo usar 22.4 L/mol vs. PV=nRT: La regla de oro es: usa 22.4 L/mol solo si las condiciones son *exactamente* STP. Para cualquier otra condición de temperatura o presión, la Ley de los Gases Ideales (PV=nRT) es indispensable. No intentes forzar el uso de 22.4 L/mol en situaciones no STP, ya que te llevará a resultados incorrectos.
- Gas Ideal vs. Gas Real: Todas estas leyes y el valor de 22.4 L/mol se basan en el comportamiento de un gas ideal. Los gases reales se desvían de este comportamiento, especialmente a altas presiones y bajas temperaturas. Sin embargo, para la mayoría de los problemas de química general, se asume el comportamiento ideal.
Dominar estas consideraciones te permitirá abordar con confianza una amplia gama de problemas de gases.
Preguntas Frecuentes (FAQ)
¿Cuál es la fórmula para los moles en condiciones normales (STP)?
En condiciones normales (STP), un mol de cualquier gas ideal ocupa 22.4 litros. Por lo tanto, si conoces el volumen (V) de un gas a STP, puedes calcular los moles (n) usando la fórmula: n = V / 22.4 L/mol. Si conoces la masa (m) del gas, primero calcula los moles dividiendo la masa por la masa molar (MM) del gas: n = m / MM.
¿Por qué el volumen molar a STP es 22.4 L/mol?
El valor de 22.4 L/mol para el volumen molar a STP se deriva de la Ley de los Gases Ideales (PV = nRT). Al sustituir los valores de STP (P=1 atm, T=273.15 K) y n=1 mol, junto con la constante de los gases ideales R=0.08206 L·atm/(mol·K), se resuelve para V, obteniendo aproximadamente 22.414 L.
¿Puedo usar siempre 22.4 L/mol para calcular el volumen o los moles de un gas?
No, solo puedes usar 22.4 L/mol cuando las condiciones del gas son exactamente las Condiciones Normales de Presión y Temperatura (STP: 273.15 K y 1 atm o 760 torr). Si la temperatura o la presión son diferentes de las condiciones STP, debes usar la Ley de los Gases Ideales (PV = nRT) para realizar tus cálculos.
¿Cómo calcular el volumen molar fuera de las condiciones normales?
Para calcular el volumen molar (el volumen que ocupa un mol de gas) fuera de las condiciones normales, debes usar la Ley de los Gases Ideales: V = (nRT) / P. Donde n=1 mol, y P y T son las condiciones específicas del problema. Por ejemplo, a 576 K y 1 atm, un mol de gas ocuparía (1 mol * 0.08206 L·atm/(mol·K) * 576 K) / 1 atm = 47.2896 L.
¿Qué es la constante de los gases ideales (R) y qué valor debo usar?
La constante de los gases ideales (R) es una constante de proporcionalidad en la Ley de los Gases Ideales (PV=nRT). Su valor numérico depende de las unidades utilizadas para la presión, el volumen y la temperatura. El valor más comúnmente utilizado en problemas de química con presión en atmósferas y volumen en litros es 0.08206 L·atm/(mol·K). Si trabajas con unidades SI (pascales para presión, metros cúbicos para volumen), usarías 8.314 J/(mol·K) o 8.314 Pa·m³/(mol·K).
¿Qué pasa si tengo una mezcla de gases a STP?
Si tienes una mezcla de gases a STP, puedes tratar la mezcla como un solo gas ideal. El volumen total ocupado por la mezcla será la suma de los volúmenes que cada gas ocuparía si estuviera solo, o puedes calcular el número total de moles de todos los gases en la mezcla y multiplicarlo por 22.4 L/mol para obtener el volumen total. Esto se basa en la Ley de Dalton de las presiones parciales y la Ley de Amagat de los volúmenes parciales, que establecen que los gases ideales no interactúan entre sí.
Conclusión
La capacidad de calcular moles y volúmenes de gases, tanto en las simplificadas Condiciones Normales (STP) como en escenarios más complejos utilizando la Ley de los Gases Ideales, es una habilidad fundamental en química. Hemos explorado que el volumen molar de 22.4 L/mol es una herramienta poderosa para cálculos rápidos a STP, pero hemos enfatizado que la versatilidad de la Ley de los Gases Ideales (PV=nRT) es indispensable para cualquier otra condición. La clave del éxito radica en comprender cuándo y cómo aplicar cada fórmula, prestando siempre atención a las unidades y asegurándote de que la temperatura esté siempre en Kelvin.
Al dominar estos conceptos y las herramientas proporcionadas, estarás bien equipado para resolver una amplia gama de problemas de gases, desde los más básicos hasta los más desafiantes. Recuerda que la práctica es esencial, y cada problema resuelto te acerca un paso más a la maestría en la química de los gases.
Si quieres conocer otros artículos parecidos a Moles y Volumen: Guía Completa en Condiciones Normales puedes visitar la categoría Química.