22/09/2023
En el vasto universo de la química, comprender las propiedades de la materia es fundamental. Desde la cantidad de sustancia hasta el espacio que ocupa, cada concepto nos acerca a desentrañar los secretos de los compuestos. Uno de estos conceptos cruciales es el Volumen Molar, una medida que nos permite relacionar la cantidad de una sustancia (expresada en moles) con el volumen que esta ocupa. Este artículo desglosará qué es el volumen molar, cómo se calcula, su relevancia en distintas áreas de la química y cómo se aplica en la vida real, proporcionando una comprensión profunda y práctica de este fascinante concepto.
- ¿Qué es el Volumen Molar? Una Definición Clara
- La Fórmula del Volumen Molar: Desglosando sus Componentes
- Condiciones Estándar de Temperatura y Presión (STP): Un Punto de Referencia Crucial
- Cálculo Práctico del Volumen Molar: Ejemplos Resueltos
- La Importancia y Aplicaciones del Volumen Molar en la Química
- Volumen Molar para Diferentes Estados de la Materia: Gases, Líquidos y Sólidos
- Tabla Comparativa de Volúmenes Molares (Ejemplos)
- Preguntas Frecuentes (FAQ) sobre el Volumen Molar
- Conclusión
¿Qué es el Volumen Molar? Una Definición Clara
El Volumen Molar (Vm) de una sustancia es el volumen ocupado por un mol de esa sustancia, ya sea un elemento químico o un compuesto químico. Es una propiedad intensiva de la materia, lo que significa que no depende de la cantidad de sustancia presente, sino de su naturaleza y de las condiciones de temperatura y presión. Nos proporciona una visión de cuán 'espaciosa' es una molécula o un átomo dado en su estado particular.
Este concepto es particularmente relevante cuando hablamos de gases, ya que, bajo ciertas condiciones, todos los gases ideales exhiben un comportamiento predecible en términos de su volumen molar. Sin embargo, el volumen molar también se aplica a líquidos y sólidos, aunque con valores muy diferentes debido a las fuerzas intermoleculares y el empaquetamiento de las partículas.
La Fórmula del Volumen Molar: Desglosando sus Componentes
El volumen molar se puede calcular a partir de dos propiedades fundamentales de una sustancia: su Masa Molar y su Densidad. La relación se expresa mediante la siguiente fórmula:
Vm = \( \frac{Masa\ Molar}{Densidad} \)
Donde:
- Vm es el volumen molar, generalmente expresado en litros por mol (L/mol) o mililitros por mol (mL/mol).
- Masa Molar (M) es la masa de un mol de una sustancia, expresada en gramos por mol (g/mol). Para un compuesto, la masa molar se calcula sumando las masas atómicas de todos los átomos presentes en su fórmula química. Por ejemplo, la masa molar del agua (H2O) es la suma de dos veces la masa atómica del hidrógeno más la masa atómica del oxígeno.
- Densidad (ρ) es la masa de una sustancia por unidad de volumen, comúnmente expresada en gramos por litro (g/L) para gases o gramos por mililitro (g/mL) para líquidos y sólidos. La densidad mide cuán compacta es la materia.
Como se puede observar en la fórmula, el volumen molar es directamente proporcional a la masa molar (a mayor masa molar, mayor volumen molar para una densidad dada) e inversamente proporcional a la densidad (a mayor densidad, menor volumen molar para una masa molar dada). Esta relación lógica nos permite entender cómo el empaquetamiento de las moléculas afecta el espacio que ocupa un mol de sustancia.
Condiciones Estándar de Temperatura y Presión (STP): Un Punto de Referencia Crucial
Cuando hablamos de gases, un término que surge constantemente en relación con el volumen molar es STP (Standard Temperature and Pressure), o Condiciones Estándar de Temperatura y Presión. Estas condiciones se definen de la siguiente manera:
- Temperatura Estándar: 0°C (que equivale a 273.15 Kelvin).
- Presión Estándar: 1 atmósfera (atm), lo que también se puede expresar como 760 milímetros de mercurio (mmHg) o 101.325 kilopascales (kPa).
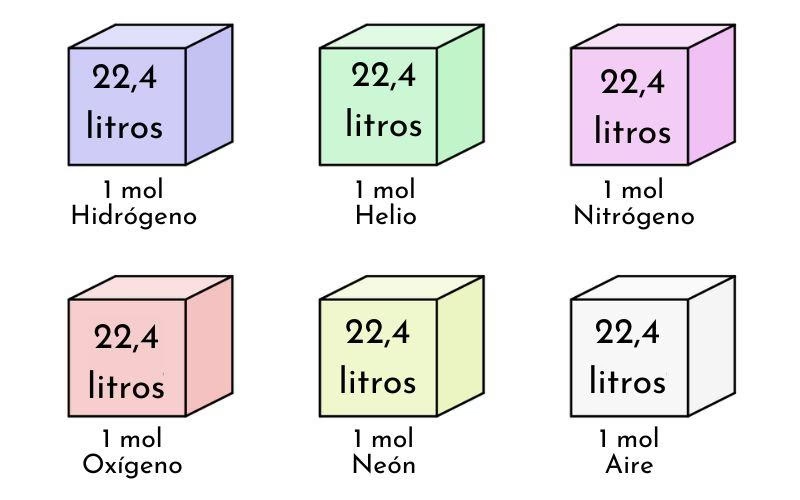
Bajo estas condiciones específicas, la comunidad científica ha determinado experimentalmente que un mol de cualquier gas ideal ocupa un volumen de aproximadamente 22.4 litros. Este valor es una constante muy útil en química y a menudo se utiliza en cálculos estequiométricos para gases. Es importante recordar que este valor de 22.4 litros es una aproximación para gases ideales; los gases reales pueden desviarse ligeramente de este valor debido a las interacciones intermoleculares y al volumen real de sus partículas, especialmente a presiones altas o temperaturas bajas.

La importancia del STP radica en que proporciona un punto de referencia universal para comparar el comportamiento de diferentes gases. Permite a los científicos y estudiantes realizar cálculos consistentes y predecir volúmenes de gases sin necesidad de conocer la identidad específica del gas, siempre y cuando se comporte de manera ideal.
Cálculo Práctico del Volumen Molar: Ejemplos Resueltos
Para consolidar la comprensión del cálculo del volumen molar, veamos un ejemplo práctico utilizando la fórmula que hemos discutido.
Ejemplo 1: Cálculo del Volumen Molar del Nitrógeno (N2)
Problema: Calcule el volumen molar de una muestra de gas nitrógeno (N2) si la Densidad del gas es 1.250 g/L.
Solución:
- Paso 1: Identificar la Masa Molar (M) del N2.
El nitrógeno molecular (N2) consta de dos átomos de nitrógeno. La masa atómica del nitrógeno es aproximadamente 14.01 g/mol. Por lo tanto, la masa molar de N2 es:
M = 2 × 14.01 g/mol = 28.02 g/mol - Paso 2: Identificar la Densidad (ρ) del N2.
La densidad del gas nitrógeno dada en el problema es ρ = 1.250 g/L. - Paso 3: Aplicar la fórmula del Volumen Molar.
Vm = \( \frac{Masa\ Molar}{Densidad} \)
Vm = \( \frac{28.02\ g/mol}{1.250\ g/L} \)
Vm = 22.416 L/mol
Resultado: El volumen molar del nitrógeno gaseoso bajo estas condiciones es de aproximadamente 22.416 L/mol. Este valor es muy cercano al valor ideal de 22.4 L/mol para un gas a STP, lo que sugiere que el nitrógeno se comporta de manera casi ideal bajo las condiciones implícitas en esta densidad.
La Importancia y Aplicaciones del Volumen Molar en la Química
El concepto de Volumen Molar no es solo una curiosidad teórica; tiene aplicaciones prácticas y es fundamental para varias áreas de la química:
- Estequiometría de Gases: Permite convertir moles de un gas a volumen y viceversa en reacciones químicas, lo que es esencial para calcular rendimientos de reacción o cantidades de reactivos necesarios. Es la base para entender la Ley de Avogadro, que establece que volúmenes iguales de gases diferentes, a la misma temperatura y presión, contienen el mismo número de moléculas (o moles).
- Leyes de los Gases: El volumen molar es una consecuencia directa de la Ley de los Gases Ideales (PV=nRT). A partir de esta ecuación, se puede derivar que a STP, el volumen de un mol de cualquier gas ideal es constante (R*T/P = 0.0821 L·atm/(mol·K) * 273.15 K / 1 atm ≈ 22.4 L/mol).
- Diseño de Procesos Industriales: En la ingeniería química, es crucial para el diseño de equipos como tanques de almacenamiento, reactores y sistemas de transporte de gases, donde el volumen ocupado por una cantidad específica de sustancia es un factor crítico para la seguridad y la eficiencia.
- Análisis de Propiedades Físicas: Al comparar el volumen molar de diferentes sustancias en sus estados sólido, líquido y gaseoso, los químicos pueden obtener información sobre las fuerzas intermoleculares y el empaquetamiento de las moléculas. Por ejemplo, el volumen molar de un sólido o líquido es significativamente menor que el de un gas, lo que refleja la mayor proximidad de las partículas.
- Química Analítica: En la preparación de soluciones y en la titulación, aunque se usa la molaridad (moles/litros de solución), la comprensión del volumen molar de los solutos puros es un conocimiento base que ayuda a entender cómo la cantidad de sustancia se traduce en espacio ocupado.
Volumen Molar para Diferentes Estados de la Materia: Gases, Líquidos y Sólidos
Aunque el concepto de Volumen Molar es universal, su valor y su interpretación varían significativamente entre los diferentes estados de la materia:
Gases
Como ya se mencionó, los gases ideales a STP tienen un volumen molar de aproximadamente 22.4 litros. Esto se debe a que las partículas de gas están muy separadas y las fuerzas intermoleculares son insignificantes. El volumen ocupado por las propias moléculas de gas es despreciable en comparación con el volumen total del recipiente. Para gases reales, este valor puede variar ligeramente, especialmente bajo condiciones extremas de presión o temperatura, donde las interacciones moleculares y el volumen de las moléculas individuales se vuelven más relevantes.

Líquidos
Los líquidos tienen volúmenes molares mucho más pequeños que los gases. Esto se debe a que las partículas en un líquido están mucho más cerca entre sí y hay fuerzas intermoleculares significativas que las mantienen unidas. El volumen molar de un líquido es específico para cada sustancia y no hay un valor 'estándar' universal como el de los gases. Por ejemplo, el volumen molar del agua líquida (H2O) a 4°C (su densidad máxima) es de aproximadamente 18 mL/mol (18.015 g/mol / 1.00 g/mL). Esto es casi mil veces menor que el volumen molar de un gas a STP.
Sólidos
Los sólidos generalmente tienen los volúmenes molares más pequeños, ya que sus partículas están muy empaquetadas en una estructura rígida y ordenada. Al igual que los líquidos, el volumen molar de un sólido es único para cada sustancia y depende de su estructura cristalina y de las fuerzas de unión. Por ejemplo, el volumen molar del oro (Au) es de aproximadamente 10.2 mL/mol (196.967 g/mol / 19.3 g/mL). La excepción notable es el agua cuando se congela a hielo, donde su volumen molar aumenta debido a la formación de una estructura cristalina abierta, lo que explica por qué el hielo flota en el agua líquida.
Tabla Comparativa de Volúmenes Molares (Ejemplos)
Para ilustrar las diferencias en el Volumen Molar entre los estados de la materia, la siguiente tabla presenta ejemplos representativos:
| Sustancia | Estado Físico y Condiciones | Masa Molar (g/mol) | Densidad (g/L o g/mL) | Volumen Molar (L/mol o mL/mol) |
|---|---|---|---|---|
| Hidrógeno (H2) | Gas (STP) | 2.016 | 0.0899 g/L | ~22.4 L/mol |
| Oxígeno (O2) | Gas (STP) | 31.999 | 1.429 g/L | ~22.4 L/mol |
| Agua (H2O) | Líquido (25°C) | 18.015 | 1.00 g/mL | 18.015 mL/mol (0.0180 L/mol) |
| Oro (Au) | Sólido (20°C) | 196.967 | 19.3 g/mL | 10.205 mL/mol (0.0102 L/mol) |
| Cloruro de Sodio (NaCl) | Sólido (20°C) | 58.44 | 2.16 g/mL | 27.056 mL/mol (0.0271 L/mol) |
Esta tabla resalta claramente la drástica diferencia en el Volumen Molar entre el estado gaseoso y los estados condensados (líquido y sólido), lo que subraya la gran cantidad de espacio vacío en los gases en comparación con la materia condensada.
Preguntas Frecuentes (FAQ) sobre el Volumen Molar
¿Es el volumen molar siempre 22.4 litros?
No, el valor de 22.4 litros es el volumen molar para un mol de cualquier gas ideal bajo las condiciones de STP (0°C y 1 atm de presión). Para gases reales, el valor puede variar ligeramente de 22.4 L/mol. Para líquidos y sólidos, el volumen molar es considerablemente menor y varía significativamente de una sustancia a otra, ya que sus moléculas están mucho más empaquetadas y las fuerzas intermoleculares son dominantes.
¿Cómo afecta la temperatura y la presión al volumen molar?
El volumen molar de una sustancia, especialmente para los gases, es altamente dependiente de la temperatura y la presión. Según la Ley de los Gases Ideales (PV=nRT), el volumen (y por lo tanto el volumen molar) es directamente proporcional a la temperatura (a mayor temperatura, mayor volumen molar si la presión se mantiene constante) e inversamente proporcional a la presión (a mayor presión, menor volumen molar si la temperatura se mantiene constante). Para líquidos y sólidos, el efecto de la temperatura y la presión sobre el volumen molar es mucho menos pronunciado debido a su incompresibilidad y al empaquetamiento denso de sus partículas.
¿Cuál es la diferencia entre volumen molar y densidad?
Aunque están relacionados por la fórmula de cálculo del volumen molar, Densidad y Volumen Molar son conceptos distintos. La densidad (ρ = masa/volumen) es una medida de cuán compacta es una sustancia, es decir, cuánta masa hay en un determinado volumen. Sus unidades suelen ser g/mL o g/L. El volumen molar (Vm = volumen/mol) es el volumen que ocupa una cantidad específica de sustancia (un mol). Sus unidades son L/mol o mL/mol. La densidad nos dice la masa por unidad de volumen, mientras que el volumen molar nos dice el volumen por unidad de cantidad de sustancia.
¿Se puede usar el volumen molar para soluciones?
El concepto de Volumen Molar se aplica principalmente a sustancias puras, ya sean elementos o compuestos. Para soluciones, el concepto más utilizado para expresar la concentración es la molaridad (M), que se define como el número de moles de soluto por litro de solución (M = moles de soluto / litros de solución). Aunque no se calcula el "volumen molar de una solución" en el mismo sentido, la molaridad nos permite relacionar la cantidad de soluto con el volumen de la solución, siendo un concepto análogo en el ámbito de las mezclas.
¿Qué es un gas ideal?
Un gas ideal es un modelo teórico que simplifica el comportamiento de los gases reales. En un gas ideal, se asume que las partículas no tienen volumen propio (son puntos sin dimensión) y que no existen fuerzas de atracción o repulsión entre ellas. Aunque ningún gas real es perfectamente ideal, muchos gases a presiones bajas y temperaturas moderadas se comportan de manera muy similar a un gas ideal, lo que permite utilizar la Ley de los Gases Ideales y el valor de 22.4 litros para el volumen molar a STP con buena precisión.
Conclusión
El Volumen Molar es un concepto piedra angular en la química, que nos permite vincular la cantidad de sustancia a un volumen medible. Desde los vastos espacios que ocupan los gases hasta el empaquetamiento compacto de líquidos y sólidos, este valor nos ayuda a comprender mejor la naturaleza de la materia a nivel macroscópico y microscópico. Dominar su cálculo y sus implicaciones, especialmente en relación con la Masa Molar y la Densidad, así como las condiciones de STP, es esencial para cualquier estudiante o profesional de la química. Con esta guía, esperamos haber desmitificado el volumen molar y proporcionado las herramientas necesarias para su comprensión y aplicación efectiva en cualquier contexto químico.
Si quieres conocer otros artículos parecidos a Calculando el Volumen Molar: Guía Completa puedes visitar la categoría Química.
