31/12/2021
En el fascinante mundo de la química analítica, la titulación es una técnica fundamental que nos permite determinar la concentración exacta de una sustancia desconocida. Es como una danza milimétrica donde se añade, gota a gota, una solución de concentración conocida (el titulante) a una solución de concentración desconocida (el analito), hasta alcanzar un punto crucial: el punto de equivalencia. Este momento mágico es el corazón de la titulación, y comprender cómo calcularlo es esencial para cualquier químico o entusiasta de la ciencia.
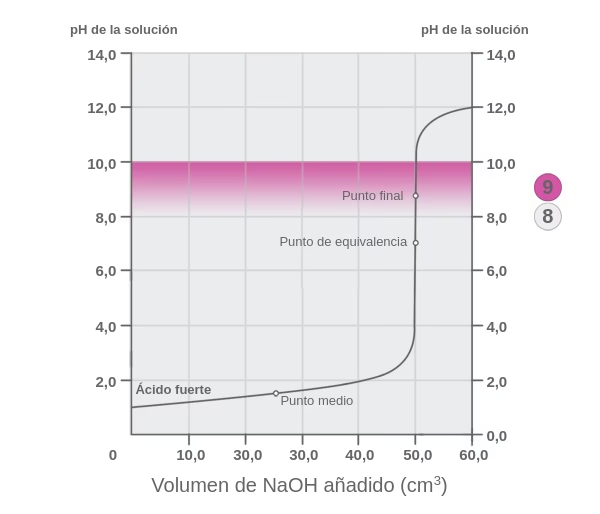
Pero, ¿qué es exactamente este punto de equivalencia y por qué es tan importante? En pocas palabras, el punto de equivalencia es el instante en el que el número de moles del titulante añadido es estequiométricamente igual al número de moles del analito presente en la muestra. Es el punto teórico de la reacción completa, donde los reactivos se han consumido en las proporciones exactas dictadas por la ecuación química balanceada. No debe confundirse con el punto final, que es el punto observable en el laboratorio, usualmente marcado por un cambio de color de un indicador o un cambio brusco en la lectura de un sensor de pH. Idealmente, el punto final debe estar lo más cerca posible del punto de equivalencia.
¿Cómo Encontrar el Punto de Equivalencia y el Punto Final?
La relación entre el punto de equivalencia y el punto final es crucial. Mientras que el punto de equivalencia es un concepto teórico y preciso, el punto final es la manifestación práctica de este. Para una titulación ácido-base, el punto de equivalencia se produce cuando los moles de iones H+ (del ácido) igualan a los moles de iones OH- (de la base). Este es el objetivo que buscamos alcanzar y medir.
Para detectar el punto final, los químicos emplean dos métodos principales:
- Indicadores Químicos: Son sustancias que cambian de color bruscamente en un rango de pH específico. Se eligen para que su cambio de color coincida lo más posible con el pH del punto de equivalencia de la titulación que se está realizando.
- Sensores de pH: Un pH-metro conectado a un electrodo de pH puede monitorear continuamente el pH de la solución a medida que se añade el titulante. Al graficar el pH frente al volumen de titulante añadido, se obtiene una curva de titulación. El punto de equivalencia se localiza en el punto de inflexión de esta curva, donde la pendiente es más pronunciada.
Cálculo del Punto de Equivalencia para Diferentes Tipos de Titulaciones
La fórmula para calcular el punto de equivalencia varía ligeramente dependiendo de la naturaleza del ácido y la base involucrados (fuertes o débiles). Sin embargo, el principio subyacente siempre es la estequiometría de la reacción.
1. Titulación de Ácido Fuerte - Base Fuerte
Cuando se titula un ácido fuerte con una base fuerte (o viceversa), ambos reactivos se disocian completamente en sus iones en solución. La reacción es típicamente una simple neutralización que produce una sal y agua. En este caso, la estequiometría es generalmente 1:1 entre los iones H+ y OH-.
La fórmula más sencilla y comúnmente utilizada para calcular el punto de equivalencia en este tipo de titulación es:
VA × MA = VB × MB
Donde:
VA= Volumen del ácidoMA= Molaridad (concentración) del ácidoVB= Volumen de la baseMB= Molaridad (concentración) de la base
Esta fórmula se deriva del hecho de que en el punto de equivalencia, los moles de ácido son iguales a los moles de base. Recordando que moles = concentración × volumen, la igualdad se vuelve evidente.

Ejemplo Práctico: Si se titulan 25.0 mL de ácido clorhídrico (HCl, un ácido fuerte) de concentración desconocida con una solución de hidróxido de sodio (NaOH, una base fuerte) 0.100 M, y se observa que el punto final se alcanza al añadir 20.0 mL de NaOH, podemos calcular la concentración del HCl:
VA = 25.0 mLMA = ?VB = 20.0 mLMB = 0.100 M
Aplicando la fórmula:
25.0 mL × MA = 20.0 mL × 0.100 MMA = (20.0 mL × 0.100 M) / 25.0 mLMA = 0.080 M
Por lo tanto, la concentración del ácido clorhídrico es 0.080 M.
Es importante destacar que, para una titulación de ácido fuerte - base fuerte, el pH en el punto de equivalencia es siempre 7.0 (neutro), ya que la sal formada no sufre hidrólisis significativa y los iones H+ y OH- se han neutralizado completamente.
2. Titulación de Ácido Débil - Base Fuerte
Las cosas se complican un poco cuando uno de los reactivos es débil. En una titulación de un ácido débil con una base fuerte, el ácido débil solo se disocia parcialmente. En el punto de equivalencia, la base fuerte ha reaccionado completamente con el ácido débil para formar su base conjugada (la sal). Esta base conjugada es una especie que puede reaccionar con el agua (hidrolizar), produciendo iones OH-.
Por esta razón, el pH en el punto de equivalencia de una titulación de ácido débil - base fuerte siempre será mayor que 7.0 (es decir, básico).
Para calcular el volumen del titulante (base fuerte) necesario para alcanzar el punto de equivalencia, el enfoque sigue siendo estequiométrico:
- Calcula los moles iniciales del ácido débil: Usa la fórmula
moles = concentración inicial del ácido × volumen inicial del ácido. - Determina los moles de la base fuerte necesarios: En el punto de equivalencia, los moles de la base fuerte añadida deben ser iguales a los moles iniciales del ácido débil (asumiendo una estequiometría 1:1 en la reacción de neutralización).
- Calcula el volumen de la base fuerte necesario: Usa la fórmula
volumen = moles de base fuerte / concentración de la base fuerte.
Ejemplo Práctico: Se titulan 50.0 mL de ácido acético (CH3COOH, un ácido débil) 0.10 M con hidróxido de sodio (NaOH, una base fuerte) 0.15 M. Calcula el volumen de NaOH necesario para alcanzar el punto de equivalencia.
1. Moles iniciales del ácido acético:Moles de CH3COOH = 0.10 M × 0.050 L = 0.005 moles (recuerda convertir mL a L)
2. Moles de NaOH necesarios:
En el punto de equivalencia, Moles de NaOH = Moles de CH3COOH = 0.005 moles
3. Volumen de NaOH necesario:Volumen de NaOH = 0.005 moles / 0.15 M = 0.0333 L o 33.3 mL
Por lo tanto, se necesitarán 33.3 mL de NaOH para alcanzar el punto de equivalencia.

3. Titulación de Base Débil - Ácido Fuerte
De manera análoga a la titulación de ácido débil - base fuerte, cuando se titula una base débil con un ácido fuerte, la base débil solo se disocia parcialmente. En el punto de equivalencia, el ácido fuerte ha reaccionado completamente con la base débil para formar su ácido conjugado. Este ácido conjugado puede hidrolizar el agua, produciendo iones H+.
Por lo tanto, el pH en el punto de equivalencia de una titulación de base débil - ácido fuerte siempre será menor que 7.0 (es decir, ácido).
Los pasos para calcular el volumen del titulante (ácido fuerte) necesario son los mismos que para el caso anterior, pero con los roles invertidos:
- Calcula los moles iniciales de la base débil.
- Determina los moles del ácido fuerte necesarios (igual a los moles iniciales de la base débil, asumiendo estequiometría 1:1).
- Calcula el volumen del ácido fuerte necesario.
La Importancia de los Indicadores y el Punto Final
Como mencionamos, el punto de equivalencia es un ideal teórico. En la práctica, nos basamos en el punto final, que es detectable. Los indicadores son sustancias cruciales que nos permiten visualizar este punto final.
Un indicador ácido-base es un ácido o una base débil que tiene diferentes colores en su forma protonada y desprotonada. El cambio de color se produce en un rango de pH específico, que idealmente debe superponerse con el salto pronunciado en el pH de la curva de titulación alrededor del punto de equivalencia.
La elección del indicador es vital para la precisión de la titulación. Un indicador mal elegido hará que el punto final observado difiera significativamente del punto de equivalencia real, llevando a resultados inexactos. Por ejemplo:
- Para titulaciones ácido fuerte-base fuerte, donde el pH en el punto de equivalencia es 7.0, un indicador como el azul de bromotimol (que cambia de color alrededor de pH 6.0-7.6) es adecuado.
- Para titulaciones ácido débil-base fuerte, donde el pH en el punto de equivalencia es básico (>7.0), se usa comúnmente la fenolftaleína (cambia de incoloro a rosa alrededor de pH 8.2-10.0).
- Para titulaciones base débil-ácido fuerte, donde el pH en el punto de equivalencia es ácido (<7.0), se puede usar el rojo de metilo o el naranja de metilo (cambian de color en rangos ácidos, por ejemplo, 4.4-6.2 para rojo de metilo).
La curva de titulación, que grafica el pH en función del volumen de titulante añadido, es una herramienta gráfica poderosa que muestra claramente el salto de pH alrededor del punto de equivalencia y ayuda a la selección adecuada del indicador.

Consideraciones Adicionales y Precisión
Al realizar titulaciones y calcular el punto de equivalencia, es fundamental tener en cuenta varios factores para asegurar la exactitud de los resultados:
- Precisión en la Medición del Volumen: El uso de material volumétrico calibrado como buretas, pipetas y matraces aforados es indispensable. Cada mililitro cuenta.
- Preparación de Soluciones: Las concentraciones de las soluciones estándar deben ser conocidas con alta precisión. La estandarización de soluciones es un paso previo importante.
- Temperatura: La temperatura puede afectar el volumen de las soluciones y la constante de disociación de ácidos/bases débiles, lo que a su vez afecta el pH del punto de equivalencia.
- Errores de Lectura: La lectura del menisco en la bureta debe hacerse de manera consistente y correcta para evitar errores sistemáticos.
- Agitación: Una agitación adecuada durante la titulación asegura una mezcla homogénea y una reacción completa.
Dominar la titulación y el cálculo del punto de equivalencia es una habilidad fundamental en química, que abre la puerta a innumerables aplicaciones analíticas, desde el control de calidad en la industria alimentaria hasta la investigación farmacéutica.
Tabla Comparativa de Tipos de Titulación y Puntos de Equivalencia
| Tipo de Titulación | pH en el Punto de Equivalencia | Características del Punto de Equivalencia | Indicador Típico Sugerido |
|---|---|---|---|
| Ácido Fuerte - Base Fuerte | 7.0 (Neutro) | Neutralización completa, sal neutra formada. | Azul de Bromotimol, Fenolftaleína (rango amplio) |
| Ácido Débil - Base Fuerte | > 7.0 (Básico) | Formación de la base conjugada del ácido débil, que hidroliza el agua. | Fenolftaleína |
| Base Débil - Ácido Fuerte | < 7.0 (Ácido) | Formación del ácido conjugado de la base débil, que hidroliza el agua. | Rojo de Metilo, Naranja de Metilo |
Preguntas Frecuentes (FAQ)
¿Es lo mismo el punto de equivalencia que el punto final?
No, no son exactamente lo mismo, aunque idealmente deberían estar muy cerca. El punto de equivalencia es el punto teórico donde los moles de titulante y analito son estequiométricamente iguales. El punto final es el punto observable experimentalmente, marcado por un cambio físico (como el color de un indicador) que señala el final de la titulación.
¿Por qué el pH en el punto de equivalencia no siempre es 7?
El pH en el punto de equivalencia solo es 7 (neutro) para titulaciones entre un ácido fuerte y una base fuerte. Cuando al menos uno de los reactivos (ácido o base) es débil, la sal que se forma en el punto de equivalencia sufrirá hidrólisis. Si se forma una sal de ácido débil y base fuerte, la base conjugada hidrolizará el agua para producir iones OH-, haciendo el pH > 7. Si se forma una sal de base débil y ácido fuerte, el ácido conjugado hidrolizará el agua para producir iones H+, haciendo el pH < 7.
¿Qué sucede si añado demasiado titulante después del punto de equivalencia?
Si se añade titulante más allá del punto de equivalencia, se estará agregando un exceso del titulante a la solución. Esto provocará que el pH de la solución cambie drásticamente más allá del punto de equivalencia, volviéndose muy ácido o muy básico dependiendo del titulante. Los cálculos basados en este volumen excesivo serían incorrectos, llevando a una determinación errónea de la concentración del analito.
¿Para qué se usa la titulación en la vida real?
La titulación tiene innumerables aplicaciones. Se utiliza en el control de calidad en la industria alimentaria para determinar la acidez de productos como jugos o vinagre; en la industria farmacéutica para verificar la concentración de principios activos en medicamentos; en el análisis ambiental para monitorear la calidad del agua (por ejemplo, alcalinidad o dureza); y en laboratorios de investigación para cuantificar una amplia gama de sustancias.
Si quieres conocer otros artículos parecidos a Calculando el Punto de Equivalencia en Titulaciones puedes visitar la categoría Química.

