28/12/2022
En el vasto y fascinante universo de la química, comprender la estructura y el comportamiento de los átomos es fundamental. Desde las partículas más diminutas que los componen hasta las fuerzas que dictan sus interacciones, cada detalle es crucial para desentrañar cómo la materia se organiza y reacciona. Uno de los conceptos más poderosos y a menudo subestimados en este campo es la Carga Nuclear Efectiva, una medida de la atracción neta que experimentan los electrones más externos de un átomo hacia su núcleo. Esta fuerza invisible, pero omnipresente, es la clave para entender por qué los elementos se comportan como lo hacen, desde su tamaño hasta su reactividad. Prepárese para un viaje al corazón del átomo, donde desvelaremos cómo esta carga, que no es la carga total del núcleo, moldea el destino de los elementos.
- ¿Qué son los Átomos y sus Componentes Fundamentales?
- Comprendiendo la Carga Nuclear Efectiva (Zeff)
- El Fenómeno del Apantallamiento Electrónico
- Cálculo de la Carga Nuclear Efectiva: Métodos y Ejemplos
- Tendencias Periódicas de la Carga Nuclear Efectiva
- Impacto de la Carga Nuclear Efectiva en las Propiedades Atómicas
- Preguntas Frecuentes sobre la Carga Nuclear Efectiva
- ¿Cómo se calcula la carga nuclear efectiva de un elemento como el Silicio?
- ¿Por qué los átomos se vuelven progresivamente más pequeños al moverse de izquierda a derecha en la tabla periódica?
- ¿Por qué la carga nuclear efectiva es siempre menor que la carga nuclear real (el número de protones en el núcleo)?
- ¿Cómo influyen las Reglas de Slater en el cálculo de Zeff?
- ¿Qué elemento tiene mayor carga nuclear efectiva entre Litio y Flúor?
¿Qué son los Átomos y sus Componentes Fundamentales?
Antes de sumergirnos en la complejidad de la carga nuclear efectiva, es vital recordar la composición básica de un átomo. Los átomos son las unidades fundamentales de la materia, los bloques de construcción de todo lo que nos rodea. Cada átomo está compuesto por tres tipos principales de partículas subatómicas:
- Protones: Partículas con carga eléctrica positiva, ubicadas en el centro del átomo. El número de protones define el número atómico de un elemento y, por lo tanto, su identidad única en la tabla periódica.
- Neutrones: Partículas sin carga eléctrica (neutras), también residiendo en el núcleo junto a los protones. Contribuyen principalmente a la masa del átomo.
- Electrones: Partículas con carga eléctrica negativa, que orbitan el núcleo en diferentes niveles de energía o “orbitales”. Son significativamente más ligeros que los protones y neutrones.
Los protones y neutrones se agrupan en el núcleo atómico, una región densa y cargada positivamente en el centro del átomo. Los electrones, por su parte, se organizan en capas o "capas electrónicas" alrededor del núcleo. Estas capas no son meras órbitas fijas, sino regiones de probabilidad donde es más probable encontrar un electrón. Los electrones más cercanos al núcleo se encuentran en niveles de energía más bajos y están fuertemente atraídos por la carga positiva del núcleo. A medida que nos alejamos del núcleo, los electrones ocupan niveles de energía más altos y experimentan una atracción nuclear diferente.
Comprendiendo la Carga Nuclear Efectiva (Zeff)
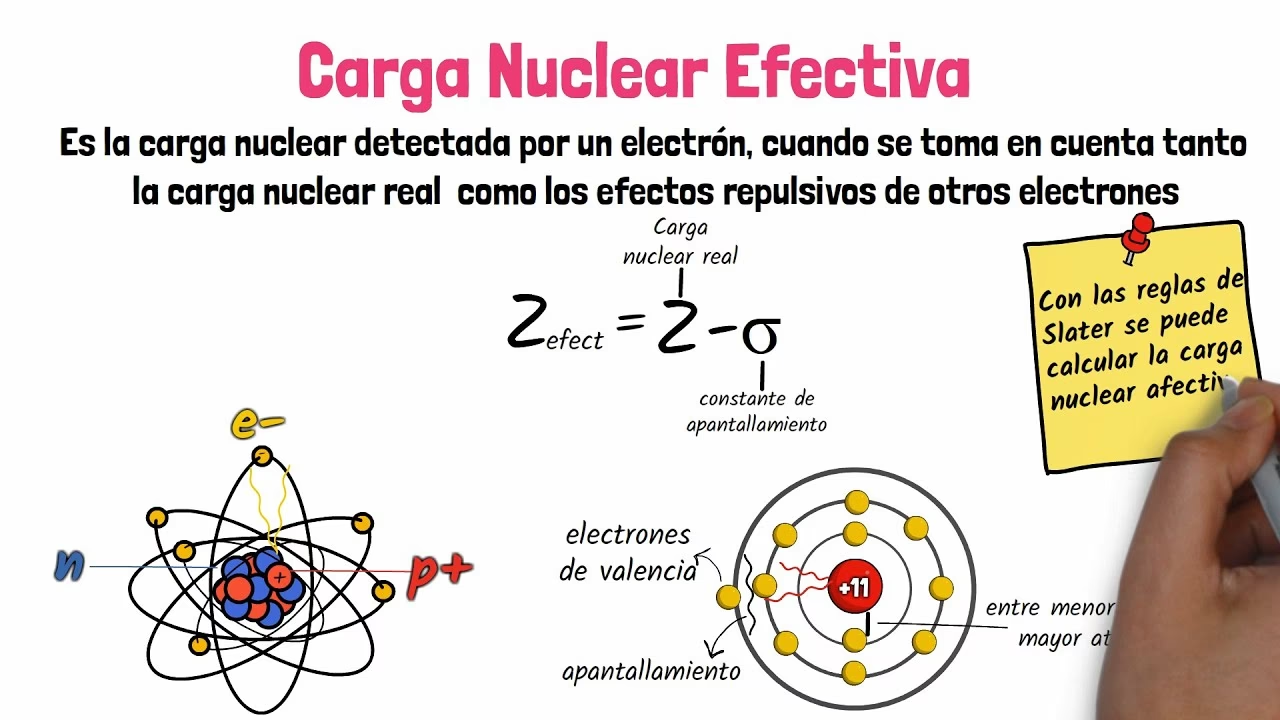
La Carga Nuclear Efectiva, denotada como Zeff (donde 'Z' es la carga nuclear real y 'eff' se refiere a 'efectiva'), es la carga positiva neta que experimenta un electrón en un átomo polielectrónico, es decir, un átomo con más de un electrón. No es simplemente la carga total del núcleo (el número de protones), sino la carga "percibida" por un electrón específico, usualmente uno de los electrones más externos o de valencia. Podemos pensar en la Carga Nuclear Efectiva como la fuerza de atracción real entre el núcleo y un electrón en particular.
¿Por qué es "efectiva" y no la carga total? La razón es que en átomos con múltiples electrones, estos no solo son atraídos por el núcleo, sino que también se repelen entre sí. Los electrones internos, aquellos que están más cerca del núcleo, ejercen un efecto de "apantallamiento" o "blindaje" sobre los electrones más externos. Esto significa que la carga positiva total del núcleo no es experimentada plenamente por los electrones de valencia, ya que parte de esa atracción se ve neutralizada por la presencia de los electrones internos con carga negativa.
En esencia, la Zeff es crucial porque determina qué tan fuertemente están unidos los electrones de valencia al átomo. Una mayor Zeff implica una mayor atracción, lo que significa que los electrones de valencia están más fuertemente sujetos y son más difíciles de remover. Por el contrario, una Zeff menor indica una atracción más débil, haciendo que los electrones de valencia sean más propensos a participar en enlaces químicos o a ser removidos. Este concepto es fundamental para entender propiedades como el tamaño atómico, la energía de ionización y la electronegatividad.
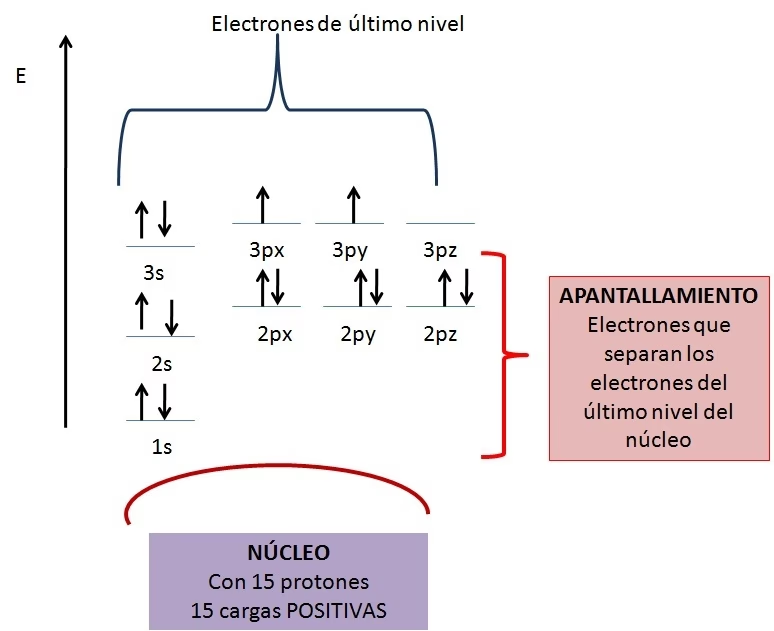
El Fenómeno del Apantallamiento Electrónico
El apantallamiento electrónico, también conocido como efecto pantalla o blindaje electrónico, es el corazón de la diferencia entre la carga nuclear real y la carga nuclear efectiva. Este fenómeno se produce porque los electrones internos (o electrones de "núcleo"), que se encuentran más cerca del núcleo, repelen a los electrones más externos (o electrones de "valencia"). Al hacerlo, los electrones internos actúan como una "cortina" o "escudo", reduciendo la atracción que los electrones de valencia sienten por parte del núcleo.
Imaginemos el núcleo positivo como un imán poderoso. Si no hubiera otros electrones, los electrones de valencia sentirían toda la fuerza de ese imán. Sin embargo, cuando hay electrones intermedios entre el núcleo y los electrones de valencia, estos electrones internos con carga negativa contrarrestan localmente parte de la carga positiva del núcleo. Esto resulta en una disminución de la cantidad de atracción nuclear sentida por los electrones de valencia. En otras palabras, la carga efectiva experimentada por los electrones de valencia es menor de lo que sería si los electrones internos no estuvieran presentes.
La magnitud del apantallamiento depende principalmente del número de electrones internos. Cuantas más capas internas de electrones tenga un átomo, mayor será el apantallamiento y, por lo tanto, menor será la carga nuclear efectiva experimentada por los electrones de valencia. Los electrones en el mismo nivel de energía también contribuyen al apantallamiento, aunque en menor medida. Este efecto es crucial para explicar las tendencias periódicas en las propiedades de los elementos, ya que influye directamente en el radio atómico y la energía necesaria para remover o atraer electrones.
Cálculo de la Carga Nuclear Efectiva: Métodos y Ejemplos
Calcular la Carga Nuclear Efectiva (Zeff) es fundamental para predecir el comportamiento químico de los elementos. La fórmula general para una aproximación simple es:
Zeff = Z – S
Donde:
- Z es la carga nuclear real, que es igual al número atómico del elemento (el número de protones en el núcleo). Este valor se obtiene directamente de la tabla periódica.
- S es la constante de apantallamiento, que representa la magnitud del apantallamiento electrónico. En su forma más simple, S se puede aproximar como el número de electrones internos o de "núcleo" que separan los electrones de valencia del núcleo.
Ejemplos de Cálculo Simplificado:
Litio (Li)
El litio tiene un número atómico de 3, lo que significa que tiene 3 protones en su núcleo (Z = 3). Su configuración electrónica es 1s²2s¹. Esto implica que tiene dos electrones internos (en el orbital 1s) y un electrón de valencia (en el orbital 2s).

Para el electrón de valencia del litio, podemos estimar el apantallamiento (S) como el número de electrones internos, que es 2.
Zeff = 3 – 2 = 1
Por lo tanto, para el electrón más externo del litio, la Carga Nuclear Efectiva es aproximadamente 1. Esto significa que la fuerza de atracción neta que siente el electrón de valencia del litio desde el núcleo es equivalente a una carga de +1.
Berilio (Be)
El berilio se encuentra a la derecha del litio en la tabla periódica y tiene un número atómico de 4 (Z = 4). Su configuración electrónica es 1s²2s². Al igual que el litio, tiene dos electrones internos (en el orbital 1s). Sin embargo, el berilio tiene dos electrones de valencia (en el orbital 2s).
Estimando S como el número de electrones internos (2):
Zeff = 4 – 2 = 2
El berilio tiene una Carga Nuclear Efectiva más alta que el litio, lo que ya nos da una pista sobre una tendencia periódica.
Flúor (F)
Saltando hacia la derecha en la tabla periódica hasta el flúor, encontramos un escenario diferente. El flúor tiene un número atómico de 9 (Z = 9). Su configuración electrónica es 1s²2s²2p⁵. Tiene dos electrones internos (en el orbital 1s) y siete electrones de valencia (dos en el orbital 2s y cinco en el 2p).
Aplicando la misma aproximación para S (número de electrones internos, que es 2):
Zeff = 9 – 2 = 7
Según esta aproximación, la Carga Nuclear Efectiva para los electrones de valencia del flúor sería significativamente mayor que la del litio y el berilio. Sin embargo, es importante señalar que esta aproximación se vuelve menos precisa para elementos con más electrones. El valor tabulado de la Carga Nuclear Efectiva para el flúor es en realidad alrededor de 5.1.
Esta discrepancia surge porque nuestra suposición simplificada de que S es igual al número de electrones internos no considera completamente el apantallamiento entre los propios electrones de valencia ni las formas de los orbitales. En el caso del flúor, tanto la forma de los orbitales de valencia (los orbitales 2p) como las fuerzas repulsivas dentro de las capas de electrones de valencia hacen que el valor real sea sustancialmente menor que nuestra estimación simple. A pesar de esto, los principios básicos de nuestros cálculos simplificados son precisos y representan correctamente por qué la Carga Nuclear Efectiva cambia a medida que nos movemos de izquierda a derecha en la tabla periódica.
Reglas de Slater: Un Enfoque Más Preciso
Para cálculos más precisos de la constante de apantallamiento (S), se utilizan las Reglas de Slater. Estas reglas proporcionan un método sistemático para estimar el valor de S, teniendo en cuenta la contribución de diferentes electrones al apantallamiento, basándose en su ubicación en la configuración electrónica del átomo. Las Reglas de Slater son más complejas que la simple resta del número de electrones internos, ya que asignan diferentes factores de apantallamiento a los electrones dependiendo de si están en el mismo grupo, en grupos con un número cuántico principal menor, o si son electrones d o f.
Aunque las reglas son detalladas, su aplicación sigue un patrón lógico:
- Organizar la configuración electrónica del átomo en grupos específicos.
- Los electrones a la derecha del electrón de interés no contribuyen al apantallamiento.
- Los electrones en el mismo grupo que el electrón de interés contribuyen con un factor de apantallamiento de 0.35 (excepto para 1s, que es 0.30).
- Para electrones s o p: los electrones con un número cuántico principal menos contribuyen con 0.85; los electrones con dos números cuánticos principales menos contribuyen con 1.00.
- Para electrones d o f: todos los electrones a la izquierda contribuyen con 1.00.
Sumando estas contribuciones se obtiene un valor de S mucho más ajustado a la realidad experimental, lo que resulta en una Zeff más precisa. Este nivel de detalle es crucial para estudios avanzados de química y física atómica.
Tendencias Periódicas de la Carga Nuclear Efectiva
La Carga Nuclear Efectiva no es un valor estático, sino que varía de manera predecible a lo largo de la tabla periódica, y estas variaciones tienen profundas implicaciones para las propiedades de los elementos:
Variación a lo Largo de un Periodo (de Izquierda a Derecha)
Al moverse de izquierda a derecha a lo largo de un mismo periodo (fila) en la tabla periódica, el número atómico (Z) aumenta en una unidad por cada elemento consecutivo. Esto significa que el número de protones en el núcleo aumenta. Sin embargo, los electrones adicionales que se añaden se colocan en la misma capa de valencia que los electrones existentes, o en una capa con un apantallamiento similar por parte de los electrones internos.
Como resultado, el aumento en la carga nuclear real (Z) es más significativo que el aumento en el apantallamiento (S) proporcionado por los nuevos electrones. Esto lleva a un incremento constante de la Carga Nuclear Efectiva al moverse de izquierda a derecha en un periodo. Por ejemplo, al pasar de Litio (Zeff ≈ 1) a Berilio (Zeff ≈ 2) y luego a Flúor (Zeff ≈ 5.1), la fuerza de atracción que sienten los electrones de valencia hacia el núcleo es cada vez mayor.
Variación a lo Largo de un Grupo (de Arriba Abajo)
Al moverse de arriba hacia abajo en un mismo grupo (columna) en la tabla periódica, el número atómico (Z) también aumenta. Sin embargo, los electrones de valencia se encuentran en capas de energía sucesivamente más altas, es decir, más lejos del núcleo. Cada nueva capa de energía significa que hay más capas de electrones internos entre el núcleo y los electrones de valencia, lo que resulta en un aumento significativo del apantallamiento.
Aunque la carga nuclear real (Z) aumenta, el efecto de apantallamiento (S) aumenta aún más drásticamente debido a la adición de nuevas capas electrónicas completas. Esto provoca una ligera disminución o un valor relativamente constante de la Carga Nuclear Efectiva para los electrones de valencia al descender por un grupo. Los electrones de valencia están cada vez más lejos del núcleo y más apantallados, lo que reduce la atracción neta.
Impacto de la Carga Nuclear Efectiva en las Propiedades Atómicas
La tendencia periódica de la Carga Nuclear Efectiva tiene implicaciones directas en varias propiedades fundamentales de los elementos:
Radio Atómico
Como se observa, el aumento de la Zeff a lo largo de un periodo (de izquierda a derecha) significa que los electrones de valencia son atraídos con mayor fuerza hacia el núcleo. Esto provoca una contracción del átomo, lo que resulta en una disminución del radio atómico. Por ejemplo, un átomo de flúor tiene un diámetro significativamente menor que un átomo de litio, precisamente porque sus electrones de valencia experimentan una fuerza atractiva mucho más fuerte hacia el núcleo. En cierto sentido, los electrones de valencia del flúor están "más apretados" que los del litio.
Por el contrario, al descender por un grupo, aunque la Zeff no cambia drásticamente o incluso disminuye ligeramente, el principal factor que determina el radio atómico es la adición de nuevas capas electrónicas. Cada nueva capa aumenta el tamaño del átomo, a pesar de que la atracción efectiva por electrón de valencia pueda ser similar o incluso menor.
Energía de Ionización
La energía de ionización es la energía mínima necesaria para remover un electrón de un átomo en estado gaseoso. Un aumento en la Zeff significa que los electrones de valencia están más fuertemente atraídos por el núcleo. Por lo tanto, se requiere más energía para superar esta atracción y remover un electrón. De izquierda a derecha en un periodo, la energía de ionización tiende a aumentar. Los elementos con alta Zeff tienen alta energía de ionización.

Electronegatividad
La electronegatividad es la capacidad de un átomo para atraer electrones hacia sí mismo en un enlace químico. Una mayor Zeff implica una mayor capacidad del núcleo para atraer y retener electrones, incluyendo aquellos compartidos en un enlace. Por lo tanto, la electronegatividad tiende a aumentar de izquierda a derecha en un periodo y a disminuir de arriba abajo en un grupo, siguiendo de cerca las tendencias de la Carga Nuclear Efectiva.
Tabla Comparativa de Zeff y Radio Atómico (Ejemplos)
Para ilustrar las tendencias, observemos la siguiente tabla comparativa para algunos elementos representativos:
| Elemento | Símbolo | Número Atómico (Z) | Electrones de Núcleo (S aproximado) | Zeff (aproximada) | Radio Atómico (pm) | Tendencia Zeff |
|---|---|---|---|---|---|---|
| Litio | Li | 3 | 2 | 1 | 152 | Baja |
| Berilio | Be | 4 | 2 | 2 | 112 | Media |
| Flúor | F | 9 | 2 | 7 (aprox. 5.1 real) | 71 | Alta |
Esta tabla demuestra cómo un aumento en Zeff (de Li a F) correlaciona con una disminución en el radio atómico, ya que los electrones de valencia son atraídos más fuertemente hacia el núcleo.
Preguntas Frecuentes sobre la Carga Nuclear Efectiva
¿Cómo se calcula la carga nuclear efectiva de un elemento como el Silicio?
El Silicio (Si) tiene un número atómico de 14 (Z = 14). Su configuración electrónica es 1s²2s²2p⁶3s²3p². Los electrones de núcleo son aquellos en las capas 1s y 2s/2p, es decir, 2 (en 1s) + 8 (en 2s/2p) = 10 electrones de núcleo. Utilizando la aproximación simple, S = 10. Por lo tanto, la Carga Nuclear Efectiva para los electrones de valencia del silicio es: Zeff = Z – S = 14 – 10 = 4. El Silicio tiene 4 electrones de valencia y una carga nuclear efectiva neta de aproximadamente +4.
¿Por qué los átomos se vuelven progresivamente más pequeños al moverse de izquierda a derecha en la tabla periódica?
Al moverse de izquierda a derecha a lo largo de una fila (periodo) en la tabla periódica, el número de protones en el núcleo atómico (Z) aumenta. Esto lleva a un incremento de la Carga Nuclear Efectiva (Zeff) experimentada por los electrones de valencia, ya que el aumento en el apantallamiento no compensa completamente el aumento de la carga nuclear real. Esta mayor fuerza atractiva sobre los electrones de valencia hace que sean atraídos más fuertemente hacia el núcleo, resultando en una disminución del diámetro del átomo.
¿Por qué la carga nuclear efectiva es siempre menor que la carga nuclear real (el número de protones en el núcleo)?
La Carga Nuclear Efectiva es siempre menor que la carga nuclear real debido al fenómeno del apantallamiento electrónico. Los electrones internos, o de "núcleo", ejercen un efecto de blindaje sobre los electrones de valencia más externos, bloqueando parcialmente la atracción completa del núcleo atómico. Su carga negativa contrarresta una porción de la carga positiva del núcleo, reduciendo la atracción neta que sienten los electrones de valencia.
¿Cómo influyen las Reglas de Slater en el cálculo de Zeff?
Las Reglas de Slater proporcionan un método más sofisticado y preciso para calcular la constante de apantallamiento (S). A diferencia de la simple aproximación que considera S como el número total de electrones internos, las Reglas de Slater asignan diferentes factores de contribución al apantallamiento dependiendo de la ubicación y tipo de orbital de cada electrón. Esto permite obtener un valor de S más exacto, lo que a su vez resulta en una Carga Nuclear Efectiva más precisa, especialmente para átomos con múltiples capas y subcapas electrónicas.
¿Qué elemento tiene mayor carga nuclear efectiva entre Litio y Flúor?
Comparando el Litio (Zeff aproximada de 1) y el Flúor (Zeff aproximada de 7, o 5.1 real), el Flúor tiene una Carga Nuclear Efectiva significativamente mayor. Esto se debe a que el Flúor tiene un número mucho mayor de protones en su núcleo (Z=9) en comparación con el Litio (Z=3), mientras que el apantallamiento de sus electrones internos (ambos tienen 2 electrones en la capa 1s) es el mismo. El aumento de la carga nuclear real en el Flúor es el factor dominante que resulta en una mayor atracción neta sobre sus electrones de valencia.
En resumen, la Carga Nuclear Efectiva es un concepto fundamental en química que correlaciona directamente con muchas de las tendencias periódicas en las propiedades de los elementos. Es la carga positiva neta experimentada por un electrón en un átomo polielectrónico y siempre es menor que la carga nuclear real debido al efecto de apantallamiento electrónico. Comprender este concepto nos permite predecir y explicar el comportamiento de los átomos y su papel en la formación de moléculas, abriendo la puerta a un conocimiento más profundo del mundo que nos rodea.
Si quieres conocer otros artículos parecidos a Carga Nuclear Efectiva: Un Concepto Esencial puedes visitar la categoría Química.

