05/12/2025
En el vasto universo de la química, las soluciones electrolíticas juegan un papel fundamental, desde procesos biológicos hasta aplicaciones industriales. Sin embargo, a diferencia de las soluciones ideales donde las interacciones entre soluto y solvente son despreciables, en las soluciones electrolíticas, los iones cargados interactúan fuertemente entre sí y con las moléculas del solvente. Estas interacciones hacen que el comportamiento real de los iones difiera significativamente de lo que predeciríamos basándonos únicamente en su concentración. Aquí es donde la teoría de Debye-Hückel emerge como una herramienta revolucionaria, proporcionando un marco teórico para entender y cuantificar estas desviaciones en soluciones diluidas.

- ¿Qué es la Teoría de Debye-Hückel?
- La Fuerza Iónica: Una Métrica Crucial
- El Coeficiente de Actividad: Más Allá de la Concentración
- La Ley Límite de Debye-Hückel: Su Forma Fundamental
- De la Ley Límite a la Ecuación Extendida de Debye-Hückel
- Más Allá de Debye-Hückel: Otras Aproximaciones para Soluciones Concentradas
- Aplicaciones de la Teoría de Debye-Hückel
- Preguntas Frecuentes (FAQ)
- ¿Por qué las soluciones electrolíticas no se comportan idealmente?
- ¿Qué es la atmósfera iónica?
- ¿Cuándo debo usar la Ley Límite vs. la Ecuación Extendida de Debye-Hückel?
- ¿Se puede medir experimentalmente el coeficiente de actividad de un solo ion?
- ¿Qué representan las constantes A y B en las ecuaciones de Debye-Hückel?
¿Qué es la Teoría de Debye-Hückel?
La teoría de Debye-Hückel, formulada por Peter Debye y Erich Hückel en 1923, fue un hito en la comprensión del comportamiento de los electrolitos fuertes en solución. Antes de esta teoría, se observaba que la conductividad eléctrica y otras propiedades de las soluciones electrolíticas no se ajustaban a las predicciones basadas en la concentración molar, especialmente a medida que la concentración aumentaba.
El núcleo de la teoría reside en un modelo electrostático que describe el entorno de un ion individual en solución. Imagina un ion central, por ejemplo, un catión, rodeado por un “halo” de iones de carga opuesta. Este “halo” no es una estructura estática, sino una distribución dinámica y esféricamente simétrica de carga, conocida como la atmósfera iónica. Esta atmósfera se forma debido a las fuerzas de Coulomb: el ion central atrae iones de carga opuesta y repele iones de la misma carga, creando una región donde la densidad de carga neta es opuesta a la del ion central.
El modelo de Debye-Hückel asume que los iones son esferas duras con carga puntual en su centro y que el solvente es un medio continuo con una constante dieléctrica uniforme. A medida que un ion cargado se introduce en una solución salina, se realiza un trabajo eléctrico para crear esta atmósfera iónica. Este trabajo eléctrico se relaciona directamente con el cambio en la energía de Gibbs libre del ion, y, por extensión, con su coeficiente de actividad.
Es crucial entender que la teoría de Debye-Hückel es más precisa para soluciones diluidas. A medida que la concentración de sal aumenta, la precisión del modelo disminuye. Como regla general, la teoría proporciona valores útiles para los coeficientes de actividad en soluciones cuya concentración total de sal es inferior a aproximadamente 0.01 molal. Esta limitación surge de las simplificaciones inherentes al modelo, como tratar los iones como cargas puntuales y el solvente como un continuo sin estructura.
La Fuerza Iónica: Una Métrica Crucial
Un concepto fundamental introducido por la teoría de Debye-Hückel es la fuerza iónica (I). Es una medida de la intensidad del campo eléctrico total generado por todos los iones en una solución. En otras palabras, cuantifica la “densidad” de la atmósfera iónica. Se define matemáticamente de la siguiente manera:
I = ½ ∑k=1n z2k mk
Donde:
Ies la fuerza iónica.zkes el número de carga del ionk(por ejemplo, +1 para Na+, -2 para SO42−).mkes la molalidad (moles de soluto por kilogramo de solvente) del ionk.- La suma se extiende a todos los tipos de iones presentes en la solución.
El factor de ½ se introduce para que la fuerza iónica de un electrolito 1:1 (como NaCl) sea igual a su molalidad. La fuerza iónica es crucial porque el efecto de los iones sobre las propiedades de la solución depende de la carga de los iones, no solo de su concentración.

Ejemplo de Cálculo de Fuerza Iónica:
Calcule la fuerza iónica de una solución 0.1 M de sulfato de aluminio, Al2(SO4)3.
Al2(SO4)3 se disocia en 2 Al3+ y 3 SO42−.
- Concentración de Al3+ = 2 × 0.1 M = 0.2 M; Carga (z) = +3
- Concentración de SO42− = 3 × 0.1 M = 0.3 M; Carga (z) = -2
I = ½ [ (0.2 M) × (+3)2 + (0.3 M) × (-2)2 ]
I = ½ [ (0.2 × 9) + (0.3 × 4) ]
I = ½ [ 1.8 + 1.2 ]
I = ½ [ 3.0 ]
I = 1.5 M
La fuerza iónica es crucial porque el efecto de los iones sobre las propiedades de la solución depende de la carga de los iones, no solo de su concentración.
El Coeficiente de Actividad: Más Allá de la Concentración
En soluciones ideales, la “concentración efectiva” de un soluto es igual a su concentración analítica. Sin embargo, en soluciones electrolíticas, las fuertes interacciones iónicas reducen la capacidad de los iones para participar libremente en reacciones químicas o para contribuir plenamente a propiedades como la presión osmótica o la conductividad. Para corregir esto, se introduce el concepto de actividad (a).
La actividad se define como la concentración efectiva de un ion o electrolito en una solución. Se relaciona con la concentración real (molalidad o molaridad, C) mediante el coeficiente de actividad (f o γ):
a = γC
Donde:
aes la actividad.γ(gamma) es el coeficiente de actividad.Ces la concentración (molalidad o molaridad).
Para soluciones muy diluidas, donde las interacciones iónicas son mínimas, el coeficiente de actividad se aproxima a 1 (γ ≈ 1), y la actividad es prácticamente igual a la concentración. Sin embargo, a medida que la concentración aumenta y las interacciones se vuelven más significativas, γ se vuelve menor que 1, indicando que la concentración efectiva es menor que la concentración real.
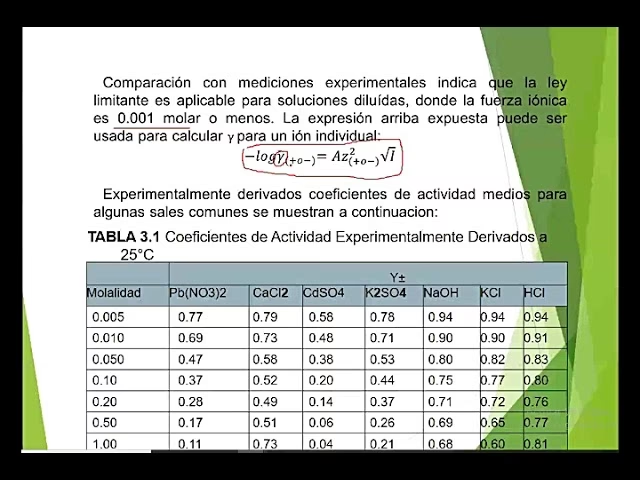
Es importante destacar que los coeficientes de actividad de iones individuales (γ+ para cationes y γ- para aniones) no pueden medirse experimentalmente de forma directa. Lo que sí se puede determinar es el coeficiente de actividad medio (γ±) para un electrolito completo, que es una especie de promedio geométrico de los coeficientes de actividad de los iones individuales.
La teoría de Debye-Hückel culmina en una ecuación que relaciona el coeficiente de actividad de un ion con la fuerza iónica de la solución. Para soluciones muy diluidas, esta ecuación se simplifica a la Ley Límite de Debye-Hückel, que es la forma más conocida y utilizada: log10 γ± = −Aγ |z+z−| √I Donde: Esta fórmula predice que el coeficiente de actividad disminuye a medida que aumenta la fuerza iónica y las cargas de los iones. La dependencia de la raíz cuadrada de la fuerza iónica es una característica distintiva de la teoría de Debye-Hückel y es resultado de las interacciones electrostáticas de largo alcance. Es fundamental recordar que esta ley es una "ley límite" porque solo es precisa en el límite de dilución infinita. A concentraciones extremadamente bajas, predice con gran exactitud el comportamiento de los electrolitos. Sin embargo, a medida que la concentración aumenta, las simplificaciones del modelo se vuelven menos válidas, y la ley límite comienza a desviarse de los valores experimentales. Las desviaciones de la Ley Límite de Debye-Hückel a concentraciones más altas se deben a varias simplificaciones en el modelo original. Estas incluyen: Para abordar algunas de estas limitaciones y extender la validez de la teoría a concentraciones ligeramente más altas, se desarrolló la Ecuación Extendida de Debye-Hückel. Esta ecuación introduce un término que considera el tamaño efectivo del ion: −log10(γ±) = &frac{A|z+z−|√I}{1 + Ba√I} Donde, además de los términos ya conocidos: Esta ecuación extendida proporciona un mejor ajuste con los datos experimentales para concentraciones electrolíticas de hasta aproximadamente 0.01-0.1 mol/L, lo que la hace mucho más útil para una gama más amplia de aplicaciones prácticas que la ley límite. A pesar de la mejora que ofrece la ecuación extendida, incluso esta tiene sus límites. Para soluciones electrolíticas de alta concentración (superiores a 0.1 mol/L), las interacciones iónicas se vuelven tan complejas que las aproximaciones de Debye-Hückel ya no son adecuadas. Para estas situaciones, se han desarrollado modelos más sofisticados, a menudo de naturaleza empírica o semi-empírica: La ecuación de Davies es una extensión empírica de la teoría de Debye-Hückel, propuesta por W. G. Davies en 1938. Es notable por su simplicidad y su capacidad para predecir coeficientes de actividad en soluciones de electrolitos a concentraciones relativamente altas (hasta aproximadamente 0.5 M) a 25 °C. Su forma es: −log10 f± = 0.5 z1z2 &left( \frac{√I}{1 + √I} − 0.30I &right) Donde Para el estudio de soluciones electrolíticas de muy alta fuerza iónica (hasta 6 mol/kg e incluso más), las ecuaciones de Pitzer, desarrolladas por Kenneth Pitzer, son el estándar de oro. Estas ecuaciones son termodinámicamente rigurosas y se basan en una expansión virial de la energía libre de Gibbs en exceso. Consideran interacciones entre pares de iones (binarias), tríos de iones (ternarias) y también las interacciones ion-solvente. La forma general de las ecuaciones de Pitzer es mucho más compleja que las de Debye-Hückel o Davies, involucrando múltiples parámetros empíricos que deben determinarse experimentalmente para cada par de iones y solvente. Son ampliamente utilizadas en geoquímica, oceanografía y en la industria para modelar sistemas de alta salinidad, como el agua de mar o las salmueras. La teoría de Debye-Hückel y sus extensiones tienen un impacto significativo en diversas ramas de la química y campos relacionados: Aunque la teoría de Debye-Hückel tiene sus limitaciones, especialmente a altas concentraciones, su contribución a la química física es inmensurable. Proporcionó el primer modelo exitoso para explicar el comportamiento no ideal de los electrolitos, sentando las bases para desarrollos posteriores y sigue siendo una herramienta fundamental para la comprensión de las propiedades de las soluciones iónicas diluidas.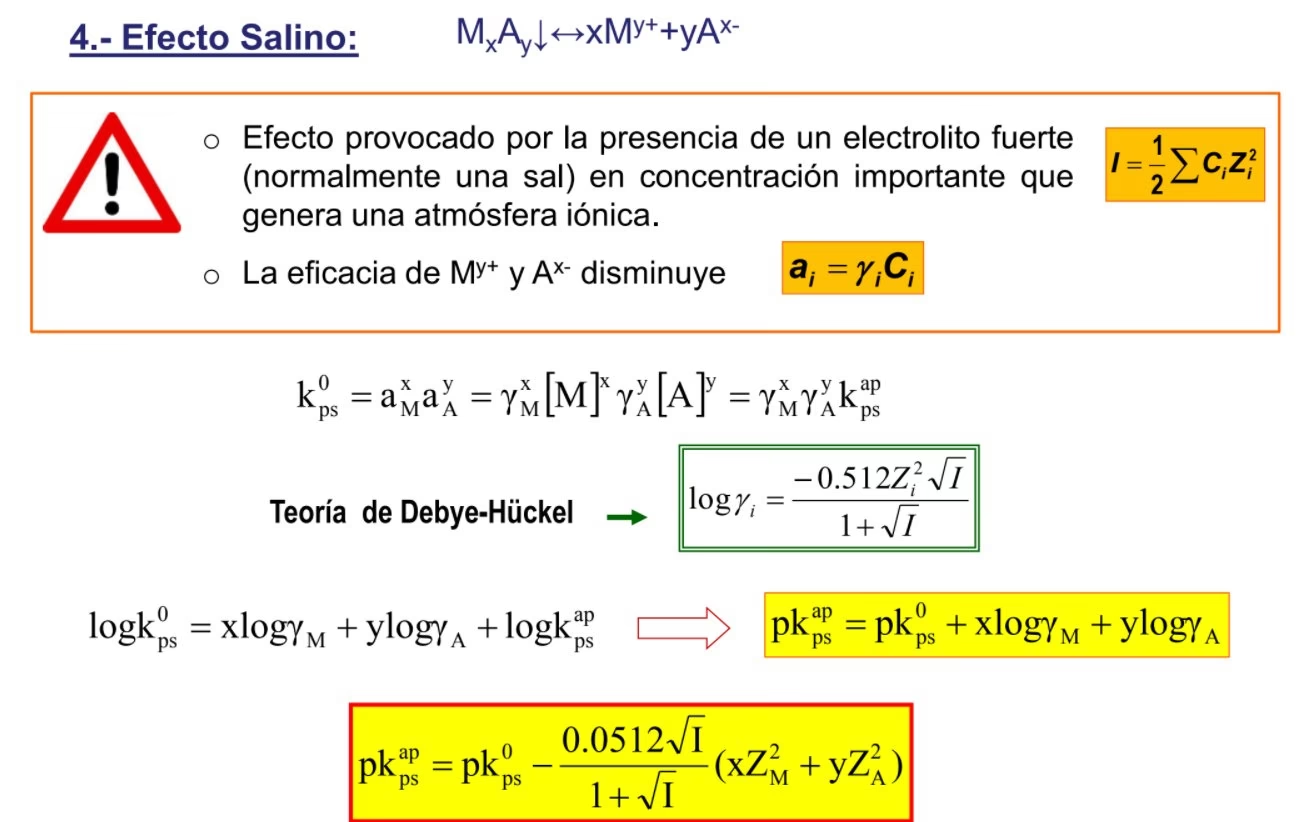
La Ley Límite de Debye-Hückel: Su Forma Fundamental
γ± es el coeficiente de actividad medio del electrolito.Aγ es una constante que depende de la temperatura, la constante dieléctrica del solvente y otras constantes fundamentales. Para soluciones acuosas a 25 °C, el valor de Aγ es aproximadamente 0.510.z+ y z− son los números de carga del catión y el anión, respectivamente (se toma el valor absoluto del producto).I es la fuerza iónica de la solución.De la Ley Límite a la Ecuación Extendida de Debye-Hückel
a es el "parámetro de acercamiento más cercano" o "diámetro iónico efectivo" (a menudo expresado en Angstroms, Å). Este valor representa el radio del ion hidratado (el ion más las moléculas de agua fuertemente unidas a él). Los iones más grandes y menos cargados tienden a unirse menos fuertemente al agua y tienen radios hidratados más pequeños que los iones más pequeños y altamente cargados. Valores típicos para iones como H+, Cl−, CN− son alrededor de 3 Å, mientras que para el ion hidronio puede ser de 9 Å.A y B son constantes que dependen del solvente y la temperatura. Para soluciones acuosas a 25 °C, A ≈ 0.5085 y B ≈ 0.3281 (cuando a está en Å y I en mol/kg).Más Allá de Debye-Hückel: Otras Aproximaciones para Soluciones Concentradas
Ecuación de Davies
f± es el coeficiente de actividad molal medio, z1 y z2 son las cargas de los iones, e I es la fuerza iónica. El término 0.30I es un término empírico que corrige las desviaciones a concentraciones más altas. A medida que la fuerza iónica tiende a cero, este término desaparece y la ecuación de Davies se reduce a la ley límite de Debye-Hückel. Aunque es más precisa que la ley límite para concentraciones intermedias, aún puede tener desviaciones significativas para electrolitos con iones de carga elevada o si hay una asociación iónica considerable.Ecuaciones de Pitzer
Aplicaciones de la Teoría de Debye-Hückel
Preguntas Frecuentes (FAQ)
¿Por qué las soluciones electrolíticas no se comportan idealmente?
Las soluciones electrolíticas contienen iones cargados que interactúan fuertemente entre sí a través de fuerzas electrostáticas de Coulomb. Estas interacciones (atracción entre cargas opuestas y repulsión entre cargas iguales) afectan la “disponibilidad” efectiva de los iones para participar en procesos químicos, haciendo que su comportamiento se desvíe de lo predicho por las concentraciones molares o molales en modelos ideales.
¿Qué es la atmósfera iónica?
La atmósfera iónica es un concepto central de la teoría de Debye-Hückel. Se refiere a la nube difusa de iones de carga opuesta que rodea a un ion central en una solución electrolítica. Esta nube es el resultado del equilibrio dinámico entre la atracción electrostática del ion central y el movimiento térmico aleatorio de los iones en el solvente. Reduce la carga efectiva del ion central, impactando su comportamiento.
¿Cuándo debo usar la Ley Límite vs. la Ecuación Extendida de Debye-Hückel?
La Ley Límite de Debye-Hückel es aplicable y precisa solo para soluciones extremadamente diluidas (generalmente con fuerza iónica inferior a 0.001 M). Para concentraciones ligeramente más altas (hasta aproximadamente 0.01-0.1 M), donde el tamaño finito de los iones comienza a ser relevante, es preferible utilizar la Ecuación Extendida de Debye-Hückel, que incorpora el diámetro iónico efectivo.
¿Se puede medir experimentalmente el coeficiente de actividad de un solo ion?
No, el coeficiente de actividad de un ion individual no puede medirse experimentalmente de forma aislada. Esto se debe a que siempre debe haber electroneutralidad en la solución; no se puede añadir o quitar solo un tipo de ion. Los experimentos solo permiten determinar el coeficiente de actividad medio de un electrolito, que es un promedio de los coeficientes de los cationes y aniones que lo componen.
¿Qué representan las constantes A y B en las ecuaciones de Debye-Hückel?
Las constantes A y B en las ecuaciones de Debye-Hückel (y sus extensiones) son parámetros que dependen de las propiedades del solvente y la temperatura. La constante A (o Aγ) está relacionada con el efecto de las interacciones electrostáticas de largo alcance, mientras que la constante B (presente en la ecuación extendida) se relaciona con el tamaño de los iones y su capacidad para acercarse entre sí. Sus valores se derivan de constantes físicas fundamentales (carga del electrón, constante dieléctrica del solvente, temperatura, etc.) y se tabulan para diferentes solventes y temperaturas.
Si quieres conocer otros artículos parecidos a Desentrañando la Ecuación de Debye-Hückel puedes visitar la categoría Química.
