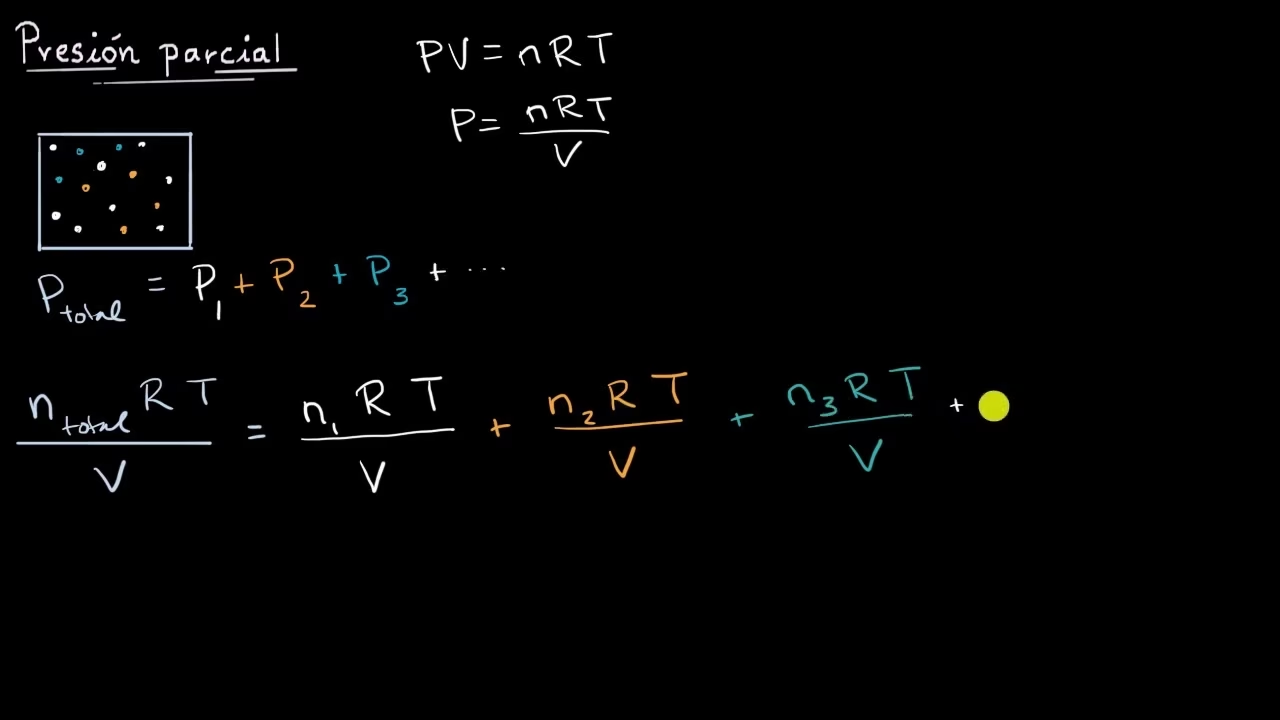21/02/2023
En el vasto universo de la química, el estudio de los gases ocupa un lugar fundamental. A diferencia de los líquidos y sólidos, los gases se expanden para llenar cualquier volumen disponible, y sus partículas se mueven de forma caótica y aleatoria. Cuando tenemos una mezcla de gases, la situación se vuelve aún más interesante, ya que cada gas contribuye de manera independiente a la presión total del recipiente. Aquí es donde entra en juego un concepto vital: la presión parcial.

La presión parcial es la presión que ejercería un gas individual si ocupara el mismo volumen total que la mezcla, a la misma temperatura. Es una herramienta indispensable para comprender el comportamiento de las mezclas gaseosas, desde la atmósfera que respiramos hasta los gases utilizados en la medicina o la industria. Este artículo te guiará a través de los principios fundamentales de la presión parcial, cómo calcularla y por qué es tan importante en diversas aplicaciones.
- ¿Qué es la Presión Parcial?
- Fracción Molar: La Clave para el Cálculo de la Presión Parcial
- Cómo Calcular la Presión Parcial: Paso a Paso
- Aplicaciones de la Presión Parcial en la Química y la Vida Cotidiana
- Diferencia entre Presión Parcial y Presión Total
- Factores que Afectan la Presión Parcial
- Limitaciones de la Ley de Dalton y Gases Reales
- Preguntas Frecuentes (FAQ)
- ¿Por qué es importante calcular la presión parcial?
- ¿La temperatura afecta la presión parcial?
- ¿Qué pasa si no conozco la presión total? ¿Puedo aún calcular la presión parcial?
- ¿La presión parcial depende del tipo de gas?
- ¿La presión parcial es lo mismo que la concentración?
- ¿Cómo se mide la presión parcial en la práctica?
- Conclusión
¿Qué es la Presión Parcial?
Imagina un recipiente lleno con una mezcla de oxígeno y nitrógeno. Aunque ambos gases están mezclados, cada uno de ellos ejerce una presión sobre las paredes del recipiente debido a las colisiones de sus moléculas. La presión parcial de cada gas es, en esencia, la contribución individual de ese gas a la presión total de la mezcla. Es como si cada gas estuviera solo en el recipiente, ejerciendo su propia presión.
Este concepto es crucial porque nos permite analizar el comportamiento de cada componente de una mezcla gaseosa de forma independiente. Por ejemplo, en el aire que respiramos, el oxígeno tiene una presión parcial específica que es vital para la respiración de los seres vivos, a pesar de que está mezclado con nitrógeno, argón y otros gases.
La Ley de Dalton de las Presiones Parciales
El concepto de presión parcial fue formulado por primera vez por el químico británico John Dalton a principios del siglo XIX. La Ley de Dalton de las Presiones Parciales establece que, en una mezcla de gases ideales, la presión total ejercida por la mezcla es igual a la suma de las presiones parciales de cada uno de los gases individuales que la componen. Matemáticamente, esto se expresa como:
Ptotal = P1 + P2 + P3 + ... + Pn
Donde Ptotal es la presión total de la mezcla, y P1, P2, P3, etc., son las presiones parciales de los gases individuales 1, 2, 3, y así sucesivamente hasta el gas n. Esta ley se cumple con bastante precisión para mezclas de gases ideales, es decir, aquellos gases cuyas moléculas no interactúan entre sí y ocupan un volumen despreciable en comparación con el volumen del recipiente.
La validez de la Ley de Dalton radica en la suposición de que las moléculas de cada gas actúan de forma independiente. No se atraen ni se repelen significativamente entre sí, y sus colisiones con las paredes del recipiente son las que generan la presión. Por lo tanto, la presencia de otros gases no altera la contribución de un gas específico a la presión total.
Fracción Molar: La Clave para el Cálculo de la Presión Parcial
Si bien la Ley de Dalton es fundamental, a menudo no conocemos directamente la presión parcial de cada gas. En su lugar, es más común conocer la composición de la mezcla en términos de la cantidad de cada gas presente, generalmente en moles. Aquí es donde la fracción molar se convierte en una herramienta indispensable.
La fracción molar (simbolizada como Xi o χi) de un componente en una mezcla es la relación entre el número de moles de ese componente y el número total de moles de todos los componentes en la mezcla. Es una forma de expresar la concentración de un componente en una mezcla en términos de moles.
La fórmula para la fracción molar de un gas 'i' es:
Xi = ni / ntotal
Donde ni es el número de moles del gas 'i', y ntotal es el número total de moles de todos los gases en la mezcla. La suma de las fracciones molares de todos los componentes en una mezcla siempre es igual a 1 (o 100% si se expresa como porcentaje).
Relación entre Fracción Molar y Presión Parcial
La belleza de la fracción molar radica en su relación directa con la presión parcial. Para una mezcla de gases ideales, la presión parcial de un gas es igual a su fracción molar multiplicada por la presión total de la mezcla. Esta es la fórmula clave para calcular la presión parcial:
Pi = Xi * Ptotal
Donde Pi es la presión parcial del gas 'i', Xi es la fracción molar del gas 'i', y Ptotal es la presión total de la mezcla gaseosa.
Esta relación se deriva de la Ley de los Gases Ideales (PV = nRT). Si consideramos un gas 'i' en una mezcla:
PiV = niRT
Y para la mezcla total:
PtotalV = ntotalRT
Dividiendo la primera ecuación por la segunda (asumiendo volumen y temperatura constantes para la mezcla y el gas individual), obtenemos:
(PiV) / (PtotalV) = (niRT) / (ntotalRT)
Simplificando, llegamos a:
Pi / Ptotal = ni / ntotal
Dado que ni / ntotal es la fracción molar (Xi), se deduce que:
Pi = Xi * Ptotal
Esta fórmula es increíblemente útil porque nos permite calcular la presión parcial de cualquier componente en una mezcla gaseosa, siempre y cuando conozcamos la composición molar de la mezcla y la presión total.
Cómo Calcular la Presión Parcial: Paso a Paso
Para calcular la presión parcial de un gas en una mezcla, sigue estos pasos:
- Identifica los gases y sus cantidades: Asegúrate de saber qué gases están presentes en la mezcla y, lo más importante, cuántos moles (o la masa para convertir a moles) de cada gas hay.
- Calcula el número total de moles (ntotal): Suma los moles de todos los gases individuales en la mezcla.
- Calcula la fracción molar (Xi) de cada gas: Divide el número de moles de cada gas individual (ni) por el número total de moles (ntotal).
- Determina la presión total (Ptotal) de la mezcla: Este valor generalmente se proporciona en el problema o se puede medir experimentalmente.
- Calcula la presión parcial (Pi) de cada gas: Multiplica la fracción molar de cada gas (Xi) por la presión total de la mezcla (Ptotal).
Ejemplo Práctico de Cálculo
Supongamos que tenemos un tanque que contiene una mezcla de gases con las siguientes cantidades a una temperatura constante de 25 °C y una presión total de 3.0 atm:
- 2.0 moles de Nitrógeno (N2)
- 1.0 mol de Oxígeno (O2)
- 0.5 moles de Dióxido de Carbono (CO2)
Vamos a calcular la presión parcial de cada gas.
Paso 1: Identificar y sumar los moles.
- Moles de N2 (nN2) = 2.0 mol
- Moles de O2 (nO2) = 1.0 mol
- Moles de CO2 (nCO2) = 0.5 mol
Paso 2: Calcular el número total de moles (ntotal).
ntotal = nN2 + nO2 + nCO2 = 2.0 mol + 1.0 mol + 0.5 mol = 3.5 mol
Paso 3: Calcular la fracción molar (Xi) de cada gas.
- Fracción molar de N2 (XN2) = nN2 / ntotal = 2.0 mol / 3.5 mol ≈ 0.571
- Fracción molar de O2 (XO2) = nO2 / ntotal = 1.0 mol / 3.5 mol ≈ 0.286
- Fracción molar de CO2 (XCO2) = nCO2 / ntotal = 0.5 mol / 3.5 mol ≈ 0.143
Verificación: 0.571 + 0.286 + 0.143 = 1.000 (la suma es 1, lo cual es correcto)
Paso 4: Determinar la presión total (Ptotal).
Ptotal = 3.0 atm (dado en el problema)
Paso 5: Calcular la presión parcial (Pi) de cada gas.
- Presión parcial de N2 (PN2) = XN2 * Ptotal = 0.571 * 3.0 atm ≈ 1.713 atm
- Presión parcial de O2 (PO2) = XO2 * Ptotal = 0.286 * 3.0 atm ≈ 0.858 atm
- Presión parcial de CO2 (PCO2) = XCO2 * Ptotal = 0.143 * 3.0 atm ≈ 0.429 atm
Verificación final (suma de presiones parciales):
PN2 + PO2 + PCO2 = 1.713 atm + 0.858 atm + 0.429 atm = 3.000 atm
La suma de las presiones parciales es igual a la presión total, lo que confirma que nuestros cálculos son correctos y que la Ley de Dalton se cumple.

Aplicaciones de la Presión Parcial en la Química y la Vida Cotidiana
El concepto de presión parcial no es solo un ejercicio académico; tiene profundas implicaciones y aplicaciones en diversas áreas:
- Buceo y Medicina Hiperbárica: La presión parcial de los gases es crítica. A medida que un buzo desciende, la presión total del agua aumenta, lo que a su vez eleva las presiones parciales de los gases en el aire que respira. Un aumento excesivo de la presión parcial de nitrógeno puede causar narcosis por nitrógeno, mientras que una presión parcial de oxígeno demasiado alta puede provocar toxicidad por oxígeno. Las mezclas de gases para buceo (como el Nitrox, que tiene más oxígeno y menos nitrógeno) se diseñan cuidadosamente para controlar las presiones parciales de los componentes. Las cámaras hiperbáricas utilizan la presión parcial controlada de oxígeno para tratar diversas afecciones, como la intoxicación por monóxido de carbono o la enfermedad de descompresión.
- Respiración y Fisiología: En el cuerpo humano, la respiración es un proceso impulsado por las diferencias en las presiones parciales. El oxígeno tiene una presión parcial más alta en los alvéolos pulmonares que en la sangre, lo que facilita su difusión hacia el torrente sanguíneo. De manera similar, el dióxido de carbono se mueve de la sangre (donde su presión parcial es más alta) a los alvéolos para ser exhalado.
- Meteorología y Ciencia Atmosférica: La atmósfera es una mezcla compleja de gases. Los meteorólogos utilizan las presiones parciales para comprender el comportamiento de los diferentes componentes, como el vapor de agua. La presión parcial de vapor de agua es un indicador clave de la humedad y es fundamental para predecir la formación de nubes y precipitaciones.
- Procesos Industriales: En la industria química, muchos procesos implican reacciones con mezclas de gases. El control de las presiones parciales de los reactivos y productos es esencial para optimizar el rendimiento de la reacción, la separación de gases y la seguridad. Por ejemplo, en la producción de amoníaco (proceso Haber-Bosch), las presiones parciales de nitrógeno e hidrógeno son cuidadosamente controladas.
- Anestesia: Los anestesiólogos deben controlar con precisión las presiones parciales de los gases anestésicos inhalados para garantizar una anestesia segura y efectiva, evitando tanto una subdosificación como una sobredosis.
Diferencia entre Presión Parcial y Presión Total
Es fundamental no confundir la presión parcial con la presión total. La presión total es la suma de todas las contribuciones de presión de cada gas individual en una mezcla. Es la medida macroscópica de la fuerza por unidad de área que la mezcla gaseosa ejerce sobre las paredes de su contenedor. Por otro lado, la presión parcial es la contribución específica de un solo gas a esa presión total, como si ese gas estuviera solo en el recipiente. Mientras que la presión total nos da una idea general de la fuerza del gas, la presión parcial nos permite entender el comportamiento individual de cada componente de la mezcla, lo cual es crucial para reacciones químicas, procesos biológicos y aplicaciones técnicas.
Factores que Afectan la Presión Parcial
Dado que la presión parcial está directamente relacionada con la presión total y la fracción molar, los factores que afectan a estos últimos también influirán en la presión parcial:
- Cantidad de Sustancia (Moles): Un aumento en el número de moles de un gas específico en la mezcla (manteniendo los demás factores constantes) aumentará su fracción molar y, por lo tanto, su presión parcial.
- Volumen: Si el volumen del recipiente que contiene la mezcla de gases disminuye (a temperatura y moles constantes), la presión total aumentará. Consecuentemente, las presiones parciales de todos los gases en la mezcla también aumentarán. Esto se debe a que las moléculas tienen menos espacio para moverse y colisionan con las paredes con mayor frecuencia.
- Temperatura: Un aumento en la temperatura de la mezcla de gases (a volumen y moles constantes) provocará un aumento en la energía cinética promedio de las moléculas, lo que resultará en colisiones más fuertes y frecuentes con las paredes del recipiente. Esto elevará la presión total y, por ende, las presiones parciales de todos los gases.
Es importante recordar que, según la Ley de Dalton, la presión parcial de un gas no se ve afectada por la presencia o ausencia de otros gases, solo por su propia cantidad, el volumen del recipiente y la temperatura.
Limitaciones de la Ley de Dalton y Gases Reales
Si bien la Ley de Dalton es una herramienta poderosa y generalmente precisa para mezclas de gases, es importante recordar que se basa en el modelo de los gases ideales. Los gases ideales son una idealización teórica que asume que las moléculas de gas no tienen volumen y no ejercen interacciones moleculares (atracción o repulsión) entre sí. En la realidad, todos los gases son "gases reales" y sus moléculas sí tienen un volumen finito y sí interactúan.
Para la mayoría de las aplicaciones a presiones moderadas y temperaturas elevadas, la Ley de Dalton proporciona una excelente aproximación. Sin embargo, en condiciones de muy alta presión o muy baja temperatura, donde las moléculas de gas están muy cerca unas de otras y las fuerzas intermoleculares se vuelven significativas, las desviaciones del comportamiento ideal pueden ser notables. En estos casos, se requerirían ecuaciones de estado más complejas, como la ecuación de Van der Waals, para predecir con mayor precisión el comportamiento de los gases reales y sus presiones parciales.
Tabla Comparativa: Leyes de los Gases Ideales
Para contextualizar la Ley de Dalton, es útil compararla con otras leyes fundamentales de los gases ideales:
| Ley del Gas | Descripción | Relación Matemática | Constantes |
|---|---|---|---|
| Ley de Boyle | La presión de una cantidad fija de gas es inversamente proporcional a su volumen. | P₁V₁ = P₂V₂ | Temperatura (T), Moles (n) |
| Ley de Charles | El volumen de una cantidad fija de gas es directamente proporcional a su temperatura absoluta. | V₁/T₁ = V₂/T₂ | Presión (P), Moles (n) |
| Ley de Gay-Lussac | La presión de una cantidad fija de gas es directamente proporcional a su temperatura absoluta. | P₁/T₁ = P₂/T₂ | Volumen (V), Moles (n) |
| Ley de Avogadro | Volúmenes iguales de todos los gases, a la misma temperatura y presión, tienen el mismo número de moléculas (o moles). | V₁/n₁ = V₂/n₂ | Temperatura (T), Presión (P) |
| Ley de Dalton | La presión total de una mezcla de gases es la suma de las presiones parciales de los gases individuales. | Ptotal = P₁ + P₂ + ... | Temperatura (T), Volumen (V) |
| Ley de los Gases Ideales | Combina las leyes anteriores en una sola ecuación que relaciona presión, volumen, temperatura y cantidad de gas. | PV = nRT | R (Constante de los gases) |
Como se puede observar, la Ley de Dalton complementa las otras leyes al enfocarse en el comportamiento de mezclas de gases, mientras que las demás suelen describir el comportamiento de un solo gas o una cantidad fija de gas bajo diferentes condiciones.
Preguntas Frecuentes (FAQ)
¿Por qué es importante calcular la presión parcial?
El cálculo de la presión parcial es crucial porque nos permite comprender el comportamiento individual de cada gas en una mezcla. Esto es fundamental en campos como la medicina (respiración, anestesia), la oceanografía (buceo), la ingeniería química (diseño de procesos) y la meteorología (humedad atmosférica), donde las concentraciones y actividades de gases específicos son más relevantes que la presión total.
¿La temperatura afecta la presión parcial?
Sí, la temperatura afecta la presión parcial. Un aumento en la temperatura, manteniendo el volumen y la cantidad de moles constantes, aumentará la presión total de la mezcla de gases. Dado que la presión parcial de cada gas es una fracción de la presión total (Pi = Xi * Ptotal), un aumento en la presión total resultará en un aumento proporcional en la presión parcial de cada gas.
¿Qué pasa si no conozco la presión total? ¿Puedo aún calcular la presión parcial?
No directamente con la fórmula Pi = Xi * Ptotal. Si no conoces la presión total, pero conoces los moles de cada gas, el volumen del recipiente y la temperatura, puedes calcular la presión parcial de cada gas individualmente utilizando la Ley de los Gases Ideales (PV = nRT). Es decir, Pi = (niRT) / V. Una vez que tengas las presiones parciales de todos los gases, puedes sumarlas para encontrar la presión total, lo que te permitiría verificar tus cálculos con la Ley de Dalton.
¿La presión parcial depende del tipo de gas?
Sí y no. La Ley de Dalton asume que los gases se comportan idealmente, lo que significa que la identidad química del gas no afecta directamente su contribución a la presión total más allá de su cantidad molar. Sin embargo, en gases reales, las interacciones moleculares entre diferentes tipos de gases pueden causar pequeñas desviaciones del comportamiento ideal. Además, la masa molar de un gas afectará su densidad, pero no su presión parcial directamente si se considera un gas ideal a la misma temperatura y volumen.
¿La presión parcial es lo mismo que la concentración?
No son lo mismo, pero están estrechamente relacionadas. La presión parcial es una medida de la presión que un gas individual ejerce en una mezcla, mientras que la concentración se refiere a la cantidad de una sustancia en un volumen dado (por ejemplo, moles por litro). Para gases ideales, la presión parcial es directamente proporcional a la concentración molar del gas en la mezcla, siempre que la temperatura sea constante. Es decir, una mayor concentración de un gas resultará en una mayor presión parcial de ese gas.
¿Cómo se mide la presión parcial en la práctica?
Directamente, es difícil medir la presión parcial de un gas específico en una mezcla sin separarlo. Sin embargo, se pueden usar técnicas como la espectrometría de masas para determinar la composición molar de la mezcla, y luego, con una medición de la presión total (usando un manómetro), se pueden calcular las presiones parciales utilizando la fracción molar. En entornos médicos, se utilizan analizadores de gases para medir las concentraciones de gases respiratorios, que luego se convierten a presiones parciales.
Conclusión
La presión parcial es un concepto fundamental en la química y en diversas disciplinas científicas y tecnológicas. Nos permite desglosar la presión total de una mezcla gaseosa en las contribuciones individuales de cada componente, ofreciendo una visión más profunda de su comportamiento. La Ley de Dalton, junto con el concepto de fracción molar, proporciona una herramienta sencilla y efectiva para calcular estas presiones parciales, abriendo la puerta a una comprensión más completa de sistemas complejos. Dominar este concepto no solo es esencial para cualquier estudiante de química, sino también para profesionales en campos donde los gases juegan un papel crucial.
Si quieres conocer otros artículos parecidos a Presión Parcial: La Clave de las Mezclas Gaseosas puedes visitar la categoría Química.