03/11/2025
En nuestro día a día, nos encontramos constantemente con soluciones: desde el aire que respiramos hasta la sal que usamos para cocinar, pasando por las bebidas que consumimos y los medicamentos que nos curan. Muchas veces, estas soluciones vienen con una etiqueta que indica un porcentaje, como “4%” o “5%”. Pero, ¿qué significa exactamente este valor? Comprender la concentración de una solución es fundamental, no solo para científicos o químicos, sino para cualquier persona que desee entender mejor el mundo que le rodea y tomar decisiones informadas sobre los productos que utiliza.
Este artículo te guiará a través de los conceptos esenciales de las soluciones, desglosando qué es un soluto y un solvente, cómo se define la concentración y qué implican esos porcentajes tan comunes. Prepárate para descubrir la ciencia detrás de las mezclas que forman parte de nuestra vida cotidiana.
- Entendiendo las Soluciones: Solutos y Solventes
- Desentrañando la Concentración: ¿Qué Significa un Porcentaje?
- La Importancia de la Concentración en la Vida Cotidiana
- Preparación de una Solución: Un Proceso Preciso
- La Solubilidad: ¿Cuánto Soluto Puede Disolverse?
- Tabla Comparativa: Conceptos Clave de Soluciones
- Preguntas Frecuentes sobre Soluciones y Concentraciones
- Conclusión
Entendiendo las Soluciones: Solutos y Solventes
Antes de sumergirnos en los porcentajes, es crucial entender qué es una solución. Una solución es una mezcla homogénea de dos o más sustancias, lo que significa que sus componentes están distribuidos de manera uniforme y no pueden distinguirse a simple vista. Piensa en el agua con sal: una vez disuelta, no puedes ver los cristales de sal individuales; solo percibes un líquido transparente.
Toda solución está compuesta por dos partes principales:
- Solvente: Es el componente que se encuentra en mayor proporción en la solución y es el medio en el cual se disuelve el otro componente. Aunque comúnmente lo asociamos con líquidos como el agua (el solvente universal por excelencia), un solvente también puede ser un gas (como el nitrógeno en el aire) o incluso un sólido.
- Soluto: Es el componente que se encuentra en menor proporción y es el que se disuelve en el solvente. El soluto puede ser un sólido (como la sal de mesa), un líquido (como el ácido acético en el vinagre) o un gas (como el oxígeno en el aire). Una solución puede contener uno o varios solutos disueltos en un único solvente.
Un ejemplo claro es el aire. Aunque no lo pensemos como una solución en el sentido tradicional de “líquido con algo disuelto”, químicamente lo es. El nitrógeno, que constituye aproximadamente el 78% del aire puro, actúa como el solvente, mientras que el oxígeno, el vapor de agua, el dióxido de carbono y otros gases nobles son los solutos. Si el aire está contaminado, contendrá aún más gases y partículas disueltas en el nitrógeno.
Tipos de Soluciones Según el Estado de Agregación
Las soluciones pueden clasificarse según el estado físico del soluto y del solvente. Aquí algunos ejemplos:
- Líquido-Sólido: Agua con sal, azúcar disuelta en café.
- Líquido-Líquido: Alcohol en agua (bebidas alcohólicas), vinagre (ácido acético en agua).
- Líquido-Gas: Bebidas carbonatadas (dióxido de carbono en agua).
- Gas-Gas: Aire (nitrógeno, oxígeno, etc.).
- Sólido-Sólido: Aleaciones metálicas como el bronce (cobre y estaño), el acero (hierro y carbono).
- Gas-Sólido: Hidrógeno disuelto en paladio.
Desentrañando la Concentración: ¿Qué Significa un Porcentaje?
La concentración de una solución es una medida que nos indica la cantidad de soluto disuelto en una determinada cantidad de solvente o de solución total. Es una forma de cuantificar “cuán fuerte” o “cuán diluida” está una solución. Los porcentajes son una de las formas más comunes y comprensibles de expresar esta concentración.
Cuando vemos un porcentaje en una solución, generalmente se refiere a una de las siguientes expresiones:
Porcentaje Volumen/Volumen (% v/v)
Esta expresión se utiliza cuando tanto el soluto como el solvente son líquidos. Indica los mililitros (ml) de soluto presentes en cada 100 ml de solución. Es muy común en bebidas alcohólicas o en productos químicos líquidos.
- Ejemplo: Si una bebida alcohólica tiene una graduación de 42° (lo que equivale a 42% v/v), significa que contiene 42 ml de alcohol puro por cada 100 ml de la bebida total. Por lo tanto, si tienes una botella de 750 ml de esta bebida, contendrá 750 ml * (42/100) = 315 ml de alcohol.
- ¿Qué significa una solución al 5% v/v? Si el vinagre es una solución acuosa al 5% de ácido acético, quiere decir que contiene 5 cm³ (que es equivalente a 5 ml) de ácido acético por cada 100 cm³ de solución total. Esto implica que los restantes 95 cm³ son agua (el solvente).
Porcentaje Masa/Volumen (% m/V) o Peso/Volumen (% p/V)
Esta expresión se utiliza cuando el soluto es un sólido y el solvente es un líquido. Indica los gramos (g) de soluto presentes en cada 100 ml de solución. Es común en soluciones salinas, medicamentos o productos de limpieza.
- Ejemplo: Si una solución salina es de 4% m/V, implica que tiene 4 gramos de sal (el soluto) disueltos en cada 100 ml de la solución total. Esto es crucial en aplicaciones médicas, donde la precisión es vital. Por ejemplo, una solución salina fisiológica estándar es de 0.9% m/V de cloruro de sodio, lo que significa 0.9 gramos de sal por cada 100 ml de solución, una concentración muy similar a la de los fluidos corporales.
- ¿Qué significa una solución al 5% m/V? En este caso, significaría que hay 5 gramos de soluto disueltos en 100 ml de la solución total. Si estuviéramos hablando de una solución de azúcar, serían 5g de azúcar por cada 100ml de la solución azucarada.
Porcentaje Masa/Masa (% m/m) o Peso/Peso (% p/p)
Aunque no se menciona explícitamente en el texto proporcionado, es otra forma común de expresar la concentración. Indica los gramos (g) de soluto presentes en cada 100 gramos de solución total. Se usa a menudo en productos sólidos o cuando se busca una alta precisión independiente de la temperatura.
La Importancia de la Concentración en la Vida Cotidiana
La concentración de una solución es un parámetro crítico que determina sus propiedades y aplicaciones. Una misma sustancia puede tener usos muy diferentes dependiendo de su concentración:
- Cloruro de Sodio (Sal): Una solución muy concentrada de cloruro de sodio se conoce como salmuera. Esta se utiliza tradicionalmente para salar y conservar alimentos, debido a sus propiedades antimicrobianas. En contraste, una solución mucho más diluida, como la solución salina fisiológica (0.9% m/V), se utiliza en medicina para hidratación intravenosa, limpieza de heridas o lentes de contacto, ya que es isotónica con los fluidos corporales, es decir, tiene una concentración de solutos similar.
- Ácido Acético: El vinagre es una solución de ácido acético al 5%. Sin embargo, el ácido acético puro (ácido acético glacial) es un corrosivo fuerte con usos industriales muy distintos.
Comprender estas diferencias es esencial para la seguridad y la efectividad de muchos productos que utilizamos a diario.
Preparación de una Solución: Un Proceso Preciso
La preparación de una solución con una concentración específica es una habilidad fundamental en química y requiere precisión. A continuación, se detalla un procedimiento general para preparar una solución de un sólido en un líquido, siguiendo los principios mencionados:
Materiales Necesarios:
- Un sólido (ej. cloruro de sodio o bicarbonato de sodio)
- Un recipiente para pesar el sólido (vaso de precipitados pequeño o papel de pesaje)
- Una balanza (analítica si se requiere alta precisión)
- Una espátula o cuchara
- Vaso de precipitados (para disolver el sólido)
- Embudo
- Matraz aforado (recipiente graduado para volumen exacto)
- Gotero (para añadir líquido con precisión)
- Agua destilada (o el solvente adecuado)
- Varilla de vidrio para agitar
Procedimiento:
- Pesaje del Soluto: Pesar el vaso de precipitados vacío y anotar su masa. Luego, añadir cuidadosamente el sólido elegido al vaso de precipitados hasta alcanzar la masa deseada del soluto. Anotar la masa total (vaso + sólido) y calcular la masa neta del sólido utilizado.
- Disolución del Soluto: Transferir el sólido pesado a un vaso de precipitados más grande (si es necesario). Añadir una parte del agua destilada (el solvente) al vaso de precipitados, pero no todo el volumen final. Agitar cuidadosamente con la varilla de vidrio hasta que el sólido se disuelva completamente. Es importante asegurarse de que el soluto esté totalmente disuelto antes de continuar.
- Transferencia a Matraz Aforado: Con la ayuda de un embudo y la varilla de vidrio, transferir la solución disuelta al matraz aforado (el recipiente de volumen exacto).
- Enjuague y Transferencia Adicional: Para asegurar que todo el soluto disuelto sea transferido, enjuagar el vaso de precipitados, el embudo y la varilla de vidrio varias veces con pequeñas porciones de agua destilada. Verter estas porciones de enjuague también al matraz aforado. Es crucial no sobrepasar la marca de aforo del matraz en esta etapa.
- Aforo Final: Una vez que la mayor parte del volumen se ha transferido, comenzar a añadir agua destilada lentamente con un gotero, hasta que el menisco (la curva de la superficie del líquido) toque exactamente la marca de aforo del matraz. Es importante que el ojo esté a nivel de la marca para evitar errores de paralaje.
- Homogeneización: Tapar el matraz aforado con un tapón y mezclar el contenido invirtiendo el matraz varias veces. Esto asegura que la solución sea completamente homogénea y que la concentración sea uniforme en todo el volumen.
Cálculo de la Concentración:
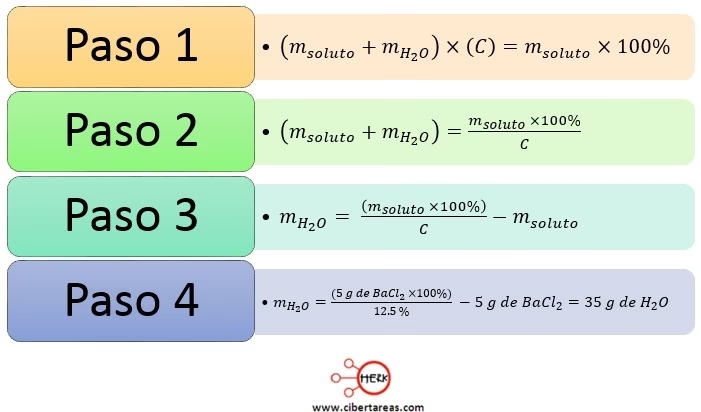
Para verificar la concentración obtenida, se pueden usar proporciones simples. Si se disolvieron 'X' gramos de sólido en 'Y' cm³ de solución, la concentración en gramos de sólido por 100 cm³ de solución (es decir, el porcentaje m/V) se calcula como:
Concentración (% m/V) = (Masa de sólido utilizado en gramos / Volumen de solución en cm³) * 100
La Solubilidad: ¿Cuánto Soluto Puede Disolverse?
Un concepto íntimamente relacionado con la concentración es la solubilidad. La solubilidad de una sustancia es la cantidad máxima de esa sustancia que puede disolverse en una determinada cantidad de solvente a una temperatura específica. Se expresa comúnmente en gramos de sustancia por 100 cm³ (o 100 ml) de solvente.
Cuanto mayor sea la masa que se puede disolver, más soluble es la sustancia. Por ejemplo, si se puede disolver una gran cantidad de azúcar en agua, decimos que el azúcar es muy soluble en agua.
La mayoría de los compuestos iónicos, como la sal de mesa (cloruro de sodio), son muy solubles en agua. Esto se debe a que las moléculas de agua son polares y pueden rodear a los iones individuales del compuesto iónico, separándolos y manteniéndolos dispersos en la solución.
Ejemplo: El Agua de Mar y la Solubilidad
El agua de mar es un excelente ejemplo de una solución compleja, con muchos minerales disueltos. La extracción de sal de mesa del agua de mar es un proceso que aprovecha las diferencias en la solubilidad y los cambios de estado. Al calentar el agua de mar (generalmente por evaporación solar en piletas), el solvente (agua) cambia de estado de líquido a gas (evaporación). A medida que el agua se evapora, la concentración de las sales disueltas aumenta. Las sales menos solubles comienzan a precipitar (cristalizar) primero, mientras que las más solubles permanecen en solución hasta que la concentración es muy alta o el agua se evapora casi por completo.
En la práctica, el cloruro de sodio (sal de mesa) es el compuesto más abundante y uno de los más solubles en el agua de mar, pero no el único. Otros compuestos como el sulfato de calcio (yeso) o el carbonato de calcio son menos solubles y precipitan antes o en diferentes etapas del proceso de evaporación.
Tabla Comparativa: Conceptos Clave de Soluciones
| Concepto | Definición | Ejemplo |
|---|---|---|
| Solución | Mezcla homogénea de dos o más sustancias. | Agua con sal, aire. |
| Solvente | Componente en mayor proporción, donde se disuelve el soluto. | Agua (en agua salada), Nitrógeno (en aire). |
| Soluto | Componente en menor proporción, que se disuelve en el solvente. | Sal (en agua salada), Oxígeno (en aire). |
| Concentración | Cantidad de soluto disuelto en una cantidad de solvente o solución. | 5% de ácido acético en vinagre. |
| Solubilidad | Cantidad máxima de sustancia que puede disolverse en un solvente a una temperatura dada. | Capacidad máxima de azúcar que se disuelve en agua. |
Preguntas Frecuentes sobre Soluciones y Concentraciones
¿Cuál es la diferencia entre una solución concentrada y una diluida?
Una solución concentrada contiene una gran cantidad de soluto disuelto en relación con la cantidad de solvente o solución. Una solución diluida, por el contrario, contiene una pequeña cantidad de soluto. Son términos relativos; por ejemplo, una solución al 10% es más concentrada que una al 2% de la misma sustancia.
¿La temperatura afecta la solubilidad de una sustancia?
Sí, la temperatura afecta significativamente la solubilidad. Para la mayoría de los sólidos en líquidos, la solubilidad aumenta con la temperatura. Esto significa que puedes disolver más azúcar en agua caliente que en agua fría. Sin embargo, para los gases en líquidos, la solubilidad generalmente disminuye a medida que aumenta la temperatura (por eso las bebidas carbonatadas pierden su burbujeo más rápido cuando están calientes).
¿Se puede disolver cualquier cantidad de soluto en un solvente?
No. Existe un límite para la cantidad de soluto que puede disolverse en un solvente a una temperatura dada. Cuando se ha disuelto la máxima cantidad de soluto posible, la solución se denomina saturada. Si se añade más soluto a una solución saturada, este no se disolverá y precipitará o quedará sin disolver en el fondo.
¿Qué otras formas hay de expresar la concentración además de los porcentajes?
Además de los porcentajes (m/V, v/v, m/m), la concentración se puede expresar de muchas otras maneras en química, dependiendo del contexto y la precisión requerida. Algunas de las más comunes incluyen:
- Molaridad (M): Moles de soluto por litro de solución.
- Molalidad (m): Moles de soluto por kilogramo de solvente.
- Partes por millón (ppm): Se usa para concentraciones muy bajas, indicando miligramos de soluto por litro de solución o por kilogramo de solución.
- Fracción molar: La relación entre el número de moles de un componente y el número total de moles de todos los componentes de la solución.
Los porcentajes son una forma sencilla y práctica para muchas aplicaciones cotidianas.
Conclusión
Entender qué significa un porcentaje en una solución nos abre las puertas a una comprensión más profunda de los productos que nos rodean, desde el café que bebemos hasta los medicamentos que nos curan. Los porcentajes de concentración son una herramienta fundamental para comunicar la composición de las mezclas y garantizar su uso adecuado y seguro. Ya sea un 4% de sal en una solución fisiológica o un 5% de ácido acético en el vinagre, cada número tiene un significado preciso que impacta directamente en las propiedades y aplicaciones de esa solución. La próxima vez que veas un porcentaje en una etiqueta, sabrás que detrás de ese número hay una ciencia fascinante que rige cómo interactúan las sustancias en el mundo que habitamos.
Si quieres conocer otros artículos parecidos a ¿Qué Significa un Porcentaje en una Solución? puedes visitar la categoría Química.

