02/01/2024
Cada vez que miramos una gota de agua, estamos presenciando una maravilla microscópica. Es una entidad tan común, tan fundamental para la vida, que rara vez nos detenemos a considerar la complejidad oculta en su interior. ¿Alguna vez te has preguntado cuántas moléculas de agua existen en esa minúscula gota que resbala por tu ventana o que cae de un grifo? La respuesta es asombrosa y nos conecta directamente con los principios fundamentales de la química. Este artículo no solo te mostrará cómo calcular este número colosal, sino que también explorará las increíbles propiedades que hacen del agua la sustancia vital que conocemos.

¿Qué es el Agua a Nivel Molecular?
El agua, conocida científicamente como oxidano o H₂O, es un compuesto químico inorgánico fundamental. Su estructura es engañosamente simple: dos átomos de hidrógeno (H) unidos a un átomo de oxígeno (O). Sin embargo, esta sencilla combinación da lugar a una molécula con propiedades extraordinarias, esenciales para la vida tal como la conocemos. El agua es el medio en el que ocurren innumerables procesos metabólicos en los seres vivos y es la base de los ecosistemas terrestres y acuáticos.
Presente en la naturaleza en sus tres estados (sólido, líquido y gaseoso), el agua líquida es la forma más común en la superficie de la Tierra, cubriendo la mayor parte de nuestro planeta en océanos, mares, ríos y lagos. Es crucial diferenciar el agua potable, que es una mezcla con sales disueltas, del agua pura o destilada, utilizada en laboratorios y aplicaciones científicas para evitar interferencias.
Históricamente, el agua fue considerada un elemento hasta que Henry Cavendish demostró en 1781 que era una sustancia compuesta. Más tarde, Antoine Laurent de Lavoisier y Joseph Louis Gay-Lussac confirmaron su composición de hidrógeno y oxígeno. La molécula de agua adopta una geometría no lineal, con los dos átomos de hidrógeno formando un ángulo de aproximadamente 104.45 grados. Esta configuración, junto con la mayor electronegatividad del átomo de oxígeno, confiere a la molécula una marcada polaridad. Esto significa que un lado de la molécula tiene una ligera carga negativa y el otro una ligera carga positiva, lo que le permite formar hasta cuatro puentes de hidrógeno con moléculas circundantes. Estos enlaces, aunque más débiles que los covalentes, son responsables de muchas de las propiedades únicas del agua.
La Clave del Conteo: El Mol y el Número de Avogadro
Contar individualmente las moléculas de agua en una gota sería una tarea imposible, dada la inmensidad de su número. Aquí es donde entra en juego el concepto de Mol y el Número de Avogadro, herramientas fundamentales en química para manejar cantidades microscópicas a escala macroscópica. Un Mol es una unidad de medida que representa una cantidad específica de partículas (átomos, moléculas, iones, etc.), análoga a una docena para huevos o un par para zapatos.
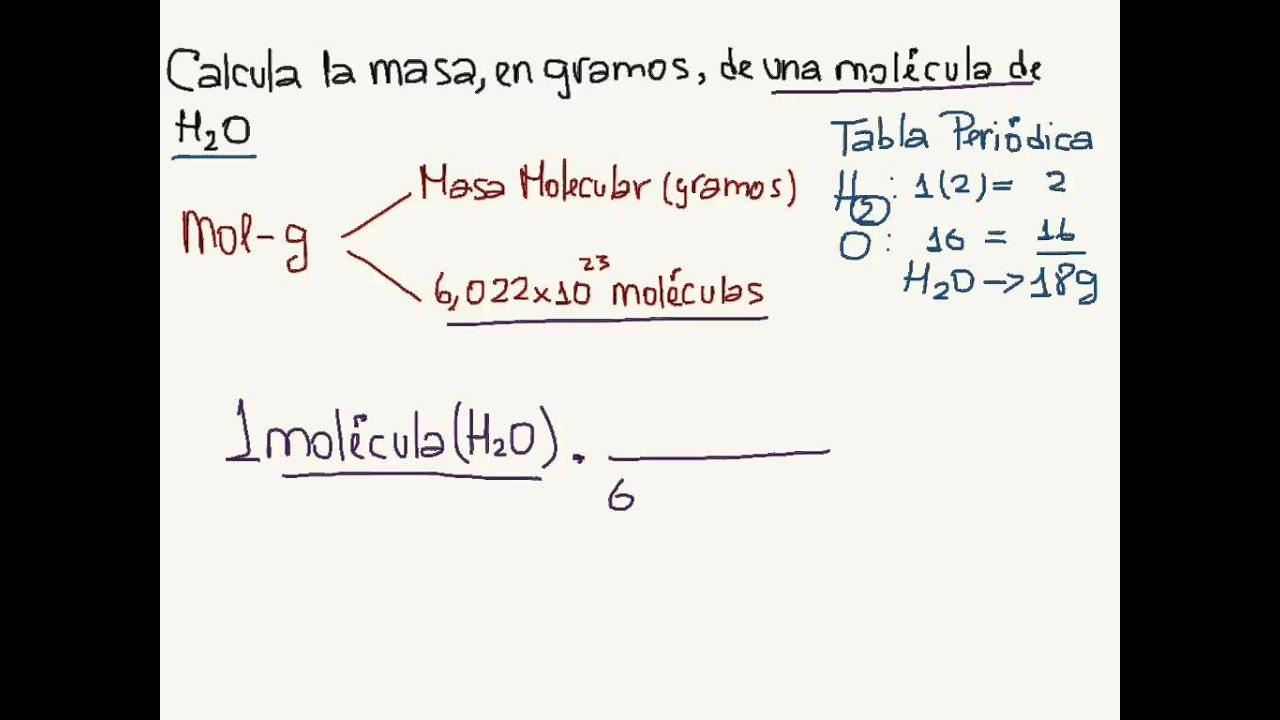
El Número de Avogadro, que tiene un valor de aproximadamente $6.022 imes 10^{23}$, es la cantidad de partículas contenidas en un mol de cualquier sustancia. Este número es una constante universal, que subraya el hecho de que un mol de hidrógeno, un mol de oro o un mol de agua, todos contienen el mismo número de partículas. Fue el físico italiano Amedeo Avogadro quien sentó las bases para este concepto, revolucionando la forma en que entendemos y medimos las sustancias químicas. La masa molar del agua, que es la masa de un mol de moléculas de agua, es de 18 gramos por mol (calculada a partir de la masa atómica del hidrógeno (aprox. 1 g/mol) y el oxígeno (aprox. 16 g/mol): $2 imes 1 + 16 = 18$ g/mol).
Desglose del Cálculo: ¿Cuántas Moléculas en una Gota de Agua?
Para ilustrar cómo se calcula el número de moléculas de agua, tomemos el ejemplo de una gota de agua con un volumen de 0.0018 mL a temperatura ambiente. El proceso implica tres pasos clave, utilizando fórmulas básicas de densidad y el concepto de mol.
Paso 1: Calcular la Masa de Agua
La densidad es una propiedad física que relaciona la masa de una sustancia con su volumen. Para el agua, a temperatura ambiente, su densidad es aproximadamente $1 ext{ g/mL}$.
La fórmula de la densidad es:
Densidad = Masa / Volumen
Rearreglando la fórmula para encontrar la masa, obtenemos:
Masa = Densidad × Volumen
Sustituyendo los valores conocidos:
Masa = 1 g/mL × 0.0018 mL = 0.0018 gramos
Por lo tanto, una gota de agua de 0.0018 mL tiene una masa de 0.0018 gramos.
Paso 2: Calcular el Número de Moles
Una vez que tenemos la masa de agua, podemos convertirla en moles utilizando la masa molar del agua. Como mencionamos, la masa molar del agua (H₂O) es de 18 g/mol.

La fórmula para calcular el número de moles es:
Número de Moles = Masa Dada / Masa Molar
Sustituyendo los valores:
Número de Moles = 0.0018 g / 18 g/mol = 0.0001 moles
Esto significa que en una gota de agua de 0.0018 mL, hay 0.0001 moles de moléculas de agua.
Paso 3: Calcular el Número de Moléculas
Finalmente, para obtener el número total de moléculas, multiplicamos el número de moles por el Número de Avogadro ($6.022 imes 10^{23}$ moléculas/mol).
Número de Moléculas = Número de Moles × Número de Avogadro
Sustituyendo los valores:
Número de Moléculas = 0.0001 moles × 6.022 × 10^23 moléculas/mol = 6.022 × 10^19 moléculas
Así, una pequeña gota de agua de 0.0018 mL contiene la asombrosa cantidad de aproximadamente $6.022 imes 10^{19}$ moléculas de agua. Este número es incomprensiblemente grande y subraya la naturaleza densamente poblada del mundo molecular.
Más Allá de los Números: Propiedades Fascinantes del Agua
La inmensa cantidad de moléculas y su particular estructura molecular confieren al agua una serie de propiedades únicas que son vitales para la vida y para los procesos geológicos y químicos. El agua es inodora, incolora e insípida, pero su importancia va mucho más allá de estas características.
Agua como Disolvente Universal
El agua es frecuentemente llamada el “solvente universal” debido a su notable capacidad para disolver una vasta gama de compuestos sólidos, líquidos y gaseosos. Su naturaleza polar le permite interactuar eficazmente con sustancias iónicas y polares, como la sal de mesa (cloruro de sodio), envolviendo sus iones y dispersándolos en la solución. Esta cualidad es de suma importancia para los procesos biológicos, facilitando el transporte de nutrientes y la eliminación de desechos en los organismos vivos. Sin embargo, el agua no disuelve sustancias fuertemente apolares, como los aceites, lo que es fundamental para la integridad de las membranas celulares.
Cohesión y Adhesión: Las Fuerzas Internas del Agua
La cohesión es la propiedad por la cual las moléculas de agua se atraen fuertemente entre sí, principalmente a través de los puentes de hidrógeno. Esta interacción crea una estructura compacta que hace que el agua sea casi incompresible, permitiendo que funcione como un esqueleto hidrostático en algunos organismos. La fuerza de cohesión es la razón por la que el agua forma gotas y se mantiene líquida a temperaturas no extremas. Por otro lado, la adhesión es la tendencia del agua a ser atraída y adherirse a otras superficies, gracias a su gran potencial de polaridad.
Tensión Superficial y Acción Capilar
La elevada cohesión entre las moléculas de agua en su superficie genera una alta tensión superficial. Esto hace que la superficie del líquido se comporte como una película elástica, permitiendo que objetos ligeros, como algunos insectos, floten o incluso caminen sobre ella sin hundirse. La tensión superficial también es la razón por la que las gotas de agua mantienen su forma esférica. Relacionada con la adhesión y cohesión, la acción capilar es la capacidad del agua para ascender o descender por tubos estrechos, o capilares. Este fenómeno es crucial para el transporte de agua y nutrientes en las plantas, desde las raíces hasta las hojas.
Calor Específico y Regulación Térmica
El agua posee un calor específico excepcionalmente alto, lo que significa que puede absorber o liberar grandes cantidades de calor con cambios mínimos en su temperatura. Esta propiedad se debe a la energía necesaria para romper y formar los puentes de hidrógeno. El alto calor específico del agua la convierte en un regulador térmico excelente, moderando las temperaturas climáticas en las zonas costeras y ayudando a los organismos vivos a mantener una temperatura corporal constante. Para evaporar el agua, se requiere una cantidad considerable de energía (calor latente de vaporización), lo que contribuye a los procesos de enfriamiento por sudoración.
Puntos de Fusión y Evaporación
El agua tiene un punto de ebullición de 100 °C y un punto de fusión de 0 °C a presión atmosférica estándar. Estos puntos son inusualmente altos para una molécula de su tamaño, nuevamente debido a la fuerza de los puentes de hidrógeno. La energía requerida para cambiar de fase (calor latente de fusión y vaporización) es significativa, lo que demuestra la estabilidad de estas interacciones moleculares.

La Anomalía de la Densidad del Agua
Una de las propiedades más fascinantes y vitales del agua es su comportamiento anómalo de la densidad. A diferencia de la mayoría de las sustancias, el agua alcanza su máxima densidad a 4 °C, no en su punto de congelación. Por debajo de 4 °C, su densidad disminuye, y cuando se congela a 0 °C, el hielo es menos denso que el agua líquida. Esta es la razón por la que el hielo flota, un fenómeno crucial que permite que la vida acuática sobreviva en climas fríos, ya que los cuerpos de agua se congelan desde la superficie hacia abajo, aislando el agua líquida inferior.
Tabla Comparativa: Densidad del Agua a Diferentes Temperaturas
La siguiente tabla ilustra cómo la densidad del agua varía con la temperatura, destacando su comportamiento anómalo.
| Temperatura (°C) | Densidad (kg/L) |
|---|---|
| 100 | 0.958 |
| 90 | 0.965 |
| 4 | 1.000 |
| 0 (líquida) | 0.9999 |
| 0 (sólida - hielo) | 0.917 |
Preguntas Frecuentes (FAQs)
¿Es el agua un elemento?
No, el agua no es un elemento. Es un compuesto químico formado por la combinación de dos elementos: hidrógeno y oxígeno (H₂O).
¿Por qué el hielo flota en el agua?
El hielo flota porque es menos denso que el agua líquida. A diferencia de la mayoría de las sustancias, el agua se expande al congelarse, lo que significa que un volumen dado de hielo tiene menos masa que el mismo volumen de agua líquida.
¿Qué diferencia hay entre el agua potable y el agua pura?
El agua potable es agua segura para beber que contiene minerales y sales disueltas. El agua pura (como el agua destilada) ha sido procesada para eliminar casi todas las impurezas, incluyendo minerales y sales, y es utilizada en experimentos científicos o aplicaciones industriales.
¿Qué tan importante es la polaridad del agua?
La polaridad del agua es fundamental para sus propiedades. Le permite actuar como un excelente disolvente, formar puentes de hidrógeno, y participar en la acción capilar y la tensión superficial, propiedades esenciales para los procesos biológicos y químicos.
¿Cómo se descubrió la composición del agua?
La composición del agua como un compuesto de hidrógeno y oxígeno fue demostrada experimentalmente por Henry Cavendish en 1781 y posteriormente explicada y confirmada por Antoine Laurent de Lavoisier.
Desde la inmensidad de los océanos hasta la más pequeña de las gotas, el agua es una sustancia de complejidad asombrosa. Entender cómo calcular el número de sus moléculas, aunque sea un ejercicio numérico, nos abre los ojos a la escala del mundo molecular y a la intrincada perfección de la naturaleza. Cada molécula de H₂O, con su estructura polar y capacidad para formar puentes de hidrógeno, es una pieza clave en el rompecabezas de la vida, haciendo posible que nuestro planeta sea el hogar vibrante que es. Así, la próxima vez que veas una gota de agua, recuerda la miríada de moléculas que contiene y el universo de interacciones que se desarrollan en su interior.
Si quieres conocer otros artículos parecidos a Descubre Cuántas Moléculas de Agua Hay en una Gota puedes visitar la categoría Química.