30/06/2022
En el fascinante mundo de la química, donde cada elemento cuenta con propiedades únicas y comportamientos específicos, uno de los conceptos más fundamentales es la masa de un átomo. Aunque los átomos son increíblemente pequeños y no podemos verlos ni pesarlos directamente con una balanza convencional, la ciencia ha desarrollado métodos precisos para determinar su masa. Comprender cómo calcular la masa de un átomo en gramos es esencial para cualquier estudiante o profesional de la química, ya que permite realizar cálculos estequiométricos, entender reacciones a nivel molecular y manipular sustancias con precisión.

Tradicionalmente, la masa de los átomos se expresa en unidades de masa atómica (uma o Da, Dalton). Sin embargo, para trabajar en el laboratorio o para realizar cálculos que involucren cantidades macroscópicas de materia, necesitamos convertir esta masa a gramos. Este proceso, que puede parecer complejo al principio, se simplifica enormemente con el uso de constantes fundamentales como el número de Avogadro y la comprensión del concepto de mol. Acompáñanos en este recorrido para desglosar paso a paso cómo determinar la masa de un solo átomo en una unidad de peso más familiar: el gramo.
- Comprendiendo la Masa Atómica: La Base de Nuestros Cálculos
- El Papel Crucial del Mol y el Número de Avogadro
- Pasos para Calcular la Masa de un Átomo en Gramos
- Tabla Comparativa de Masas Atómicas
- Preguntas Frecuentes (FAQs)
- ¿Por qué la masa atómica se expresa en uma y no directamente en gramos?
- ¿Es la masa de un átomo de un isótopo diferente a la masa atómica promedio?
- ¿Cuál es la diferencia entre masa atómica y masa molar?
- ¿Por qué el número de Avogadro es tan específico y grande?
- ¿Este cálculo es válido también para moléculas?
- Conclusión
Comprendiendo la Masa Atómica: La Base de Nuestros Cálculos
Antes de sumergirnos en los cálculos, es crucial entender qué representa la masa atómica. En la tabla periódica, cada elemento químico tiene un número decimal debajo de su símbolo. Este valor es la masa atómica promedio del elemento, expresada en unidades de masa atómica (uma). Una unidad de masa atómica se define como 1/12 de la masa de un átomo de carbono-12. Esto se estableció así para tener una referencia estándar y universalmente aceptada.
Por ejemplo, si observamos el hidrógeno (H), su masa atómica es aproximadamente 1.008 uma. Esto significa que un átomo de hidrógeno tiene una masa que es aproximadamente 1.008 veces la doceava parte de la masa de un átomo de carbono-12. Es importante recordar que esta es una masa promedio, ya que la mayoría de los elementos tienen isótopos (átomos del mismo elemento con diferente número de neutrones y, por lo tanto, diferente masa). La masa atómica promedio que vemos en la tabla periódica es un promedio ponderado de las masas de todos los isótopos naturales de ese elemento, tomando en cuenta su abundancia relativa.
La Relación entre uma y Gramos
Para convertir uma a gramos, necesitamos una constante de conversión. Se ha determinado experimentalmente que 1 uma es aproximadamente igual a 1.660539 × 10-24 gramos. Este número es extremadamente pequeño, lo que subraya lo increíblemente diminutos que son los átomos. Si bien esta conversión directa es válida, no es la forma más práctica de abordar el cálculo de la masa de un solo átomo en gramos en la mayoría de los contextos químicos. La razón es que rara vez trabajamos con un solo átomo; en cambio, trabajamos con moles de átomos.
El Papel Crucial del Mol y el Número de Avogadro
Aquí es donde entran en juego dos conceptos pilares de la química: el mol y el número de Avogadro. Un mol es una unidad de cantidad de sustancia en el Sistema Internacional de Unidades (SI). Se define como la cantidad de sustancia que contiene tantas entidades elementales (átomos, moléculas, iones, etc.) como átomos hay en 0.012 kilogramos (12 gramos) de carbono-12. Este número de entidades es el número de Avogadro, aproximadamente 6.022 × 1023.
La magia del mol radica en su relación directa con la masa atómica. La masa de un mol de cualquier sustancia, expresada en gramos, es numéricamente igual a su masa atómica o molecular expresada en uma. Es decir, si la masa atómica del carbono es 12.011 uma, entonces la masa molar del carbono es 12.011 gramos por mol (g/mol). Esta conveniente equivalencia es lo que nos permite transitar del mundo atómico al mundo macroscópico.
¿Por qué esta equivalencia es tan útil?
Esta equivalencia significa que si tenemos 12.011 gramos de carbono, sabemos que tenemos exactamente 6.022 × 1023 átomos de carbono. Y si tenemos 1.008 gramos de hidrógeno, también tenemos 6.022 × 1023 átomos de hidrógeno. Esta relación es la clave para calcular la masa de un solo átomo en gramos de manera práctica.
Pasos para Calcular la Masa de un Átomo en Gramos
Ahora que hemos sentado las bases conceptuales, podemos proceder con los pasos específicos para realizar el cálculo:
- Identificar la Masa Atómica del Elemento: Consulta la tabla periódica para encontrar la masa atómica del elemento que te interesa. Este valor estará en unidades de masa atómica (uma).
- Relacionar con la Masa Molar: Recuerda que la masa atómica en uma es numéricamente igual a la masa molar del elemento en gramos por mol (g/mol). Por ejemplo, si el oxígeno tiene una masa atómica de 15.999 uma, su masa molar es 15.999 g/mol.
- Aplicar el Número de Avogadro: La masa molar (en g/mol) representa la masa de 6.022 × 1023 átomos de ese elemento. Para encontrar la masa de un solo átomo, simplemente divide la masa molar entre el número de Avogadro.
Fórmula General:
Masa de 1 átomo (g) = Masa Molar del elemento (g/mol) / Número de Avogadro (átomos/mol)
Masa de 1 átomo (g) = Masa Atómica (uma) / (1 uma / g)
Donde la relación 1 uma / g es 1 / (1.660539 × 10-24 g/uma) = 6.022 × 1023 uma/g. Este es el inverso del número de Avogadro si se expresa en uma/g. Pero la forma más directa es usar la masa molar y el número de Avogadro.
Ejemplos Prácticos
Ejemplo 1: Calcular la masa de un átomo de Hidrógeno (H) en gramos.
- Paso 1: Masa atómica del H (de la tabla periódica) = 1.008 uma.
- Paso 2: Masa molar del H = 1.008 g/mol.
- Paso 3: Masa de 1 átomo de H = (1.008 g/mol) / (6.022 × 1023 átomos/mol)
- Resultado: Masa de 1 átomo de H ≈ 1.674 × 10-24 gramos.
Ejemplo 2: Calcular la masa de un átomo de Carbono (C) en gramos.
- Paso 1: Masa atómica del C (de la tabla periódica) = 12.011 uma.
- Paso 2: Masa molar del C = 12.011 g/mol.
- Paso 3: Masa de 1 átomo de C = (12.011 g/mol) / (6.022 × 1023 átomos/mol)
- Resultado: Masa de 1 átomo de C ≈ 1.994 × 10-23 gramos.
Ejemplo 3: Calcular la masa de un átomo de Oro (Au) en gramos.
- Paso 1: Masa atómica del Au (de la tabla periódica) = 196.967 uma.
- Paso 2: Masa molar del Au = 196.967 g/mol.
- Paso 3: Masa de 1 átomo de Au = (196.967 g/mol) / (6.022 × 1023 átomos/mol)
- Resultado: Masa de 1 átomo de Au ≈ 3.271 × 10-22 gramos.
Como puedes observar, la masa de un solo átomo es siempre un número extremadamente pequeño, lo que reafirma la naturaleza submicroscópica de estas partículas fundamentales.
Tabla Comparativa de Masas Atómicas
Para ilustrar mejor estos conceptos, la siguiente tabla muestra la masa atómica en uma y su correspondiente masa molar en g/mol para algunos elementos comunes, lo que facilita el cálculo de la masa de un átomo individual en gramos.
| Elemento | Símbolo | Masa Atómica (uma) | Masa Molar (g/mol) | Masa de 1 Átomo (g) |
|---|---|---|---|---|
| Hidrógeno | H | 1.008 | 1.008 | 1.674 × 10-24 |
| Helio | He | 4.003 | 4.003 | 6.647 × 10-24 |
| Carbono | C | 12.011 | 12.011 | 1.994 × 10-23 |
| Oxígeno | O | 15.999 | 15.999 | 2.656 × 10-23 |
| Sodio | Na | 22.990 | 22.990 | 3.818 × 10-23 |
| Cloro | Cl | 35.453 | 35.453 | 5.887 × 10-23 |
| Oro | Au | 196.967 | 196.967 | 3.271 × 10-22 |
Los valores de la columna "Masa de 1 Átomo (g)" se obtienen dividiendo la "Masa Molar (g/mol)" entre el Número de Avogadro (6.022 × 1023).
Preguntas Frecuentes (FAQs)
¿Por qué la masa atómica se expresa en uma y no directamente en gramos?
Originalmente, se definió la uma para comparar las masas de los átomos de manera relativa. Trabajar con números tan pequeños como 10-24 gramos era impráctico y propenso a errores. La uma proporciona una escala más manejable para describir las masas individuales de los átomos y moléculas en relación con un estándar (el carbono-12).
¿Es la masa de un átomo de un isótopo diferente a la masa atómica promedio?
Sí, la masa de un átomo de un isótopo específico (por ejemplo, Carbono-12 o Carbono-14) tiene una masa isotópica que es ligeramente diferente a la masa atómica promedio que se encuentra en la tabla periódica. La masa atómica promedio es un promedio ponderado de las masas de todos los isótopos naturales de un elemento, considerando su abundancia. Para calcular la masa de un átomo de un isótopo específico, se usaría su masa isotópica en uma en lugar de la masa atómica promedio.
¿Cuál es la diferencia entre masa atómica y masa molar?
La masa atómica se refiere a la masa de un solo átomo (o el promedio ponderado de sus isótopos) expresada en unidades de masa atómica (uma). La masa molar es la masa de un mol de ese elemento o compuesto, expresada en gramos por mol (g/mol). Numéricamente, la masa atómica en uma es igual a la masa molar en g/mol, lo que simplifica enormemente los cálculos en química.
¿Por qué el número de Avogadro es tan específico y grande?
El número de Avogadro (6.022 × 1023) es un valor experimental que fue determinado para establecer una conexión entre la escala atómica y la escala macroscópica. Su magnitud asegura que un mol de cualquier sustancia contenga una cantidad de partículas que, cuando se pesa en gramos, es numéricamente igual a la masa atómica o molecular de esa sustancia en uma. Es un factor de conversión que nos permite pasar de "unidades atómicas" a "unidades de laboratorio".
¿Este cálculo es válido también para moléculas?
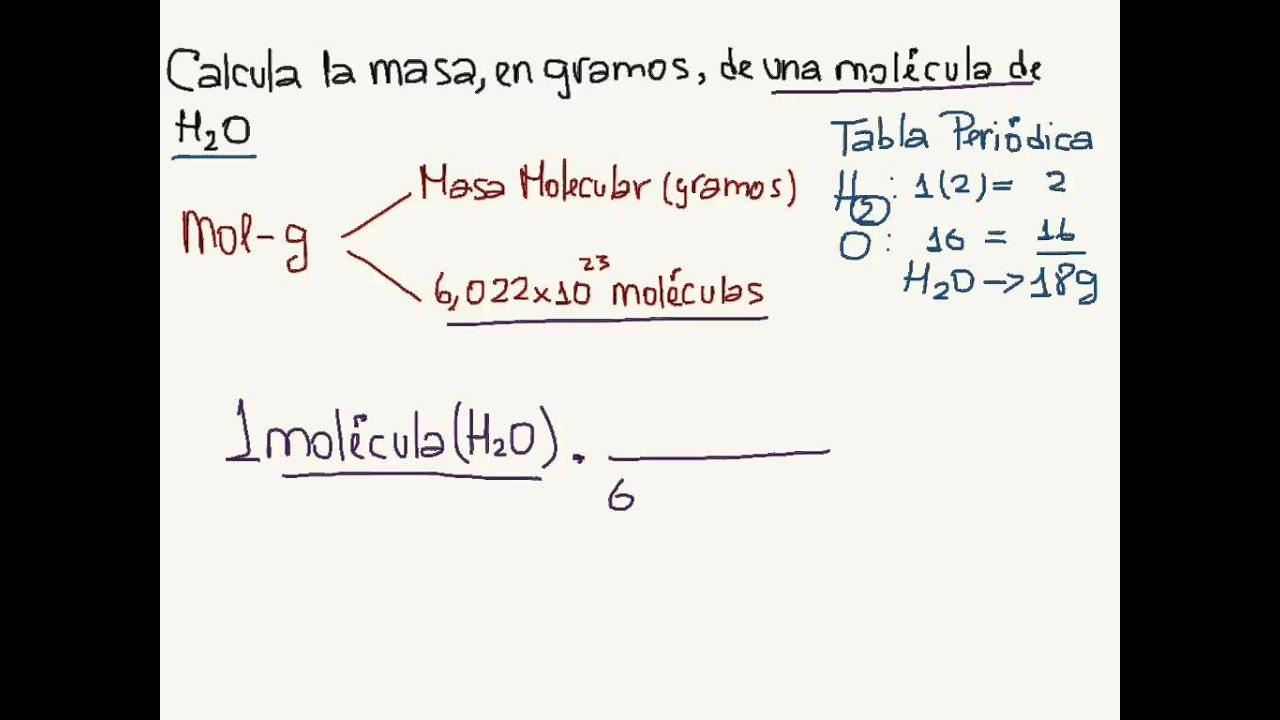
Sí, el principio es el mismo. Para calcular la masa de una sola molécula en gramos, primero se calcula la masa molecular de la molécula sumando las masas atómicas de todos los átomos que la componen (en uma). Luego, esta masa molecular en uma es numéricamente igual a la masa molar de la molécula en g/mol. Finalmente, se divide la masa molar de la molécula por el número de Avogadro para obtener la masa de una sola molécula en gramos.
Conclusión
El cálculo de la masa de un átomo en gramos es una habilidad fundamental en química que une el mundo subatómico con las cantidades que podemos medir y manipular en el laboratorio. Aunque los átomos son increíblemente pequeños, el concepto de mol y el número de Avogadro nos proporcionan una herramienta poderosa para cuantificarlos de manera significativa. Al entender que la masa atómica en uma es numéricamente equivalente a la masa molar en g/mol, y al aplicar una simple división por el número de Avogadro, podemos determinar con precisión la masa de un solo átomo. Este conocimiento es la base para comprender la composición de la materia, predecir el resultado de las reacciones químicas y avanzar en la ciencia y la tecnología.
Si quieres conocer otros artículos parecidos a Calculando la Masa de un Átomo en Gramos puedes visitar la categoría Química.