03/05/2022
El agua, la molécula fundamental para la vida en la Tierra, es mucho más que un simple líquido. En el vasto campo de la química, comprender sus propiedades y cómo interactúa con otras sustancias es crucial. Una de las propiedades más interesantes y a menudo malentendidas del agua es su concentración molar, especialmente cuando hablamos de agua pura. Aunque parezca contradictorio referirse a la "concentración" de un solvente, el agua tiene una concentración molar bien definida que juega un papel vital en innumerables procesos químicos y bioquímicos.

En este artículo, desglosaremos el concepto de concentración molar, exploraremos cómo se calcula la concentración molar del agua pura y discutiremos su relevancia en diversos contextos. Abordaremos también conceptos relacionados como la masa molar y las diferencias con la molalidad, proporcionando una guía completa para desentrañar los misterios de la química acuosa.
¿Qué es la Molaridad y Cómo se Calcula?
Antes de sumergirnos en la concentración del agua, es fundamental entender qué es la molaridad. La molaridad (M) es una medida de la concentración de un soluto en una solución. Se define como el número de moles de soluto disueltos por litro de solución. Es una de las unidades de concentración más utilizadas en química debido a su relación directa con la cantidad de sustancia (moles).
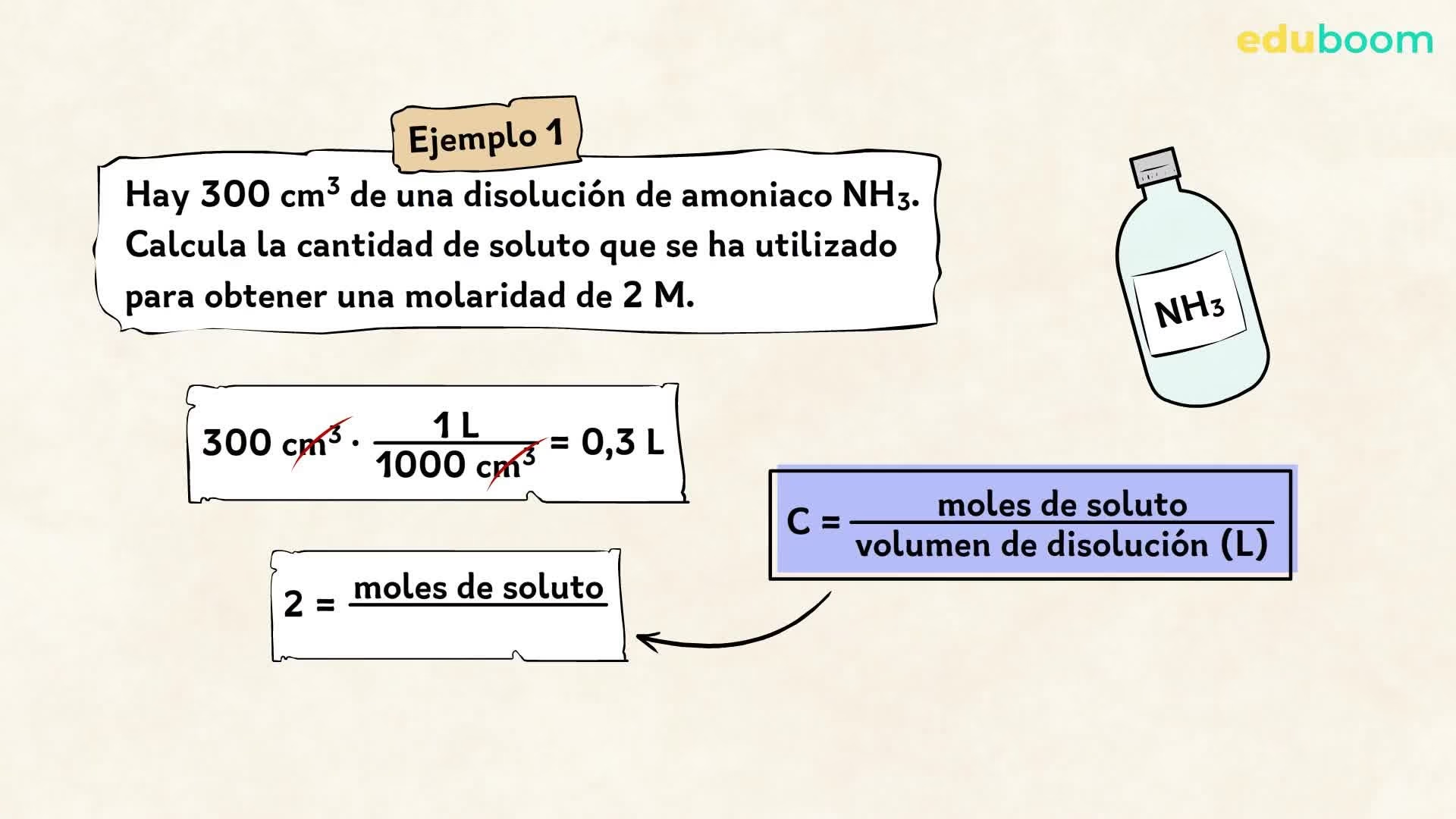
La fórmula general para calcular la molaridad es la siguiente:
Molaridad (M) = Moles de Soluto / Litros de Solución
Para aplicar esta fórmula, generalmente se siguen estos pasos:
- Calcular los moles de soluto: Si tienes la masa del soluto en gramos, divídela por su masa molar (peso molecular) para obtener los moles. La masa molar se expresa en gramos por mol (g/mol).
- Asegurarse de que el volumen de la solución esté en litros: Si el volumen está en mililitros (mL), divídelo por 1000 para convertirlo a litros.
- Dividir los moles de soluto por el volumen en litros: El resultado será la molaridad de la solución, expresada en moles por litro (mol/L) o simplemente M.
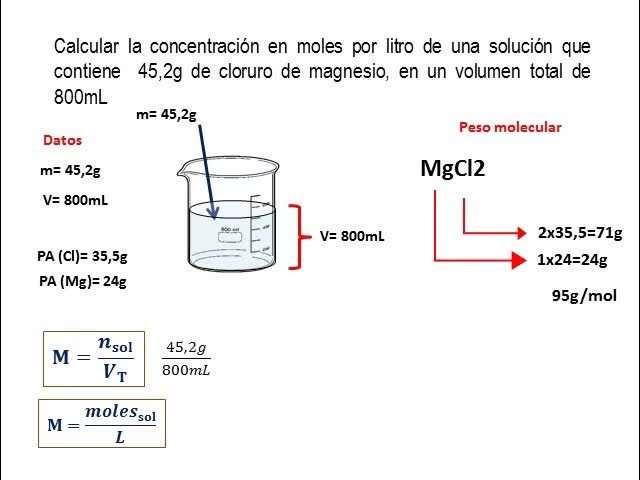
Ejemplo práctico: Supongamos que tienes 5.85 gramos de cloruro de sodio (NaCl) disueltos en 500 mL de solución.
- Primero, calculamos los moles de NaCl. La masa molar del NaCl es aproximadamente 58.44 g/mol (22.99 g/mol para Na + 35.45 g/mol para Cl).
- Moles de NaCl = 5.85 g / 58.44 g/mol ≈ 0.1001 mol.
- Luego, convertimos el volumen de la solución a litros: 500 mL = 0.500 L.
- Finalmente, calculamos la molaridad: M = 0.1001 mol / 0.500 L = 0.2002 M.
Este ejemplo ilustra cómo se aplica la fórmula de molaridad para un soluto común. Ahora, ¿cómo se aplica esto al agua misma?
La Masa Molar del Agua (H2O)
Antes de calcular la concentración molar del agua, necesitamos saber su masa molar. La masa molar es la masa de un mol de una sustancia y se calcula sumando las masas atómicas de todos los átomos presentes en la fórmula molecular.
Para el agua (H2O):
- Masa atómica del Hidrógeno (H) ≈ 1.008 u (o g/mol)
- Masa atómica del Oxígeno (O) ≈ 15.999 u (o g/mol)
La molécula de agua tiene dos átomos de hidrógeno y un átomo de oxígeno. Por lo tanto, su masa molar se calcula como:
Masa Molar (H₂O) = (2 × Masa Atómica de H) + (1 × Masa Atómica de O)
Masa Molar (H₂O) = (2 × 1.008 g/mol) + (1 × 15.999 g/mol)
Masa Molar (H₂O) = 2.016 g/mol + 15.999 g/mol
Masa Molar (H₂O) ≈ 18.015 g/mol
Este valor, 18.015 g/mol, es crucial para determinar la concentración molar del agua.

Calculando la Concentración Molar del Agua Pura
Aquí es donde el concepto se vuelve particularmente interesante. Cuando hablamos de la concentración molar del agua pura, el agua actúa tanto como soluto como solvente. Para calcular su molaridad, consideramos una cantidad definida de agua pura y la tratamos como si fuera el "soluto" en su propio "volumen de solución".
Consideremos 1 litro (L) de agua pura. Para agua a 4°C, su densidad es aproximadamente 1 gramo por mililitro (1 g/mL) o 1000 gramos por litro (1000 g/L). Esta es una aproximación muy utilizada para cálculos a temperatura ambiente.
Ahora, aplicamos la fórmula de molaridad:
- Masa de agua en 1 Litro: Si la densidad del agua es 1000 g/L, entonces 1 Litro de agua tiene una masa de 1000 gramos.
- Moles de agua en 1 Litro: Usamos la masa molar que calculamos anteriormente (18.015 g/mol).
Moles de H₂O = Masa de H₂O / Masa Molar de H₂OMoles de H₂O = 1000 g / 18.015 g/mol ≈ 55.508 moles - Volumen de la "solución" (agua pura): 1 Litro.
- Calcular la Molaridad:
Molaridad (H₂O) = Moles de H₂O / Litros de H₂OMolaridad (H₂O) = 55.508 mol / 1 L ≈ 55.5 M
Por lo tanto, la concentración molar del agua pura es aproximadamente 55.5 M. Este valor es un pilar fundamental en química y bioquímica, especialmente cuando se discuten las propiedades del agua como solvente y su papel en las reacciones.
La Actividad del Agua en Soluciones Diluidas
En muchas aplicaciones termodinámicas y bioquímicas, especialmente en soluciones acuosas diluidas, la concentración de agua se considera casi constante e igual a la del agua pura. De hecho, su "actividad" se establece comúnmente en 1.00. La actividad es un concepto más refinado que la concentración y se utiliza para reflejar la "concentración efectiva" de una sustancia, especialmente en sistemas no ideales o muy concentrados. Para el agua como solvente en soluciones diluidas, su concentración es tan alta y relativamente inalterada por la presencia de pequeñas cantidades de soluto que su actividad se aproxima a la unidad, lo que simplifica muchos cálculos.
Otras Formas de Calcular Molaridad y Conceptos Relacionados
Calculando la Molaridad a Partir del pH
En el contexto de soluciones ácidas o básicas, la molaridad de los iones H+ (o H3O+) y OH- puede calcularse a partir del pH. Este método es aplicable principalmente a ácidos y bases fuertes, ya que se asume una disociación completa en la solución.
- Para un ácido fuerte: La concentración molar del ácido es igual a la concentración de iones H+.
Molaridad (M) = 10^(-pH)Por ejemplo, si una solución de ácido fuerte tiene un pH de 2, su molaridad sería 10-2 M = 0.01 M.
3) Calcular la masa molecular del agua: H2O. Ma(H) = 1 u; Ma(O) = 16 u. Mm(H2O) = 2 · 1 + 16 = 18 u. - Para una base fuerte: Primero se calcula el pOH, y luego la concentración de iones OH-.
pOH = 14 - pHMolaridad (M) = 10^(-pOH)Por ejemplo, si una solución de base fuerte tiene un pH de 12, su pOH sería 14 - 12 = 2. Su molaridad sería 10-2 M = 0.01 M.
Es crucial recordar que esta relación directa solo es válida para ácidos y bases fuertes que se disocian completamente en solución. Para ácidos y bases débiles, se requieren cálculos de equilibrio más complejos.
Convirtiendo Molaridad a Molalidad
Mientras que la molaridad se basa en el volumen de la solución, la molalidad (m) se basa en la masa del solvente. La molalidad se define como el número de moles de soluto por kilogramo de solvente. La principal ventaja de la molalidad es que no se ve afectada por los cambios de temperatura, ya que la masa no varía con la temperatura, a diferencia del volumen.
La fórmula para convertir molaridad (M) a molalidad (m) es:
m = M / (ρ - (M * MW_soluto / 1000))
Donde:
m= molalidad (mol/kg)M= molaridad (mol/L)ρ(rho) = densidad de la solución (g/mL o kg/L)MW_soluto= peso molecular (masa molar) del soluto (g/mol)
Esta conversión requiere conocer la densidad de la solución y la masa molar del soluto, y es fundamental cuando se trabaja con propiedades coligativas o cuando la temperatura es un factor variable.
Tabla Comparativa: Molaridad vs. Molalidad
Para clarificar las diferencias entre estas dos importantes unidades de concentración, presentamos la siguiente tabla:
| Característica | Molaridad (M) | Molalidad (m) |
|---|---|---|
| Definición | Moles de soluto por litro de solución | Moles de soluto por kilogramo de solvente |
| Unidades | mol/L o M | mol/kg o m |
| Dependencia de la Temperatura | Sí (el volumen cambia con la temperatura) | No (la masa no cambia con la temperatura) |
| Usos Comunes | Reacciones químicas en solución, titulaciones | Propiedades coligativas (punto de ebullición, punto de congelación), estudios termodinámicos |
| Precisión en Rangos de Temperatura | Menos precisa si la temperatura varía significativamente | Más precisa en un amplio rango de temperaturas |
Importancia de la Concentración Molar del Agua
Aunque a menudo se pasa por alto porque el agua es el solvente omnipresente, comprender su concentración molar es de gran importancia en varios campos:
- Bioquímica y Biología: En sistemas biológicos, donde la mayoría de las reacciones ocurren en un entorno acuoso, la alta concentración del agua (55.5 M) y su actividad constante (aproximada a 1.00) son fundamentales para entender la cinética y el equilibrio de las reacciones enzimáticas y los procesos celulares. A menudo, el agua se considera un "reactivo" en el balance de masas, pero su actividad se incorpora de una manera que simplifica los cálculos, asumiendo que su concentración es tan alta que permanece relativamente constante.
- Termodinámica: En los cálculos de energía libre de Gibbs (ΔG), las concentraciones de reactivos y productos se expresan como actividades. Para el agua, especialmente en soluciones diluidas, su actividad se toma como 1.00, lo que simplifica la ecuación y refleja su estado de referencia como líquido puro.
- Química Analítica: Aunque no se calcula directamente la molaridad del agua en la mayoría de los análisis, el conocimiento de su densidad y masa molar es esencial para preparar soluciones con concentraciones precisas de solutos.
- Educación Química: Es un concepto clave para que los estudiantes comprendan la naturaleza del agua no solo como un medio pasivo, sino como un componente activo con una concentración definida, lo que ayuda a cimentar una comprensión más profunda de las soluciones y los estados de referencia.
Preguntas Frecuentes sobre la Concentración Molar del Agua
¿Por qué la concentración molar del agua pura es 55.5 M?
La concentración molar de 55.5 M para el agua pura se deriva de su densidad y masa molar. Un litro de agua pesa aproximadamente 1000 gramos. Dividiendo esta masa por la masa molar del agua (aproximadamente 18.015 g/mol), obtenemos aproximadamente 55.5 moles. Dado que estamos considerando un volumen de 1 litro, la molaridad resulta ser 55.5 mol/L, o 55.5 M. Este valor representa la cantidad de moléculas de agua presentes en un litro de agua pura.

¿La concentración molar del agua cambia en una solución acuosa?
Sí, la concentración molar del agua disminuye ligeramente cuando se disuelve un soluto en ella, ya que el soluto ocupa espacio y desplaza algunas moléculas de agua. Sin embargo, en soluciones diluidas, la cantidad de soluto es tan pequeña en comparación con la cantidad de agua que la concentración del agua permanece muy cercana a 55.5 M. Por esta razón, en muchos cálculos químicos y bioquímicos, la concentración (o más precisamente, la actividad) del agua en soluciones diluidas se considera constante e igual a 1.00.
¿Cuándo es importante considerar la actividad del agua en lugar de su concentración molar?
La actividad del agua es un concepto más relevante que su concentración molar cuando se trabaja con soluciones muy concentradas o cuando se realizan cálculos termodinámicos precisos, como la energía libre de Gibbs (ΔG) de una reacción. En estos casos, la desviación del comportamiento ideal (donde la actividad es igual a la concentración molar) se vuelve significativa. Para soluciones diluidas, la actividad del agua se aproxima a la unidad (1.00), simplificando los cálculos.
¿Cuál es la diferencia principal entre molaridad y molalidad?
La diferencia principal radica en el denominador de su definición: la molaridad utiliza el volumen total de la solución (litros), mientras que la molalidad utiliza la masa del solvente (kilogramos). Esto hace que la molaridad sea dependiente de la temperatura (ya que el volumen cambia con la temperatura), mientras que la molalidad es independiente de la temperatura. La molalidad es preferida en estudios donde la temperatura es una variable importante, como las propiedades coligativas.
¿Se puede calcular la masa a partir de la concentración?
Sí, si conoces la molaridad de una solución y su volumen, puedes calcular la masa del soluto. Primero, calcula los moles de soluto multiplicando la molaridad por el volumen en litros (Moles = Molaridad × Volumen). Luego, convierte los moles a masa multiplicando por la masa molar del soluto (Masa = Moles × Masa Molar). Por ejemplo, si tienes 0.2 M de NaCl en 1 L de solución, tendrías 0.2 moles de NaCl. Multiplicando 0.2 mol por 58.44 g/mol (masa molar de NaCl), obtendrías 11.688 gramos de NaCl.
Conclusión
La concentración molar del agua, un valor aparentemente simple de 55.5 M para su estado puro, es un concepto de profunda importancia en la química y más allá. Desde la comprensión de las propiedades fundamentales del agua como solvente universal hasta su papel en las intrincadas vías bioquímicas, su concentración molar y actividad son puntos de referencia esenciales. Al desglosar cómo se calcula, diferenciándola de otras unidades de concentración y explorando su impacto en diversas aplicaciones, hemos arrojado luz sobre la omnipresente pero a menudo subestimada importancia de esta molécula vital. Dominar estos conceptos no solo enriquece nuestra comprensión de la química, sino que también nos equipa con las herramientas para analizar y predecir el comportamiento de las soluciones en un sinfín de escenarios científicos.
Si quieres conocer otros artículos parecidos a Calculando la Concentración Molar del Agua: Una Guía Completa puedes visitar la categoría Química.