21/08/2023
En el vasto universo de la química, cada elemento posee una identidad única definida por sus propiedades, y una de las más fundamentales es su masa atómica. Pero, ¿qué ocurre cuando nos enfrentamos a un elemento completamente desconocido, quizás sintetizado en un laboratorio o descubierto en condiciones extremas? Determinar su masa atómica no es solo un ejercicio académico, sino un paso crucial para comprender su comportamiento y su lugar en la tabla periódica. Este artículo explorará las metodologías y cálculos necesarios para desvelar este enigma.

La masa atómica es un concepto central en la química. Se refiere a la masa promedio ponderada de los isótopos de un elemento, donde cada isótopo es una variante de ese elemento con un número diferente de neutrones en su núcleo. Esta masa se expresa comúnmente en unidades de masa atómica (uma) o, en el contexto de un mol de átomos, en gramos por mol (g/mol). Para un elemento ya conocido, simplemente consultamos la tabla periódica. Sin embargo, para un elemento cuyo número atómico o composición isotópica es un misterio, el desafío es mucho mayor.
Fundamentos de la Masa Atómica: El ADN de un Elemento
Antes de sumergirnos en la determinación de la masa de un elemento desconocido, es esencial comprender los pilares sobre los que se asienta este concepto. La masa atómica de un elemento natural es el promedio ponderado de las masas de sus isótopos estables, considerando sus abundancias relativas en la naturaleza. Por ejemplo, el cloro tiene dos isótopos principales: cloro-35 y cloro-37. El cloro-35 es mucho más abundante, lo que hace que la masa atómica promedio del cloro sea de aproximadamente 35.45 uma, más cercana a 35 que a 37.
- Isótopos: Átomos del mismo elemento (mismo número de protones) pero con diferente número de neutrones. Por lo tanto, tienen diferentes masas.
- Abundancia Natural: El porcentaje en que cada isótopo de un elemento se encuentra en una muestra natural.
- Unidad de Masa Atómica (uma): Una unidad de masa definida como 1/12 de la masa de un átomo de carbono-12. Es la escala en la que se miden las masas atómicas.
La determinación de la masa atómica para un elemento desconocido, ya sea porque es un nuevo descubrimiento o porque su identidad es incierta, requiere técnicas analíticas avanzadas que puedan medir directamente las masas de sus isótopos y sus proporciones.
El Pilar de la Determinación: La Espectrometría de Masas
Cuando hablamos de determinar la masa atómica de un elemento desconocido con precisión, la espectrometría de masas es la herramienta por excelencia. Esta técnica analítica permite identificar compuestos y determinar sus masas moleculares, o en el caso de elementos, las masas de sus isótopos y sus abundancias relativas.
¿Cómo Funciona la Espectrometría de Masas?
El principio básico de un espectrómetro de masas es la ionización de una muestra, la aceleración de los iones resultantes y su posterior separación en función de su relación masa/carga (m/z) mediante campos eléctricos y magnéticos. Los pasos generales son los siguientes:
- Ionización: La muestra (elemento desconocido) se introduce en el espectrómetro y se bombardea con electrones de alta energía, lo que provoca la expulsión de uno o más electrones de los átomos, creando iones positivos (o negativos, dependiendo de la técnica).
- Aceleración: Los iones formados son acelerados a través de una diferencia de potencial eléctrico, adquiriendo una energía cinética uniforme.
- Deflexión: Los iones acelerados pasan a través de un campo magnético o eléctrico (o una combinación de ambos). La trayectoria de cada ion se curva en proporción a su relación masa/carga. Los iones más ligeros o con mayor carga se desvían más que los iones más pesados o con menor carga.
- Detección: Un detector registra los iones que llegan a diferentes puntos, generando un espectro de masas. Este espectro muestra la abundancia relativa de cada ion en función de su relación masa/carga.
A partir del espectro de masas, se pueden identificar los diferentes isótopos del elemento desconocido y determinar sus masas exactas y sus abundancias relativas. Por ejemplo, si el espectro muestra picos a 19.99 uma y 21.99 uma con ciertas intensidades, estos representarían las masas de los isótopos y sus abundancias.
Cálculo de la Masa Atómica Promedio con Espectrometría de Masas
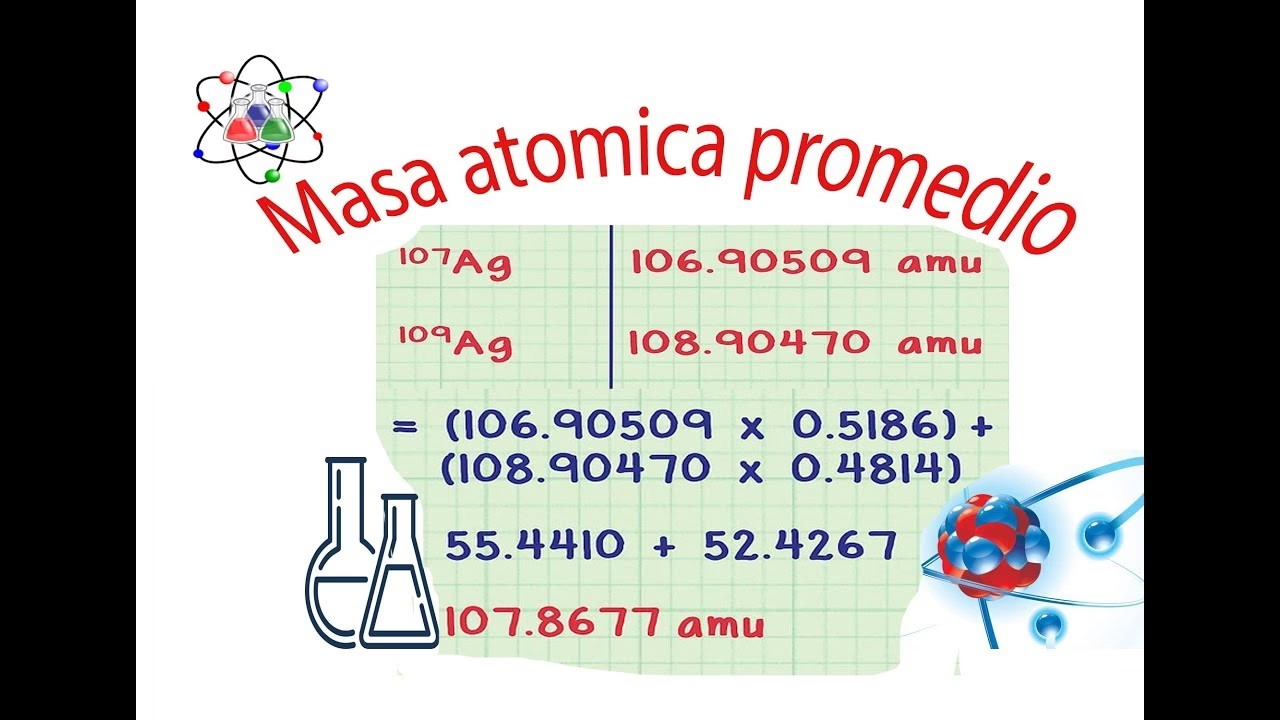
Una vez que el espectrómetro de masas ha proporcionado las masas isotópicas y sus abundancias relativas, el cálculo de la masa atómica promedio del elemento desconocido es directo. Se utiliza la siguiente fórmula:
Masa Atómica = Σ (Masa del Isótopoi × Abundancia Fraccional del Isótopoi)
Donde:
- Masa del Isótopoi es la masa exacta de un isótopo específico (en uma).
- Abundancia Fraccional del Isótopoi es la abundancia relativa de ese isótopo dividida por 100 (si se da en porcentaje).
Ejemplo Práctico:
Supongamos que un espectrómetro de masas analiza una muestra de un elemento desconocido 'X' y detecta dos isótopos:
- Isótopo X-1: Masa = 24.01 uma, Abundancia = 78.99%
- Isótopo X-2: Masa = 26.01 uma, Abundancia = 11.01%
- Isótopo X-3: Masa = 25.01 uma, Abundancia = 10.00%
Calculamos la masa atómica promedio:
Masa Atómica de X = (24.01 uma × 0.7899) + (26.01 uma × 0.1101) + (25.01 uma × 0.1000)
Masa Atómica de X = 18.965799 + 2.863101 + 2.501
Masa Atómica de X = 24.33 uma
Este resultado nos daría una fuerte indicación de que el elemento desconocido 'X' podría ser Magnesio, cuya masa atómica es aproximadamente 24.305 uma.
Métodos Indirectos y Químicos: Deducir la Masa Atómica
Aunque la espectrometría de masas es el método más directo y preciso, existen situaciones o contextos donde se pueden emplear métodos indirectos para deducir la masa atómica, especialmente si el elemento desconocido ya ha formado compuestos o se ha comportado de una manera predecible en reacciones químicas.
1. Análisis de la Composición de Compuestos (Estequiometría)
Si el elemento desconocido 'Y' reacciona con un elemento conocido 'Z' para formar un compuesto con una estequiometría definida y su masa molar puede determinarse, entonces la masa atómica de 'Y' puede inferirse. Por ejemplo, si se sabe que 'Y' forma un óxido Y2O3 y se determina que la masa molar de Y2O3 es de 102 g/mol, y sabiendo que la masa atómica del oxígeno es 16 g/mol:
Masa Molar de Y2O3 = (2 × Masa Atómica de Y) + (3 × Masa Atómica de O)
102 g/mol = (2 × Masa Atómica de Y) + (3 × 16 g/mol)
102 g/mol = (2 × Masa Atómica de Y) + 48 g/mol
2 × Masa Atómica de Y = 102 - 48
2 × Masa Atómica de Y = 54 g/mol
Masa Atómica de Y = 27 g/mol
Esto sugeriría que el elemento 'Y' es el Aluminio, cuya masa atómica es aproximadamente 26.98 uma.
2. Determinación de Propiedades Coligativas
Las propiedades coligativas (como el descenso crioscópico, el aumento ebulloscópico o la presión osmótica) dependen del número de partículas de soluto en una solución, no de su identidad. Si el elemento desconocido forma un soluto molecular o iónico en una solución, y se puede determinar su masa molar a través de estas propiedades, se puede inferir su masa atómica si la fórmula del compuesto es conocida.
Por ejemplo, si se disuelve una masa conocida de un compuesto que contiene el elemento desconocido en un solvente y se mide el descenso del punto de congelación, se puede calcular la molalidad de la solución y, a partir de ella, la masa molar del compuesto. Una vez que se conoce la masa molar del compuesto y las masas atómicas de los otros elementos, la masa atómica del elemento desconocido puede ser calculada.
3. Densidad de Gases (Ley de los Gases Ideales)
Si el elemento desconocido es un gas o puede convertirse en uno, su masa molar puede determinarse a partir de su densidad, presión y temperatura, utilizando la Ley de los Gases Ideales (PV = nRT o PM = dRT, donde M es la masa molar, d es la densidad). Si el gas es monoatómico (como un gas noble), su masa molar será directamente su masa atómica. Si es diatómico (como O2), la masa atómica sería la mitad de la masa molar.
Por ejemplo, si se mide la densidad de un gas desconocido a una temperatura y presión dadas, se puede calcular su masa molar. Si se sospecha que es un gas monoatómico, esa masa molar sería su masa atómica.
Consideraciones y Desafíos
La determinación de la masa atómica de un elemento desconocido no está exenta de desafíos:
- Pureza de la Muestra: Cualquier impureza puede distorsionar los resultados, especialmente en la espectrometría de masas.
- Estabilidad del Elemento: Los elementos muy pesados o sintetizados en laboratorio suelen ser extremadamente inestables y tienen vidas medias muy cortas, lo que dificulta su análisis.
- Precisión Instrumental: La exactitud de los resultados depende en gran medida de la calibración y la precisión del equipo utilizado.
- Existencia de Múltiples Isótopos: Si un elemento tiene muchos isótopos con abundancias muy bajas, puede ser difícil detectarlos todos o determinar sus abundancias con precisión.
- Interpretación de Datos: Los espectros de masas pueden ser complejos, y la identificación de los picos correctos requiere experiencia.
Tabla Comparativa de Métodos
| Método | Principio | Ventajas | Desventajas / Limitaciones |
|---|---|---|---|
| Espectrometría de Masas | Separación de iones por relación masa/carga. | Alta precisión, determina masas isotópicas y abundancias. | Requiere equipos costosos y especializados, muestra ionizable. |
| Análisis Estequiométrico | Determinación de la composición de un compuesto conocido. | Útil si el elemento forma compuestos estables y conocidos. | Depende del conocimiento previo de la estequiometría y pureza del compuesto. |
| Propiedades Coligativas | Medición de propiedades de solución que dependen de la concentración. | Aplicable a solutos moleculares/iónicos. | Requiere que el elemento forme un soluto, menos preciso que la espectrometría. |
| Densidad de Gases | Uso de la Ley de los Gases Ideales. | Directo para elementos gaseosos. | Solo aplicable a gases, requiere condiciones controladas. |
Preguntas Frecuentes
¿Es posible determinar la masa atómica de un elemento que solo existe por unos milisegundos?
Sí, aunque es extremadamente difícil. Los elementos superpesados, que solo existen por fracciones de segundo, se estudian utilizando técnicas de espectrometría de masas adaptadas para trabajar con cantidades mínimas y vidas medias muy cortas. Los detectores deben ser extremadamente sensibles y rápidos.
¿La masa atómica es siempre un número entero?
No. Solo la masa de un isótopo individual es cercana a un número entero (su número de masa). La masa atómica que aparece en la tabla periódica es una masa promedio ponderada de todos los isótopos naturales de un elemento, por lo que casi siempre es un número decimal.
¿Qué papel juega la calculadora en estos procesos?
La calculadora es fundamental para realizar los cálculos de promedios ponderados, resolver ecuaciones estequiométricas, aplicar la Ley de los Gases Ideales o procesar los datos de propiedades coligativas. Aunque los espectrómetros de masas modernos tienen software integrado, la comprensión de los cálculos subyacentes y la verificación manual son esenciales para la validación de los resultados.
¿Por qué es importante conocer la masa atómica de un elemento?
Conocer la masa atómica es crucial para la estequiometría (cálculos de reacciones químicas), para comprender la composición de materiales, para aplicaciones en medicina (por ejemplo, isótopos para diagnóstico o tratamiento), en ciencia de materiales, y para la investigación fundamental en física nuclear y química.
Conclusión
Determinar la masa atómica de un elemento desconocido es una tarea compleja que combina la sofisticación de la instrumentación científica con la precisión de los cálculos químicos. La espectrometría de masas se erige como la herramienta más potente y directa para este fin, permitiendo desentrañar la composición isotópica de la materia. Sin embargo, los métodos indirectos, basados en principios químicos fundamentales, también ofrecen vías valiosas para deducir esta propiedad esencial. La capacidad de identificar y cuantificar la masa atómica de un elemento, ya sea un nuevo descubrimiento o un enigma por resolver, es un testimonio del ingenio humano y un pilar para el avance de la ciencia.
Si quieres conocer otros artículos parecidos a ¿Cómo calcular la masa atómica de un elemento desconocido? puedes visitar la categoría Química.