07/03/2024
En el vasto y fascinante mundo de la química, el pH es un concepto fundamental que nos permite entender la acidez o alcalinidad de una solución acuosa. Desde la acidez de nuestro estómago hasta la calidad del agua que bebemos, el pH juega un papel crucial en innumerables procesos biológicos, industriales y ambientales. Saber cómo calcular el pH, y sus conceptos relacionados como el pOH, pKa y pKb, no solo es esencial para estudiantes y profesionales de la química, sino también para cualquier persona interesada en comprender mejor el mundo que nos rodea. En este artículo, desentrañaremos las fórmulas y los pasos necesarios para realizar estos cálculos, proporcionando ejemplos claros y explicaciones detalladas que te permitirán dominar estas importantes herramientas químicas.
- ¿Qué es el pH y por qué es importante?
- Cálculo del pH a partir de la Concentración de Iones Hidronio [H3O+]
- Cálculo de la Concentración de Iones Hidronio [H3O+] a partir del pH
- Cálculo del pOH a partir de la Concentración de Iones Hidróxido [OH-]
- Cálculo de la Concentración de Iones Hidróxido [OH-] a partir del pOH
- La Relación Fundamental entre pH y pOH
- Comprendiendo los Ácidos y Bases Fuertes
- Introducción a pKa y pKb: Constantes de Disociación Logarítmicas
- Preguntas Frecuentes (FAQ)
¿Qué es el pH y por qué es importante?
El pH es una medida de la concentración de iones de hidrógeno (específicamente, iones hidronio, H3O+) en una solución. La escala de pH va de 0 a 14, donde un pH de 7 se considera neutro. Los valores por debajo de 7 indican acidez, y los valores por encima de 7 indican alcalinidad o basicidad. Esta escala logarítmica es una forma conveniente de expresar concentraciones muy pequeñas de H3O+ que, de otra manera, serían difíciles de manejar. La importancia del pH radica en su influencia directa sobre la velocidad de las reacciones químicas, la solubilidad de las sustancias, la actividad enzimática en sistemas biológicos y la corrosión de materiales, entre muchos otros aspectos. Comprender y poder calcular el pH es, por tanto, una habilidad indispensable en muchos campos científicos y tecnológicos.
Cálculo del pH a partir de la Concentración de Iones Hidronio [H3O+]
El cálculo del pH es una de las operaciones más comunes en química de soluciones. Para determinar el pH de una solución acuosa, es necesario conocer la concentración de los iones hidronio (H3O+) en moles por litro, también conocida como molaridad. La fórmula para calcular el pH es la siguiente:
pH = - log [H3O+]
Aquí, "log" se refiere al logaritmo en base 10. El signo negativo se utiliza porque las concentraciones de iones hidronio en soluciones típicas son muy bajas (generalmente entre 10-1 y 10-14 M), y el logaritmo de un número menor que 1 es negativo. Al aplicar el signo negativo, obtenemos valores de pH positivos, que son más fáciles de interpretar.
Ejemplo Práctico: Calcular el pH de una solución de HCl
Imaginemos que tenemos una solución de HCl 0.0025 M. El ácido clorhídrico (HCl) es un ácido fuerte, lo que significa que se ioniza completamente (100%) en agua. Esto implica que cada molécula de HCl se disocia para formar un ion H3O+ y un ion Cl-. Por lo tanto, la concentración de iones hidronio [H3O+] en la solución será igual a la concentración inicial del HCl.
En este caso, [H3O+] = 0.0025 M.
Ahora, aplicamos la fórmula del pH:
pH = - log (0.0025)
Utilizando una calculadora, encontramos que log(0.0025) es aproximadamente -2.60.
pH = - (-2.60)
pH = 2.60
Este valor de pH, 2.60, indica que la solución es ácida, lo cual es consistente con la presencia de ácido clorhídrico.
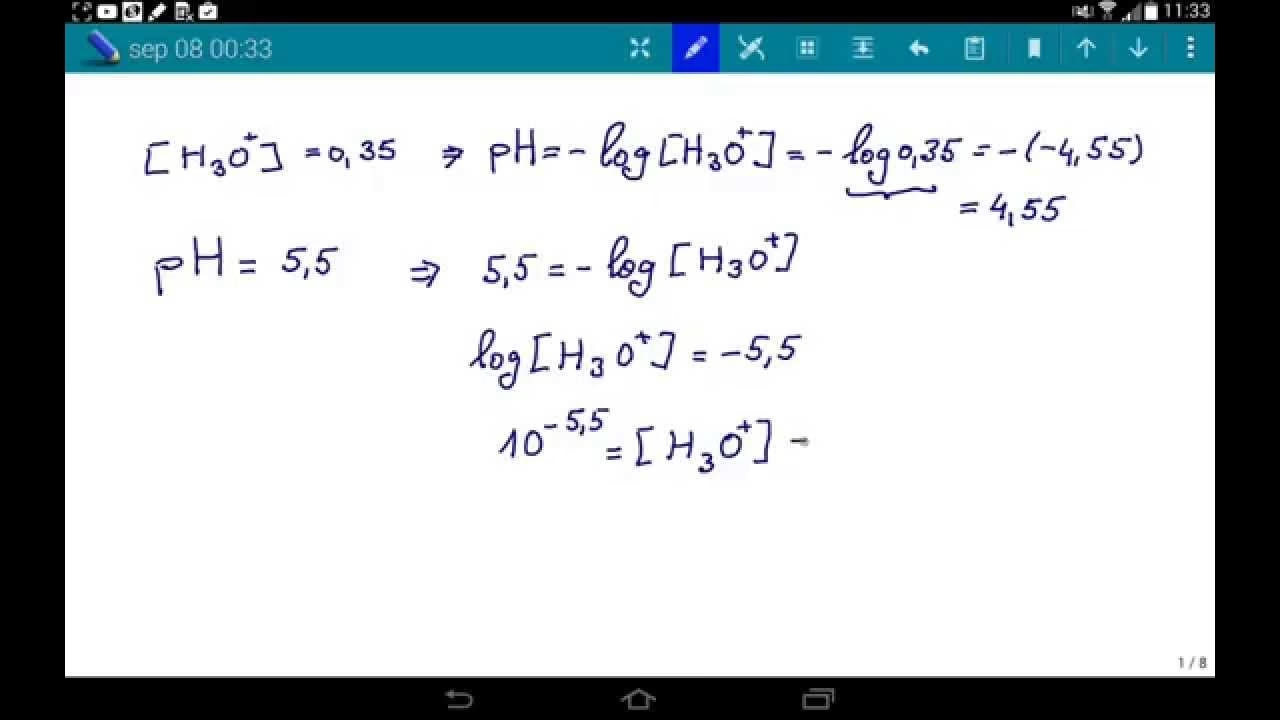
Cálculo de la Concentración de Iones Hidronio [H3O+] a partir del pH
Si conocemos el pH de una solución y necesitamos determinar la concentración de iones hidronio, podemos revertir la operación matemática utilizada para calcular el pH. La relación es la siguiente:
[H3O+] = 10-pH
Esta operación es lo que a menudo se conoce como el antilogaritmo de -pH. En la mayoría de las calculadoras científicas, esta función se encuentra como 10x o "inv log".
Ejemplo Práctico: Encontrar [H3O+] a partir del pH
Supongamos que tenemos una solución con un pH de 8.34. Para encontrar la concentración de iones hidronio, seguimos estos pasos:
Partimos de la definición de pH:
8.34 = - log [H3O+]
Multiplicamos ambos lados por -1:
-8.34 = log [H3O+]
Aplicamos la operación inversa del logaritmo (antilogaritmo o 10x):
[H3O+] = 10-8.34
Al calcular esto en una calculadora, obtenemos:
[H3O+] = 4.57 x 10-9 M
Esta concentración extremadamente baja de H3O+ es consistente con un pH de 8.34, que indica una solución básica.
Cálculo del pOH a partir de la Concentración de Iones Hidróxido [OH-]
Así como el pH mide la acidez basándose en la concentración de H3O+, el pOH mide la basicidad basándose en la concentración de iones hidróxido (OH-). Para calcular el pOH de una solución, necesitamos conocer la concentración de iones hidróxido en moles por litro (molaridad). La expresión para el pOH es similar a la del pH:
pOH = - log [OH-]
Esta medida es particularmente útil cuando se trabaja con bases fuertes, ya que estas liberan iones hidróxido directamente en la solución.
Ejemplo Práctico: Calcular el pOH de una solución con [OH-]
Consideremos una solución que tiene una concentración de iones hidróxido de 4.82 x 10-5 M. Para encontrar el pOH, sustituimos este valor en la fórmula:
pOH = - log [4.82 x 10-5]
Calculando el logaritmo de 4.82 x 10-5, obtenemos aproximadamente -4.32.
pOH = - (-4.32)
pOH = 4.32
Un pOH de 4.32 indica que la solución es básica. Cuanto menor sea el pOH, mayor será la concentración de OH- y, por lo tanto, más básica será la solución.
Cálculo de la Concentración de Iones Hidróxido [OH-] a partir del pOH
De manera análoga al cálculo de [H3O+] a partir del pH, podemos determinar la concentración de iones hidróxido a partir del pOH mediante la operación inversa del logaritmo:
[OH-] = 10-pOH
Esta es la función antilogaritmo aplicada al valor negativo del pOH.
Ejemplo Práctico: Encontrar [OH-] a partir del pOH
Si una solución tiene un pOH de 5.70, podemos calcular la concentración de iones hidróxido de la siguiente manera:
Partimos de la definición de pOH:
5.70 = - log [OH-]
Multiplicamos ambos lados por -1:
-5.70 = log [OH-]
Aplicamos la función 10x:
[OH-] = 10-5.70
Al realizar este cálculo en una calculadora, obtenemos:
[OH-] = 2.00 x 10-6 M
Esta concentración de OH- es consistente con un pOH de 5.70, lo que nuevamente confirma que la solución es básica.
La Relación Fundamental entre pH y pOH
En cualquier solución acuosa a 25°C, existe una relación fundamental y constante entre el pH y el pOH. Esta relación se deriva del producto iónico del agua (Kw), que es 1.0 x 10-14 a 25°C. La ecuación que los vincula es sorprendentemente simple y extremadamente útil:
pH + pOH = 14
Esta ecuación nos permite calcular rápidamente uno de los valores si conocemos el otro, lo cual es invaluable en la resolución de problemas de química. Por ejemplo, si calculamos el pOH de una base fuerte, podemos obtener su pH de forma instantánea usando esta relación. Es importante recordar que esta relación de suma igual a 14 es válida específicamente a 25°C. Aunque el pH y el pOH existen a otras temperaturas, el valor de Kw y, por lo tanto, la suma de pH + pOH, varía ligeramente.
Ejemplo Práctico: Calcular el pH a partir del pOH
Supongamos que una solución tiene un pOH de 11.76. Para encontrar el pH de esta solución, simplemente reorganizamos la ecuación de la siguiente manera:
pH = 14 - pOH
Sustituimos el valor del pOH:
pH = 14 - 11.76
pH = 2.24
Un pH de 2.24 indica que la solución es ácida, lo cual tiene sentido, ya que un pOH de 11.76 implica una concentración muy baja de OH- y, por lo tanto, una concentración relativamente alta de H3O+.
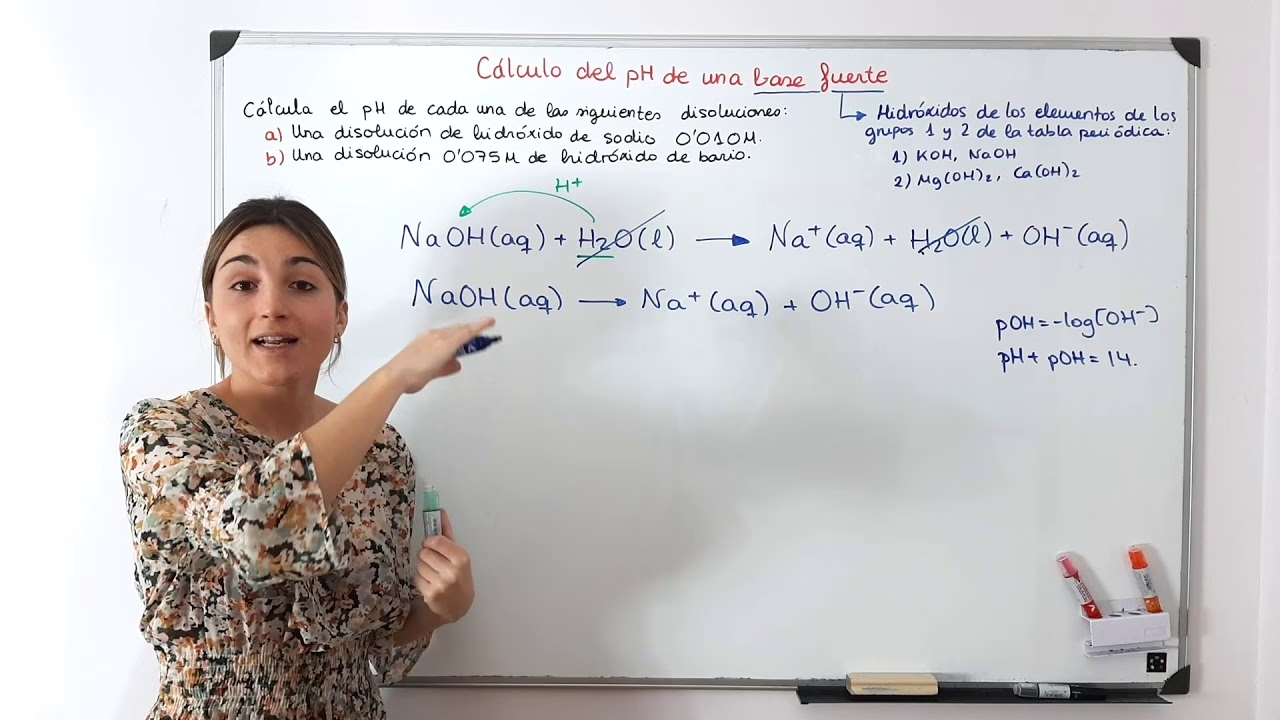
Comprendiendo los Ácidos y Bases Fuertes
La capacidad de calcular el pH y el pOH de soluciones de ácidos y bases fuertes es un pilar de la química de soluciones. Pero, ¿qué define exactamente a un ácido o una base como "fuerte"?
Ácidos Fuertes
Un ácido fuerte es aquel que se disocia o ioniza completamente (100%) en una solución acuosa. Esto significa que cuando un ácido fuerte (HA) se disuelve en agua, cada molécula de HA cede su protón (H+) a una molécula de agua (H2O) para formar un ion hidronio (H3O+) y un anión (A-). La reacción se representa como:
HA + H2O → H3O+ (aq) + A- (aq)
Debido a esta disociación completa, la concentración de iones hidronio [H3O+] en una solución de un ácido fuerte es directamente igual a la concentración inicial del ácido. Por ejemplo, una solución 0.1 M de HCl tendrá una [H3O+] de 0.1 M.
Los ácidos fuertes tienen un valor de Ka (constante de disociación ácida) muy grande, lo que indica su alta tendencia a disociarse. Consecuentemente, su valor de pKa (el logaritmo negativo de Ka) es muy pequeño, a menudo negativo. El pH de los ácidos fuertes suele ser muy bajo, generalmente entre 0 y 1, lo que refleja su alta concentración de H3O+.
La base conjugada de un ácido fuerte (el anión A-) es una base muy débil. Esto significa que tiene una afinidad extremadamente baja por los protones y no afectará significativamente el pH de la solución. Por ejemplo, el ion cloruro (Cl-), la base conjugada del HCl, es una base tan débil que las sales que lo contienen (como el NaCl) forman soluciones casi neutras (pH ~7).
Bases Fuertes
De manera similar, una base fuerte es aquella que se disocia o ioniza completamente (100%) en una solución acuosa, liberando iones hidróxido (OH-). Las bases fuertes son excelentes aceptores de protones. La mayoría de las bases fuertes son hidróxidos de metales alcalinos y alcalinotérreos, que son altamente solubles en agua. La reacción general de disociación de una base fuerte (BOH) en agua es:
BOH + H2O → B+ (aq) + OH- (aq)
Similar a los ácidos fuertes, la concentración de iones hidróxido [OH-] en una solución de una base fuerte es directamente igual a la concentración inicial de la base (ajustando por la estequiometría si la base libera más de un OH- por molécula, como Ca(OH)2). Por ejemplo, una solución 0.1 M de NaOH tendrá una [OH-] de 0.1 M.
Las bases fuertes tienen un valor de Kb (constante de disociación básica) muy grande, lo que indica su completa disociación. Por lo tanto, su valor de pKb (el logaritmo negativo de Kb) es muy pequeño. El pOH de las bases fuertes es muy bajo, lo que significa que su pH es muy alto, generalmente entre 13 y 14.
Ejemplos de Cálculo de pH para Ácidos y Bases Fuertes
Ejemplo 1: Solución de Ácido Clorhídrico (HCl)
Calcule el pH de una solución 0.1 M de HCl.
Dado que HCl es un ácido fuerte, se disocia completamente:
HCl + H2O → H3O+ (aq) + Cl- (aq)
Por lo tanto, [H3O+] = 0.1 M.
pH = -log [H3O+] = -log (0.1) = 1
El pH de la solución es 1.
Ejemplo 2: Solución de Hidróxido de Sodio (NaOH)
Calcule el pH de una solución 0.1 M de NaOH.
Dado que NaOH es una base fuerte, se disocia completamente:
NaOH + H2O → Na+ (aq) + OH- (aq)
Por lo tanto, [OH-] = 0.1 M.
Primero, calculamos el pOH:
pOH = -log [OH-] = -log (0.1) = 1
Luego, usamos la relación pH + pOH = 14 para encontrar el pH:
pH = 14 - pOH = 14 - 1 = 13
El pH de la solución es 13.
Lista de Ácidos y Bases Fuertes Comunes
Conocer los ácidos y bases fuertes más comunes es crucial, ya que simplifica enormemente los cálculos de pH y pOH. Aquí hay una tabla con los más importantes:
| Ácidos Fuertes | Bases Fuertes |
|---|---|
| Ácido Clorhídrico (HCl) | Hidróxido de Litio (LiOH) |
| Ácido Nítrico (HNO3) | Hidróxido de Sodio (NaOH) |
| Ácido Sulfúrico (H2SO4) | Hidróxido de Potasio (KOH) |
| Ácido Bromhídrico (HBr) | Hidróxido de Rubidio (RbOH) |
| Ácido Yodhídrico (HI) | Hidróxido de Cesio (CsOH) |
| Ácido Clórico (HClO3) | Hidróxido de Calcio (Ca(OH)2) |
| Ácido Perclórico (HClO4) | Hidróxido de Estroncio (Sr(OH)2) |
| Hidróxido de Bario (Ba(OH)2) |
Es importante notar que el ácido sulfúrico (H2SO4) es el único ácido fuerte común con más de un protón ácido (ácido diprótico), y su disociación completa solo ocurre para el primer protón. La segunda disociación es la de un ácido débil.
Introducción a pKa y pKb: Constantes de Disociación Logarítmicas
Además del pH y pOH, existen otras constantes de equilibrio logarítmicas fundamentales en química: pKa y pKb. Estas constantes son inversamente proporcionales a las constantes de disociación ácida (Ka) y básica (Kb), respectivamente, y nos proporcionan una medida de la fuerza intrínseca de un ácido o una base.
Cálculo de pKa a partir de Ka
La pKa se calcula utilizando la expresión:
pKa = - log (Ka)
Donde "Ka" es la constante de equilibrio para la ionización de un ácido. Un valor de Ka grande indica un ácido fuerte (mayor disociación), lo que se traduce en un valor de pKa pequeño (o incluso negativo). Conversely, un ácido débil tendrá un Ka pequeño y un pKa grande.
Ejemplo Práctico: Calcular el pKa del ácido acético
Si la Ka para el ácido acético es 1.78 x 10-5, calculamos su pKa así:
pKa = - log (1.78 x 10-5)
Calculando el logaritmo de 1.78 x 10-5, obtenemos aproximadamente -4.75.
pKa = - (-4.75)
pKa = 4.75
Este valor de pKa (4.75) es característico de un ácido débil, lo cual es consistente con el ácido acético.
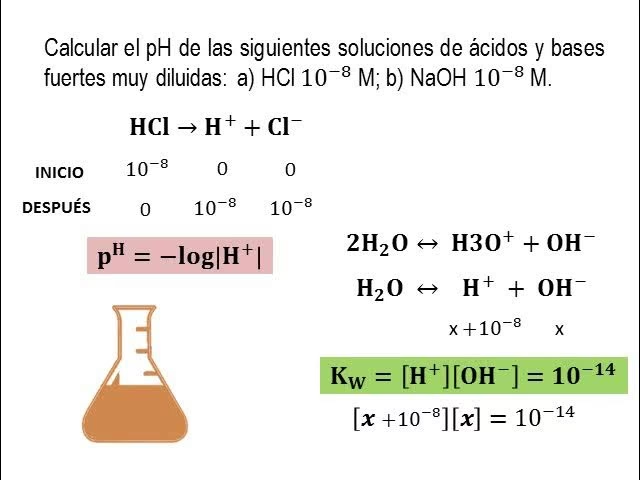
Cálculo de Ka a partir de pKa
Si conocemos el pKa de un ácido y necesitamos encontrar su Ka, realizamos la operación inversa:
Ka = 10-pKa
Esto es equivalente a "antilog (-pKa)".
Ejemplo Práctico: Calcular la Ka del ion amonio
Calcule el valor de la constante de ionización para el ion amonio (NH4+), Ka, si su pKa es 9.74.
Partimos de la definición de pKa:
9.74 = - log (Ka)
Multiplicamos por -1:
-9.74 = log (Ka)
Aplicamos la función 10x:
Ka = 10-9.74
Al calcular esto en una calculadora, obtenemos:
Ka = 1.82 x 10-10
Un valor de Ka tan pequeño confirma que el ion amonio es un ácido muy débil.
Cálculo de pKb a partir de Kb
De manera similar, la pKb se calcula a partir de la constante de equilibrio de la base (Kb) usando la expresión:
pKb = - log (Kb)
Donde Kb es la constante de equilibrio para la ionización de una base. Una Kb grande indica una base fuerte (mayor disociación), lo que resulta en un pKb pequeño. Una base débil tendrá una Kb pequeña y un pKb grande.
Ejemplo Práctico: Calcular el pKb de la metilamina
Si el valor de Kb para la metilamina es 4.4 x 10-4, calculamos su pKb así:
pKb = - log (4.4 x 10-4)
Calculando el logaritmo de 4.4 x 10-4, obtenemos aproximadamente -3.36.
pKb = - (-3.36)
pKb = 3.36
Este pKb de 3.36 es característico de una base relativamente fuerte, aunque no tan fuerte como los hidróxidos de metales alcalinos.
Cálculo de Kb a partir de pKb
Para encontrar la Kb a partir de la pKb, también se utiliza la operación inversa:
Kb = 10-pKb
Esto es lo mismo que "antilog (-pKb)".
Ejemplo Práctico: Calcular la Kb de la anilina
Calcule el valor de la constante de ionización, Kb, para la anilina si su pKb es 9.38.
Partimos de la definición de pKb:
9.38 = - log (Kb)
Multiplicamos por -1:
-9.38 = log (Kb)
Aplicamos la función 10x:
Kb = 10-9.38
Al calcular esto en una calculadora, obtenemos:
Kb = 4.17 x 10-10
Un valor de Kb tan pequeño indica que la anilina es una base muy débil.
Preguntas Frecuentes (FAQ)
¿Qué indica un pH bajo y un pH alto?
Un pH bajo (cercano a 0) indica una solución altamente ácida, lo que significa una alta concentración de iones hidronio (H3O+). Por otro lado, un pH alto (cercano a 14) indica una solución altamente básica o alcalina, lo que significa una alta concentración de iones hidróxido (OH-) y una muy baja concentración de H3O+. Un pH de 7 es neutro.
¿Qué es una base conjugada de un ácido fuerte?
La base conjugada de un ácido se forma cuando el ácido pierde un protón. En el caso de un ácido fuerte, que se disocia completamente, su base conjugada es extremadamente débil. Esto significa que tiene una afinidad muy baja por los protones y, por lo tanto, no afectará significativamente el pH de la solución. Por ejemplo, el ion Cl- es la base conjugada del HCl. Las sales formadas con estas bases conjugadas débiles (como NaCl) suelen producir soluciones neutras.
¿Por qué es importante la temperatura en la relación pH + pOH = 14?
La relación pH + pOH = 14 es estrictamente válida a 25°C. Esto se debe a que el producto iónico del agua (Kw = [H3O+][OH-]) varía con la temperatura. A 25°C, Kw es 1.0 x 10-14. Si la temperatura cambia, el valor de Kw también lo hace, y por lo tanto, la suma de pH + pOH será diferente de 14. Por ejemplo, a temperaturas más altas, el agua se autoioniza más, aumentando Kw y, por ende, reduciendo la suma de pH + pOH.
¿Cómo sé si un ácido o una base es fuerte?
Generalmente, se memorizan las listas de ácidos y bases fuertes más comunes. Los ácidos fuertes son aquellos que se disocian completamente en agua, como HCl, HNO3, H2SO4, HBr, HI, HClO3 y HClO4. Las bases fuertes son los hidróxidos de los metales alcalinos (LiOH, NaOH, KOH, RbOH, CsOH) y algunos hidróxidos de metales alcalinotérreos (Ca(OH)2, Sr(OH)2, Ba(OH)2). Si un ácido o base no está en estas listas, es probable que sea débil y requerirá cálculos de equilibrio más complejos.
¿Se puede tener un pH negativo?
Sí, aunque es menos común en soluciones cotidianas, se puede tener un pH negativo. Esto ocurre en soluciones de ácidos muy concentrados, donde la concentración de iones hidronio [H3O+] es mayor que 1 Molar. Por ejemplo, si [H3O+] = 10 M, entonces pH = -log(10) = -1. Aunque un pH negativo no es físicamente "negativo" en el sentido de una cantidad, es una consecuencia matemática de la definición logarítmica del pH.
Dominar los cálculos de pH, pOH, pKa y pKb es esencial para cualquiera que se adentre en el estudio de la química de soluciones. Estas herramientas no solo nos permiten cuantificar la acidez y basicidad, sino también predecir el comportamiento de las sustancias en diferentes entornos. Con las fórmulas y ejemplos proporcionados, esperamos que ahora te sientas más seguro al abordar estos conceptos fundamentales. La práctica constante es la clave para la maestría, así que te animamos a aplicar estos conocimientos en diversos problemas y escenarios.
Si quieres conocer otros artículos parecidos a Desentrañando el pH: Cálculos y Conceptos Clave puedes visitar la categoría Química.
