05/01/2023
En el vasto y complejo universo de la química, cada elemento posee propiedades únicas que lo definen y lo distinguen de los demás. Una de las características más fundamentales y determinantes es su masa atómica. Lejos de ser un simple número, la masa atómica es la clave para comprender la composición y el comportamiento de la materia, siendo esencial para cálculos estequiométricos, diseño de experimentos y la comprensión de las reacciones químicas. Pero, ¿cómo se llega a ese valor aparentemente preciso que vemos en la tabla periódica? La respuesta reside en una combinación de la naturaleza isotópica de los elementos y un cálculo ponderado que refleja la abundancia de cada uno de sus componentes.
Este artículo te guiará a través del concepto de masa atómica, desglosando los elementos que la componen, explicando el papel crucial de los isótopos y mostrándote, paso a paso, cómo se calcula. También exploraremos la importancia de la unidad de masa atómica unificada (u) y su equivalencia en gramos, un valor diminuto pero de inmensa relevancia. Prepárate para adentrarte en las profundidades de la química y desentrañar los secretos detrás del peso de los átomos.
- ¿Qué es la Masa Atómica? Una Definición Clara
- La Unidad de Masa Atómica Unificada (u o uma): El Estándar de Medida
- Isótopos: La Clave para el Cálculo de la Masa Atómica Promedio
- Cómo se Calcula la Masa Atómica Promedio: Un Paso a Paso
- Masa Atómica vs. Peso Atómico vs. Número de Masa vs. Masa Molar
- Importancia de la Masa Atómica en la Química
- Preguntas Frecuentes (FAQ)
- Conclusión
¿Qué es la Masa Atómica? Una Definición Clara
La masa atómica es, en esencia, la masa de un átomo. Sin embargo, esta definición simple esconde una complejidad inherente. Cuando hablamos de la masa atómica de un elemento que aparece en la tabla periódica, nos referimos más precisamente a la masa atómica promedio o peso atómico. Esto se debe a que la mayoría de los elementos existen en la naturaleza como una mezcla de diferentes isótopos, que son átomos del mismo elemento con el mismo número de protones, pero diferente número de neutrones y, por lo tanto, diferente masa.
Por ejemplo, si tomamos el elemento carbono, no todos los átomos de carbono tienen exactamente la misma masa. La gran mayoría son carbono-12 (con 6 protones y 6 neutrones), pero una pequeña fracción son carbono-13 (con 6 protones y 7 neutrones) y trazas de carbono-14 (con 6 protones y 8 neutrones). Cada uno de estos isótopos tiene su propia masa atómica específica. La masa atómica que se lista en la tabla periódica es un promedio ponderado de las masas de todos los isótopos naturales de ese elemento, teniendo en cuenta la abundancia relativa de cada isótopo.
Diferencia con el Número de Masa
Es fundamental no confundir la masa atómica con el número de masa. El número de masa (A) es simplemente la suma total de protones y neutrones en el núcleo de un átomo individual y siempre es un número entero. La masa atómica, en cambio, es la masa real del átomo y, debido a la contribución de la masa de los electrones y al defecto de masa nuclear (la energía liberada al formar el núcleo), no es exactamente un número entero, incluso para un isótopo específico, y menos aún para el promedio ponderado de un elemento.
La Unidad de Masa Atómica Unificada (u o uma): El Estándar de Medida
Medir la masa de un átomo en gramos es extremadamente complicado debido a su diminuto tamaño. Para simplificar estos cálculos y proporcionar una escala más manejable, los científicos introdujeron la unidad de masa atómica unificada, abreviada como 'u' o, anteriormente, 'uma' (unidad de masa atómica). Esta unidad se define en relación con un estándar: un átomo de carbono-12.
Específicamente, una unidad de masa atómica (1 u) se define como exactamente 1/12 de la masa de un átomo de carbono-12 sin enlaces y en su estado fundamental. Esta elección de carbono-12 como referencia es conveniente porque el carbono es un elemento abundante y su isótopo-12 es muy estable. Gracias a esta definición, la masa de un átomo de carbono-12 es exactamente 12 u.
Valor de 1 u en Gramos
Aunque la unidad de masa atómica facilita los cálculos relativos en el nivel atómico, es crucial conocer su equivalencia en unidades de masa más convencionales, como los gramos. El valor que corresponde a 1 unidad de masa atómica (u) en gramos es aproximadamente:
1 u ≈ 1.660539 x 10-24 gramos
Este número extremadamente pequeño subraya lo increíblemente ligeros que son los átomos, y por qué se necesita una unidad de medida especializada para trabajar con ellos de manera práctica en química.
Isótopos: La Clave para el Cálculo de la Masa Atómica Promedio
Como mencionamos, la existencia de isótopos es la razón principal por la que la masa atómica de un elemento en la tabla periódica no es un número entero exacto. Cada isótopo de un elemento tiene una masa atómica ligeramente diferente debido a su distinto número de neutrones. Sin embargo, la identidad química del elemento (determinada por el número de protones) permanece constante.

La abundancia isotópica es el porcentaje de cada isótopo presente en una muestra natural de un elemento. Esta abundancia se determina experimentalmente, a menudo utilizando una técnica llamada espectrometría de masas. Es este porcentaje de abundancia el que se utiliza para calcular la masa atómica promedio del elemento.
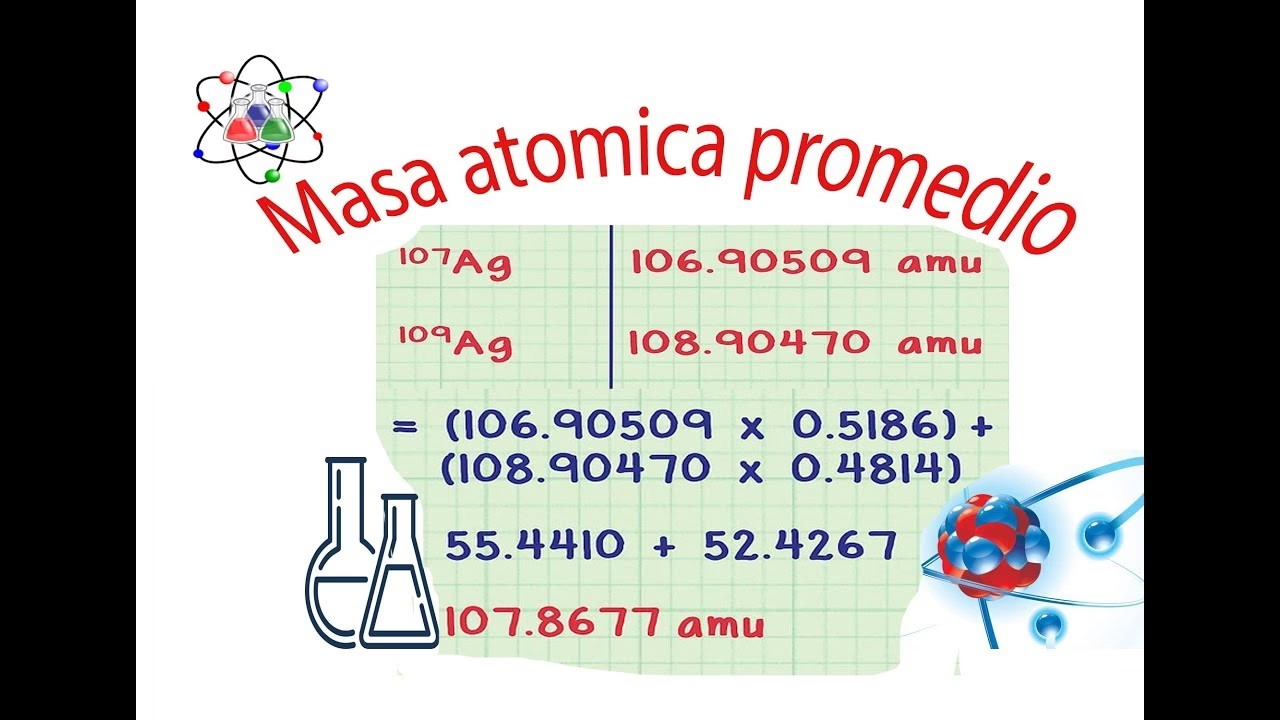
Cómo se Calcula la Masa Atómica Promedio: Un Paso a Paso
El cálculo de la masa atómica promedio de un elemento es un promedio ponderado de las masas de sus isótopos, donde el 'peso' de cada isótopo en el promedio es su abundancia natural. La fórmula general es la siguiente:
Masa Atómica Promedio = Σ (Masa Isotópicai × Abundancia Fraccionali)
Donde:
- Masa Isotópicai es la masa atómica de un isótopo específico (en u).
- Abundancia Fraccionali es la abundancia natural de ese isótopo expresada como una fracción (porcentaje dividido por 100).
- Σ (sigma) indica la suma de todos los productos para cada isótopo del elemento.
Ejemplo de Cálculo: El Cloro (Cl)
El cloro es un excelente ejemplo para ilustrar este cálculo, ya que tiene dos isótopos principales:
- Cloro-35: Masa isotópica = 34.96885 u; Abundancia natural = 75.77%
- Cloro-37: Masa isotópica = 36.96590 u; Abundancia natural = 24.23%
Paso 1: Convertir los porcentajes de abundancia a fracciones.
- Cloro-35: 75.77% / 100 = 0.7577
- Cloro-37: 24.23% / 100 = 0.2423
Paso 2: Multiplicar la masa de cada isótopo por su abundancia fraccional.
- Contribución del Cloro-35: 34.96885 u × 0.7577 = 26.4958 u
- Contribución del Cloro-37: 36.96590 u × 0.2423 = 8.9568 u
Paso 3: Sumar las contribuciones de todos los isótopos.
- Masa Atómica Promedio del Cloro = 26.4958 u + 8.9568 u = 35.4526 u
Este valor, 35.453 u (redondeado), es el que encontrarás para el cloro en la tabla periódica, reflejando la masa promedio de un átomo de cloro tal como se encuentra naturalmente en la Tierra.
Masa Atómica vs. Peso Atómico vs. Número de Masa vs. Masa Molar
Es común que estos términos se utilicen indistintamente o se confundan, pero es importante entender sus diferencias precisas:
| Concepto | Descripción | Unidades Típicas | Notas Clave |
|---|---|---|---|
| Masa Atómica | Masa de un átomo específico (isótopo particular). | u (unidad de masa atómica) | No es un número entero exacto debido a la masa de electrones y el defecto de masa. |
| Peso Atómico (Masa Atómica Promedio) | Media ponderada de las masas de los isótopos naturales de un elemento, considerando su abundancia. | u (unidad de masa atómica) | Es el valor que se encuentra en la tabla periódica para cada elemento. |
| Número de Masa (A) | Suma total de protones y neutrones en el núcleo de un átomo individual. | Sin unidades | Siempre es un número entero. Identifica un isótopo específico (ej. Carbono-12). |
| Masa Molar | Masa de un mol (6.022 x 1023 partículas) de una sustancia. Numéricamente igual al peso atómico o masa molecular/fórmula. | g/mol | Permite la conversión entre gramos y moles en cálculos de estequiometría. |
Importancia de la Masa Atómica en la Química
La masa atómica es más que un simple valor; es un pilar fundamental en la química, con aplicaciones cruciales en diversas áreas:
- Estequiometría: Es la base para todos los cálculos estequiométricos, permitiendo a los químicos predecir las cantidades de reactivos y productos en una reacción. Sin masas atómicas precisas, sería imposible balancear ecuaciones o determinar rendimientos.
- Análisis Químico: En técnicas analíticas como la espectrometría de masas, el conocimiento de las masas atómicas es vital para identificar compuestos y determinar su composición elemental.
- Diseño de Materiales: Comprender la masa de los átomos individuales y cómo se combinan es crucial para el diseño y síntesis de nuevos materiales con propiedades específicas.
- Física Nuclear: Aunque es un concepto químico, la masa atómica tiene implicaciones en la física nuclear, especialmente en el estudio de la estabilidad de los núcleos y las reacciones nucleares.
- Biología y Medicina: Las masas atómicas son fundamentales en el estudio de biomoléculas, la dosificación de medicamentos y el rastreo de procesos biológicos utilizando isótopos estables o radiactivos.
Preguntas Frecuentes (FAQ)
¿La masa atómica es siempre un número exacto?
No, la masa atómica de un isótopo específico no es un número entero exacto, aunque está muy cerca del número de masa (protones + neutrones). Esto se debe a la masa de los electrones y al 'defecto de masa' (la energía de enlace nuclear convertida en masa). La masa atómica promedio de un elemento (la que se ve en la tabla periódica) es aún menos probable que sea un número entero, ya que es un promedio ponderado de las masas de varios isótopos.
¿Cómo se mide la abundancia isotópica?
La abundancia isotópica se mide experimentalmente utilizando una técnica llamada espectrometría de masas. En un espectrómetro de masas, las muestras se ionizan y se aceleran a través de un campo magnético. Los iones se desvían de su trayectoria en función de su relación masa-carga. Al detectar dónde impactan los iones, se puede determinar la masa de cada isótopo y su abundancia relativa.
¿Por qué se usa el carbono-12 como referencia para la unidad de masa atómica?
El carbono-12 fue elegido como el estándar de referencia por varias razones: es un elemento abundante, su isótopo-12 es muy estable, y su masa puede medirse con gran precisión. Históricamente, el oxígeno y el hidrógeno también se utilizaron como referencias, pero el carbono-12 se adoptó universalmente en 1961 para evitar confusiones y asegurar la consistencia en las mediciones atómicas a nivel internacional.
¿Cuál es la diferencia entre masa atómica y masa molecular?
La masa atómica se refiere a la masa de un átomo individual o al promedio ponderado de los isótopos de un elemento. La masa molecular, por otro lado, es la suma de las masas atómicas de todos los átomos que componen una molécula. Por ejemplo, la masa atómica del hidrógeno es aproximadamente 1.008 u, mientras que la masa molecular del agua (H2O) es aproximadamente (2 × 1.008 u) + 15.999 u = 18.015 u.
¿La masa atómica cambia con las condiciones ambientales?
No, la masa atómica de un elemento es una propiedad intrínseca y no cambia con las condiciones ambientales como la temperatura, la presión o el estado físico. La composición isotópica natural de un elemento es bastante constante en la Tierra, aunque pueden existir ligeras variaciones en muestras de diferentes orígenes geológicos o biológicos.
Conclusión
El cálculo de la masa atómica de un elemento es un proceso fundamental en la química que nos permite comprender el "peso" de los bloques de construcción de la materia. Al considerar la masa de cada isótopo y su abundancia natural, obtenemos un valor promedio que es esencial para innumerables cálculos y aplicaciones científicas. La unidad de masa atómica (u) simplifica el manejo de estas masas diminutas, mientras que su equivalencia en gramos nos conecta con el mundo macroscópico. Dominar este concepto no solo te proporciona una comprensión más profunda de la tabla periódica, sino que también te equipa con una herramienta indispensable para navegar por el vasto y fascinante campo de la química.
Si quieres conocer otros artículos parecidos a ¿Cómo Calcular la Masa Atómica de un Elemento? puedes visitar la categoría Química.
