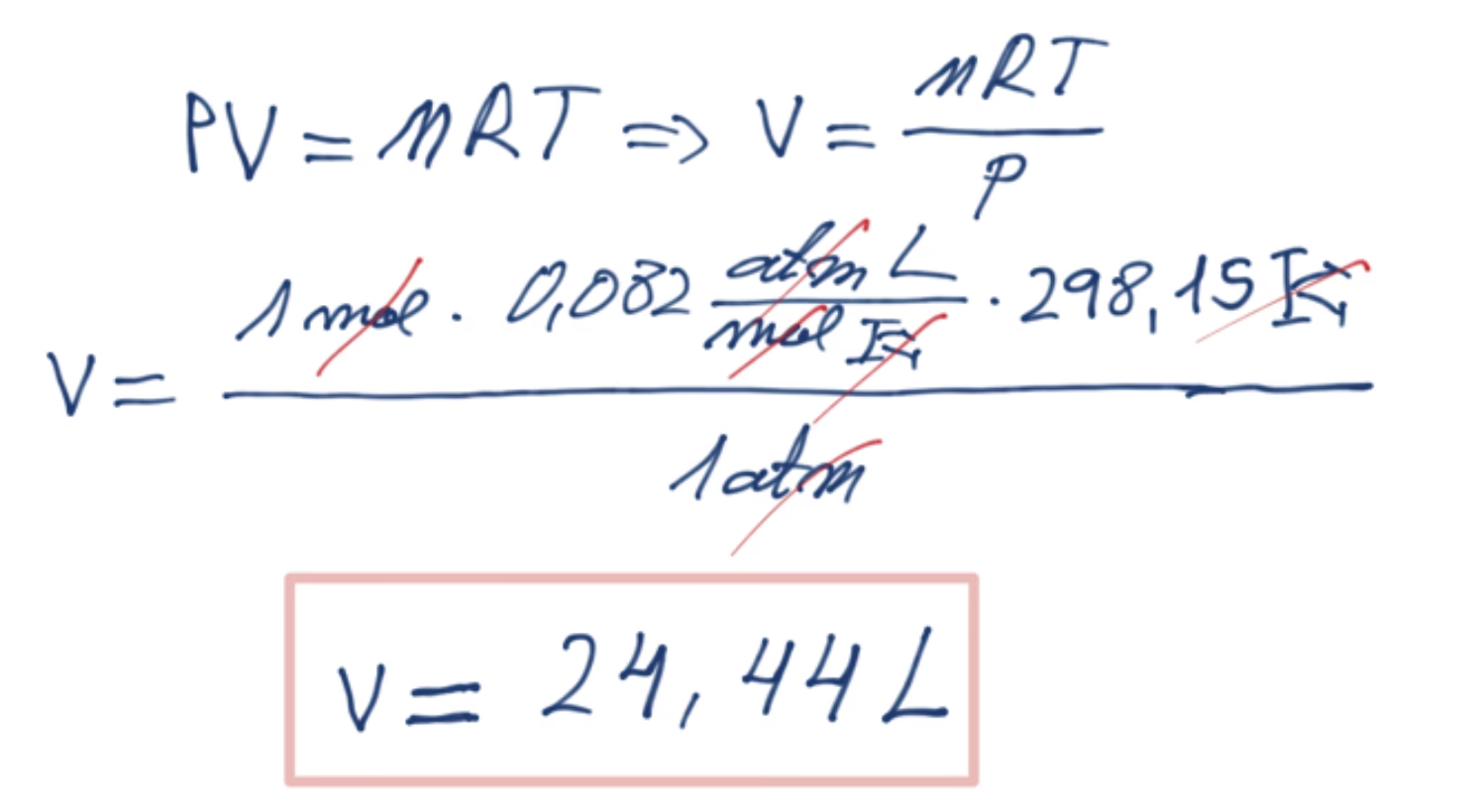23/09/2022
En el vasto universo de la química y la termodinámica, la comprensión de las condiciones bajo las cuales se comportan los gases es fundamental. Uno de los términos más recurrentes es el de “Volumen CNPT”, un concepto que, si bien suena técnico, es esencial para realizar cálculos precisos y entender fenómenos naturales. Pero, ¿qué significa exactamente CNPT y por qué es tan importante para el estudio de los gases?
El acrónimo CNPT se refiere a las Condiciones Normales de Presión y Temperatura. Este término es una convención utilizada en laboratorios y en el ámbito científico para estandarizar las mediciones y los cálculos, especialmente aquellos relacionados con el volumen de los gases. Sin una referencia común, sería imposible comparar resultados experimentales o predecir el comportamiento de una sustancia gaseosa bajo diferentes escenarios. Acompáñanos en este recorrido para desentrañar el significado, el cálculo y la relevancia del volumen CNPT, diferenciándolo de otras condiciones de referencia igualmente importantes.
- ¿Qué son las Condiciones Normales de Presión y Temperatura (CNPT)?
- La Ley de los Gases Ideales y el Cálculo del Volumen CNPT
- CNPT vs. Condiciones Estándar: Una Diferenciación Crucial
- ¿Por qué 22.4 Litros por Mol es tan Frecuente?
- Cálculo del Volumen Molar: Un Enfoque Práctico
- Preguntas Frecuentes sobre CNPT y Volumen Molar
- Conclusión
¿Qué son las Condiciones Normales de Presión y Temperatura (CNPT)?
Las Condiciones Normales de Presión y Temperatura (CNPT) son un conjunto de valores de referencia para la presión y la temperatura. Aunque su definición puede variar ligeramente según el contexto o la institución, la Unión Internacional de Química Pura y Aplicada (IUPAC) las describe como un término cualitativo, cuya elección depende de la preferencia del investigador. Usualmente, estas condiciones implican la presión ambiental y la temperatura del lugar donde se realiza el estudio.
La intención principal de establecer estas "condiciones normales" es proporcionar un marco de referencia consistente. Es muy común, por ejemplo, tomar como condiciones normales aquellas que consideran una temperatura de 25ºC (o 298.15 Kelvin) y una presión de 1 atmósfera (definida como 101.325 Kilopascales). Se les denomina normales precisamente porque son las que imperan habitualmente en un laboratorio o en el ambiente cotidiano, aunque también es posible encontrar referencias a 15ºC o 20ºC como temperaturas normales en ciertos contextos.
Este término es de gran utilidad en campos como la Termodinámica y la Química, donde la medición y el estudio del volumen de los gases son cruciales. Al especificar que un experimento o un cálculo se realiza bajo CNPT, se garantiza que los resultados puedan ser interpretados y replicados globalmente, asumiendo un ambiente de laboratorio típico.
La Ley de los Gases Ideales y el Cálculo del Volumen CNPT
Para comprender cómo se calcula el volumen de un gas en condiciones CNPT, es indispensable recurrir a la Ley de los Gases Ideales. Esta ley es una ecuación de estado que describe el comportamiento de un gas ideal, una idealización que simplifica el análisis de las propiedades de los gases reales bajo ciertas condiciones.
La fórmula de la Ley de los Gases Ideales es: PV = nRT
- P: Presión del gas
- V: Volumen del gas
- n: Cantidad de sustancia del gas (en moles)
- R: Constante de los gases ideales (un valor constante que depende de las unidades de presión, volumen y temperatura)
- T: Temperatura absoluta del gas (en Kelvin)
Si tomamos los valores más comúnmente aceptados para CNPT (Temperatura = 25ºC = 298.15 K y Presión = 1 atm) y queremos calcular el volumen ocupado por un mol de un gas ideal bajo estas condiciones, podemos despejar V de la ecuación:
V = (n * R * T) / P
Para n = 1 mol, R = 0.082 L·atm/(mol·K) (la constante de los gases ideales adecuada para estas unidades), T = 298.15 K y P = 1 atm:
V = (1 mol * 0.082 L·atm/(mol·K) * 298.15 K) / 1 atm
V = 24.436 litros
Este valor, 24.436 litros, representa el volumen que ocupa un mol de cualquier gas ideal bajo las condiciones normales de 25ºC y 1 atm. Es un valor de referencia muy utilizado en cálculos estequiométricos y termodinámicos cuando se trabaja con gases en un ambiente de laboratorio común.

CNPT vs. Condiciones Estándar: Una Diferenciación Crucial
Es muy importante no confundir las Condiciones Normales de Presión y Temperatura (CNPT) con las Condiciones Estándar (a menudo abreviadas como STP por Standard Temperature and Pressure, o simplemente "condiciones estándar" en español). Aunque ambos conceptos se utilizan como puntos de referencia para el estudio de gases, difieren en sus valores específicos de temperatura y presión y, por ende, en el volumen molar que un gas ideal ocupa bajo estas condiciones.
Las condiciones estándar, especialmente en termodinámica, son un conjunto de valores de referencia que son más cómodos y fácilmente reproducibles para el cálculo de propiedades como las entalpías y energías libres de reacción. Tradicionalmente, las condiciones estándar se definían como:
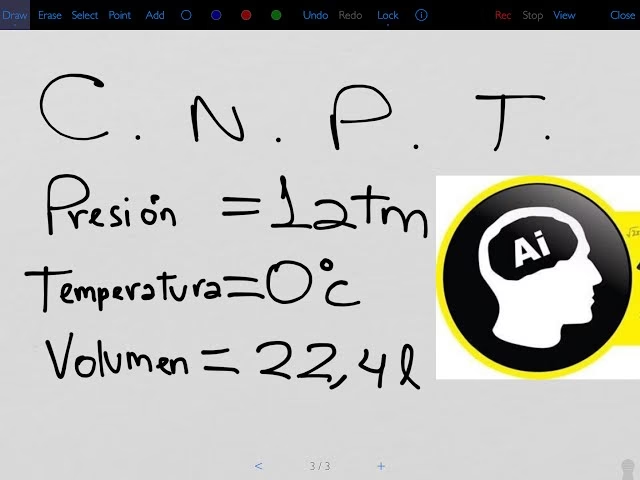
- Temperatura: 0ºC (273.15 K)
- Presión: 1 atmósfera (101.325 Pascales)
Bajo estas condiciones estándar originales, el volumen ocupado por un mol de un gas ideal es:
V = (1 mol * 0.082 L·atm/(mol·K) * 273.15 K) / 1 atm
V = 22.386 litros
Este valor se ha simplificado y popularizado comúnmente a 22.4 litros, siendo una cifra muy recurrente en libros de texto y problemas de química. La diferencia principal con CNPT (24.436 L) radica en la temperatura de referencia: 25ºC para CNPT frente a 0ºC para las condiciones estándar tradicionales. Esta variación en la temperatura, aunque parezca pequeña, tiene un impacto significativo en el volumen que ocupa el gas.
La Evolución de la Presión Estándar según la IUPAC
La definición de las condiciones estándar ha experimentado una modificación importante recomendada por la IUPAC a partir de 1982. Con el objetivo de simplificar y estandarizar aún más, la IUPAC recomendó emplear un valor para la presión estándar de 105 Pascales (100.000 Pa), que es equivalente a 1 bar, en lugar de la presión de 1 atmósfera (101.325 Pa).
Si recalculamos el volumen de un mol de un gas ideal bajo estas nuevas condiciones estándar (Temperatura = 0ºC = 273.15 K y Presión = 1 bar = 100.000 Pa), utilizando el valor de R adecuado (8.314 J/(mol·K) o 0.08314 L·bar/(mol·K)):
V = (1 mol * 0.08314 L·bar/(mol·K) * 273.15 K) / 1 bar
V = 22.71 litros (aproximadamente, si se usa R con más precisión)
Sin embargo, la cifra de 22.4 litros se sigue utilizando ampliamente como una aproximación práctica para las condiciones estándar, independientemente de si se usa 1 atm o 1 bar como presión, debido a su conveniencia y la pequeña diferencia que representa en muchos cálculos.
¿Por qué 22.4 Litros por Mol es tan Frecuente?
La cifra de 22.4 litros por mol es probablemente el valor más grabado en la memoria de cualquier estudiante de química. Su recurrencia se debe a que representa el volumen molar de un gas ideal bajo las condiciones estándar de temperatura y presión (0°C y 1 atm o 1 bar), que históricamente han sido el punto de referencia más común para la estequiometría de gases.

Mientras que el volumen CNPT (24.436 L a 25°C y 1 atm) es más representativo de las condiciones de un laboratorio típico, el 22.4 L se utiliza como un valor estándar y simplificado para cálculos teóricos y comparaciones de propiedades de gases. Es una herramienta poderosa para estimar rápidamente la cantidad de sustancia o el volumen de un gas sin necesidad de especificar continuamente las condiciones exactas, asumiendo que se está trabajando bajo las condiciones estándar.
Cálculo del Volumen Molar: Un Enfoque Práctico
El volumen molar de un gas, es decir, el volumen ocupado por un mol de ese gas, se calcula siempre utilizando la Ley de los Gases Ideales (PV=nRT), pero los valores de P y T deben ser los específicos para las condiciones que se estén considerando. No hay un único "volumen molar" universal, sino que este depende directamente de la presión y la temperatura.
Para calcular el volumen molar (V/n), simplemente reorganizamos la ecuación:
V/n = RT/P
Esto significa que si conoces la temperatura y la presión (y utilizas la constante de los gases R adecuada para tus unidades), puedes calcular el volumen que ocuparía un mol de cualquier gas ideal bajo esas condiciones específicas. Por lo tanto, la clave está en identificar claramente si te refieres a CNPT, a condiciones estándar antiguas, o a las condiciones estándar modernas de la IUPAC, ya que cada una arrojará un volumen molar ligeramente diferente.
Tabla Comparativa de Condiciones de Referencia para Gases Ideales
Para facilitar la comprensión y el uso de estas diferentes condiciones, presentamos la siguiente tabla comparativa:
| Condición | Temperatura | Presión | Volumen Molar (1 mol de gas ideal) | Uso Principal |
|---|---|---|---|---|
| CNPT (Común) | 25°C (298.15 K) | 1 atm (101.325 kPa) | 24.436 Litros | Condiciones ambientales de laboratorio. |
| Condiciones Estándar (Tradicional) | 0°C (273.15 K) | 1 atm (101.325 kPa) | 22.386 Litros (aprox. 22.4 L) | Cálculos termodinámicos de referencia, estequiometría clásica. |
| Condiciones Estándar (IUPAC, 1982+) | 0°C (273.15 K) | 1 bar (100.000 kPa) | 22.71 Litros (aprox. 22.4 L) | Cálculos termodinámicos modernos, estandarización IUPAC. |
Preguntas Frecuentes sobre CNPT y Volumen Molar
¿Es lo mismo CNPT que Condiciones Estándar?
No, no son lo mismo. Aunque ambos son conjuntos de condiciones de referencia para gases, difieren en sus valores de temperatura y, en algunos casos, de presión. CNPT comúnmente se refiere a 25°C y 1 atm, mientras que las condiciones estándar tradicionalmente son 0°C y 1 atm (o 1 bar según la IUPAC más reciente). Esta diferencia de temperatura lleva a un volumen molar diferente para un gas ideal.
¿Por qué el volumen molar de un gas ideal cambia según las condiciones?
El volumen molar de un gas ideal cambia porque el volumen de un gas es directamente proporcional a su temperatura absoluta e inversamente proporcional a su presión. Esto se describe por la Ley de los Gases Ideales (PV=nRT). Si se modifican la temperatura o la presión, el volumen ocupado por la misma cantidad de moles de gas también cambiará.

¿Qué es exactamente un mol de gas?
Un mol es una unidad de cantidad de sustancia, definida como la cantidad de sustancia que contiene tantas entidades elementales (átomos, moléculas, iones, etc.) como átomos hay en 0.012 kilogramos de carbono-12. Este número es el número de Avogadro, aproximadamente 6.022 x 10^23 entidades. Por lo tanto, un mol de gas representa una cantidad específica de partículas de gas, independientemente de su tipo.
¿Dónde se utilizan comúnmente los conceptos de CNPT y volumen molar?
Estos conceptos son fundamentales en la química (especialmente en estequiometría de reacciones con gases), la termodinámica, la ingeniería química y ambiental, la física y cualquier campo que requiera la medición y el cálculo de propiedades de gases. Son cruciales para diseñar procesos industriales, evaluar la contaminación del aire o comprender reacciones químicas a gran escala.
¿Es un gas real igual que un gas ideal?
No, un gas ideal es un modelo teórico que asume que las partículas de gas no tienen volumen y no interactúan entre sí. Los gases reales, por otro lado, sí tienen volumen y sus partículas ejercen fuerzas de atracción o repulsión. Sin embargo, en condiciones de baja presión y alta temperatura (lejos de su punto de licuefacción), el comportamiento de los gases reales se aproxima mucho al de los gases ideales, haciendo que la Ley de los Gases Ideales sea una herramienta muy útil en la práctica.
Conclusión
El concepto de Volumen CNPT y las Condiciones Normales de Presión y Temperatura son pilares en el estudio de los gases y sus propiedades. Comprender qué significan, cómo se calculan y, crucialmente, cómo se diferencian de las condiciones estándar, es indispensable para cualquier persona que trabaje con cálculos químicos o termodinámicos. Aunque los valores específicos pueden variar ligeramente según la convención (CNPT, condiciones estándar tradicionales o IUPAC), la Ley de los Gases Ideales proporciona la herramienta fundamental para calcular el volumen molar bajo cualquier conjunto de condiciones dadas de presión y temperatura. Dominar estos conceptos no solo facilita la resolución de problemas, sino que también profundiza nuestra comprensión del comportamiento de la materia en estado gaseoso.
Si quieres conocer otros artículos parecidos a Volumen CNPT y Gases Ideales: Guía Completa puedes visitar la categoría Cálculos.