26/05/2022
El número de coordinación es uno de los conceptos más fundamentales en la química, especialmente en el estudio de los complejos metálicos y las estructuras cristalinas. Nos permite entender cómo los átomos o iones se agrupan en el espacio, formando las estructuras tridimensionales que definen las propiedades de los materiales. Desde la forma en que una proteína se pliega con un ion metálico en su centro hasta la disposición de los iones en un mineral, el número de coordinación es una clave esencial.
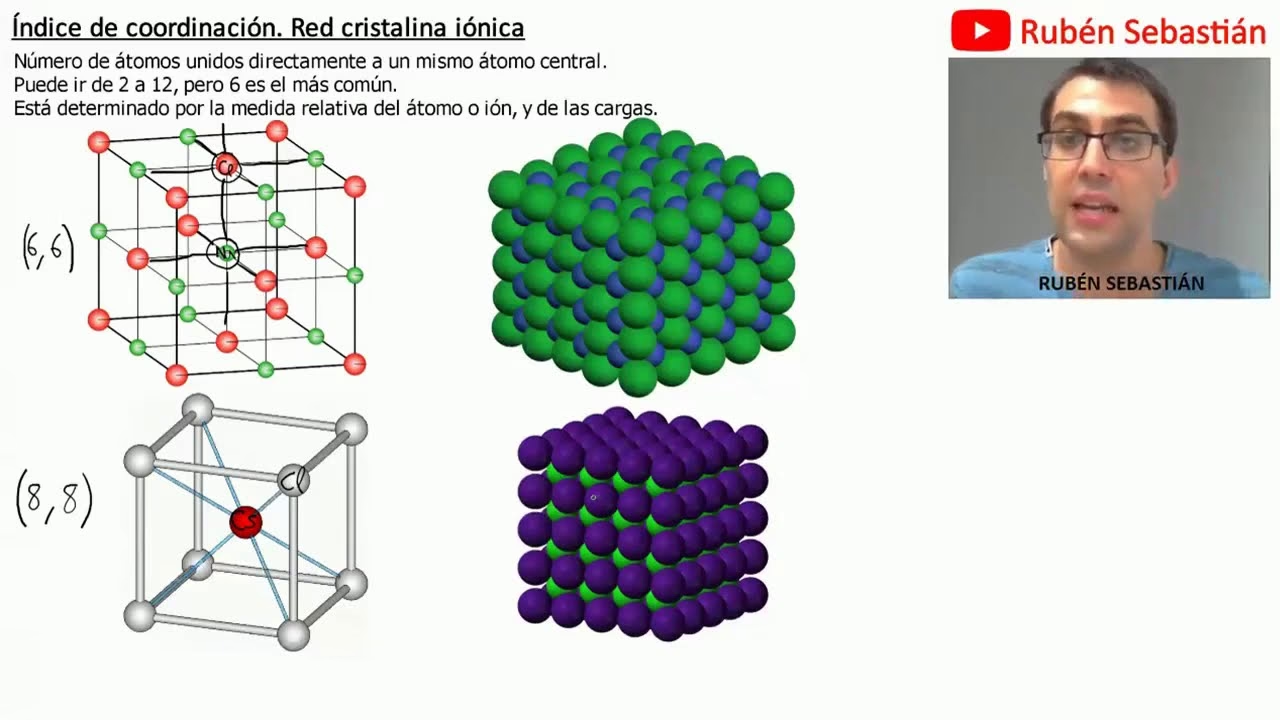
A menudo, la idea de "contar vecinos" parece sencilla, pero, como veremos, los factores que influyen en esta cuenta y las reglas que la rigen pueden ser sorprendentemente complejos y profundos. Este artículo desglosará qué es el número de coordinación, cómo se determina, los factores que lo afectan y las implicaciones de sus reglas en la arquitectura de la materia.
¿Qué es el Número de Coordinación?
En su definición más simple, el número de coordinación de un átomo o ion central es la cantidad de otros átomos, iones o moléculas (conocidos como ligandos) que se encuentran directamente unidos a él o que son sus vecinos más cercanos en una estructura. Estos vecinos forman lo que se conoce como la primera esfera de coordinación.
Por ejemplo, en el complejo [Fe(CN)6]3-, el ion central es el hierro (Fe). A este ion de hierro están unidos seis iones cianuro (CN-). Por lo tanto, el número de coordinación del hierro en este complejo es 6. Es una relación directa: se cuenta el número de átomos donantes que están enlazados al ion metálico central.
Este concepto es crucial porque no solo nos da una cifra, sino que también nos orienta sobre la geometría de coordinación alrededor del átomo central. Un número de coordinación de 4, por ejemplo, puede indicar una geometría tetraédrica o cuadrada plana, mientras que un 6 casi siempre sugiere una geometría octaédrica.
Factores que Influyen en el Número de Coordinación
Aunque la definición de contar ligandos parece sencilla, el número de coordinación que un átomo o ion puede adoptar no es arbitrario. Depende de una variedad de factores, incluyendo el tamaño del ion central, el tamaño y la naturaleza de los ligandos (es decir, su capacidad donante y su volumen estérico), y las condiciones del entorno, como la estabilidad de la red cristalina o la presencia de disolventes.
Consideremos el zinc (Zn), un metal que es notablemente flexible en su número y geometría de coordinación. Para el zinc, los números de coordinación más comunes varían de cuatro a seis. Sin embargo, también se han observado números de coordinación de dos, tres, siete y ocho, aunque son menos frecuentes y dependen en gran medida del tipo de donantes o ligandos involucrados.
Geometrías Comunes y Ejemplos Específicos:
- Número de Coordinación 2: Es raro para el zinc, pero se observa con ligandos extremadamente voluminosos como amidas, sililos, alquilos o tioles/selenofenolatos voluminosos. Por ejemplo, Zn[Si(SiMe3)3]2. La geometría suele ser lineal.
- Número de Coordinación 3: Más común, especialmente con ligandos alquilo, amida y fenolato/tiolato voluminosos. La geometría más frecuente es la trigonal plana. También se ha observado la trigonal piramidal con ligandos adecuadamente restringidos.
- Número de Coordinación 4: Muy común. La geometría tetraédrica distorsionada es frecuente. El zinc de cuatro coordenadas juega un papel estructural vital en las metaloproteínas, como las proteínas de dedo de zinc.
- Número de Coordinación 5: Observado con frecuencia. Las geometrías pueden ser piramidal cuadrada o bipiramidal trigonal distorsionadas.
- Número de Coordinación 6: También muy común. La geometría octaédrica es la más esperada. El zinc puede adoptar una variedad de geometrías de coordinación distorsionadas sin una penalización energética significativa.
- Números de Coordinación 7 y 8: Son inusuales para el zinc, pero se han documentado en casos específicos, como en una estructura de calixareno de tetraamida de zinc, donde se observa un número de coordinación de ocho.
La flexibilidad del zinc para adoptar diferentes números y geometrías de coordinación es importante tanto en solución como en estado sólido, lo que puede llevar a equilibrios entre especies con distintos números de coordinación. Por ejemplo, el zinc con el ligando 1,2-etilendiamina puede formar complejos con relaciones metal-ligando de 1:1 y 1:2 en solución acuosa, existiendo equilibrios entre especies tetraédricas y octaédricas.
Influencia de la Estructura de la Red y Ligandos Rígidos:
En algunos casos, la geometría de coordinación está fuertemente influenciada por la rigidez del ligando o la estabilidad de la red cristalina. Por ejemplo, el zinc cuadrado plano es más común en complejos de porfirina y ftalocianina, donde el ligando restringe la geometría de enlace. Incluso se han encontrado ejemplos de geometría cuadrada plana con oxígeno en la estructura de capas de Ba2Zn3As2O2, donde la estabilidad de la red supera la penalización energética de una geometría menos favorable para el oxígeno.
| Número de Coordinación | Geometría Típica | Ejemplo/Comentario (para Zinc) |
|---|---|---|
| 2 | Lineal | Con ligandos muy voluminosos (amidas, sililos) |
| 3 | Trigonal Plana / Piramidal | Común con alquilos, amidas, fenolatos voluminosos |
| 4 | Tetraédrica (distorsionada) / Cuadrada Plana | Muy común, clave en metaloproteínas; cuadrada plana con porfirinas |
| 5 | Bipiramidal Trigonal / Piramidal Cuadrada | Frecuentemente observada |
| 6 | Octaédrica (distorsionada) | Muy común |
| 7, 8 | Poliedros complejos | Inusuales, observados en casos específicos con ligandos grandes |
La Regla del Número de Coordinación en Cristalografía
Más allá de la simple cuenta de ligandos en un complejo molecular, el número de coordinación adquiere una dimensión más profunda en la cristalografía. En las estructuras cristalinas, donde los átomos están dispuestos en una red tridimensional repetitiva, las relaciones entre los números de coordinación de los diferentes tipos de átomos y sus coeficientes estequiométricos no son aleatorias. Se rigen por una regla fundamental conocida como la "regla del número de coordinación" o "regla de O'Keeffe y Hyde".
Esta regla expresa el hecho simple pero poderoso de que el número total de contactos de coordinación de los aniones es igual al de los cationes en una estructura. Para un compuesto ternario con dos componentes catiónicos (A, B) y una matriz aniónica (X), donde p, q y r son los números de coordinación respectivos de los componentes tipo A, B y X, la regla se formula como:
ap + bq = cr
Donde 'a', 'b' y 'c' son los coeficientes estequiométricos de A, B y X en la fórmula del compuesto (AaBbXc). Esta ecuación aparentemente sencilla tiene profundas implicaciones para la arquitectura de las estructuras cristalinas.
El Principio de Simplicidad y sus Consecuencias
El "principio de simplicidad" y el "principio de simetría" son conceptos clave que guían la formación de las estructuras cristalinas. Estos principios sugieren que la naturaleza tiende a crear interacciones y entornos similares para especies atómicas similares, y que la topología de la estructura buscará la "solución más simple" en las relaciones numéricas entre los números de coordinación y los coeficientes estequiométricos.
Sin embargo, la aplicación de esta regla puede llevar a números no enteros para 'r' (el número de coordinación del anión) en el cálculo. Dado que los números de coordinación son por definición enteros, el principio de simplicidad exige que 'r' se exprese como un promedio de números enteros adyacentes. Esto implica que, para satisfacer la regla, un anión puede necesitar estar presente en diferentes sitios cristalográficos, cada uno con un entorno de coordinación ligeramente distinto pero que, en promedio, satisface la relación estequiométrica.
Por ejemplo, en la estructura tipo K2NiF4, la regla del número de coordinación para K, Ni y F requiere que el flúor (F) tenga un número de coordinación promedio de 6. Sin embargo, para que esto sea posible con los números de coordinación específicos de K y Ni, el flúor debe ocupar al menos dos sitios cristalográficamente diferentes, F(1) y F(2), cada uno con un entorno de coordinación entero (por ejemplo, F(1) rodeado por 4 K y 2 Ni, y F(2) por 5 K y 1 Ni), de modo que el promedio de estos entornos dé el valor esperado.
Esto nos permite "predecir" o al menos entender por qué ciertas estructuras tienen múltiples sitios para el mismo tipo de átomo, o por qué ciertos grupos espaciales no pueden "albergar" una combinación dada de átomos y números de coordinación. La regla y el principio de simplicidad son herramientas poderosas para racionalizar la topología de estructuras de coordinación inorgánicas, incluso las muy complejas.
Casos Especiales y Efectos de Segregación
Aunque el "principio de simplicidad" y la solución numérica derivada de la regla del número de coordinación suelen ser excelentes para predecir o entender las estructuras, existen casos donde estas "soluciones simples" son violadas. Estas desviaciones no son errores en la regla, sino que reflejan la influencia de otros factores, que a menudo se denominan "efectos químicos".
Un ejemplo clásico es la estructura de Cr2F5, donde el cromo (Cr) tiene dos estados de oxidación (CrII y CrIII). Aunque la solución numérica simple podría sugerir una distribución homogénea, la estructura real muestra una "segregación" de los iones CrII y CrIII en diferentes entornos de coordinación. Los octaedros de CrIIF6 y CrIIIF6 se conectan de maneras específicas (por esquinas o aristas) que minimizan la repulsión CrII-CrIII y acomodan los diferentes tamaños de los iones de cromo. Esta "segregación" no es puramente numérica, sino que es impulsada por consideraciones químicas como el tamaño iónico y la repulsión electrostática.
Segregación Numérica vs. Segregación Química:
Podemos distinguir dos tipos de segregación en las estructuras cristalinas:
- Segregación Numérica (Σnum): Ocurre cuando la "solución numérica simple" de la regla del número de coordinación ya implica que los aniones se distribuyan en varios sitios cristalográficos distintos para satisfacer el promedio de los números de coordinación enteros. Es una consecuencia directa de las relaciones estequiométricas y los números de coordinación promedio.
- Segregación Química (Σchem): Se refiere a la segregación que ocurre por razones distintas a las numéricas, es decir, cuando la estructura real se desvía de la solución numérica simple. Esto suele deberse a "incompatibilidades químicas" entre los cationes (diferencias en los tipos de enlace, efectos de pares solitarios, o la tendencia a formar clústeres). La estructura de FeNb2O6, por ejemplo, muestra una segregación química donde los iones de Fe y Nb se separan en diferentes secciones de la estructura, a pesar de que sus números de coordinación catiónicos son iguales.
La segregación total (Σtot) se define como la suma de la segregación numérica y la segregación química (Σtot = Σnum + Σchem). Cuantificar esta segregación nos permite entender mejor las fuerzas que moldean la topología de una estructura cristalina.
Preguntas Frecuentes sobre el Número de Coordinación
¿El número de coordinación siempre es un número entero?
Sí, por definición, el número de coordinación es el número de vecinos más cercanos y, por lo tanto, debe ser un número entero. Sin embargo, en el contexto de la regla del número de coordinación en cristalografía, los cálculos basados en la estequiometría pueden arrojar valores no enteros. Esto implica que el átomo en cuestión debe ocupar múltiples sitios cristalográficos, cada uno con un número de coordinación entero, de modo que el promedio de estos sitios coincida con el valor no entero calculado.
¿Cómo se relaciona el número de coordinación con la geometría molecular?
El número de coordinación determina directamente la geometría molecular alrededor del átomo central. Por ejemplo, un número de coordinación de 2 suele implicar una geometría lineal; 3, trigonal plana; 4, tetraédrica o cuadrada plana; 5, bipiramidal trigonal o piramidal cuadrada; y 6, octaédrica. La elección exacta entre geometrías isoméricas (como tetraédrica vs. cuadrada plana para 4) depende de los ligandos y del metal central.
¿Puede un mismo elemento tener diferentes números de coordinación?
Absolutamente. Como vimos con el zinc, un mismo elemento puede exhibir una variedad de números de coordinación dependiendo de los ligandos a los que se une, su estado de oxidación y las condiciones ambientales (por ejemplo, si está en solución, en un complejo molecular aislado o en una red cristalina). La flexibilidad en el número de coordinación es común para muchos metales de transición.
¿El tamaño de los átomos influye en el número de coordinación?
Sí, el tamaño relativo del ion central y de los ligandos es un factor crucial. Los iones centrales más grandes pueden acomodar un mayor número de ligandos, mientras que los ligandos muy voluminosos pueden restringir el número de ligandos que pueden rodear al ion central debido a impedimentos estéricos. Las relaciones de radio iónico a menudo se utilizan como una guía para predecir los números de coordinación.
Conclusión
El número de coordinación es mucho más que una simple cifra. Es una herramienta poderosa que nos permite desentrañar la intrincada arquitectura de los complejos químicos y las estructuras cristalinas. Desde la definición básica de contar ligandos hasta la aplicación de la compleja regla del número de coordinación en el estado sólido, este concepto subraya cómo las interacciones a nivel atómico se traducen en las propiedades macroscópicas de los materiales.
Comprender los factores que influyen en la geometría de coordinación, así como las sutilezas de los principios de simplicidad y los efectos de segregación, nos proporciona una visión más profunda de por qué las estructuras se forman de la manera en que lo hacen. En el vasto campo de la química, el número de coordinación sigue siendo una piedra angular para el diseño y la caracterización de nuevos materiales y para la comprensión de los sistemas biológicos.
Si quieres conocer otros artículos parecidos a ¿Cómo Determinar el Número de Coordinación? puedes visitar la categoría Química.

