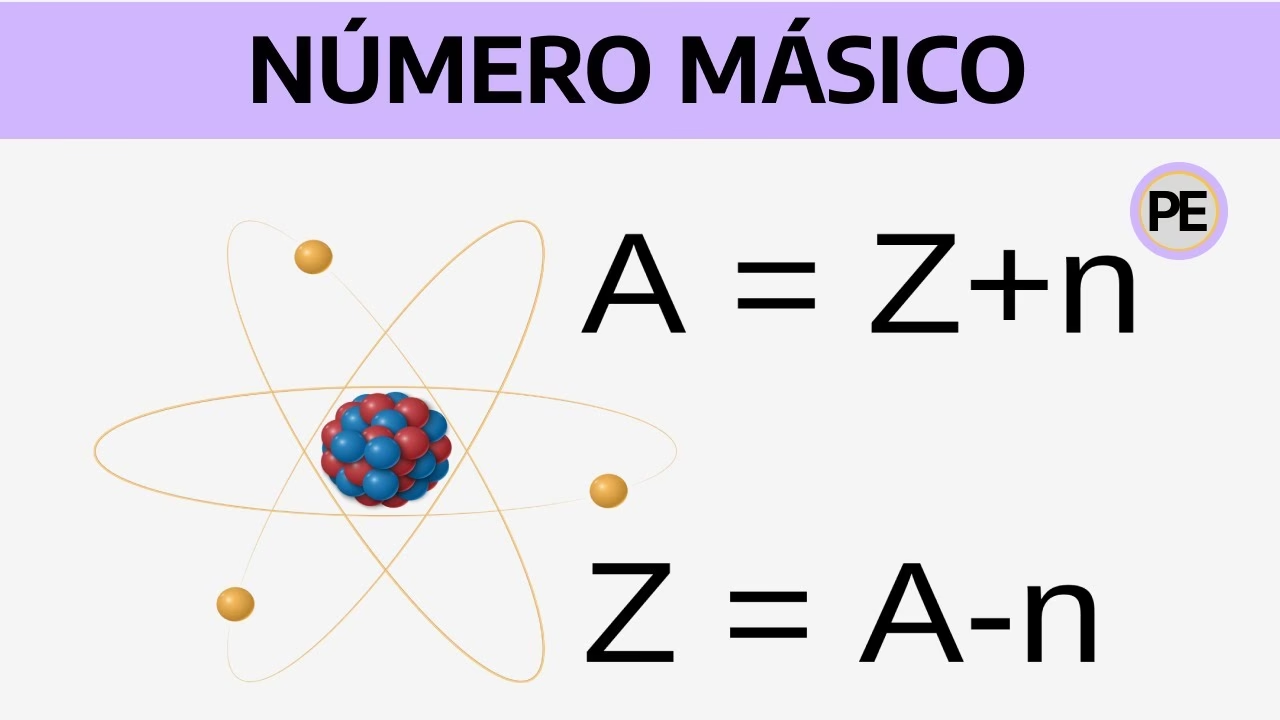06/04/2025
En el fascinante universo de la química, cada elemento tiene una huella dactilar única, una característica fundamental que lo distingue de todos los demás. Esta característica es el número atómico, representado por la letra Z. Comprender qué significa la Z y cómo se determina es crucial para desentrañar los misterios de la materia y su comportamiento. Si alguna vez te has preguntado cómo los científicos identifican los elementos o cómo se organizan en la tabla periódica, la respuesta reside en el valor de Z.

A menudo, cuando pensamos en 'calcular', imaginamos una fórmula matemática compleja. Sin embargo, en el caso de la Z, su 'cálculo' o determinación es más una cuestión de comprender su definición y su relación intrínseca con la estructura del átomo. Este artículo te guiará a través de lo que la Z realmente significa, por qué es tan importante y cómo puedes identificarla o deducirla a partir de otra información atómica.
- ¿Qué Significa la Z en Química? La Identidad Fundamental de un Átomo
- Desentrañando la Identidad: ¿Cómo se "Calcula" o Determina Z?
- La Profunda Importancia de Z en la Estructura Atómica y la Química
- Z en Acción: Ejemplos y Relaciones Clave
- Preguntas Frecuentes sobre el Número Atómico (Z)
- ¿Puede un elemento cambiar su número atómico?
- ¿Es Z siempre igual al número de electrones?
- ¿Cuál es la diferencia entre el número atómico (Z) y el número másico (A)?
- ¿Quién fue el científico clave en el descubrimiento del número atómico?
- ¿Por qué es el número atómico más fundamental que la masa atómica?
- Conclusión
¿Qué Significa la Z en Química? La Identidad Fundamental de un Átomo
En química, la letra Z representa el número atómico de un átomo. Pero, ¿qué es exactamente el número atómico? Es, ni más ni menos, que el número total de protones que se encuentran en el núcleo de un átomo. Esta es una propiedad fundamental e inmutable que define la identidad de un elemento químico.
Cada elemento en el universo posee un número atómico único. Por ejemplo, todos los átomos de hidrógeno tienen 1 protón (Z=1), todos los átomos de helio tienen 2 protones (Z=2), y así sucesivamente. Si un átomo ganara o perdiera un protón, se transformaría instantáneamente en un elemento completamente diferente. Esto subraya la importancia crítica de Z: es la característica definitoria que otorga a cada elemento sus propiedades químicas distinticas y determina su posición específica en la tabla periódica.
Es importante destacar que el número de protones no cambia bajo condiciones químicas normales; solo se ve afectado por reacciones nucleares. Esto significa que la Z es una constante para un elemento dado, sin importar si el átomo forma enlaces, se ioniza o participa en reacciones químicas.
Desentrañando la Identidad: ¿Cómo se "Calcula" o Determina Z?
La pregunta de cómo se "calcula" Z es interesante, ya que Z no se "calcula" en el sentido tradicional de una fórmula que utiliza múltiples variables para obtener un resultado. Más bien, Z es una propiedad intrínseca que se *define* como el número de protones. Sin embargo, hay formas de *determinar* o *inferir* Z si se te da otra información sobre el átomo.
1. Z es el Número de Protones: La Definición Central
La forma más directa de "saber" Z es conocer el número de protones. Si un problema te dice que un átomo tiene 6 protones en su núcleo, entonces su número atómico (Z) es 6. Sin necesidad de cálculos complejos, esta es la base de la identidad de un elemento.
2. Identificación a Través de la Tabla Periódica
La manera más común y sencilla de determinar Z para cualquier elemento es consultando la tabla periódica. Cada elemento en la tabla periódica está ordenado secuencialmente por su número atómico creciente. El número atómico (Z) generalmente se muestra en la parte superior del símbolo del elemento en cada casilla. Por ejemplo:
- Para el Hidrógeno (H), Z = 1.
- Para el Carbono (C), Z = 6.
- Para el Oxígeno (O), Z = 8.
- Para el Oro (Au), Z = 79.
La tabla periódica es, en esencia, una lista organizada de elementos por su Z.
3. Cálculo a Partir del Número Másico y el Número de Neutrones: La Fórmula de Deducción
Aunque Z es el número de protones, se puede "calcular" o deducir si se conocen otras dos propiedades atómicas: el número másico (A) y el número de neutrones (N). El número másico (A) representa la masa total del núcleo de un átomo, que es la suma de sus protones y neutrones.
La relación es la siguiente:
Número Másico (A) = Número Atómico (Z) + Número de Neutrones (N)
De esta ecuación, podemos despejar Z:
Z = A - N
Esta es la única situación en la que realmente "calculamos" Z a partir de otros valores. Por ejemplo, si tienes un átomo con un número másico de 12 y sabes que tiene 6 neutrones, entonces:
Z = 12 - 6 = 6
Este átomo con Z=6 es el Carbono.
4. Relación con los Electrones en Átomos Neutros
En un átomo eléctricamente neutro (es decir, que no tiene carga neta), el número de protones (cargas positivas) debe ser igual al número de electrones (cargas negativas) para que las cargas se cancelen. Por lo tanto, para un átomo neutro:
Z = Número de Electrones
Sin embargo, es crucial recordar que esta igualdad solo se aplica a átomos neutros. Cuando un átomo gana o pierde electrones, se convierte en un ion (un átomo con carga eléctrica). En un ion, el número de electrones cambia, pero el número de protones (Z) permanece constante, ya que cambiar el número de protones cambiaría la identidad del elemento.
Por ejemplo, un átomo de oxígeno (Z=8) neutro tiene 8 protones y 8 electrones. Si gana dos electrones para formar el ion O2-, seguirá teniendo 8 protones (Z=8), pero ahora tendrá 10 electrones.

La Profunda Importancia de Z en la Estructura Atómica y la Química
La Z no es solo un número; es la base de cómo entendemos la materia y sus interacciones.
Organización de la Tabla Periódica: De Mendeleev a Moseley
Originalmente, Dmitri Mendeleev organizó la tabla periódica basándose en la masa atómica. Sin embargo, esta organización tenía algunas anomalías. Fue Henry Moseley, a principios del siglo XX, quien, mediante experimentos con rayos X, descubrió que la propiedad más fundamental para organizar los elementos era el número de protones, es decir, el número atómico (Z). La tabla periódica moderna está organizada rigurosamente por Z creciente, lo que explica mejor las tendencias periódicas en las propiedades químicas de los elementos.
Propiedades Químicas y Configuración Electrónica
El número atómico (Z) determina directamente el número de electrones en un átomo neutro. La disposición de estos electrones en las capas y subcapas atómicas (conocida como configuración electrónica) es lo que rige el comportamiento químico de un elemento. Los electrones de valencia (los electrones en la capa más externa) son los que participan en la formación de enlaces químicos. Dado que Z define el número de electrones, indirectamente define cómo un átomo interactuará con otros átomos, formando moléculas y compuestos.
Isótopos: La Diversidad Dentro de la Misma Identidad
La Z también es clave para entender los isótopos. Los isótopos son átomos del mismo elemento (es decir, tienen el mismo número atómico Z y, por lo tanto, el mismo número de protones) pero difieren en su número de neutrones. Esto significa que tienen un diferente número másico (A). Por ejemplo, el carbono-12 (6 protones, 6 neutrones, A=12) y el carbono-14 (6 protones, 8 neutrones, A=14) son isótopos de carbono. Ambos tienen Z=6, lo que confirma que son el mismo elemento, pero sus diferentes números de neutrones les otorgan propiedades físicas ligeramente distintas, como su masa o estabilidad nuclear.
Z en Acción: Ejemplos y Relaciones Clave
Para solidificar nuestra comprensión, veamos algunos ejemplos y una tabla comparativa:
- Hidrógeno (H): Z = 1. Esto significa que cada átomo de hidrógeno tiene 1 protón. Un átomo neutro de hidrógeno también tendrá 1 electrón. Si estamos hablando del isótopo más común, protio, también tendrá 0 neutrones (A=1).
- Oxígeno (O): Z = 8. Todos los átomos de oxígeno tienen 8 protones. Un átomo neutro de oxígeno tiene 8 electrones. El isótopo más común, oxígeno-16, tiene 8 neutrones (A=16).
- Hierro (Fe): Z = 26. Cada átomo de hierro tiene 26 protones. Un átomo neutro de hierro tiene 26 electrones. El isótopo más común, hierro-56, tiene 30 neutrones (A=56).
Tabla Comparativa de Elementos y sus Propiedades Atómicas
| Elemento | Símbolo | Número Atómico (Z) | Número de Protones | Número de Electrones (en átomo neutro) | Número Másico (A) del Isótopo Más Común | Número de Neutrones (N = A - Z) |
|---|---|---|---|---|---|---|
| Hidrógeno | H | 1 | 1 | 1 | 1 | 0 |
| Helio | He | 2 | 2 | 2 | 4 | 2 |
| Carbono | C | 6 | 6 | 6 | 12 | 6 |
| Oxígeno | O | 8 | 8 | 8 | 16 | 8 |
| Sodio | Na | 11 | 11 | 11 | 23 | 12 |
| Hierro | Fe | 26 | 26 | 26 | 56 | 30 |
Preguntas Frecuentes sobre el Número Atómico (Z)
¿Puede un elemento cambiar su número atómico?
No, un elemento no puede cambiar su número atómico bajo condiciones químicas normales. Si el número de protones (Z) cambia, el átomo se transforma en un elemento diferente. Esto solo ocurre en reacciones nucleares, como la desintegración radiactiva o la fusión nuclear, donde el núcleo del átomo se modifica.
¿Es Z siempre igual al número de electrones?
No, Z solo es igual al número de electrones cuando el átomo es eléctricamente neutro. Si el átomo ha ganado o perdido electrones, se convierte en un ion, y el número de electrones ya no será igual al número atómico. Sin embargo, Z (el número de protones) siempre permanecerá constante para ese elemento.
¿Cuál es la diferencia entre el número atómico (Z) y el número másico (A)?
El número atómico (Z) es el número de protones en el núcleo y define la identidad del elemento. El número másico (A) es la suma total de protones y neutrones en el núcleo. Mientras que Z es único para cada elemento, diferentes isótopos del mismo elemento tendrán el mismo Z pero diferentes valores de A debido a sus diferentes números de neutrones.
¿Quién fue el científico clave en el descubrimiento del número atómico?
Aunque la idea de que los elementos se podían ordenar por alguna propiedad intrínseca del átomo existía, fue el físico británico Henry Moseley quien, en 1913, demostró experimentalmente que el número de protones (el número atómico) era la propiedad fundamental que determinaba la identidad de un elemento y su posición en la tabla periódica. Su trabajo fue crucial para corregir las anomalías de la tabla periódica de Mendeleev.
¿Por qué es el número atómico más fundamental que la masa atómica?
El número atómico es más fundamental porque es el que determina las propiedades químicas de un elemento. Los protones definen la carga nuclear, que a su vez atrae a los electrones. La configuración de estos electrones es lo que dicta cómo un átomo interactúa con otros. La masa atómica, por otro lado, puede variar ligeramente entre isótopos del mismo elemento, lo que no afecta sus propiedades químicas pero sí su masa.
Conclusión
El número atómico (Z) es mucho más que una simple letra o un número en la tabla periódica; es la clave maestra para entender la identidad de cada elemento en el universo. Define cuántos protones tiene un átomo, lo que a su vez determina su lugar en la tabla periódica y, fundamentalmente, su comportamiento químico. Aunque no se 'calcula' en el sentido de una operación matemática compleja a partir de múltiples variables, se determina directamente por el número de protones, se identifica fácilmente en la tabla periódica o se deduce a partir del número másico y los neutrones. Dominar el concepto de Z es un paso esencial para cualquier persona que desee comprender la química en su nivel más básico y profundo.
Si quieres conocer otros artículos parecidos a ¿Cómo Determinar el Número Atómico (Z) en Química? puedes visitar la categoría Química.