23/10/2022
Imagínese intentar medir algo tan increíblemente diminuto que es invisible incluso bajo los microscopios más potentes. Los átomos, los bloques fundamentales de toda la materia, desafían nuestra percepción cotidiana. Sin embargo, gracias a la química y la física, no solo podemos entender su estructura, sino también calcular su volumen. Esta tarea, que a primera vista parece imposible, es crucial para comprender las propiedades de los elementos y cómo interactúan entre sí. Desde la definición de volumen atómico hasta los métodos experimentales para determinar el tamaño de un átomo individual, este artículo desglosará las complejidades y la fascinante lógica detrás de estas mediciones.
¿Qué es el Volumen Atómico y Cómo se Define?
El volumen atómico es una propiedad periódica fundamental que nos da una idea del espacio que ocupa un mol de átomos de un elemento dado. No debe confundirse con el volumen de un átomo individual, aunque ambos conceptos están intrínsecamente relacionados. La forma más común de definir el volumen atómico (también conocido como volumen molar atómico) es a través de una relación sencilla entre la masa atómica y la densidad del elemento. La fórmula es la siguiente:
Volumen Atómico = Masa Atómica (M) / Densidad (ρ)
Se mide típicamente en unidades de volumen por mol, como centímetros cúbicos por mol (cm³/mol) o mililitros por mol (mL/mol).
Consideraciones Importantes al Calcular el Volumen Atómico
Aunque la fórmula parece sencilla, su aplicación requiere algunas consideraciones específicas para garantizar la precisión:
- Elementos Gaseosos: Para elementos que son gases a temperatura y presión ambiente, la densidad utilizada en el cálculo debe ser la de su estado líquido en el punto de ebullición. Esto se debe a que la densidad de un gas es muy baja y depende en gran medida de las condiciones de presión y temperatura, lo que no reflejaría el volumen intrínseco de los átomos.
- Sólidos con Estructuras Moleculares Alotrópicas: Algunos elementos, como el azufre, pueden existir en diferentes formas alotrópicas (con la misma composición, pero diferente disposición de los átomos). En estos casos, para el cálculo del volumen atómico, se elige la densidad de la forma alotrópica más estable en condiciones estándar.
- Sólidos con Estructuras Cristalinas Alotrópicas: Similar a los alotropos moleculares, los sólidos con diferentes estructuras cristalinas (como el carbono en grafito o diamante) requieren una elección. Se utiliza la densidad de la forma que posee un número de coordinación 6, que es un arreglo común y representativo.
Estas consideraciones son vitales para obtener valores de volumen atómico que sean comparables y significativos dentro de la tabla periódica.
Tendencias del Volumen Atómico en la Tabla Periódica
El volumen atómico no es una propiedad estática; muestra claras tendencias periódicas a lo largo de la tabla. Estas tendencias son fundamentales para entender el comportamiento químico de los elementos.
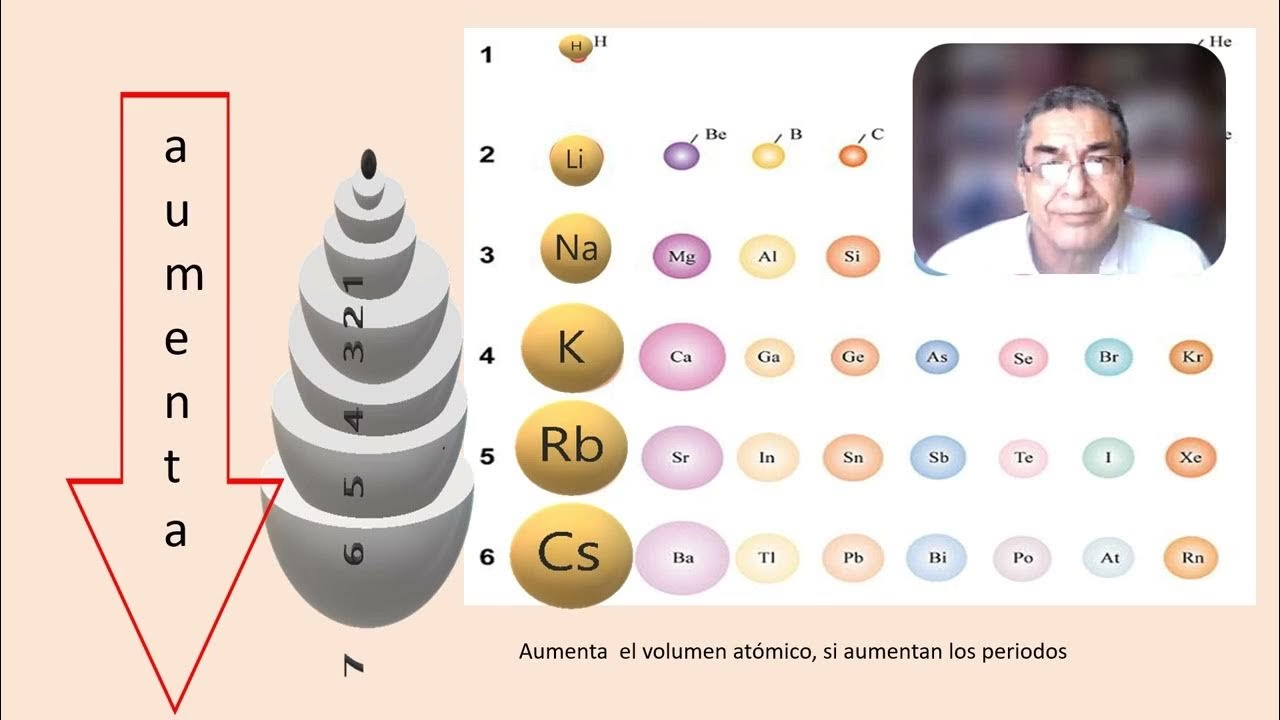
A lo Largo de un Grupo (Verticalmente)
Generalmente, el volumen atómico aumenta con el número atómico a medida que descendemos en un mismo grupo de la tabla periódica. Esto se debe a que, al bajar en un grupo, se añaden capas electrónicas adicionales al átomo, lo que hace que el radio atómico (y por ende, el volumen) sea mayor. Por ejemplo, el volumen atómico del potasio será mayor que el del sodio, y el del rubidio mayor que el del potasio, y así sucesivamente.

Los grupos con mayor volumen atómico suelen ser los metales alcalinos (del bloque s), seguidos por los no metales, y finalmente los metales de transición, que tienden a tener volúmenes atómicos más pequeños debido a la contracción de los electrones d.
A lo Largo de un Periodo (Horizontalmente)
En un periodo, la tendencia es generalmente opuesta: el volumen atómico disminuye hacia la derecha de la tabla periódica. Esto ocurre porque, a medida que avanzamos hacia la derecha en un periodo, el número de protones en el núcleo aumenta, lo que incrementa la carga nuclear efectiva. Esta mayor carga atrae con más fuerza a los electrones de la capa más externa hacia el núcleo, reduciendo el tamaño del átomo. Aunque se añaden más electrones, se añaden a la misma capa principal, y el efecto de la carga nuclear es dominante.
Existen, sin embargo, algunas excepciones notables a esta tendencia. Por ejemplo, en los elementos cobre (Cu), zinc (Zn) y galio (Ga), el volumen atómico muestra un ligero aumento en lugar de una disminución continua. Estas anomalías pueden atribuirse a las complejidades en el llenado de los orbitales d y a las interacciones electrónicas.
El estudio de estas tendencias ha sido crucial en el desarrollo de la química. Lothar Meyer, un contemporáneo de Dmitri Mendeléyev, fue uno de los primeros en graficar el volumen atómico frente al número atómico, revelando las claras periodicidades que ayudaron a establecer la base de la tabla periódica moderna. Las curvas de volumen atómico muestran picos pronunciados en los metales alcalinos (Li, Na, K, Rb, Cs), que tienen los volúmenes atómicos más grandes en sus respectivos periodos, y valles en los elementos cerca del centro de cada periodo, como B, C; Al, Si; y los metales de transición.
Calculando el Volumen de un Átomo Individual: Más Allá de la Fórmula
Mientras que el volumen atómico nos da una medida molar, surge la pregunta de cómo determinar el volumen de un solo átomo. Aquí es donde los experimentos y los cálculos basados en propiedades macroscópicas y el Número de Avogadro entran en juego. Un enfoque común implica el uso de un objeto de metal puro, como una barra de aluminio (Al), y aplicar una serie de mediciones y cálculos.

El principio es simple: si podemos determinar el volumen total de un objeto macroscópico hecho de un elemento puro y luego calcular cuántos átomos individuales contiene ese objeto, podemos dividir el volumen total por el número de átomos para obtener el volumen de un solo átomo.
Pasos para Determinar el Volumen y el Radio de un Átomo de Aluminio (Ejemplo Experimental)
Este proceso es un excelente ejemplo de cómo la química conecta el mundo macroscópico con el subatómico:
- Medición Macroscópica: Se mide con precisión las dimensiones de la barra de aluminio (por ejemplo, diámetro y longitud si es cilíndrica) y su masa.
- Cálculo del Volumen Total del Objeto: Utilizando las dimensiones medidas, se calcula el volumen total del objeto. Para una barra cilíndrica, se usaría la fórmula del volumen de un cilindro:
Volumen = π * (radio)² * Longitud
- Determinación de la Densidad Experimental: Con la masa medida y el volumen calculado, se puede determinar la densidad experimental de la barra (Densidad = Masa / Volumen). Esta se puede comparar con la densidad teórica conocida del aluminio (aproximadamente 2.702 g/cm³) para verificar la precisión.
- Cálculo del Número de Átomos: Este es un paso crucial. Se usa la masa medida de la barra y la masa molar del aluminio para encontrar el número de moles. Luego, se multiplica el número de moles por el Número de Avogadro (6.022 x 1023 átomos/mol) para obtener el número total de átomos en la barra.
- Volumen de un Átomo Individual: Se divide el volumen total de la barra (calculado en el paso 2) por el número total de átomos (calculado en el paso 4). Este resultado es el volumen de un solo átomo de aluminio.
- Cálculo del Radio Atómico: Asumiendo que un átomo es una esfera (una simplificación común y útil), se puede usar la fórmula del volumen de una esfera (V = 4/3 π r³) para despejar el radio (r). La fórmula para el radio sería:
Radio = ³√[(3 * Volumen del Átomo) / (4 * π)]
Es importante señalar que también se puede calcular el volumen de la barra de aluminio usando su masa medida y la densidad teórica conocida (Volumen = Masa / Densidad). Este método es particularmente útil para objetos de forma irregular, como una pepita de oro, donde las dimensiones directas son difíciles de medir. Los pasos subsiguientes para determinar el volumen y el radio de un átomo individual serían los mismos.
Aplicación a Moléculas: El Caso de la Glucosa
El mismo principio puede aplicarse para estimar el tamaño de moléculas. Por ejemplo, para determinar el radio promedio de una molécula de glucosa (C6H12O6), que es el componente principal de la celulosa en el papel, se seguirían pasos análogos:
- Medir las dimensiones (largo, ancho, espesor) de una hoja de papel para calcular su volumen total.
- Pesar la hoja de papel.
- Usar la masa molar de la glucosa (180 g/mol) y el Número de Avogadro para determinar el número de moléculas de glucosa en la hoja de papel.
- Dividir el volumen total del papel por el número de moléculas para obtener el volumen de una sola molécula de glucosa.
- Calcular el radio de una molécula de glucosa a partir de su volumen, asumiéndola como una esfera.
Estos experimentos demuestran la ingeniosidad de la química para desvelar propiedades a escalas inalcanzables a simple vista, utilizando propiedades medibles a gran escala.
Fórmulas Útiles para Cálculos de Volumen Atómico y Molecular
Para facilitar la comprensión, aquí hay un resumen de las fórmulas clave mencionadas:
| Concepto | Fórmula | Notas |
|---|---|---|
| Volumen Atómico (Molar) | Va = M / ρ | M = Masa Atómica; ρ = Densidad del elemento |
| Volumen de un Cilindro | V = π * r² * L | r = radio; L = longitud (para barras cilíndricas) |
| Volumen de una Esfera | V = 4/3 * π * r³ | r = radio (modelo simplificado para átomos/moléculas) |
| Número de Moles | n = masa / masa molar | |
| Número de Átomos/Moléculas | N = n * NA | n = número de moles; NA = Número de Avogadro (6.022 x 1023) |
| Radio de una Esfera (despejado) | r = ³√[(3 * V) / (4 * π)] | V = volumen de la esfera (átomo o molécula) |
Preguntas Frecuentes (FAQ) sobre el Volumen Atómico
¿Es el volumen de un átomo realmente esférico?
No, los átomos no son esferas sólidas perfectas con un límite definido. Su volumen está determinado por la distribución de sus nubes electrónicas, que son probabilísticas y no tienen un borde nítido. Sin embargo, para propósitos de cálculo y para entender las tendencias de tamaño, modelar un átomo como una esfera es una aproximación muy útil y ampliamente aceptada. El radio atómico se define a menudo como la mitad de la distancia entre los núcleos de dos átomos idénticos enlazados.

¿Por qué el volumen atómico no siempre aumenta con el número atómico en un periodo?
Aunque la regla general es una disminución del volumen atómico a lo largo de un periodo debido al aumento de la carga nuclear efectiva, existen excepciones. Los casos del cobre, zinc y galio son ejemplos donde la contracción de los orbitales d llenos y las interacciones electrónicas pueden llevar a un ligero aumento en el volumen. Estas desviaciones demuestran la complejidad de las interacciones cuánticas dentro de los átomos.
¿Cómo se relaciona el volumen atómico con otras propiedades periódicas?
El volumen atómico está estrechamente relacionado con otras propiedades periódicas. Por ejemplo, está inversamente relacionado con la densidad de los elementos en estado sólido (a mayor volumen atómico, menor densidad, y viceversa). También influye en propiedades como la energía de ionización (los átomos más grandes suelen tener energías de ionización más bajas porque sus electrones más externos están menos fuertemente unidos al núcleo) y la electronegatividad (los átomos más pequeños tienden a ser más electronegativos porque sus núcleos ejercen una mayor atracción sobre los electrones de enlace).
¿Por qué se usan densidades de líquidos para gases en el cálculo del volumen atómico?
Las densidades de los gases son extremadamente bajas y varían significativamente con la temperatura y la presión, ya que las partículas de gas están muy separadas. Si usáramos la densidad de un gas, el volumen atómico calculado sería engañosamente grande y no representaría el volumen intrínseco de los átomos en un estado más condensado. Al usar la densidad del líquido en el punto de ebullición, obtenemos una medida que refleja mejor el volumen que ocupan los átomos cuando están más juntos, aunque no estén en una red sólida. Esto permite una comparación más justa con los elementos sólidos y líquidos.
Conclusión
El cálculo del volumen de un átomo, ya sea a nivel molar o individual, es un testimonio de la capacidad humana para entender el universo a escalas que van más allá de nuestra percepción directa. Desde la sencilla relación de masa atómica y densidad para el volumen atómico hasta los complejos experimentos que utilizan el Número de Avogadro para desvelar el tamaño de un átomo único, cada método contribuye a nuestro conocimiento fundamental de la materia. Comprender cómo se mide y qué factores influyen en el tamaño de los átomos no solo es un ejercicio académico, sino una piedra angular para entender la periodicidad química y las propiedades de todos los elementos que nos rodean.
Si quieres conocer otros artículos parecidos a ¿Cómo se Calcula el Volumen de un Átomo? puedes visitar la categoría Química.