15/02/2024
En el vasto universo de la termodinámica, la entalpía emerge como uno de los conceptos más fundamentales y, a menudo, más intrigantes. Es una función de estado que nos permite cuantificar la energía total de un sistema, especialmente cuando consideramos los procesos que ocurren a presión constante, una condición muy común en la naturaleza y en los laboratorios. Desde la combustión de un combustible hasta las reacciones químicas que sustentan la vida, la variación de entalpía es la métrica que nos revela si un proceso libera o absorbe energía en forma de calor y trabajo.
- ¿Qué es la Entalpía y por Qué es Tan Crucial?
- ¿Cuándo Varía la Entalpía?
- ¿Qué Nos Permite Calcular la Entalpía?
- ¿Cómo se Calcula la Variación de Entalpía?
- ¿Por Qué el Cambio de Entalpía Calculado Usando Entalpías de Enlace a Menudo es Diferente del Cambio de Entalpía Estándar que se Encuentra en los Libros de Datos?
- Tabla Comparativa de Variaciones de Entalpía
- Preguntas Frecuentes sobre la Entalpía
- Conclusión
¿Qué es la Entalpía y por Qué es Tan Crucial?
La entalpía, simbolizada comúnmente como H, es una propiedad termodinámica que representa el contenido total de calor de un sistema a presión constante. Se define matemáticamente como la suma de la energía interna (U) del sistema y el producto de su presión (P) y volumen (V). Es decir:
H = U + PV
Esta definición es crucial porque encapsula no solo la energía interna del sistema (la suma de las energías cinética y potencial de sus partículas), sino también la energía asociada con el trabajo de expansión o compresión (PV) que el sistema puede realizar o que se puede realizar sobre él a presión constante. La entalpía se mide en unidades de energía, como julios (J) en el Sistema Internacional, o kilocalorías (kcal) y BTU en otros sistemas.
La Entalpía como Función de Estado
Una de las características más importantes de la entalpía es que es una función de estado. Esto significa que su valor solo depende del estado actual del sistema (es decir, de sus propiedades como la temperatura, la presión y la composición), y no de la trayectoria que el sistema siguió para llegar a ese estado. Esta propiedad simplifica enormemente los cálculos, ya que no necesitamos conocer los detalles de un proceso para determinar su cambio de entalpía; solo necesitamos los estados inicial y final.
Además, la entalpía es una propiedad extensiva, lo que significa que es proporcional al tamaño o la cantidad de sustancia en el sistema. Para facilitar la comparación entre diferentes sistemas, a menudo se utilizan propiedades intensivas como la entalpía específica (h = H/m, entalpía por unidad de masa) o la entalpía molar (Hm = H/n, entalpía por mol).
¿Cuándo Varía la Entalpía?
La entalpía de un sistema varía cuando hay un cambio en su energía interna, volumen o presión. Sin embargo, la mayor utilidad de la entalpía radica en su capacidad para describir los cambios de energía en procesos que ocurren a presión constante. En estas condiciones, la variación de entalpía (ΔH) se convierte en una medida directa del calor intercambiado entre el sistema y su entorno.
Procesos a Presión Constante: La Clave de la Entalpía
Consideremos un proceso infinitesimal para un sistema cerrado. La primera ley de la termodinámica establece que: dU = δQ - δW, donde δQ es el calor añadido y δW es el trabajo realizado. Si el único trabajo es el de expansión-compresión (δW = PdV) y el proceso es reversible (δQ = TdS), entonces dU = TdS - PdV. Si ahora diferenciamos la entalpía (H = U + PV), obtenemos: dH = dU + PdV + VdP. Sustituyendo dU:
dH = (TdS - PdV) + PdV + VdP
Simplificando, llegamos a la expresión fundamental de la variación de entalpía:
dH = TdS + VdP
Esta ecuación es vital. Si el proceso ocurre a presión constante (dP = 0), la expresión se simplifica a:
dH = TdS
Para un proceso reversible, TdS es igual al calor intercambiado (δQ). Por lo tanto, en un proceso reversible a presión constante, la variación de entalpía es directamente igual al calor absorbido o liberado por el sistema. Esta es la razón por la que la entalpía es tan útil para analizar reacciones químicas, que a menudo se llevan a cabo en condiciones de presión constante (por ejemplo, en un vaso de precipitados abierto a la atmósfera).
Variaciones de Entalpía en Reacciones Químicas
En el contexto de las reacciones químicas, la variación de entalpía (ΔH) nos indica si una reacción es exotérmica o endotérmica:
- Reacciones Exotérmicas: Liberan energía al entorno en forma de calor. Para estas reacciones, la variación de entalpía del sistema es negativa (ΔH < 0). Un ejemplo clásico es la combustión.
- Reacciones Endotérmicas: Absorben energía del entorno en forma de calor. Para estas reacciones, la variación de entalpía del sistema es positiva (ΔH > 0). Un ejemplo es la disolución de ciertas sales en agua que enfría la solución.
Entalpía Estándar de Combustión (ΔH°comb)
La variación de la entalpía estándar de combustión es un caso específico y muy importante. Se refiere a la variación de la entalpía cuando un mol de una sustancia reacciona completamente con oxígeno bajo condiciones estándar (presión de 1 bar o 1 atm, y una temperatura específica, comúnmente 25 °C o 298.15 K). Por definición, las reacciones de combustión son siempre exotérmicas, lo que significa que sus entalpías de combustión son siempre negativas. Estos valores se denotan comúnmente como ΔH°comb o ΔH°c. La medición de estas entalpías se realiza típicamente con una bomba de calorimetría, un dispositivo que permite medir con precisión el calor liberado en una reacción a volumen constante, que luego se ajusta a presión constante para obtener la entalpía.
Entalpía Estándar de Formación (ΔH°f)
La entalpía estándar de formación es la variación de entalpía cuando un mol de una sustancia se forma a partir de sus elementos constituyentes en sus estados estándar más estables. Por definición, la entalpía estándar de formación de un elemento en su estado más estable (por ejemplo, O2 gaseoso, C grafito, H2 gaseoso) es cero. Estos valores son fundamentales porque permiten calcular la entalpía de cualquier reacción química.
¿Qué Nos Permite Calcular la Entalpía?
La entalpía es una herramienta poderosa que nos permite realizar una amplia gama de cálculos y predicciones en termodinámica y química:
1. Cuantificar el Calor de Reacción
Como ya se mencionó, la aplicación más directa de la entalpía es la determinación del calor liberado o absorbido en reacciones químicas a presión constante. La variación de entalpía de una reacción (ΔrH) se calcula a partir de las entalpías de formación de los productos y los reactivos, ponderadas por sus coeficientes estequiométricos (n):
ΔrH = ∑p npΔfHp - ∑r nrΔfHr
Donde np y nr son los coeficientes estequiométricos de los productos y reactivos, y ΔfHp y ΔfHr son sus respectivas entalpías de formación.
2. Predecir la Espontaneidad de Procesos (en Combinación con la Entropía)
Aunque la entalpía por sí sola no determina la espontaneidad de un proceso, es un componente clave de la energía libre de Gibbs (ΔG = ΔH - TΔS), que sí lo hace. Un proceso es espontáneo a temperatura y presión constantes si ΔG < 0. Por lo tanto, el cálculo de ΔH es un paso esencial para predecir la viabilidad de una reacción o proceso.
3. Analizar Ciclos Termodinámicos
En ingeniería, especialmente en el estudio de motores y refrigeradores, la entalpía se utiliza extensamente para analizar ciclos termodinámicos como el ciclo Rankine o el ciclo Brayton. Permite agrupar los términos de presión y energía interna de forma compacta, simplificando los balances de energía.
4. Relacionar Cambios de Temperatura con la Capacidad Calorífica
Para una sustancia que sufre un cambio de temperatura a presión constante, la variación de entalpía se puede calcular utilizando la capacidad calorífica a presión constante (Cp):
h2 - h1 = Cp(T2 - T1)
Esta fórmula es válida siempre y cuando Cp sea constante en el intervalo de temperatura considerado. Para casos más generales o cuando la presión también varía, se utiliza la expresión diferencial:
dH = Cp dT + V(1 - αT) dp
Donde α es el coeficiente de expansión térmica. Esta expresión permite determinar la entalpía si se conocen Cp y V como funciones de p y T.

5. Principio de Mínima Entalpía
El segundo principio de la termodinámica establece que un sistema en equilibrio alcanzará un estado de entropía máxima. En la representación entálpica, este principio se traduce en el principio de mínima entalpía: un sistema alcanzará el estado de equilibrio cuando, para una presión dada, la entalpía del sistema sea la mínima posible.
¿Cómo se Calcula la Variación de Entalpía?
La variación de entalpía (ΔH) de un sistema se calcula como la diferencia entre la entalpía final y la entalpía inicial del sistema:
ΔH = Hfinal - Hinicial
Como la entalpía total de un sistema no puede medirse directamente, se recurre a métodos experimentales y cálculos basados en valores tabulados:
1. Calorimetría
La calorimetría es el método experimental más común para medir los cambios de entalpía. Implica medir el cambio de temperatura (ΔT) de un sistema o de su entorno (generalmente agua) cuando ocurre una reacción. La cantidad de calor (q) transferida se calcula con la fórmula:
q = C · ΔT = m · c · ΔT
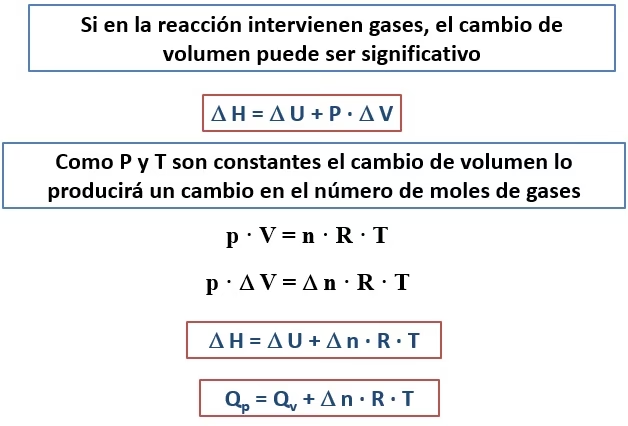
Donde C es la capacidad calorífica del calorímetro, m es la masa de la sustancia (usualmente agua), y c es el calor específico. Si la reacción se lleva a cabo a presión constante (por ejemplo, en un calorímetro de vaso de café), entonces q = ΔH. Si se realiza a volumen constante (como en una bomba calorimétrica), se mide el cambio de energía interna (ΔU), que luego se convierte a ΔH usando ΔH = ΔU + Δ(PV).
2. Usando Entalpías Estándar de Formación
Este es el método de cálculo más utilizado para reacciones químicas. Se basa en la ley de Hess, que establece que la variación de entalpía de una reacción es independiente de la ruta tomada, siempre que los estados inicial y final sean los mismos. Utilizando los valores tabulados de las entalpías estándar de formación (ΔH°f) para reactivos y productos, se aplica la fórmula:
ΔrH = ∑p npΔfHp - ∑r nrΔfHr
3. Usando Entalpías de Enlace Medias
Para estimar la variación de entalpía de una reacción, especialmente cuando no se dispone de las entalpías de formación, se pueden utilizar las entalpías de enlace medias. Este método implica calcular la energía necesaria para romper todos los enlaces en los reactivos y la energía liberada al formar nuevos enlaces en los productos. La variación de entalpía se estima como:
ΔH ≈ ∑ (energía de enlaces rotos) - ∑ (energía de enlaces formados)
Es una excelente pregunta que resalta una distinción importante entre los valores teóricos y experimentales. Cuando calculamos los cambios de entalpía utilizando entalpías de enlace, estamos empleando valores promedio.
Las entalpías de enlace son la energía requerida para romper un mol de un tipo específico de enlace en una molécula gaseosa. Sin embargo, el valor exacto de la energía de un enlace particular (por ejemplo, C-H) puede variar ligeramente dependiendo de la molécula específica en la que se encuentre ese enlace y de su entorno químico. Por ejemplo, la energía del enlace C-H en el metano (CH4) no es idéntica a la del enlace C-H en el etano (C2H6), aunque sean el mismo tipo de enlace.
Los valores de entalpía de enlace que se encuentran en los libros de datos son, por lo tanto, promedios obtenidos de una gran cantidad de compuestos diferentes. Son útiles para estimaciones rápidas y para comprender la energía involucrada en la formación y ruptura de enlaces, pero no son exactos para una reacción específica. En contraste, las entalpías estándar de formación (ΔH°f) y, por ende, los ΔH° de reacción calculados a partir de ellas, son valores determinados experimentalmente para compuestos específicos bajo condiciones estándar, lo que los hace mucho más precisos. Por ello, es común que haya una pequeña discrepancia entre los valores calculados con entalpías de enlace medias y los valores estándar tabulados.
Tabla Comparativa de Variaciones de Entalpía
Para clarificar los diferentes tipos de variaciones de entalpía discutidos, aquí se presenta una tabla comparativa:
| Tipo de Variación de Entalpía | Símbolo | Descripción | Características Clave | Signo Común (Exo/Endo) |
|---|---|---|---|---|
| Entalpía de Reacción Estándar | ΔrH° | Cambio de entalpía para una reacción química bajo condiciones estándar. | Calculado a partir de ΔH°f de productos y reactivos. | Puede ser positivo (endotérmica) o negativo (exotérmica). |
| Entalpía Estándar de Formación | ΔH°f | Cambio de entalpía cuando un mol de una sustancia se forma a partir de sus elementos en estado estándar. | ΔH°f de elementos en su estado estándar = 0. | Puede ser positivo o negativo. |
| Entalpía Estándar de Combustión | ΔH°comb | Cambio de entalpía cuando un mol de una sustancia reacciona completamente con oxígeno. | Siempre exotérmica (libera calor). | Siempre negativo. |
| Entalpía de Enlace Media | (Valor promedio) | Energía requerida para romper un mol de un tipo específico de enlace en fase gaseosa. | Valores promedio, no exactos para cada molécula. | Siempre positivo (energía absorbida para romper). |
Preguntas Frecuentes sobre la Entalpía
¿Es la entalpía lo mismo que el calor?
No exactamente. La entalpía (H) es una función de estado que representa la energía total de un sistema a presión constante. La variación de entalpía (ΔH) es igual al calor (q) intercambiado por el sistema, pero solo cuando el proceso ocurre a presión constante y, preferiblemente, de manera reversible. En otras condiciones (por ejemplo, a volumen constante), el calor intercambiado sería igual a la variación de la energía interna (ΔU).
¿Por qué la entalpía de combustión siempre es negativa?
La combustión es una reacción química que libera una gran cantidad de energía, generalmente en forma de calor y luz. Esto significa que la energía de los productos de la combustión es menor que la de los reactivos iniciales. Por definición, cuando un sistema libera energía al entorno, su variación de entalpía es negativa, indicando un proceso exotérmico.
¿Cómo se mide la entalpía experimentalmente?
La entalpía no se mide directamente, sino su variación (ΔH). Esto se hace a través de la calorimetría. Un calorímetro mide el calor liberado o absorbido por una reacción al observar el cambio de temperatura de una masa conocida de agua o de los componentes del calorímetro. Este calor medido, a presión constante, es igual a ΔH.
¿Qué significa que la entalpía es una función de estado?
Significa que el valor de la entalpía de un sistema solo depende de su estado actual (definido por su temperatura, presión, volumen y composición), y no de cómo llegó a ese estado. Esto es muy útil porque permite calcular los cambios de entalpía de un proceso basándose únicamente en los valores de entalpía inicial y final, sin importar los pasos intermedios.
¿Puede la entalpía ser cero?
La entalpía absoluta de un sistema no puede ser medida o definida de forma absoluta. Sin embargo, las variaciones de entalpía (ΔH) sí pueden ser cero si no hay intercambio neto de calor o trabajo PV a presión constante. Además, por convención, la entalpía estándar de formación de un elemento en su estado más estable a 25 °C y 1 bar de presión se define como cero, lo que sirve como punto de referencia para los cálculos.
Conclusión
La entalpía es un pilar fundamental en la termodinámica, proporcionando una comprensión profunda de cómo la energía se transforma y se intercambia en los sistemas. Su importancia radica en su capacidad para cuantificar el calor de reacción a presión constante, lo que es invaluable en campos tan diversos como la química, la biología, la ingeniería y la meteorología. Comprender cuándo y cómo varía la entalpía, y las herramientas para calcularla, nos empodera para predecir el comportamiento de los sistemas y diseñar procesos más eficientes, haciendo de esta función de estado una de las más aplicadas en la ciencia y la tecnología modernas.
Si quieres conocer otros artículos parecidos a Entalpía: Comprende la Energía en tus Cálculos puedes visitar la categoría Cálculos.
