02/09/2022
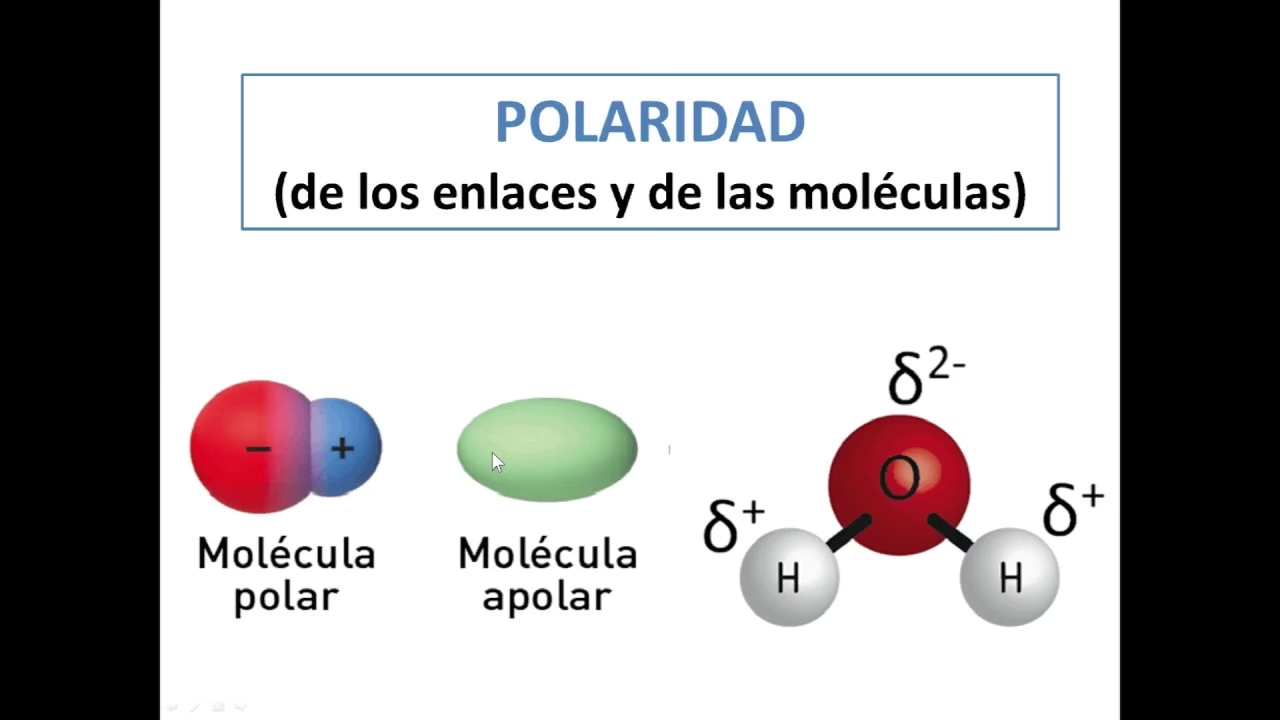
La polaridad molecular es un concepto fundamental en la química que nos ayuda a entender por qué las sustancias interactúan de la manera en que lo hacen. Desde la disolución de la sal en agua hasta la función de las membranas celulares en nuestro cuerpo, la polaridad juega un papel crucial. En esencia, se refiere a la distribución desigual de la carga eléctrica dentro de una molécula, lo que crea regiones con cargas parciales positivas y negativas, transformando a la molécula en un pequeño imán con polos. Esta propiedad inherente a la estructura de las moléculas determina gran parte de sus características físicas y químicas, incluyendo su solubilidad, puntos de ebullición y reactividad. Comprender cómo se mide y determina la polaridad es, por tanto, una puerta de entrada para desentrañar muchos de los misterios del comportamiento de la materia.
- Fundamentos de la Polaridad: Electronegatividad y Enlaces
- Polaridad de las Moléculas: La Geometría es Clave
- Moléculas Polares: Ejemplos y Características
- Moléculas No Polares: Ejemplos y Características
- Moléculas Anfifílicas: Un Mundo de Dos Caras
- Cómo Predecir la Polaridad Molecular
- Mitos Comunes sobre la Polaridad del Agua
- Preguntas Frecuentes sobre la Polaridad Molecular
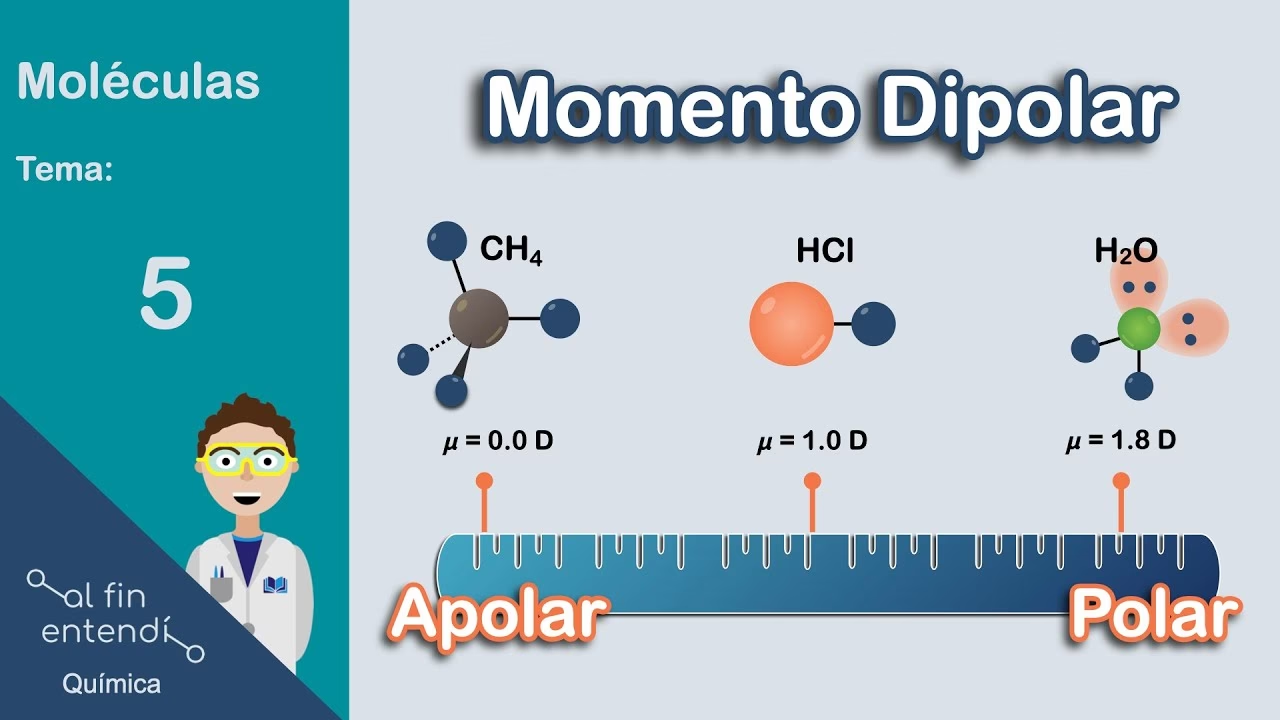
- ¿Qué es el momento dipolar?
- ¿Por qué la polaridad es importante en la vida cotidiana?
- ¿Puede una molécula tener enlaces polares pero ser no polar en general?
- ¿Siempre que hay un par de electrones no compartidos en el átomo central, la molécula es polar?
- ¿Cómo puedo saber la electronegatividad de un átomo?
- ¿La polaridad afecta el punto de ebullición de una sustancia?
Fundamentos de la Polaridad: Electronegatividad y Enlaces
Para comprender la polaridad de una molécula en su conjunto, primero debemos entender la polaridad de los enlaces individuales que la componen. La polaridad de un enlace químico es el resultado de la diferencia de electronegatividad entre los átomos que lo forman. La electronegatividad es la capacidad de un átomo para atraer hacia sí los electrones compartidos en un enlace covalente.
Cuando dos átomos con electronegatividades diferentes se unen, el átomo más electronegativo atrae los electrones del enlace con mayor fuerza, lo que provoca una distribución desigual de la densidad electrónica. Esto significa que el átomo más electronegativo adquiere una carga parcial negativa (δ-), mientras que el átomo menos electronegativo adquiere una carga parcial positiva (δ+). Este tipo de enlace se conoce como enlace covalente polar. Por ejemplo, en el fluoruro de hidrógeno (HF), el flúor es mucho más electronegativo que el hidrógeno. Como resultado, los electrones compartidos en el enlace H-F se desplazan hacia el flúor, haciendo que el flúor sea ligeramente negativo y el hidrógeno ligeramente positivo.
Por el contrario, si los dos átomos tienen electronegatividades muy similares o idénticas (como en una molécula diatómica de un solo elemento, por ejemplo, O₂ o N₂), los electrones se comparten de manera equitativa. En este caso, no hay separación de cargas y el enlace se considera no polar.
Polaridad de las Moléculas: La Geometría es Clave
La polaridad de una molécula no solo depende de la polaridad de sus enlaces, sino también, y de manera crucial, de su geometría molecular. Los momentos dipolares de los enlaces son cantidades vectoriales, lo que significa que tienen tanto magnitud (la fuerza de la polaridad) como dirección (hacia dónde se desplaza la carga negativa). Para determinar si una molécula es polar, debemos sumar vectorialmente todos los momentos dipolares de sus enlaces.
Si los momentos dipolares individuales de los enlaces se cancelan mutuamente debido a una disposición simétrica, la molécula en su conjunto será no polar, incluso si contiene enlaces polares. Sin embargo, si los momentos dipolares de los enlaces no se cancelan, la molécula tendrá un momento dipolo neto y será considerada polar. La teoría de Repulsión de Pares de Electrones de la Capa de Valencia (VSEPR) es una herramienta invaluable para predecir la geometría molecular y, por ende, la polaridad.
Moléculas Polares: Ejemplos y Características
Una molécula Polar es aquella que posee un momento dipolar neto, lo que significa que tiene un extremo ligeramente positivo y otro ligeramente negativo. Esta asimetría en la distribución de la carga es lo que les confiere sus propiedades distintivas.
El Agua (H₂O): El Solvente Universal
El agua es, quizás, el ejemplo más conocido de una molécula polar. Está compuesta por un átomo de oxígeno y dos de hidrógeno. La electronegatividad del oxígeno (3.44) es significativamente mayor que la del hidrógeno (2.20), lo que polariza cada enlace H-O, desplazando los electrones hacia el oxígeno. Además, la molécula de agua tiene una geometría angular (doblada) debido a la presencia de dos pares de electrones no compartidos en el átomo de oxígeno central. Debido a esta geometría no lineal, los momentos dipolares de los dos enlaces O-H no se cancelan. En cambio, se suman vectorialmente, dando como resultado un momento dipolar neto considerable que apunta hacia el átomo de oxígeno. Esta polaridad es la razón por la que el agua es un excelente solvente para muchas sustancias iónicas y polares, formando puentes de hidrógeno que son vitales para la vida. El momento dipolar del agua varía ligeramente con su estado: aproximadamente 1.86 debye (D) en fase gaseosa, 2.95 D en estado líquido y 3.09 D en hielo, debido a las interacciones de puentes de hidrógeno.
Fluoruro de Hidrógeno (HF): Un Dipolo Sencillo
Como se mencionó anteriormente, el HF es una molécula diatómica con un enlace covalente polar. La gran diferencia de electronegatividad entre el flúor y el hidrógeno crea un dipolo claro, con el flúor siendo el extremo negativo y el hidrógeno el positivo.
Amoníaco (NH₃): La Influencia de los Pares Solitarios
La molécula de amoníaco (NH₃) es otro ejemplo de molécula polar. Aunque los enlaces N-H tienen una polaridad moderada (hacia el nitrógeno más electronegativo), la geometría molecular del amoníaco es piramidal trigonal, no plana. Esto se debe a que el átomo de nitrógeno central tiene un par de electrones no compartidos. Este par solitario ejerce una fuerte repulsión sobre los pares de electrones enlazantes, distorsionando la geometría y evitando que los momentos dipolares de los enlaces N-H se cancelen. El resultado es un momento dipolar neto significativo a través de toda la molécula de amoníaco.
Otras Moléculas Polares
- Azúcares (como la sacarosa): Estas moléculas suelen tener muchos grupos hidroxilo (-OH) polares, lo que las hace altamente polares en general.
- Clorometano (CH₃Cl): Aunque el metano (CH₄) es no polar, la sustitución de un hidrógeno por un átomo de cloro (mucho más electronegativo) rompe la simetría tetraédrica, creando un momento dipolar neto.
Moléculas No Polares: Ejemplos y Características
Una molécula es No Polar cuando no tiene un momento dipolar neto. Esto puede ocurrir de dos maneras principales:
Compartición Equitativa de Electrones
En moléculas diatómicas compuestas por el mismo elemento, como el oxígeno (O₂) o el nitrógeno (N₂), los dos átomos tienen la misma electronegatividad. Por lo tanto, los electrones se comparten por igual, y no hay polaridad en el enlace ni en la molécula.
Disposición Simétrica de Enlaces Polares
Esta es la situación más interesante. Una molécula puede contener enlaces individuales que son polares, pero si estos enlaces están dispuestos de manera perfectamente simétrica alrededor de un átomo central, sus momentos dipolares se cancelarán mutuamente, resultando en una molécula no polar.
Dióxido de Carbono (CO₂): La Geometría Lineal
El dióxido de carbono es un ejemplo clásico. Tiene dos enlaces C=O, y el oxígeno es más electronegativo que el carbono, por lo que cada enlace C=O es polar. Sin embargo, la molécula de CO₂ tiene una geometría lineal. Los dos momentos dipolares de los enlaces C=O son iguales en magnitud y apuntan en direcciones opuestas (180° entre sí). Como resultado, se cancelan perfectamente, y la molécula de CO₂ es no polar.
Trifluoruro de Boro (BF₃): La Geometría Plana Trigonal
En el BF₃, hay tres enlaces B-F polares. El flúor es más electronegativo que el boro. Sin embargo, la molécula tiene una geometría trigonal plana, con los tres enlaces B-F espaciados uniformemente a 120° entre sí. Debido a esta disposición simétrica, los momentos dipolares de los enlaces se cancelan, haciendo que el BF₃ sea una molécula no polar.
Metano (CH₄): La Geometría Tetraédrica
El metano tiene cuatro enlaces C-H. Aunque estos enlaces tienen una polaridad muy ligera (el carbono es ligeramente más electronegativo que el hidrógeno), la molécula de metano tiene una geometría tetraédrica altamente simétrica. Los cuatro enlaces están dispuestos de tal manera que sus momentos dipolares se cancelan entre sí, resultando en una molécula no polar.
Ejemplos Cotidianos de Compuestos No Polares
Muchos compuestos orgánicos, especialmente los hidrocarburos puros como las grasas, los aceites y la gasolina, son no polares. Su naturaleza no polar explica por qué no se mezclan con el agua (una molécula polar), un principio conocido como "lo similar disuelve a lo similar".
Moléculas Anfifílicas: Un Mundo de Dos Caras
Existen moléculas grandes que presentan una característica muy peculiar: tienen una parte con grupos polares y otra con grupos no polares. Estas moléculas se denominan anfifílicas (o anfipáticas). Son increíblemente importantes en la biología y la industria debido a sus propiedades como surfactantes (o tensioactivos).
Los surfactantes son sustancias que reducen la tensión superficial o interfacial entre dos líquidos inmiscibles, como el aceite y el agua. Lo logran adsorbiéndose en la interfaz líquido-líquido. La parte polar de la molécula anfifílica es "hidrofílica" (amante del agua), mientras que la parte no polar es "hidrofóbica" (que repele el agua) o "lipofílica" (amante de las grasas).
Un ejemplo clásico de la acción de un surfactante es la formación de una micela. Cuando los surfactantes se mezclan con aceite y agua, las colas lipofílicas de las moléculas de surfactante se disuelven en las gotas de aceite, mientras que las cabezas hidrofílicas cargadas permanecen fuera, en la fase acuosa. De esta manera, las pequeñas gotas de aceite se vuelven "solubles" en agua, formando una emulsión estable.
Los fosfolípidos son surfactantes naturales muy efectivos y tienen funciones biológicas vitales. Son los componentes principales de las membranas celulares, donde forman una bicapa lipídica que separa el interior de la célula del exterior, controlando el paso de sustancias.
Cómo Predecir la Polaridad Molecular
Predecir la polaridad de una molécula es una habilidad crucial en química. Aunque la visualización de la geometría molecular es a menudo la forma más directa, existen algunas pautas y herramientas adicionales.
- Identificar Enlaces Polares: Primero, determine si existen enlaces polares dentro de la molécula. Esto se hace comparando las electronegatividades de los átomos unidos. Si la diferencia es significativa, el enlace es polar.
- Determinar la Geometría Molecular: Utilice la teoría VSEPR para predecir la forma tridimensional de la molécula. Los pares de electrones no compartidos en el átomo central son cruciales aquí, ya que a menudo rompen la simetría.
- Evaluar la Simetría de los Momentos Dipolares:
- Si la molécula es perfectamente simétrica y todos los átomos periféricos son idénticos (como en CH₄, CO₂, BF₃), los momentos dipolares de los enlaces tienden a cancelarse, y la molécula es no polar.
- Si la molécula es asimétrica, ya sea por tener pares de electrones no compartidos en el átomo central (como en H₂O, NH₃) o por tener diferentes átomos periféricos que rompen la simetría (como en CH₃Cl), los momentos dipolares no se cancelan, y la molécula es polar.
A continuación, una tabla con algunos ejemplos comunes y su polaridad:
Tabla Comparativa de Polaridad Molecular
| Molécula | Fórmula/Estructura | Geometría Molecular | Polaridad de Enlaces | Momentos Dipolares Netos | Polaridad Molecular |
|---|---|---|---|---|---|
| Agua | H₂O | Angular/Doblada | Polar (O-H) | No se cancelan | Polar |
| Dióxido de Carbono | CO₂ | Lineal | Polar (C=O) | Se cancelan | No Polar |
| Amoníaco | NH₃ | Piramidal Trigonal | Polar (N-H) | No se cancelan | Polar |
| Metano | CH₄ | Tetraédrica | Ligeramente Polar (C-H) | Se cancelan | No Polar |
| Trifluoruro de Boro | BF₃ | Trigonal Plana | Polar (B-F) | Se cancelan | No Polar |
| Fluoruro de Hidrógeno | HF | Lineal (Diatómica) | Polar (H-F) | No hay cancelación | Polar |
| Oxígeno Diatómico | O₂ | Lineal (Diatómica) | No Polar | Cero | No Polar |
Uso de Grupos Puntuales (Más Avanzado)
Para una predicción más rigurosa, especialmente en moléculas complejas, se puede utilizar la teoría de grupos puntuales. En general, una molécula no poseerá un momento dipolar si los momentos dipolares de los enlaces individuales se anulan entre sí. Cualquier molécula con un centro de inversión ("i") o un plano de espejo horizontal ("σh") no poseerá momentos dipolares. Del mismo modo, una molécula con más de un eje de rotación Cn (simetría diedral Dn) no tendrá un momento dipolar. Por el contrario, los grupos puntuales C₁, Cs, Cn y Cnv (que no tienen centro de inversión, planos de espejo horizontales o múltiples ejes Cn) suelen tener un momento dipolar.
Mitos Comunes sobre la Polaridad del Agua
Existe una idea errónea muy difundida de que la desviación de un chorro de agua por un objeto cargado eléctricamente es una prueba directa de la polaridad del agua. Sin embargo, esta desviación no se basa directamente en la polaridad de las moléculas de agua en sí. La desviación ocurre porque el objeto cargado induce cargas eléctricas en las gotas del chorro de agua. Estas gotas, al cargarse, son atraídas o repelidas por el objeto. Un chorro de agua también puede ser desviado en un campo eléctrico uniforme, el cual no puede ejercer fuerza sobre moléculas polares neutras. Además, si un chorro de agua se conecta a tierra, ya no puede ser desviado. Incluso es posible una ligera desviación para líquidos no polares bajo ciertas condiciones. La polaridad del agua se demuestra mejor por sus propiedades de disolución y sus elevados puntos de ebullición y fusión, resultado de los fuertes puentes de hidrógeno entre sus moléculas.
Preguntas Frecuentes sobre la Polaridad Molecular
¿Qué es el momento dipolar?
El momento dipolar es una medida cuantitativa de la polaridad de una molécula. Se representa como un vector que apunta desde el centro de carga positiva hacia el centro de carga negativa. Su magnitud depende de la cantidad de carga parcial y la distancia que las separa. Se mide comúnmente en unidades de debye (D).
¿Por qué la polaridad es importante en la vida cotidiana?
La polaridad es fundamental para muchos fenómenos cotidianos. Por ejemplo:
- Solubilidad: "Lo similar disuelve a lo similar". Las sustancias polares se disuelven en solventes polares (como el agua), y las no polares en solventes no polares (como el aceite). Esto explica por qué el agua limpia la sal, pero no la grasa.
- Biología: Las membranas celulares, compuestas por fosfolípidos anfifílicos, dependen de la polaridad para su estructura y función. La forma en que las proteínas se pliegan y funcionan también está influenciada por la polaridad de sus aminoácidos.
- Cocina: La emulsificación (mezcla de líquidos inmiscibles como el aceite y el vinagre en aderezos) a menudo requiere agentes anfifílicos (como la yema de huevo en la mayonesa).
- Limpieza: Los jabones y detergentes son surfactantes que permiten que el agua disuelva y arrastre la grasa y la suciedad.
¿Puede una molécula tener enlaces polares pero ser no polar en general?
Sí, absolutamente. Este es un punto clave para entender la polaridad molecular. Si los enlaces polares están dispuestos de manera simétrica alrededor del átomo central, sus momentos dipolares individuales se cancelan vectorialmente, lo que resulta en un momento dipolar neto de cero para la molécula. Ejemplos clásicos son el dióxido de carbono (lineal), el metano (tetraédrico) y el trifluoruro de boro (trigonal planar).
¿Siempre que hay un par de electrones no compartidos en el átomo central, la molécula es polar?
En la mayoría de los casos, sí. Los pares de electrones no compartidos (pares solitarios) en el átomo central rompen la simetría de la molécula. Estos pares solitarios ocupan espacio y ejercen repulsión sobre los pares de electrones enlazantes, lo que distorsiona la geometría molecular y generalmente impide la cancelación de los momentos dipolares de los enlaces. Ejemplos claros son el agua (dos pares solitarios en el oxígeno) y el amoníaco (un par solitario en el nitrógeno). Sin embargo, hay excepciones muy específicas en moléculas con geometrías muy complejas, pero para la mayoría de los casos introductorios, esta regla es muy útil.
¿Cómo puedo saber la electronegatividad de un átomo?
La electronegatividad se puede encontrar en la tabla periódica, a menudo como un valor asignado por la escala de Pauling (u otras escalas). Generalmente, la electronegatividad aumenta de izquierda a derecha a través de un período y disminuye de arriba hacia abajo en un grupo. El flúor es el elemento más electronegativo, mientras que el francio es el menos electronegativo.
¿La polaridad afecta el punto de ebullición de una sustancia?
Sí, la polaridad tiene un impacto significativo en el punto de ebullición. Las moléculas polares experimentan fuerzas intermoleculares más fuertes (como interacciones dipolo-dipolo y puentes de hidrógeno) que las moléculas no polares (que solo tienen fuerzas de dispersión de London). Se requiere más energía para superar estas fuerzas de atracción más fuertes, lo que resulta en puntos de ebullición más altos para las sustancias polares en comparación con las no polares de masa molecular similar.
Si quieres conocer otros artículos parecidos a La Polaridad Molecular: Clave del Comportamiento Químico puedes visitar la categoría Química.
