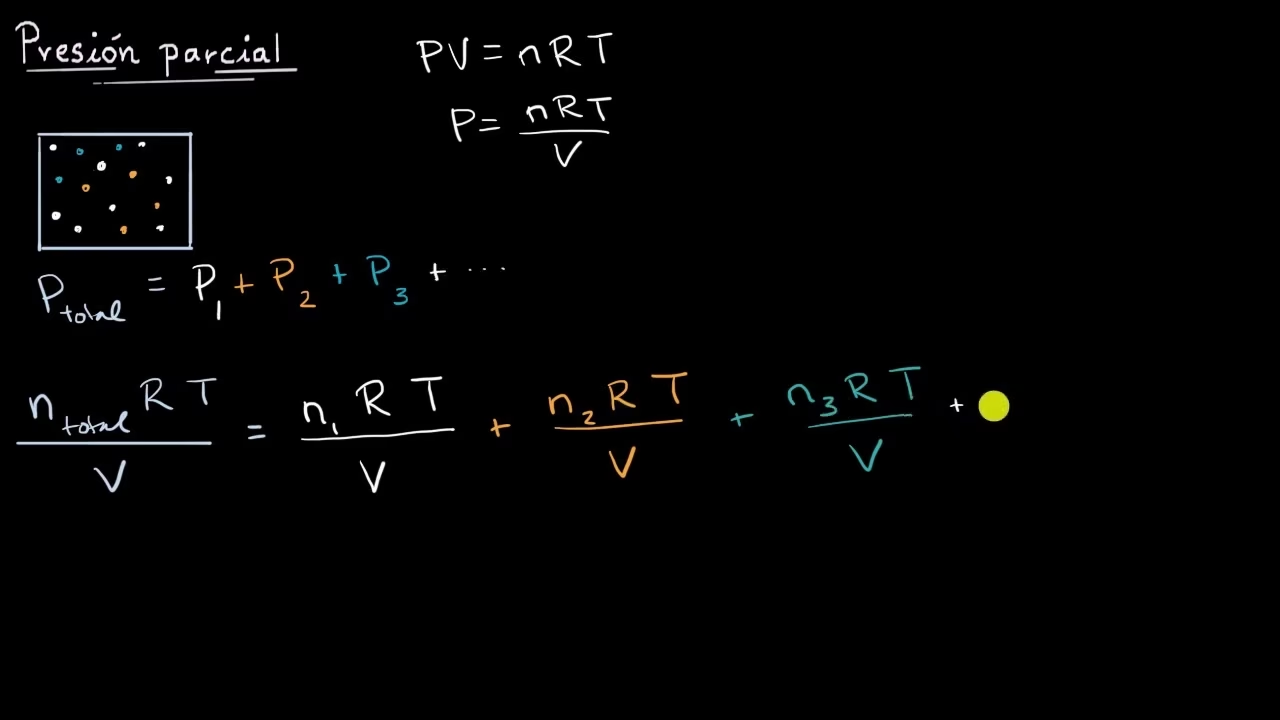22/02/2024
En el vasto universo de la física y la química, los gases ocupan un lugar especial debido a su comportamiento dinámico y su omnipresencia en nuestra vida diaria. Desde el aire que respiramos hasta los procesos industriales más complejos, entender cómo se comportan los gases es fundamental. Uno de los conceptos más importantes es la presión que ejercen, y en particular, cómo se calcula la presión total cuando tenemos una mezcla de diferentes gases. Esta es una pregunta crucial que nos lleva directamente a una de las leyes fundamentales de la química: la Ley de Dalton de las Presiones Parciales.
¿Qué es la Presión y Cómo se Mide?
Antes de sumergirnos en las complejidades de las mezclas de gases, es vital comprender qué es la presión en sí misma. En términos simples, la presión es la fuerza ejercida por unidad de área. Imagina las moléculas de gas dentro de un recipiente; estas moléculas están en constante movimiento, chocando contra las paredes del contenedor. Cada una de estas colisiones ejerce una pequeña fuerza, y la suma de todas esas fuerzas distribuidas sobre la superficie interna del recipiente es lo que percibimos como presión.
La presión se mide en diversas unidades, siendo las más comunes el Pascal (Pa), que es la unidad del Sistema Internacional (SI), el milímetro de mercurio (mmHg), la atmósfera (atm) y el psi (libras por pulgada cuadrada). La elección de la unidad a menudo depende del contexto o de la región geográfica.
El Concepto de Gas Ideal: La Base de la Ley de Dalton
La Ley de Dalton, como muchas otras leyes de los gases, se formula basándose en el modelo de los gases ideales. Un gas ideal es un modelo teórico que simplifica el comportamiento de los gases bajo ciertas condiciones. En un gas ideal, se asume que las moléculas tienen un volumen insignificante en comparación con el volumen total del contenedor y que no existen fuerzas de atracción o repulsión entre ellas. Aunque ningún gas real es perfectamente ideal, muchos gases se comportan de manera muy similar a un gas ideal bajo condiciones de baja presión y alta temperatura, lo que hace que este modelo sea increíblemente útil para predicciones y cálculos.

Es importante destacar que la validez de la Ley de Dalton es más precisa cuando se aplica a mezclas de gases que se comportan idealmente. En condiciones de alta presión o baja temperatura, donde las interacciones intermoleculares se vuelven significativas, las desviaciones del comportamiento ideal pueden hacer que la Ley de Dalton sea menos precisa.
La Ley de Dalton de las Presiones Parciales: Desentrañando la Presión Total
La Ley de Dalton de las Presiones Parciales, formulada por John Dalton, establece que en una mezcla de gases ideales, la presión total ejercida por la mezcla es igual a la suma de las presiones que cada gas ejercería si estuviera solo en el mismo volumen y a la misma temperatura. En otras palabras, cada gas en la mezcla contribuye de forma independiente a la presión total del sistema.
Matemáticamente, esta ley se expresa de la siguiente manera:
Ptotal = P1 + P2 + P3 + ... + Pn
Donde:
Ptotales la presión total de la mezcla de gases.P1, P2, P3, ..., Pnson las presiones parciales de cada uno de los gases individuales presentes en la mezcla.
La presión parcial de un gas se define como la presión que ese gas ejercería si ocupara todo el volumen del recipiente por sí mismo, a la misma temperatura que la mezcla. Es decir, la presencia de otros gases no afecta la presión parcial de un gas individual; solo afecta la presión total al sumarse a las demás presiones parciales.
¿Cómo se Calcula la Presión Parcial?
Para calcular la presión parcial de un gas en una mezcla, a menudo se utiliza la Ley de los Gases Ideales (PV=nRT). Si conocemos el número de moles (n) de un gas específico, el volumen (V) del recipiente y la temperatura (T), podemos calcular su presión parcial (P) de la siguiente manera:
Pi = (ni * R * T) / V
Donde:
Pies la presión parcial del gas 'i'.nies el número de moles del gas 'i'.Res la constante de los gases ideales.Tes la temperatura absoluta (en Kelvin).Ves el volumen total del recipiente.
Una relación muy útil que se deriva de la Ley de Dalton y la Ley de los Gases Ideales es que la presión parcial de un gas es proporcional a su fracción molar en la mezcla. La fracción molar (Xi) de un componente 'i' en una mezcla es la relación entre el número de moles de ese componente y el número total de moles de todos los gases en la mezcla (ntotal):
Xi = ni / ntotal
Entonces, la presión parcial de un gas también puede calcularse como:
Pi = Xi * Ptotal
Esta fórmula es particularmente útil cuando ya se conoce la presión total de la mezcla y se desea encontrar la contribución individual de cada gas.

Aplicaciones Prácticas de la Ley de Dalton
La Ley de Dalton no es solo un concepto teórico; tiene numerosas aplicaciones en el mundo real que impactan nuestra vida y diversas industrias:
- Buceo Submarino: Los buzos respiran mezclas de gases (como aire, que es principalmente nitrógeno y oxígeno) a profundidades donde la presión total es muy alta. Entender las presiones parciales es crucial para prevenir condiciones como la narcosis de nitrógeno o la toxicidad por oxígeno, ajustando la composición de la mezcla de gases para mantener las presiones parciales de O2 y N2 dentro de límites seguros.
- Meteorología: La presión atmosférica es la suma de las presiones parciales de todos los gases que componen el aire (nitrógeno, oxígeno, argón, dióxido de carbono, vapor de agua, etc.). Los cambios en la presión parcial del vapor de agua, por ejemplo, son indicativos de cambios en el clima y la humedad.
- Anestesia: En medicina, los anestesiólogos deben controlar cuidadosamente las presiones parciales de los gases anestésicos y el oxígeno que se administran a los pacientes para asegurar una dosis efectiva y segura.
- Procesos Industriales: En la industria química, la Ley de Dalton se utiliza para diseñar y operar equipos que manejan mezclas de gases, como torres de destilación, reactores y sistemas de separación.
- Fisiología Respiratoria: Nuestros pulmones intercambian oxígeno y dióxido de carbono basándose en los gradientes de presión parcial de estos gases entre el aire alveolar y la sangre.
Ejemplo de Cálculo de Presión Total
Para ilustrar la aplicación de la Ley de Dalton, consideremos un ejemplo sencillo:
Imaginemos un tanque que contiene una mezcla de tres gases ideales: Oxígeno (O2), Nitrógeno (N2) y Dióxido de Carbono (CO2). Las presiones parciales medidas de cada gas son las siguientes:
- Presión Parcial de O2 (PO2) = 0.21 atm
- Presión Parcial de N2 (PN2) = 0.78 atm
- Presión Parcial de CO2 (PCO2) = 0.01 atm
Para calcular la presión total (Ptotal) del sistema, simplemente sumamos las presiones parciales de cada gas, de acuerdo con la Ley de Dalton:
Ptotal = PO2 + PN2 + PCO2
Ptotal = 0.21 atm + 0.78 atm + 0.01 atm
Ptotal = 1.00 atm
Este ejemplo demuestra la simplicidad y la eficacia de la Ley de Dalton para determinar la presión total de una mezcla de gases. Podemos ver que la presión total de la mezcla es la suma directa de las contribuciones individuales de cada gas.
Tabla Comparativa: Comportamiento Ideal vs. Real en Mezclas de Gases
Aunque la Ley de Dalton es muy precisa para gases ideales, es importante reconocer sus limitaciones cuando se aplica a gases reales, especialmente bajo ciertas condiciones. La siguiente tabla resume las diferencias clave:
| Característica | Gases Ideales (Base de Ley de Dalton) | Gases Reales |
|---|---|---|
| Volumen Molecular | Insignificante (cero) | Considerable (no cero) |
| Interacciones Intermoleculares | Inexistentes | Existen (fuerzas de atracción/repulsión) |
| Comportamiento de la Ley de Dalton | Muy preciso | Preciso a bajas presiones/altas temperaturas; menos preciso a altas presiones/bajas temperaturas |
| Aplicabilidad | Predicciones teóricas simples | Comportamiento observado en el mundo real |
Esta tabla resalta por qué, aunque la Ley de Dalton es una herramienta poderosa, siempre debemos considerar las condiciones bajo las cuales se está aplicando para asegurar la precisión de nuestros cálculos.
Preguntas Frecuentes (FAQ)
- ¿Qué es la presión parcial?
- La presión parcial de un gas en una mezcla es la presión que ese gas ejercería si ocupara solo el volumen total del recipiente, a la misma temperatura que la mezcla. Es la contribución individual de un gas a la presión total de la mezcla.
- ¿La Ley de Dalton aplica a todos los gases?
- La Ley de Dalton es más precisa para mezclas de gases ideales. Para gases reales, especialmente a altas presiones o bajas temperaturas, donde las interacciones intermoleculares son significativas, la ley puede presentar desviaciones. Sin embargo, en muchas condiciones prácticas, se considera una aproximación muy buena.
- ¿Por qué es importante la Ley de Dalton?
- Es fundamental para entender el comportamiento de las mezclas de gases y tiene aplicaciones críticas en campos como la medicina (anestesia, fisiología respiratoria), la ingeniería (diseño de procesos químicos), la meteorología y el buceo, donde el control de las presiones de los diferentes componentes gaseosos es vital para la seguridad y la eficiencia.
- ¿Cómo se relaciona la Ley de Dalton con la Ley de los Gases Ideales (PV=nRT)?
- La Ley de Dalton se puede derivar directamente de la Ley de los Gases Ideales. Cada presión parcial (Pi) de un gas en la mezcla se puede calcular usando PV=nRT para ese gas específico (Pi = niRT/V). Al sumar todas estas presiones parciales, se obtiene la presión total, que también obedece a PV=nRT con el número total de moles (Ptotal = ntotalRT/V).
- ¿Qué unidades se utilizan comúnmente para la presión?
- Las unidades más comunes incluyen el Pascal (Pa), la atmósfera (atm), el milímetro de mercurio (mmHg o Torr) y el psi (libras por pulgada cuadrada). La elección de la unidad depende del contexto y la convención.
Conclusión
La Ley de Dalton de las Presiones Parciales es un pilar fundamental en la comprensión del comportamiento de las mezclas de gases. Su simplicidad, al establecer que la presión total es simplemente la suma de las contribuciones individuales de cada gas, la convierte en una herramienta invaluable para científicos, ingenieros y profesionales en una amplia gama de disciplinas. Aunque formulada para gases ideales, su aplicabilidad se extiende a muchos escenarios del mundo real, proporcionando una base sólida para el cálculo y la predicción del comportamiento gaseoso. Entender esta ley no solo nos permite calcular con precisión la presión total de un sistema, sino que también nos abre las puertas a una comprensión más profunda de cómo los gases interactúan y afectan nuestro entorno.
Si quieres conocer otros artículos parecidos a La Presión Total: Un Vistazo a la Ley de Dalton puedes visitar la categoría Química.