09/01/2024
El pH es una medida fundamental en química que nos indica la acidez o basicidad de una solución. Desde la sangre en nuestro cuerpo hasta los productos de limpieza que usamos a diario, comprender el pH es crucial. Sin embargo, para muchos estudiantes, los ejercicios de pH pueden parecer un laberinto de logaritmos y concentraciones. No te preocupes más. Este artículo está diseñado para ser tu guía definitiva, desglosando los conceptos y ofreciendo un camino claro para resolver cualquier problema de pH con confianza. Prepárate para entender no solo cómo calcular el pH, sino también por qué es importante cada paso y cómo aplicar este conocimiento en diversos escenarios.
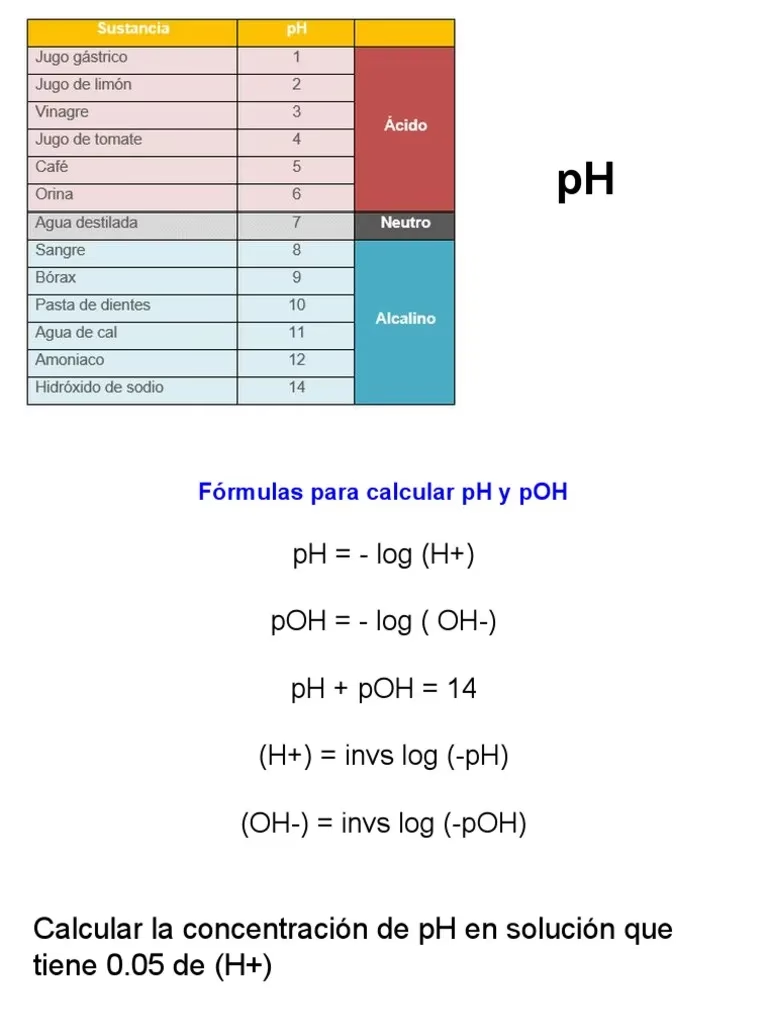
¿Qué es el pH y por qué es tan importante?
El pH, que significa 'potencial de hidrógeno', es una escala logarítmica que mide la concentración de iones de hidrógeno (H+) en una solución acuosa. Esta escala va típicamente de 0 a 14, donde un pH de 7 se considera neutro (como el agua pura a 25°C), un pH menor a 7 indica acidez, y un pH mayor a 7 indica basicidad o alcalinidad.
La importancia del pH radica en su influencia directa sobre las reacciones químicas y los procesos biológicos. Por ejemplo, el pH del suelo afecta la capacidad de las plantas para absorber nutrientes, el pH de la piscina es vital para la eficacia del cloro y la seguridad del baño, y el pH de nuestro cuerpo debe mantenerse en un rango muy estrecho (alrededor de 7.4 para la sangre) para que las enzimas y las funciones celulares operen correctamente. Comprender el pH es, por lo tanto, esencial en campos tan diversos como la medicina, la agricultura, la industria alimentaria y el tratamiento de aguas.
Conceptos Fundamentales para el Cálculo de pH
Para abordar los ejercicios de pH, es imprescindible dominar algunos conceptos básicos y sus respectivas fórmulas:
1. Autoionización del Agua y la Escala de pH
El agua no es solo un solvente pasivo; tiene la capacidad de autoionizarse, es decir, de disociarse en iones H+ y OH- (iones hidróxido) en una pequeña extensión. Esta reacción de equilibrio se representa como:
H2O(l) ⇌ H+(aq) + OH-(aq)
A 25°C, el producto iónico del agua (Kw) es una constante de 1.0 x 10-14. Esto significa que en cualquier solución acuosa a esta temperatura, el producto de las concentraciones de iones H+ y OH- siempre será 1.0 x 10-14:
[H+][OH-] = Kw = 1.0 x 10-14
A partir de esto, se derivan las definiciones de pH y pOH:
- pH = -log[H+]: El negativo del logaritmo de la concentración molar de iones de hidrógeno.
- pOH = -log[OH-]: El negativo del logaritmo de la concentración molar de iones hidróxido.
- pH + pOH = 14: Esta relación es clave y se deriva de la ecuación del Kw.
También es útil saber cómo calcular la concentración de iones a partir del pH o pOH:
- [H+] = 10-pH
- [OH-] = 10-pOH
2. Ácidos y Bases Fuertes vs. Débiles
La distinción entre ácidos/bases fuertes y débiles es crucial porque afecta directamente la forma en que calculamos el pH.
- Ácidos y Bases Fuertes: Se disocian completamente en agua. Esto significa que la concentración inicial del ácido o la base es igual a la concentración de los iones H+ o OH- que produce. Ejemplos comunes de ácidos fuertes incluyen HCl, HBr, HI, HNO3, H2SO4, HClO4. Ejemplos de bases fuertes son los hidróxidos de metales alcalinos y alcalinotérreos, como NaOH, KOH, Ca(OH)2, Ba(OH)2.
- Ácidos y Bases Débiles: Se disocian solo parcialmente en agua, estableciendo un equilibrio químico. Para estos, necesitamos usar constantes de disociación ácida (Ka) o básica (Kb), que reflejan el grado de disociación. Cuanto mayor sea el valor de Ka o Kb, más fuerte será el ácido o la base (dentro de los débiles).
Paso a Paso: Resolución de Ejercicios de pH
La metodología para resolver ejercicios de pH varía según si estamos tratando con ácidos/bases fuertes o débiles. A continuación, se detallan los casos más comunes:
Caso 1: Ácidos y Bases Fuertes
Para ácidos y bases fuertes, el cálculo es relativamente directo debido a su disociación completa.
Ejemplo 1: Calcular el pH de una solución de HCl 0.01 M.
- Identificar el tipo de sustancia: HCl es un ácido fuerte. Se disocia completamente: HCl → H+ + Cl-.
- Determinar la concentración de H+: Dado que la disociación es completa, [H+] = [HCl inicial] = 0.01 M.
- Aplicar la fórmula del pH: pH = -log[H+] = -log(0.01) = -log(10-2) = 2.00.
Ejemplo 2: Calcular el pH de una solución de NaOH 0.005 M.
- Identificar el tipo de sustancia: NaOH es una base fuerte. Se disocia completamente: NaOH → Na+ + OH-.
- Determinar la concentración de OH-: Dado que la disociación es completa, [OH-] = [NaOH inicial] = 0.005 M.
- Calcular el pOH: pOH = -log[OH-] = -log(0.005) = -log(5 x 10-3) ≈ 2.30.
- Calcular el pH usando la relación pH + pOH = 14: pH = 14 - pOH = 14 - 2.30 = 11.70.
Caso 2: Ácidos y Bases Débiles
Para ácidos y bases débiles, la disociación parcial requiere el uso de constantes de equilibrio (Ka o Kb) y, a menudo, tablas ICE (Inicial, Cambio, Equilibrio).
Ejemplo 3: Calcular el pH de una solución de ácido acético (CH3COOH) 0.10 M. Ka = 1.8 x 10-5.
- Escribir la ecuación de disociación y la expresión de Ka:
CH3COOH(aq) ⇌ H+(aq) + CH3COO-(aq)
Ka = ([H+][CH3COO-]) / [CH3COOH] - Construir una tabla ICE:
[CH3COOH] [H+] [CH3COO-] Inicial (I) 0.10 M ~0 M 0 M Cambio (C) -x +x +x Equilibrio (E) 0.10 - x x x - Sustituir en la expresión de Ka y resolver para x:
1.8 x 10-5 = (x * x) / (0.10 - x)
Dado que Ka es pequeña y la concentración inicial es relativamente alta, podemos asumir que x es mucho menor que 0.10. Así, 0.10 - x ≈ 0.10. (Regla del 5%: Si x es menor al 5% de la concentración inicial, la aproximación es válida).1.8 x 10-5 = x2 / 0.10
x2 = 1.8 x 10-6
x = √(1.8 x 10-6) ≈ 0.00134 MVerificación de la aproximación: (0.00134 / 0.10) * 100% = 1.34%, que es menor al 5%, por lo que la aproximación es válida.
- Calcular el pH: x representa [H+] en el equilibrio.
[H+] = 0.00134 M
pH = -log(0.00134) ≈ 2.87.
Caso 3: Sales y su Efecto en el pH (Hidrólisis)
Algunas sales pueden hidrolizarse en agua, produciendo iones H+ u OH- y, por lo tanto, afectando el pH de la solución. El efecto depende de los iones que forman la sal:
- Sal de ácido fuerte + base fuerte: Neutra (ej. NaCl, KNO3).
- Sal de ácido débil + base fuerte: Básica (ej. CH3COONa). El anión del ácido débil hidroliza el agua para formar OH-.
- Sal de ácido fuerte + base débil: Ácida (ej. NH4Cl). El catión de la base débil hidroliza el agua para formar H+.
- Sal de ácido débil + base débil: Puede ser ácida, básica o neutra, dependiendo de los valores relativos de Ka y Kb.
Para sales que afectan el pH, necesitamos calcular la constante de hidrólisis (Kh) utilizando Kw y Ka o Kb:
- Para aniones de ácidos débiles: Kh = Kw / Ka
- Para cationes de bases débiles: Kh = Kw / Kb
Ejemplo 4: Calcular el pH de una solución de acetato de sodio (CH3COONa) 0.10 M. Ka del ácido acético = 1.8 x 10-5.
- Identificar la sal y su hidrólisis: CH3COONa es la sal de un ácido débil (ácido acético) y una base fuerte (NaOH). Solo el anión acetato (CH3COO-) hidrolizará el agua.
- Escribir la ecuación de hidrólisis y la expresión de Kb:
CH3COO-(aq) + H2O(l) ⇌ CH3COOH(aq) + OH-(aq)
Kb = ([CH3COOH][OH-]) / [CH3COO-] - Calcular Kb para el ion acetato:
Kb = Kw / Ka = (1.0 x 10-14) / (1.8 x 10-5) ≈ 5.6 x 10-10 - Construir una tabla ICE y resolver para x (similar al caso de ácidos/bases débiles):
[CH3COO-] [CH3COOH] [OH-] Inicial (I) 0.10 M 0 M ~0 M Cambio (C) -x +x +x Equilibrio (E) 0.10 - x x x 5.6 x 10-10 = x2 / (0.10 - x)
Asumiendo 0.10 - x ≈ 0.10:
x2 = 5.6 x 10-11
x = √(5.6 x 10-11) ≈ 7.5 x 10-6 M - Calcular el pOH y luego el pH:
[OH-] = x = 7.5 x 10-6 M
pOH = -log(7.5 x 10-6) ≈ 5.12
pH = 14 - pOH = 14 - 5.12 = 8.88.
Errores Comunes y Consejos para el Éxito
- Confundir [H+] con [Ácido inicial]: Esto solo es válido para ácidos fuertes. Para los débiles, la concentración de H+ es menor que la concentración inicial del ácido.
- Olvidar la relación pH + pOH = 14: Es una herramienta invaluable para cambiar entre escalas.
- Errores de calculadora: Asegúrate de usar correctamente la función de logaritmo (log base 10) y de antilogaritmo (10^x).
- Ignorar las unidades: La concentración siempre debe estar en Molaridad (mol/L).
- No verificar la aproximación del 5%: Si x resulta ser más del 5% de la concentración inicial, debes resolver la ecuación cuadrática completa.
- Identificar incorrectamente la sustancia: ¿Es un ácido fuerte, una base fuerte, un ácido débil, una base débil o una sal? Este es el primer y más importante paso.
Consejos Adicionales:
- Práctica Constante: La química, y el pH en particular, se aprende haciendo. Cuantos más problemas resuelvas, más intuitivo se volverá.
- Entender el Concepto, No Solo la Fórmula: Saber por qué se usa una fórmula específica te ayudará a aplicarla correctamente en diferentes situaciones.
- Organiza tus Datos: Especialmente con las tablas ICE, mantener tus valores iniciales, cambios y equilibrios bien organizados previene errores.
Tabla Comparativa: Ácidos Fuertes vs. Ácidos Débiles
Para consolidar las diferencias en el enfoque de cálculo, aquí hay una tabla comparativa:
| Característica | Ácidos Fuertes | Ácidos Débiles |
|---|---|---|
| Disociación en Agua | Completa (100%) | Parcial (establece un equilibrio) |
| Relación [H+] y [Ácido inicial] | [H+] = [Ácido inicial] | [H+] < [Ácido inicial] |
| Constante de Equilibrio | No se usa Ka (se asume infinita) | Se usa Ka (Constante de disociación ácida) |
| Método de Cálculo | Directo: pH = -log[Ácido inicial] | Tabla ICE y Ka para encontrar [H+] en el equilibrio |
| Ejemplo de Sustancia | HCl, H2SO4, HNO3 | CH3COOH, H2CO3, HF |
Preguntas Frecuentes (FAQ) sobre el pH
¿Qué es la diferencia entre pH y pOH?
El pH mide la concentración de iones de hidrógeno (H+), indicando acidez. El pOH mide la concentración de iones hidróxido (OH-), indicando basicidad. Ambos están relacionados por la ecuación pH + pOH = 14 a 25°C, lo que significa que si conoces uno, puedes calcular el otro.
¿Puede el pH ser negativo o mayor que 14?
Sí, teóricamente. Aunque la escala de pH más común va de 0 a 14, en soluciones muy concentradas de ácidos o bases fuertes, el pH puede ser menor que 0 (por ejemplo, para [H+] = 10 M, pH = -1) o mayor que 14 (por ejemplo, para [OH-] = 10 M, pOH = -1, pH = 15). Sin embargo, esto es poco común en soluciones diluidas y en la mayoría de los ejercicios de química general.
¿Qué son las soluciones amortiguadoras (buffers) y cómo se relacionan con el pH?
Las soluciones amortiguadoras, o buffers, son mezclas de un ácido débil y su base conjugada (o una base débil y su ácido conjugado) que resisten cambios significativos en el pH cuando se añaden pequeñas cantidades de ácido o base fuerte. Son cruciales en sistemas biológicos (como la sangre) y en muchos procesos químicos industriales para mantener un pH estable.
¿Por qué se usa una escala logarítmica para el pH?
La concentración de iones H+ en las soluciones acuosas puede variar en un rango muy amplio (desde 10-15 M hasta 10 M o más). Usar una escala logarítmica comprime este vasto rango en una escala más manejable y fácil de interpretar, como la de 0 a 14.
¿Qué significa el valor de Ka o Kb?
Ka (constante de disociación ácida) y Kb (constante de disociación básica) son medidas cuantitativas de la fuerza de un ácido o una base débil, respectivamente. Un valor de Ka o Kb más grande indica un ácido o una base débil más fuerte, lo que significa que se disocia en mayor medida en solución.
Conclusión
Resolver ejercicios de pH es una habilidad fundamental en química que requiere una comprensión clara de los conceptos de acidez, basicidad, disociación y equilibrio. Al dominar las fórmulas clave, diferenciar entre ácidos/bases fuertes y débiles, y practicar con ejemplos variados, transformarás la incertidumbre en confianza. Recuerda que la clave está en la práctica constante y en la aplicación lógica de los principios. Con esta guía, tienes las herramientas necesarias para enfrentar cualquier problema de pH. ¡Ahora es el momento de poner en práctica lo aprendido y convertirte en un experto en pH!
Si quieres conocer otros artículos parecidos a Dominando el pH: Guía Completa para Resolver Ejercicios puedes visitar la categoría Química.
