10/10/2023
El concepto de masa molecular, junto con la masa molar y la masa atómica, son pilares fundamentales para comprender a cabalidad el vasto y complejo mundo de la química. En el ámbito microscópico, las moléculas de los compuestos químicos poseen una masa extraordinariamente baja, lo que dificulta su estudio directo. Sin embargo, al dominar estos conceptos, no solo podemos cuantificar la masa de un elemento o compuesto, sino también determinar las proporciones en que los elementos se combinan e incluso predecir su comportamiento en diversas reacciones. La habilidad de manejar estas magnitudes es crucial para cualquier persona que desee adentrarse en la composición, estructura y propiedades de la materia.

La química, en su esencia, busca entender cómo interactúan los átomos y las moléculas para formar todo lo que nos rodea. Para ello, es indispensable una forma de medir y comparar las cantidades de estas partículas diminutas. Aquí es donde la masa molecular y la masa molar se vuelven herramientas indispensables, sirviendo como puentes entre el mundo atómico invisible y las cantidades de sustancias que podemos manipular en un laboratorio o en un proceso industrial. Sin una comprensión clara de estos términos, sería imposible llevar a cabo cálculos precisos, formular nuevas sustancias o incluso entender procesos biológicos básicos.
- ¿Qué es la Masa Molecular?
- La Masa Atómica: El Fundamento Esencial
- Masa Molecular de los Elementos Diatómicos
- ¿Cómo Determinamos la Masa Molecular de Elementos y Compuestos Químicos?
- Masa Molecular vs. Masa Molar: La Distinción Crucial
- La Inmensa Utilidad de Conocer la Masa Molar de una Sustancia
- Preguntas Frecuentes (FAQs)
- Conclusión
¿Qué es la Masa Molecular?
La masa molecular de un compuesto químico se define como la suma total de las masas atómicas de todos los elementos que lo componen. Es una medida directa de la masa de una única molécula de una sustancia. La masa molecular de una molécula específica depende directamente de qué átomos la constituyen y en qué cantidad. Dada la ínfima magnitud de estas masas (a menudo del orden de 10-24 gramos), se ha adoptado una unidad de medida más práctica para evitar el manejo de números tan pequeños: la unidad de masa atómica (u). Esta unidad se define convencionalmente como 1/12 de la masa del isótopo de carbono-12 (12C), un estándar universal que simplifica enormemente los cálculos en química.
Por ejemplo, si consideramos una molécula de agua (H2O), su masa molecular se calcularía sumando la masa atómica de dos átomos de hidrógeno y un átomo de oxígeno. Cada átomo de hidrógeno tiene una masa atómica aproximada de 1.008 u, y el oxígeno tiene una masa atómica de aproximadamente 15.999 u. Por lo tanto, la masa molecular del agua sería (2 × 1.008 u) + 15.999 u = 18.015 u. Esta unidad, la 'u', nos permite expresar las masas de átomos y moléculas de una manera sencilla y comparable, liberándonos de la necesidad de usar notación científica constante para valores tan pequeños.
La Masa Atómica: El Fundamento Esencial
Para determinar correctamente la masa molecular de cualquier compuesto químico, el primer paso es conocer la masa atómica de cada uno de los elementos que lo conforman. La masa de los elementos químicos se expresa habitualmente en unidades de masa atómica (u), tal como se mencionó anteriormente. Un aspecto crucial a considerar es que la mayoría de los elementos químicos presentes en la Tierra no existen como un único tipo de átomo, sino como mezclas de varios isótopos. Los isótopos son variantes de un mismo elemento químico que poseen el mismo número de protones en su núcleo (y por lo tanto el mismo número atómico), pero difieren en el número de neutrones. Esta diferencia en el número de neutrones se traduce en una diferencia en su número de masa.
Al determinar la masa atómica de un elemento químico en la tabla periódica, lo que vemos es en realidad un promedio ponderado de las masas de todos sus isótopos naturales, teniendo en cuenta su abundancia relativa. Por ejemplo, el cloro tiene dos isótopos principales, el cloro-35 y el cloro-37, y su masa atómica en la tabla periódica (aproximadamente 35.453 u) es el resultado de la abundancia de cada uno de ellos. Esta masa atómica es una característica única e identificativa para cada elemento. Es fundamental destacar que no existen dos elementos químicos con la misma masa atómica promedio, lo que convierte a esta propiedad en una herramienta invaluable para la identificación y clasificación de los elementos. La tabla periódica es, en este sentido, una fuente directa y accesible para consultar las masas atómicas de todos los elementos conocidos.

Masa Molecular de los Elementos Diatómicos
Algunos elementos químicos no existen naturalmente como átomos individuales, sino que forman moléculas que consisten en dos átomos unidos. Estos son los elementos diatómicos. Ejemplos comunes incluyen el nitrógeno (N2), el hidrógeno (H2), el oxígeno (O2), el flúor (F2), el bromo (Br2), el yodo (I2) y el cloro (Cl2). En estos casos, es más apropiado hablar de la ‘masa molecular de un elemento’ en lugar de su masa atómica.
Para calcular la masa molecular de un elemento diatómico, simplemente se multiplica la masa atómica de un solo átomo de ese elemento por dos. Por ejemplo, la masa atómica de un solo átomo de nitrógeno (N) es de aproximadamente 14 u. Dado que el nitrógeno existe como una molécula diatómica (N2), su masa molecular es de 2 × 14 u = 28 u. De manera similar, la masa atómica del oxígeno (O) es aproximadamente 16 u, por lo que la masa molecular del oxígeno diatómico (O2) es 2 × 16 u = 32 u. Este concepto es vital para comprender la composición y el comportamiento de estos elementos en su estado natural.
¿Cómo Determinamos la Masa Molecular de Elementos y Compuestos Químicos?
El proceso para determinar la masa molecular, ya sea de elementos o de compuestos, es sistemático y requiere conocer la fórmula molecular de la sustancia en cuestión. Una vez que tenemos la fórmula química, podemos utilizar las masas atómicas de los elementos para establecer la participación de cada uno en la masa total de la molécula y, por extensión, en el porcentaje de composición de un compuesto.
Para los elementos diatómicos, como se mencionó, la determinación de su masa molecular se basa en multiplicar la masa atómica de un solo átomo de ese elemento por el número de átomos en la molécula (generalmente dos). El procedimiento es similar, aunque un poco más elaborado, para los compuestos químicos. Aquí se detalla el método paso a paso para establecer su masa molecular:
- Determine la fórmula química del compuesto cuya masa molecular desea definir (ej., H2SO4 para el ácido sulfúrico).
- Especifique los elementos incluidos en el compuesto e indique la cantidad de cada elemento presente en una molécula (ej., en H2SO4 hay 2 átomos de H, 1 átomo de S y 4 átomos de O).
- Determine las masas atómicas de cada elemento utilizando la tabla periódica (ej., H ≈ 1.008 u, S ≈ 32.06 u, O ≈ 15.999 u).
- Multiplique la masa atómica de cada elemento por el número de veces que aparece en la molécula. Si la molécula contiene más de un átomo de un elemento específico, su masa atómica debe ser multiplicada por ese subíndice (ej., para H2SO4: H: 2 × 1.008 u; S: 1 × 32.06 u; O: 4 × 15.999 u).
- Sume las masas atómicas de todos los elementos (ya multiplicadas por sus respectivos subíndices) para obtener la masa molecular total del compuesto. (ej., para H2SO4: (2 × 1.008) + (1 × 32.06) + (4 × 15.999) = 2.016 + 32.06 + 63.996 = 98.072 u).
Este procedimiento es fundamental para la base de muchos cálculos en química, desde la estequiometría de reacciones hasta la preparación de soluciones.
Masa Molecular vs. Masa Molar: La Distinción Crucial
A menudo, los términos masa molecular y masa molar se utilizan de forma intercambiable, pero es vital comprender que, aunque tienen el mismo valor numérico, representan conceptos y escalas de medición diferentes. La distinción radica principalmente en la unidad y la cantidad de sustancia a la que se refieren. Comprender esta diferencia es crucial para realizar cálculos estequiométricos precisos y entender la química a una escalamacroscópica.
La masa molecular, como ya se ha explicado, se refiere a la masa de una única molécula y se expresa en unidades de masa atómica (u). Es una propiedad a nivel microscópico, que describe la masa de una entidad individual.
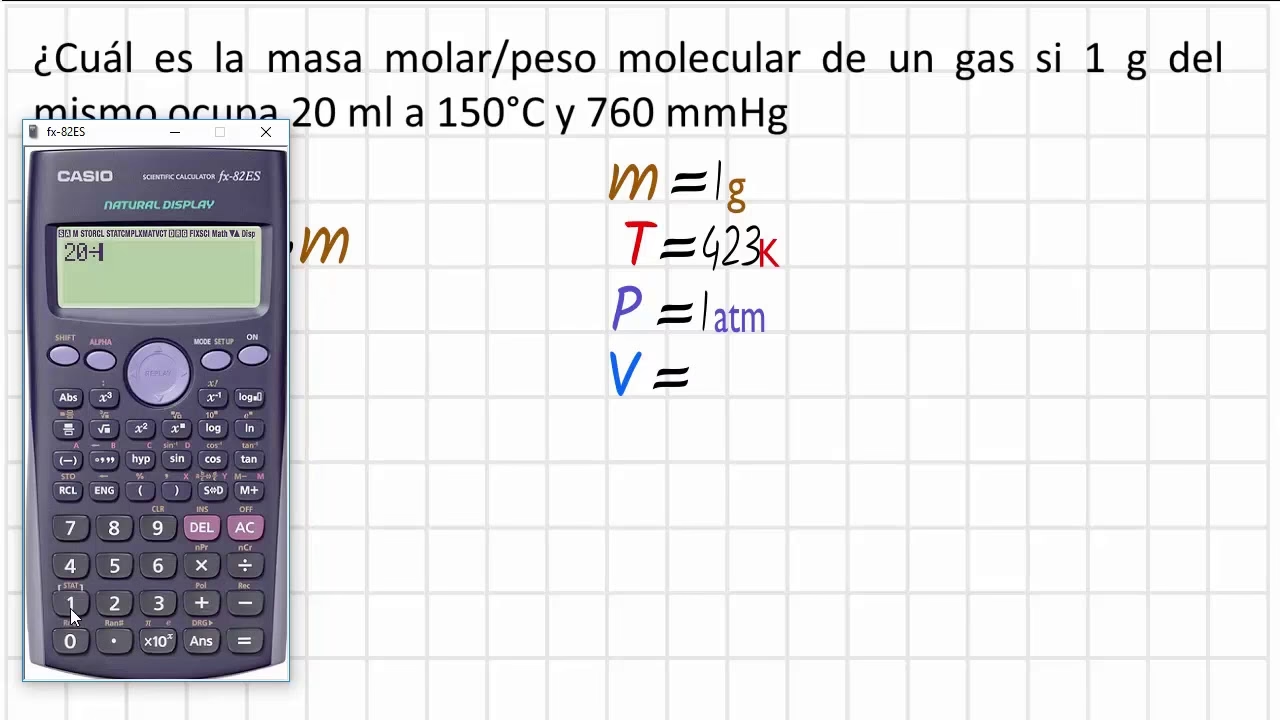
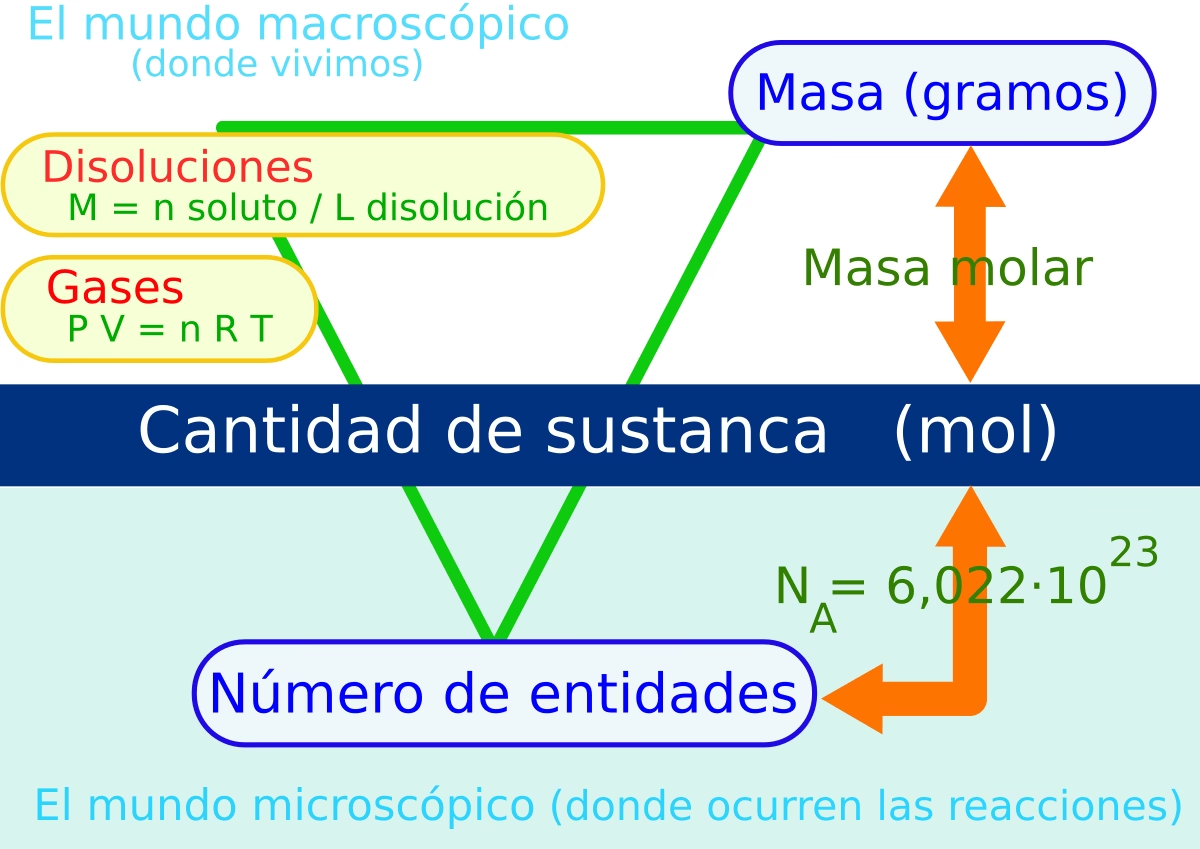
Por otro lado, la masa molar es la masa de un mol de una sustancia específica. Se expresa en gramos por mol (g/mol). El mol es una unidad fundamental en el Sistema Internacional (SI) para la cantidad de sustancia. Un mol se define como la cantidad de sustancia que contiene exactamente 6.022141 × 1023 entidades elementales (conocida como el número de Avogadro). Estas entidades pueden ser átomos, iones, moléculas o cualquier otra partícula.
La magia del concepto de mol reside en su capacidad para vincular el mundo microscópico (átomos y moléculas) con el mundo macroscópico (gramos que podemos pesar en un laboratorio). El valor numérico de la masa molecular en 'u' es idéntico al valor numérico de la masa molar en 'g/mol'. Por ejemplo, si la masa molecular del agua es 18.015 u, esto significa que la masa molar del agua es 18.015 g/mol. Esto implica que 6.022141 × 1023 moléculas de agua (un mol de agua) tienen una masa de 18.015 gramos. Esta relación es increíblemente útil porque nos permite trabajar con cantidades medibles en el laboratorio mientras entendemos lo que sucede a nivel atómico y molecular. La masa molar es la que se utiliza comúnmente en cálculos para reacciones químicas, preparación de soluciones y cualquier manipulación de sustancias en el laboratorio o la industria, ya que nos permite convertir directamente entre la cantidad de sustancia (moles) y su masa medible (gramos).
La Inmensa Utilidad de Conocer la Masa Molar de una Sustancia
Conocer la masa molar de una sustancia es una herramienta indispensable en una multitud de aplicaciones dentro y fuera del laboratorio. Su utilidad va más allá de un simple dato numérico; es el puente que conecta la teoría atómica con la práctica experimental y la aplicación industrial.
La masa molar de un compuesto químico nos permite:
- Realizar Cálculos Estequiométricos: Es la base para determinar las proporciones de reactivos y productos en una reacción química. Permite calcular cuánto de un reactivo se necesita para producir una cierta cantidad de producto, o cuánto producto se formará a partir de una cantidad dada de reactivo. Esto es crucial para la síntesis de nuevos materiales, la optimización de procesos químicos y la producción a gran escala.
- Determinar la Composición Porcentual: Permite calcular el porcentaje en masa de cada elemento dentro de un compuesto. Esto es vital para la caracterización de nuevas sustancias, el control de calidad en la industria y la verificación de la pureza de los materiales. Si conocemos la masa molecular, no solo podemos especificar el peso de un elemento dado, sino también determinar las proporciones de masa de los elementos en los compuestos o indicar su contenido a modo de porcentaje.
- Preparar Soluciones con Concentraciones Precisas: En química, muchas reacciones se llevan a cabo en solución. Con la masa molar, podemos calcular con exactitud la cantidad de soluto necesaria para preparar una solución con una concentración molar específica, lo cual es fundamental en laboratorios de investigación, análisis clínicos y producción farmacéutica.
- Analizar la Pureza de Sustancias: Comparando la masa molar esperada de una sustancia pura con la masa molar determinada experimentalmente de una muestra, se puede inferir el grado de pureza de dicha muestra.
- Entender el Tamaño de las Moléculas (especialmente Polímeros): Como se mencionó en la información de partida, el peso molecular (o masa molecular, en este contexto) es un criterio para determinar el tamaño de la cadena polimérica. A mayor peso molecular, corresponde un mayor tamaño de cadena. Esto es fundamental en la ciencia de materiales para diseñar polímeros con propiedades específicas como resistencia, elasticidad o punto de fusión, ya que la naturaleza estadística de las reacciones de polimerización implica que el tamaño de las cadenas no es uniforme.
- Aplicaciones en la Industria Farmacéutica y Química: Desde el diseño de fármacos hasta la fabricación de productos químicos, la masa molar es esencial para formular recetas, calcular rendimientos de reacción y asegurar la consistencia y calidad del producto final.
- Investigación y Desarrollo: En la investigación, la masa molar ayuda a identificar compuestos desconocidos, a confirmar la síntesis de nuevas moléculas y a comprender los mecanismos de reacción.
En resumen, la masa molar trasciende el ámbito académico para convertirse en una herramienta práctica e indispensable que permite a científicos, ingenieros y técnicos manipular y comprender las sustancias a un nivel fundamental, impactando directamente en la innovación y el progreso tecnológico.
Tabla Comparativa: Masa Molecular vs. Masa Molar
Para clarificar aún más estos conceptos, la siguiente tabla resume las diferencias clave entre masa molecular y masa molar:
| Característica | Masa Molecular | Masa Molar |
|---|---|---|
| Definición | Masa de una sola molécula. | Masa de un mol (6.022 × 1023) de entidades. |
| Unidad | Unidades de masa atómica (u). | Gramos por mol (g/mol). |
| Escala | Microscópica (partícula individual). | Macroscópica (cantidad de sustancia medible). |
| Uso Principal | Descripción teórica de una molécula. | Cálculos estequiométricos, preparación de soluciones, análisis cuantitativo. |
| Valor Numérico | Idéntico al de la masa molar. | Idéntico al de la masa molecular. |
Preguntas Frecuentes (FAQs)
¿Cuál es la diferencia clave entre masa atómica, masa molecular y masa molar?
La diferencia radica en la entidad a la que se refieren y la escala de medición. La masa atómica es la masa promedio de un átomo de un elemento, considerando sus isótopos naturales, y se mide en unidades de masa atómica (u). La masa molecular es la suma de las masas atómicas de todos los átomos en una única molécula de un compuesto y también se mide en 'u'. Por último, la masa molar es la masa de un mol (el número de Avogadro de partículas) de una sustancia y se mide en gramos por mol (g/mol). Mientras que la masa atómica y molecular describen entidades individuales a nivel microscópico, la masa molar conecta esa información con cantidades que podemos pesar y manipular a nivel macroscópico.

¿Por qué se usa el mol en química?
El mol se usa en química para salvar la brecha entre el mundo microscópico de los átomos y las moléculas y el mundo macroscópico en el que trabajamos. Los átomos y las moléculas son tan pequeños y numerosos que sería impráctico contarlos individualmente. El mol nos proporciona una unidad conveniente que representa una cantidad muy grande pero específica de partículas (el número de Avogadro). Esto permite a los químicos convertir fácilmente entre la masa de una sustancia (medida en gramos) y el número de partículas que contiene, facilitando los cálculos de reacciones y la formulación de compuestos.
¿Cómo se relaciona la masa molar con la tabla periódica?
La masa molar está directamente relacionada con la tabla periódica. La masa atómica promedio que se encuentra para cada elemento en la tabla periódica es numéricamente igual a la masa molar de ese elemento. Por ejemplo, la masa atómica del carbono es aproximadamente 12.011 u, lo que significa que la masa molar del carbono es 12.011 g/mol. Para un compuesto, la masa molar se calcula sumando las masas atómicas de todos los átomos en su fórmula molecular, tal como se obtienen de la tabla periódica. Así, la tabla periódica es la fuente fundamental para obtener los datos necesarios para calcular la masa molar de cualquier sustancia.
¿Para qué se utiliza la masa molar en la industria?
En la industria, la masa molar es fundamental para el control de calidad, la optimización de procesos y el diseño de productos. Se utiliza para calcular las cantidades exactas de reactivos necesarias para una producción eficiente, minimizar residuos y asegurar que los productos finales tengan la pureza y las propiedades deseadas. Por ejemplo, en la industria farmacéutica, se usa para formular medicamentos con dosis precisas; en la petroquímica, para optimizar los rendimientos de los procesos de refinación; y en la producción de materiales, para controlar la composición y las propiedades de polímeros y aleaciones. Es una herramienta esencial para la estandarización y la escalabilidad de la producción.
¿La masa molar es siempre un número entero?
No, la masa molar no es siempre un número entero. Si bien las masas de los protones y neutrones son aproximadamente 1 u, y las masas de los isótopos individuales son casi números enteros (ej., Carbono-12 tiene una masa de 12 u), la masa atómica promedio de un elemento (y por ende su masa molar) es un promedio ponderado de las masas de sus isótopos naturales. Dado que los isótopos no suelen tener abundancias perfectamente iguales y sus masas exactas no son números enteros perfectos, las masas atómicas y molares suelen ser números decimales. Por ejemplo, la masa molar del cloro es aproximadamente 35.453 g/mol, no un número entero.
Conclusión
La comprensión de la masa atómica, la masa molecular y, sobre todo, la masa molar, es mucho más que un ejercicio académico; es una habilidad fundamental que desbloquea la capacidad de comprender, predecir y manipular el comportamiento de la materia. Estos conceptos nos permiten transitar desde el mundo invisible de los átomos y las moléculas hasta las cantidades tangibles que podemos medir y utilizar en la vida real. Desde la síntesis de nuevos materiales hasta el control de calidad en procesos industriales y la investigación científica, la masa molar es la clave para la precisión y la eficiencia en el vasto universo de la química. Su dominio es indispensable para cualquier persona que aspire a interactuar de manera significativa con las sustancias que nos rodean y a contribuir al avance del conocimiento científico y tecnológico.
Si quieres conocer otros artículos parecidos a La Masa Molar: Clave para Entender la Química puedes visitar la categoría Química.