08/12/2023
En el vasto universo de la química, las soluciones juegan un papel fundamental, siendo la base de innumerables procesos industriales, biológicos y cotidianos. Comprender cómo se preparan y cómo se expresa la cantidad de sus componentes es crucial. En el corazón de cualquier solución se encuentra el soluto, la sustancia que se disuelve, y el solvente, el medio en el que se disuelve. La relación entre estos dos, conocida como concentración, es lo que define las propiedades y aplicaciones de una solución. Calcular la cantidad de soluto necesaria o presente en una solución es una habilidad esencial para químicos, farmacéuticos, ingenieros y cualquier persona que trabaje con mezclas homogéneas.
Este artículo tiene como objetivo desmitificar el cálculo de solutos, explorando las diversas formas en que se puede expresar la concentración de una solución. Desde las unidades más comunes como la molaridad, hasta las concentraciones porcentuales y las empleadas para trazas, como las partes por millón, te guiaremos a través de las fórmulas, los conceptos clave y ejemplos prácticos. Prepárate para dominar el arte de la cuantificación en el laboratorio y más allá.
- ¿Qué es un Soluto y Cómo se Determina?
- Conceptos Clave de Concentración: Una Visión General
- Molaridad: La Concentración por Excelencia
- Cálculo de Gramos de Soluto a partir de Molaridad
- Molalidad: Una Alternativa Resistente a la Temperatura
- Concentraciones Porcentuales: Versatilidad en la Medida
- Partes por Millón (ppm) y Partes por Billón (ppb): Para Concentraciones Traza
- Dilución de Soluciones: Ajustando la Concentración
- Tabla Comparativa de Unidades de Concentración
- Preguntas Frecuentes sobre el Cálculo de Solutos
- Conclusión
¿Qué es un Soluto y Cómo se Determina?
Antes de sumergirnos en los cálculos, es vital entender qué es un soluto y cómo se comporta dentro de una solución. Un soluto es la sustancia que se disuelve en otra, el solvente, para formar una solución. Por ejemplo, en una solución de agua con sal, la sal es el soluto y el agua es el solvente. Cuando un sólido (soluto) se añade a un líquido (solvente), las fuerzas entre las partículas del soluto se superan, permitiendo que estas se mezclen con las partículas del solvente. Este proceso de mezcla se conoce como disolución y da como resultado la formación de una solución.
Para entender la cantidad de soluto, es importante conocer algunos términos clave:
- Solución: Una mezcla homogénea de un soluto y un solvente.
- Soluto: La sustancia que se disuelve.
- Solvente: El líquido en el que se disuelve el soluto.
- Soluble: Describe una sustancia que puede disolverse.
- Insoluble: Describe una sustancia que no puede disolverse.
- Solubilidad: Una medida de la cantidad máxima de soluto que puede disolverse en un volumen o masa dado de solvente a una temperatura específica.
- Solución saturada: Una solución en la que no se puede disolver más soluto a una temperatura dada. Cualquier soluto adicional se observaría como un sólido sin disolver.
La solubilidad de un soluto se mide típicamente como la masa en gramos que puede disolverse en 100 g de solvente a una temperatura dada. Por ejemplo, si la solubilidad del cloruro de aluminio en agua es de 45.8 g por 100 g de agua a 20°C, significa que esa es la cantidad máxima que se disolverá. Si se añade más, el exceso permanecerá sin disolver.
La solubilidad de un soluto puede determinarse experimentalmente midiendo la masa máxima de soluto que se puede añadir a una muestra de solvente antes de que comience a aparecer como un sólido sin disolver. Este valor puede variar y está influenciado por varios factores:
- Solvente utilizado: Algunos solventes son mejores para disolver ciertos sólidos que otros debido a la polaridad y las interacciones moleculares.
- Soluto disuelto: La naturaleza del soluto, su estructura y las fuerzas intermoleculares afectan su capacidad para disolverse.
- Temperatura: Generalmente, un aumento en la temperatura del solvente aumenta la solubilidad de los sólidos, ya que las partículas tienen más energía para superar las fuerzas intermoleculares y mezclarse.
Las curvas de solubilidad son gráficos que muestran la relación entre la temperatura y la solubilidad de un soluto, permitiendo predecir la cantidad de soluto que se disolverá a diferentes temperaturas.
Conceptos Clave de Concentración: Una Visión General
La concentración de una solución nos indica la cantidad de soluto disuelto en una cantidad dada de solución o solvente. Es una propiedad intensiva, lo que significa que no depende de la cantidad total de solución. Existen diversas formas de expresar la concentración, cada una útil para diferentes aplicaciones. A continuación, exploraremos las más comunes y cómo calcular el soluto en cada caso.
Molaridad: La Concentración por Excelencia
La molaridad (M) es la unidad de concentración más utilizada en química. Expresa los moles de soluto por litro de solución. Su fórmula es:
Molaridad (M) = Moles de Soluto / Volumen de Solución (L)
Para calcular la cantidad de moles de soluto o el volumen de solución, podemos reorganizar la fórmula. Por ejemplo, si conocemos la molaridad y el volumen de la solución, podemos calcular los moles de soluto:
Moles de Soluto = Molaridad (M) × Volumen de Solución (L)
Ejemplo 1: ¿Cuántos moles de NaOH hay en 2.50 L de una solución de NaOH 1.12 M?
Datos: Volumen de solución = 2.50 L, Concentración = 1.12 M NaOH
Cálculo: Moles de NaOH = 1.12 mol/L × 2.50 L = 2.80 moles de NaOH
Ejemplo 2: ¿Qué volumen de solución de HCl 0.211 M se necesita para proporcionar 0.400 mol de HCl?
Datos: Moles de HCl = 0.400 mol, Concentración = 0.211 M HCl
Cálculo: Volumen de Solución (L) = Moles de Soluto / Molaridad = 0.400 mol / 0.211 mol/L = 1.896 L de solución de HCl
Ejemplo 3: ¿Cuál es la molaridad (M) de una solución preparada disolviendo 50.0 g de NaOH en suficiente agua para hacer 250 mL de solución?
Primero, necesitamos convertir los gramos de NaOH a moles. La masa molar (MM) de NaOH es aproximadamente 22.99 (Na) + 15.99 (O) + 1.01 (H) = 40.00 g/mol.
Moles de NaOH = 50.0 g / 40.00 g/mol = 1.25 moles de NaOH
Luego, convertimos el volumen de la solución de mL a L: 250 mL = 0.250 L.

Molaridad = 1.25 moles / 0.250 L = 5.00 M NaOH
Cálculo de Gramos de Soluto a partir de Molaridad
A menudo, necesitamos saber cuántos gramos de soluto se requieren para preparar una solución de una molaridad y volumen específicos. La fórmula para esto es:
g de soluto = M · V(L) · MM
Donde:
- M: Concentración molar o molaridad de la solución, en mol/L.
- V(L): Volumen de la solución en litros.
- MM: Masa Molar del soluto (también conocido como 'peso fórmula' o 'peso molecular'), en g/mol.
Esta fórmula es una herramienta poderosa para la preparación precisa de soluciones en el laboratorio.
Molalidad: Una Alternativa Resistente a la Temperatura
La molalidad (m) es otra forma de expresar la concentración, definida como el número de moles de soluto disueltos en 1 kilogramo de solvente. Su unidad es mol/kg. Aunque el sistema SI considera el término 'molal' y el símbolo 'm' como obsoletos en favor de mol/kg, sigue siendo un concepto importante.
Molalidad (m) = Moles de Soluto / Kilogramos de Solvente
La principal ventaja de la molalidad es que, a diferencia de la molaridad, no se ve afectada por los cambios de temperatura. Esto se debe a que la masa (tanto del soluto como del solvente) no cambia con la temperatura, mientras que el volumen de una solución sí puede variar. Esto hace que la molalidad sea particularmente útil en estudios que implican cambios de temperatura, como los de propiedades coligativas (punto de ebullición, punto de congelación).
En soluciones acuosas cercanas a la temperatura ambiente, la diferencia entre molaridad y molalidad es insignificante, ya que la densidad del agua es aproximadamente 1 kg/L. Sin embargo, para otros solventes o temperaturas extremas, la distinción es crucial.
Concentraciones Porcentuales: Versatilidad en la Medida
Las concentraciones porcentuales son formas sencillas de expresar la cantidad de soluto en relación con la solución total. Se presentan en tres formatos principales:
1. Porcentaje Masa/Masa (% m/m)
Expresa la masa de soluto en cien unidades de masa de la solución.
Masa (%) = (masa de soluto (g) / masa de solución (g)) × 100
Es importante recordar que la masa de la solución es la suma de la masa del soluto y la masa del solvente.
Ejemplo: ¿Cuál es el % m/m de NaOH en una solución preparada disolviendo 10.0 g de NaOH en 100 g de agua?
Masa de soluto = 10.0 g NaOH
Masa de solvente = 100 g agua
Masa de solución = 10.0 g + 100 g = 110 g
Masa (%) = (10.0 g NaOH / 110 g solución) × 100 = 9.09% m/m NaOH
Ejemplo de aplicación inversa: Neosporin es una solución de neomicina al 3.5% m/m. ¿Cuántos gramos de neomicina hay en 50 g de ungüento?
3.5% m/m significa 3.5 g de neomicina por cada 100 g de solución.
Gramos de neomicina = (3.5 g neomicina / 100 g solución) × 50 g solución = 1.75 g de neomicina
2. Porcentaje Masa/Volumen (% m/v)
Expresa la masa de soluto en cien unidades de volumen de la solución.

Masa/Volumen (%) = (masa de soluto (g) / volumen de solución (mL)) × 100
Ejemplo: ¿Cuál es el % m/v de una solución de glucosa preparada disolviendo 50 g de glucosa en suficiente agua para hacer 1000 mL de solución?
Masa/Volumen (%) = (50 g glucosa / 1000 mL solución) × 100 = 5.0% m/v de glucosa
Ejemplo de aplicación inversa: ¿Cuántos gramos de antibiótico clindamicina hay en una cápsula de 45 mL de clindamicina al 1.0% (m/v)?
1.0% m/v significa 1.0 g de clindamicina por cada 100 mL de solución.
Gramos de clindamicina = (1.0 g clindamicina / 100 mL solución) × 45 mL solución = 0.45 g de clindamicina
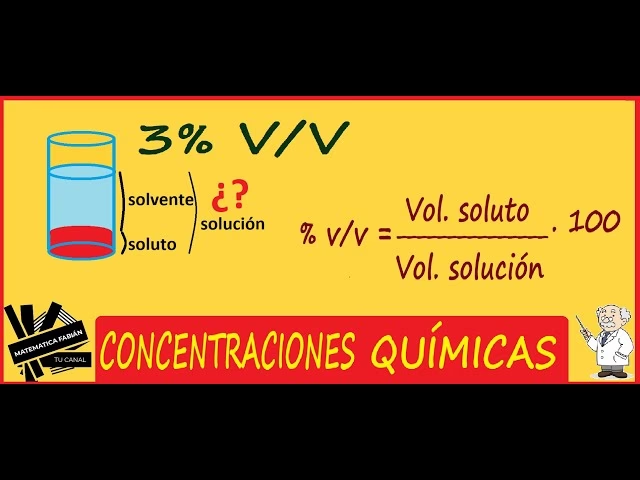
3. Porcentaje Volumen/Volumen (% v/v)
Expresa el volumen de soluto en cien unidades de volumen de la solución.
Volumen (%) = (volumen de soluto (mL) / volumen de solución (mL)) × 100
Ejemplo: ¿Cuál es el volumen % de extracto de rosa en una solución preparada disolviendo 14.0 mL de extracto de rosa en un solvente para hacer 200 mL de solución?
Volumen (%) = (14.0 mL extracto de rosa / 200 mL solución) × 100 = 7.0% v/v de extracto de rosa
Ejemplo de aplicación inversa: ¿Cuál es el volumen de bromo (Br2) en 250 mL de una solución de Br2 al 4.8% v/v en tetracloruro de carbono?
4.8% v/v significa 4.8 mL de Br2 por cada 100 mL de solución.
Volumen de Br2 = (4.8 mL Br2 / 100 mL solución) × 250 mL solución = 12 mL de Br2
Partes por Millón (ppm) y Partes por Billón (ppb): Para Concentraciones Traza
Cuando las concentraciones de soluto son muy bajas, como en el análisis de contaminantes en agua, se utilizan las unidades de partes por millón (ppm) y partes por billón (ppb).
Partes por Millón (ppm)
Las partes por millón (ppm) son un número o una relación que representa una fracción de un millón (10^6). Similar a los porcentajes, pueden ser masa/masa (m/m), volumen/volumen (v/v) o masa/volumen (m/v).
Concentración en ppm = (parte / total) × 10^6
Ejemplo: Una solución de NaCl de 50.0 g se disuelve en agua para hacer una solución de 500 g. ¿Cuál es el porcentaje de NaCl en la solución?
Esto es un ejemplo de porcentaje, pero si quisiéramos expresarlo en ppm:
Concentración en ppm (m/m) = (50.0 g NaCl / 500 g solución) × 10^6 = 100,000 ppm
Ejemplo práctico (m/v): El límite de acción de la EPA para el cobre es de 1.3 mg/L en agua potable. ¿Cuál es este límite en ppm de cobre m/v en el agua potable?
Sabemos que 1 L = 1000 mL y 1 mg = 0.001 g. Para ppm m/v, necesitamos gramos de soluto y mL de solución.
1.3 mg/L = 0.0013 g / 1000 mL
Concentración en ppm (m/v) = (0.0013 g cobre / 1000 mL solución) × 10^6 = 1.3 ppm (m/v) de cobre
Partes por Billón (ppb)
Las partes por billón (ppb) son un número o una relación expresada como una fracción de mil millones (10^9). Al igual que las ppm, pueden ser m/m, v/v o m/v.
Concentración en ppb = (parte / total) × 10^9
Ejemplo práctico (m/v): El límite de acción de la EPA para el plomo es de 0.015 mg/L en agua potable. ¿Cuál es este límite en ppb de plomo m/v en el agua potable?
0.015 mg/L = 0.000015 g / 1000 mL
Concentración en ppb (m/v) = (0.000015 g plomo / 1000 mL solución) × 10^9 = 15 ppb (m/v) de plomo
Dilución de Soluciones: Ajustando la Concentración
La dilución de una solución implica añadir más solvente para disminuir la concentración del soluto. Es un proceso común en el laboratorio para preparar soluciones de menor concentración a partir de soluciones madre más concentradas. Lo fundamental a recordar es que la cantidad de soluto permanece constante durante la dilución; solo el volumen de la solución cambia, lo que a su vez altera la concentración.
La relación que gobierna la dilución es la siguiente:
C1V1 = C2V2
Donde:
- C1: Concentración inicial de la solución.
- V1: Volumen inicial de la solución.
- C2: Concentración final de la solución después de la dilución.
- V2: Volumen final de la solución después de la dilución.
Es crucial que las unidades de concentración (C) y volumen (V) sean consistentes en ambos lados de la ecuación.
Ejemplo 1: ¿Qué volumen de HCl 11.3 M se necesita para preparar 250 mL de HCl 2.00 M?
Datos: C1 = 11.3 M HCl, C2 = 2.00 M HCl, V2 = 250 mL solución, Deseado: V1
Fórmula: C1V1 = C2V2, despejando V1: V1 = (C2 × V2) / C1
Cálculo: V1 = (2.00 M HCl × 250 mL solución) / 11.3 M HCl = 44.2 mL de solución
Ejemplo 2: ¿Cuál es la molaridad de la solución de NaOH preparada diluyendo 100 mL de solución de NaOH 0.521 M a 500 mL?
Datos: C1 = 0.521 M NaOH, V1 = 100 mL solución, V2 = 500 mL solución, Deseado: C2
Fórmula: C1V1 = C2V2, despejando C2: C2 = (C1 × V1) / V2
Cálculo: C2 = (0.521 M NaOH × 100 mL NaOH) / 500 mL NaOH = 0.104 M NaOH
Ejemplo 3: La dopamina se administra por vía intravenosa a un paciente para aumentar la presión arterial. ¿Cuántos mililitros (mL) de una solución de dopamina al 4.0% (m/v) se necesitan para preparar 250 mL de una solución al 0.030% (m/v)?
Datos: C1 = 4.0% (m/v), C2 = 0.030% (m/v), V2 = 250 mL solución, Deseado: V1
Fórmula: C1V1 = C2V2, despejando V1: V1 = (C2 × V2) / C1
Cálculo: V1 = (0.030% × 250 mL solución) / 4.0% = 1.875 mL de solución (redondeado a 1.9 mL o 2.0 mL según cifras significativas)
Tabla Comparativa de Unidades de Concentración
Para facilitar la comprensión y el uso, la siguiente tabla resume las principales unidades de concentración y sus aplicaciones:
| Unidad de Concentración | Definición | Fórmula | Aplicación Típica |
|---|---|---|---|
| Molaridad (M) | Moles de soluto por litro de solución | Moles de Soluto / Volumen de Solución (L) | Reacciones químicas, estequiometría |
| Molalidad (m) | Moles de soluto por kilogramo de solvente | Moles de Soluto / Kilogramos de Solvente | Propiedades coligativas, estudios con cambios de temperatura |
| Porcentaje Masa/Masa (% m/m) | Gramos de soluto por 100 gramos de solución | (masa de soluto / masa de solución) × 100 | Formulaciones farmacéuticas, análisis gravimétricos |
| Porcentaje Masa/Volumen (% m/v) | Gramos de soluto por 100 mililitros de solución | (masa de soluto / volumen de solución) × 100 | Soluciones médicas, preparados líquidos |
| Porcentaje Volumen/Volumen (% v/v) | Mililitros de soluto por 100 mililitros de solución | (volumen de soluto / volumen de solución) × 100 | Mezclas de líquidos, disolventes orgánicos |
| Partes por Millón (ppm) | Partes de soluto por 1 millón de partes de solución | (parte / total) × 10^6 | Contaminantes ambientales, análisis de trazas |
| Partes por Billón (ppb) | Partes de soluto por 1 mil millones de partes de solución | (parte / total) × 10^9 | Contaminantes ultratraza, toxicología |
Preguntas Frecuentes sobre el Cálculo de Solutos
¿Cuál es la diferencia fundamental entre molaridad y molalidad?
La diferencia clave radica en el denominador de sus fórmulas. La molaridad utiliza el volumen de la solución (litros), mientras que la molalidad utiliza la masa del solvente (kilogramos). Esto hace que la molaridad sea sensible a los cambios de temperatura (ya que el volumen varía con la temperatura), mientras que la molalidad no lo es, lo que la hace preferible para estudios donde la temperatura es una variable importante.
¿Por qué es importante conocer la concentración de una solución?
Conocer la concentración es vital para garantizar la precisión y la seguridad en una amplia gama de aplicaciones. En química, permite realizar reacciones estequiométricas precisas. En medicina, asegura la dosis correcta de medicamentos. En la industria, controla la calidad de los productos y la eficiencia de los procesos. En el monitoreo ambiental, permite detectar y cuantificar contaminantes para proteger la salud pública.
¿Cómo convierto de una unidad de concentración a otra?
La conversión entre unidades de concentración a menudo requiere conocer la densidad de la solución y la masa molar del soluto. Por ejemplo, para convertir de molaridad a porcentaje m/v, necesitarías la masa molar para convertir moles a gramos, y luego ajustar por el volumen. Para convertir entre unidades basadas en masa y volumen, la densidad de la solución es esencial.
¿Qué significa que una solución esté saturada?
Una solución saturada es aquella que ha disuelto la máxima cantidad de soluto posible a una temperatura y presión dadas. Si se añade más soluto a una solución ya saturada, este no se disolverá y permanecerá como un sólido en el fondo del recipiente. La solubilidad de una sustancia es la medida de la concentración de una solución saturada.
Conclusión
El cálculo de solutos y la expresión de la concentración son pilares fundamentales de la química y disciplinas afines. Desde la preparación de soluciones cotidianas hasta el análisis de sustancias a nivel de trazas, comprender las diversas unidades (molaridad, molalidad, porcentajes, ppm, ppb) y sus respectivas fórmulas es indispensable. Dominar estos conceptos no solo permite la precisión en el laboratorio, sino que también fomenta una comprensión más profunda de cómo las sustancias interactúan y se distribuyen en las mezclas. Con esta guía, esperamos haber proporcionado las herramientas necesarias para que te sientas seguro y competente al abordar cualquier cálculo de solutos en el futuro.
Si quieres conocer otros artículos parecidos a Cálculo de Solutos: Guía Definitiva de Concentraciones puedes visitar la categoría Química.

