04/10/2025
La sal, ese ingrediente omnipresente en nuestras cocinas, es mucho más que un simple condimento. Detrás de su sabor característico y su apariencia cristalina, se esconde un universo fascinante de química, enlaces iónicos y propiedades sorprendentes. En este artículo, desentrañaremos los secretos de la sal, no solo la que usamos a diario, sino también la amplia familia de compuestos químicos conocidos como "sales", explorando su composición, su formación y su papel indispensable en innumerables procesos naturales e industriales. Prepárese para un viaje que transformará su percepción de este humilde, pero poderoso, compuesto.

¿Qué es la Sal Químicamente? La Fórmula Secreta de NaCl
Cuando hablamos de "sal" en el contexto culinario, nos referimos casi exclusivamente al cloruro de sodio, cuya fórmula química es NaCl. Esta fórmula, aparentemente simple, encierra una estructura fundamental de la química: un compuesto iónico. Para entenderla, debemos adentrarnos en el mundo de los iones.
Un ion es un átomo que ha perdido o ganado uno o más electrones, adquiriendo así una carga eléctrica. En el caso del NaCl, intervienen dos elementos clave:
- Sodio (Na): Un metal alcalino altamente reactivo que, en su estado neutro, tiene un electrón en su capa más externa. Tiende a perder este electrón para alcanzar una configuración electrónica estable, formando un ion con carga positiva, el catión sodio (Na+).
- Cloro (Cl): Un no metal del grupo de los halógenos, que tiene siete electrones en su capa más externa. Tiende a ganar un electrón para completar su octeto, formando un ion con carga negativa, el anión cloruro (Cl-).
La magia ocurre cuando estos dos iones, con cargas opuestas, se atraen mutuamente a través de una fuerza electrostática muy potente. Esta atracción da lugar a un enlace iónico, formando una red cristalina altamente organizada en lugar de moléculas discretas. Es por eso que la sal de mesa se presenta en pequeños cristales: cada cristal es una vasta red tridimensional de iones Na+ y Cl- alternados, mantenidos firmemente unidos. La fórmula NaCl representa la proporción más simple de estos iones en la red cristalina, es decir, un ion sodio por cada ion cloruro, asegurando que el compuesto sea eléctricamente neutro en su conjunto. Esta neutralidad eléctrica es una característica definitoria de todas las sales.
Más Allá de la Mesa: La Diversidad de las Sales
Si bien el cloruro de sodio es la sal más conocida, el término "sal" en química se refiere a una clase mucho más amplia de compuestos. Una sal se define como un compuesto iónico que resulta de la reacción de neutralización entre un ácido y una base, produciendo, además de la sal, moléculas de agua. La ecuación general que describe esta reacción es:
Ácido + Base → Sal + Agua
Esta definición amplía enormemente el espectro de lo que consideramos una sal. Las sales están compuestas por un catión (que no es H+) y un anión (que no es OH-). Estos iones pueden ser inorgánicos u orgánicos, y pueden ser monoatómicos (como Cl-) o poliatómicos (como SO₄²⁻ o NO₃⁻).
Existen miles de sales diferentes, cada una con propiedades y aplicaciones únicas. Se pueden clasificar de varias maneras, pero una clasificación común se basa en su comportamiento en solución acuosa:
- Sales Neutras: Son aquellas que, al disolverse en agua, no alteran significativamente el pH de la solución. Se forman generalmente a partir de la reacción de un ácido fuerte con una base fuerte. El cloruro de sodio (NaCl) es un ejemplo clásico de sal neutra.
- Sales Ácidas: Son aquellas que, al disolverse en agua, producen una solución ácida (pH < 7). Esto ocurre cuando el catión de la sal es el ácido conjugado de una base débil, o cuando el anión de la sal puede donar un protón. Un ejemplo es el bisulfato de sodio (NaHSO₄).
- Sales Alcalinas (o Básicas): Son aquellas que, al disolverse en agua, producen una solución básica (pH > 7). Esto sucede cuando el anión de la sal es la base conjugada de un ácido débil. Un ejemplo es el carbonato de sodio (Na₂CO₃).
Es importante mencionar que existen también los zwitteriones, que son moléculas que contienen tanto un centro aniónico como uno catiónico en la misma molécula, pero no se consideran sales en el sentido tradicional. Ejemplos de zwitteriones incluyen los aminoácidos, que son los bloques constructores de las proteínas.
Para ilustrar la diversidad de las sales, aquí presentamos una tabla con diez ejemplos comunes y sus usos:
| Nombre de la Sal | Fórmula Química | Tipo de Sal (Ejemplo) | Uso Común |
|---|---|---|---|
| Cloruro de Sodio | NaCl | Neutra | Condimento, preservación de alimentos, suero fisiológico. |
| Sulfato de Cobre (II) | CuSO₄ | Ácida | Fungicida, algicida, electrolito en galvanoplastia. |
| Carbonato de Calcio | CaCO₃ | Alcalina | Antiácido, material de construcción (mármol, caliza), suplemento de calcio. |
| Cloruro de Níquel (II) | NiCl₂ | Ácida | Galvanoplastia, catalizador en química orgánica. |
| Permanganato de Potasio | KMnO₄ | Neutra (oxidante) | Agente oxidante fuerte, desinfectante, tratamiento de agua. |
| Dicromato de Potasio | K₂Cr₂O₇ | Neutra (oxidante) | Agente oxidante, limpieza de material de laboratorio. |
| Sulfato de Magnesio Heptahidratado | MgSO₄·7H₂O (Sales de Epsom) | Neutra | Laxante, sales de baño, suplemento de magnesio. |
| Cromato de Sodio | Na₂CrO₄ | Alcalina | Inhibidor de corrosión, pigmento. |
| Bisulfato de Sodio | NaHSO₄ | Ácida | Limpiador de inodoros, aditivo alimentario (regulador de acidez). |
| Nitrato de Plata | AgNO₃ | Neutra | Reacciones de precipitación, fotografía, medicina (antiséptico). |
Propiedades Fascinantes de las Sales
Las sales, como clase de compuestos, comparten una serie de propiedades características que derivan de su naturaleza iónica. Comprender estas propiedades es crucial para predecir su comportamiento y sus aplicaciones.
Una de las propiedades más notables es su alto punto de fusión. Debido a las fuertes fuerzas electrostáticas entre los iones en la red cristalina, se requiere una gran cantidad de energía para romper estos enlaces y transformar la sal de un sólido a un líquido. Por ejemplo, el NaCl tiene un punto de fusión de 801 °C.

Otra propiedad fundamental es su conductividad eléctrica. En estado sólido, la mayoría de las sales son aislantes, lo que significa que no conducen la electricidad. Esto se debe a que los iones están fijos en la red cristalina y no pueden moverse libremente para transportar la carga eléctrica. Sin embargo, cuando las sales se funden (se convierten en líquido) o se disuelven en un solvente polar como el agua, sus iones se disocian y se mueven libremente. En este estado, los iones actúan como portadores de carga, permitiendo que la solución o el líquido fundido conduzcan la electricidad de manera eficiente. Por esta razón, las soluciones de sales y las sales fundidas se conocen como electrolitos, un concepto vital en campos como la biología (equilibrio electrolítico en el cuerpo) y la ingeniería (baterías, galvanoplastia).
Además, la mayoría de las sales son solubles en agua hasta cierto punto, aunque la solubilidad varía enormemente de una sal a otra. Esta solubilidad se debe a la capacidad de las moléculas de agua para rodear y separar los iones individuales de la red cristalina, un proceso llamado hidratación. La solubilidad de una sal es un factor crítico en muchas aplicaciones, desde la química analítica hasta los procesos industriales.
La Sal en el Mundo Real: Aplicaciones y Cálculos
La importancia de las sales se extiende mucho más allá de la cocina. Son componentes vitales en la industria, la medicina, la agricultura y la investigación científica.
En la industria química, las sales son materias primas esenciales para la fabricación de una vasta gama de productos, desde plásticos y fertilizantes hasta detergentes y productos farmacéuticos. Por ejemplo, el cloruro de sodio se utiliza para producir cloro gaseoso e hidróxido de sodio, dos productos químicos industriales fundamentales.
En la medicina, las sales son cruciales. El suero fisiológico es una solución de NaCl que se utiliza para rehidratar a los pacientes. Las sales de Epsom (sulfato de magnesio) se usan como laxantes y para aliviar dolores musculares. Muchos medicamentos son sales o contienen sales para mejorar su solubilidad y biodisponibilidad.
En la agricultura, los fertilizantes son a menudo sales que proporcionan nutrientes esenciales como nitratos, fosfatos y potasio a los cultivos. La comprensión de la química de estas sales es vital para optimizar la nutrición de las plantas.
Para los cálculos en química, las sales son objetos de estudio constantes. Los químicos y los estudiantes utilizan calculadoras para:
- Determinar la masa molar de una sal a partir de su fórmula química y las masas atómicas de sus elementos constituyentes. Esto es fundamental para la estequiometría de las reacciones.
- Calcular la concentración de soluciones salinas (por ejemplo, molaridad, molalidad, porcentaje en masa) para preparar soluciones con una exactitud específica. Esto es crucial en cualquier laboratorio.
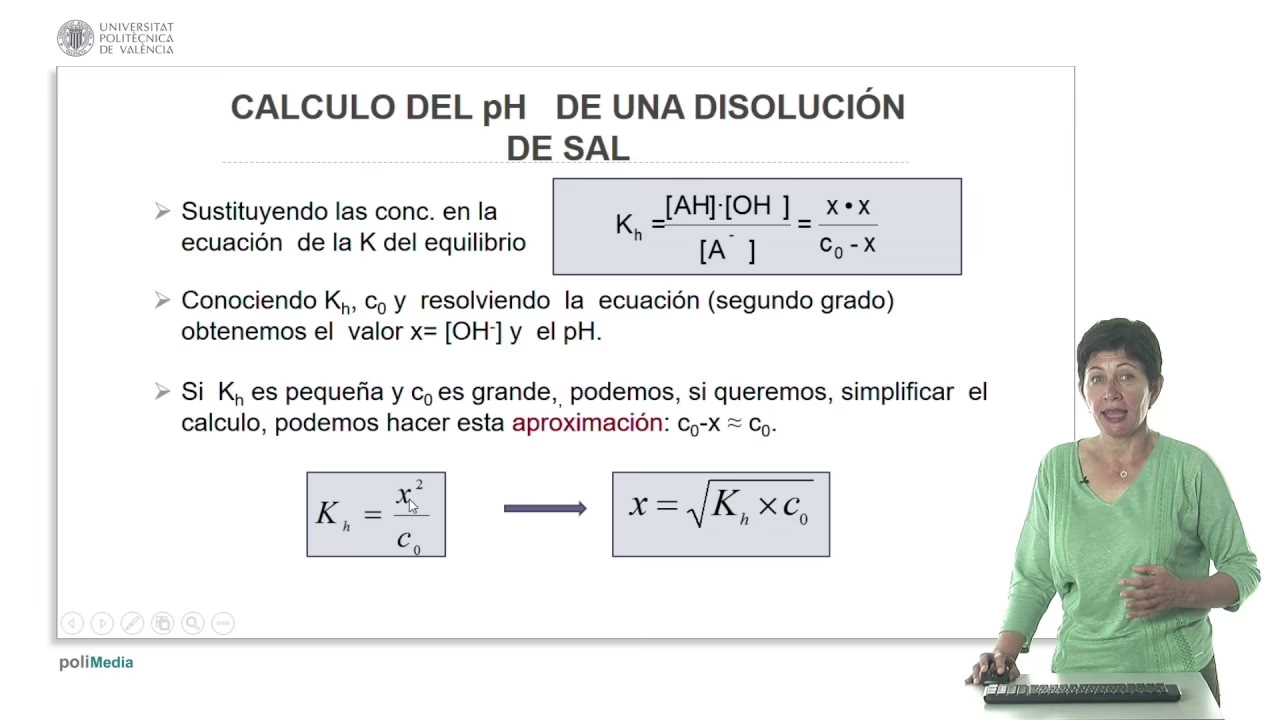
- Realizar cálculos de pH para soluciones de sales ácidas o alcalinas, lo que ayuda a entender su comportamiento en el agua y su impacto en sistemas biológicos o ambientales.
- Predecir la solubilidad de sales en diferentes condiciones de temperatura o la presencia de otros iones, utilizando constantes de producto de solubilidad (Ksp).
- Determinar la cantidad de reactivos necesarios o productos formados en reacciones de neutralización o precipitación que involucran sales.
La precisión en estos cálculos es fundamental para garantizar la seguridad, la eficiencia y la calidad en cualquier proceso químico o biológico que involucre sales.

Preguntas Frecuentes sobre las Sales
¿Qué diferencia hay entre un átomo y un ion?
Un átomo es la unidad básica de la materia que mantiene la identidad química de un elemento. Es eléctricamente neutro, con un número igual de protones (cargas positivas) y electrones (cargas negativas). Un ion, por otro lado, es un átomo (o grupo de átomos) que ha ganado o perdido uno o más electrones, adquiriendo así una carga eléctrica neta (positiva si pierde electrones, negativa si los gana). Las sales están compuestas por iones.
¿Por qué la sal se disuelve en agua?
La sal se disuelve en agua porque el agua es un solvente polar. Sus moléculas tienen una distribución de carga desigual (el oxígeno es ligeramente negativo y los hidrógenos ligeramente positivos). Estas cargas parciales del agua son lo suficientemente fuertes como para atraer y rodear los iones cargados de la sal (Na+ y Cl-), separándolos de la red cristalina y dispersándolos en la solución.
¿Todas las sales son comestibles?
¡Absolutamente no! La sal de mesa (NaCl) es comestible y esencial para la vida en pequeñas cantidades. Sin embargo, muchas otras sales son tóxicas, corrosivas o irritantes y no deben ser ingeridas. Por ejemplo, el cianuro de potasio (KCN) es una sal extremadamente tóxica, y el sulfato de cobre (CuSO₄) es un veneno. Siempre es crucial conocer la composición química de cualquier sustancia antes de manipularla o consumirla.
¿Cómo se determina si una sustancia es una sal?
Químicamente, una sustancia se determina como una sal si es un compuesto iónico formado por un catión que no es H+ y un anión que no es OH-. Generalmente, se forman de la reacción de un ácido y una base. Sus propiedades físicas, como la estructura cristalina, el alto punto de fusión y la conductividad eléctrica en estado fundido o en solución acuosa, también son indicadores clave.
¿La sal es un mineral?
Sí, el cloruro de sodio (NaCl) se encuentra en la naturaleza como el mineral halita. Es un mineral evaporítico, lo que significa que se forma por la evaporación de agua salada. Otros compuestos que llamamos sales también pueden encontrarse como minerales en la corteza terrestre, como la calcita (carbonato de calcio) o el yeso (sulfato de calcio dihidratado).
Desde el salero en nuestra mesa hasta las intrincadas reacciones químicas en nuestros cuerpos y en la industria, la sal es un pilar fundamental de nuestro mundo. Su fórmula simple esconde una complejidad química asombrosa, y su diversidad abarca desde compuestos inofensivos hasta sustancias altamente reactivas. Comprender la naturaleza iónica de las sales, sus propiedades y cómo se forman es esencial no solo para los químicos, sino para cualquiera que desee apreciar la riqueza del universo que nos rodea y la importancia de los cálculos que nos permiten manipular y aprovechar sus infinitas posibilidades. La próxima vez que vea un cristal de sal, recuerde la fascinante historia química que hay detrás de él.
Si quieres conocer otros artículos parecidos a Descifrando la Sal: Más Allá del Sabor, la Química de NaCl y Otras Sales puedes visitar la categoría Química.