25/10/2022
En el fascinante mundo de la química, los elementos que nos rodean no son tan uniformes como a primera vista podría parecer. Cada átomo de un mismo elemento comparte el mismo número de protones, lo que define su identidad, pero su número de neutrones puede variar. Estas variaciones dan lugar a lo que conocemos como isótopos, versiones de un mismo elemento con masas atómicas ligeramente diferentes. Comprender la proporción en que estos isótopos se encuentran en la naturaleza, lo que llamamos su abundancia relativa, es crucial para una infinidad de cálculos y aplicaciones científicas. Este artículo desglosará cómo puedes determinar el porcentaje de un isótopo, proporcionando las herramientas y ejemplos necesarios para dominar este concepto fundamental.
Desde la base de la tabla periódica hasta los complejos análisis en laboratorios avanzados, la abundancia isotópica es un pilar. No solo influye en la masa atómica promedio que vemos en la tabla periódica, sino que también es vital en campos como la datación por carbono, la medicina nuclear y el estudio del cambio climático. Acompáñanos en este viaje para desvelar los secretos detrás del cálculo de la abundancia de isótopos, transformando un concepto aparentemente complejo en un proceso claro y sistemático.
- Entendiendo los Isótopos: La Base de Todo Cálculo
- La Clave: Abundancia Relativa de Isótopos
- Cálculo de la Abundancia Isótopica Paso a Paso
- Cálculo de la Masa Atómica Promedio a partir de la Abundancia Isótopica
- Aplicaciones de los Isótopos en la Vida Cotidiana y la Ciencia
- Preguntas Frecuentes (FAQ)
- Conclusión
Entendiendo los Isótopos: La Base de Todo Cálculo
Antes de sumergirnos en los cálculos, es esencial tener una comprensión sólida de qué son los isótopos y cómo se relacionan con la estructura atómica. Esta base te permitirá abordar los problemas de abundancia con total claridad y confianza.
¿Qué es un Isótopo?
Los isótopos son átomos de un mismo elemento que poseen el mismo número de protones, pero un número diferente de neutrones. Esta variación en el número de neutrones es lo que provoca que los isótopos de un mismo elemento tengan masas atómicas distintas. A pesar de esta diferencia en masa, al tener el mismo número de protones (y por ende, el mismo número atómico), mantienen las mismas propiedades químicas. Es como tener diferentes modelos de un mismo coche: todos son el mismo modelo, pero pueden tener motores ligeramente diferentes que afectan su peso.
Notación de los Isótopos
Para identificar los isótopos, los científicos utilizan una notación específica que incluye el símbolo del elemento y su número de masa. El número de masa (la suma de protones y neutrones) se escribe como un superíndice antes del símbolo del elemento. Por ejemplo, el carbono-14 se escribe como 14C, donde '14' es el número de masa y 'C' es el símbolo del carbono. Otro ejemplo común es el hidrógeno, que tiene tres isótopos: el protio (1H), el deuterio (2H) y el tritio (3H).
Estructura Atómica: Protones, Neutrones y Electrones
Para recordar, un átomo se compone de un núcleo central y electrones que orbitan alrededor de él. El núcleo contiene:
- Protones: Partículas con carga positiva que definen el número atómico del elemento y, por lo tanto, su identidad.
- Neutrones: Partículas sin carga (neutras) que contribuyen a la masa del átomo. La variación en su número es lo que crea los isótopos.
Los electrones, con carga negativa, orbitan el núcleo y su número suele ser igual al de protones en un átomo neutro, equilibrando la carga eléctrica del átomo. Es importante destacar que los neutrones, al ser neutros, pueden variar en número sin alterar la identidad química del elemento, solo su masa. Esta variación de masa es lo que da lugar a los isótopos y es el punto central de nuestro cálculo de abundancia.
La Clave: Abundancia Relativa de Isótopos
La abundancia relativa, o abundancia isotópica, se refiere al porcentaje o la proporción en que cada isótopo de un elemento se encuentra en una muestra natural. Esta es una medida crucial porque los diferentes isótopos de un elemento no suelen existir en la misma cantidad en la naturaleza. Algunos son mucho más comunes que otros, y esta proporción es lo que determina la masa atómica promedio de un elemento que se lista en la tabla periódica.
Por ejemplo, el mercurio tiene siete isótopos naturales, y sus abundancias varían significativamente, desde un 0.146% para el 196Hg hasta un 29.80% para el 202Hg. La suma de las abundancias relativas de todos los isótopos estables de un elemento siempre debe ser igual al 100 por ciento.
Espectrometría de Masas: La Herramienta Crucial
La principal técnica utilizada por los científicos para determinar la abundancia relativa de cada isótopo es la espectrometría de masas. Este método permite separar los iones de los diferentes isótopos de un elemento basándose en su relación masa-carga. El espectrómetro de masas genera un "espectro" que muestra la abundancia relativa de cada isótopo en función de su número de masa, proporcionando así los datos necesarios para nuestros cálculos.
Cálculo de la Abundancia Isótopica Paso a Paso
Para determinar la abundancia relativa de isótopos, especialmente cuando solo se conocen las masas de los isótopos y la masa atómica promedio del elemento, se sigue un procedimiento algebraico. Aquí te presentamos los pasos detallados:
Paso 1: Identificar la Masa Atómica Promedio del Elemento
El primer paso es consultar la tabla periódica para encontrar la masa atómica promedio del elemento en cuestión. Este valor es un promedio ponderado de las masas de todos sus isótopos naturales, considerando su abundancia. Es el dato clave que nos permitirá establecer la ecuación.

Paso 2: Establecer la Ecuación de Abundancia Relativa
La fórmula general para un elemento con dos isótopos es la siguiente:
(M1)(x) + (M2)(1-x) = M(E)
- M1: Denota la masa atómica del primer isótopo.
- x: Representa la abundancia relativa (en forma decimal) del primer isótopo. Este es el valor desconocido que queremos encontrar.
- M2: Denota la masa atómica del segundo isótopo.
- (1-x): Representa la abundancia relativa (en forma decimal) del segundo isótopo. Dado que las abundancias de todos los isótopos deben sumar 1 (o 100%), si 'x' es la abundancia del primero, '1-x' será la del segundo.
- M(E): Denota la masa atómica promedio del elemento, obtenida de la tabla periódica.
Esta ecuación se basa en el principio de que la masa atómica promedio es la suma de las masas de cada isótopo multiplicadas por su respectiva abundancia. Es una media ponderada.
Paso 3: Resolver la Ecuación para 'x'
Una vez establecida la ecuación, el siguiente paso es resolverla algebraicamente para encontrar el valor de 'x'.
a. Aplicar la Propiedad Distributiva:
M1x + M2 - M2x = M(E)
b. Agrupar Términos Similares:
(M1 - M2)x + M2 = M(E)
c. Despejar 'x':
(M1 - M2)x = M(E) - M2
x = (M(E) - M2) / (M1 - M2)
Paso 4: Determinar el Porcentaje de Abundancia
El valor de 'x' que obtendrás en el Paso 3 será un número decimal (entre 0 y 1). Para expresarlo como un porcentaje, simplemente multiplícalo por 100.
Porcentaje de abundancia del isótopo 1 = x * 100%
Y para el segundo isótopo:
Porcentaje de abundancia del isótopo 2 = (1 - x) * 100%
Ejemplos Resueltos de Cálculo de Abundancia Isótopica
Veamos cómo aplicar estos pasos con ejemplos prácticos para consolidar tu comprensión.
Ejemplo 1: Nitrógeno
Determina la abundancia relativa de los isótopos de nitrógeno si las masas de nitrógeno-14 (14N) son 14.003 uma y las de nitrógeno-15 (15N) son 15.000 uma. La masa atómica promedio del nitrógeno es 14.007 uma.
Solución:
- Masa atómica promedio del Nitrógeno (M(E)) = 14.007 uma
- Masa del isótopo 1 (M1, 14N) = 14.003 uma
- Masa del isótopo 2 (M2, 15N) = 15.000 uma
- Abundancia relativa de 14N = x (desconocida)
- Abundancia relativa de 15N = (1-x) (desconocida)
Aplicando la fórmula (M1)(x) + (M2)(1-x) = M(E):
14.003(x) + 15.000(1 - x) = 14.007
14.003x + 15.000 - 15.000x = 14.007
Combina términos similares:
(14.003 - 15.000)x + 15.000 = 14.007
-0.997x + 15.000 = 14.007
Resta 15.000 de ambos lados:
-0.997x = 14.007 - 15.000
-0.997x = -0.993
Divide por -0.997:
x = -0.993 / -0.997
x ≈ 0.996
Por lo tanto, la abundancia en porcentaje para 'x' (14N) es 0.996 * 100% = 99.6%.
Y para (1-x) (15N) es (1 - 0.996) * 100% = 0.004 * 100% = 0.4%.
La abundancia del isótopo nitrógeno-14 es 99.6%, mientras que la abundancia del isótopo nitrógeno-15 es 0.4%.
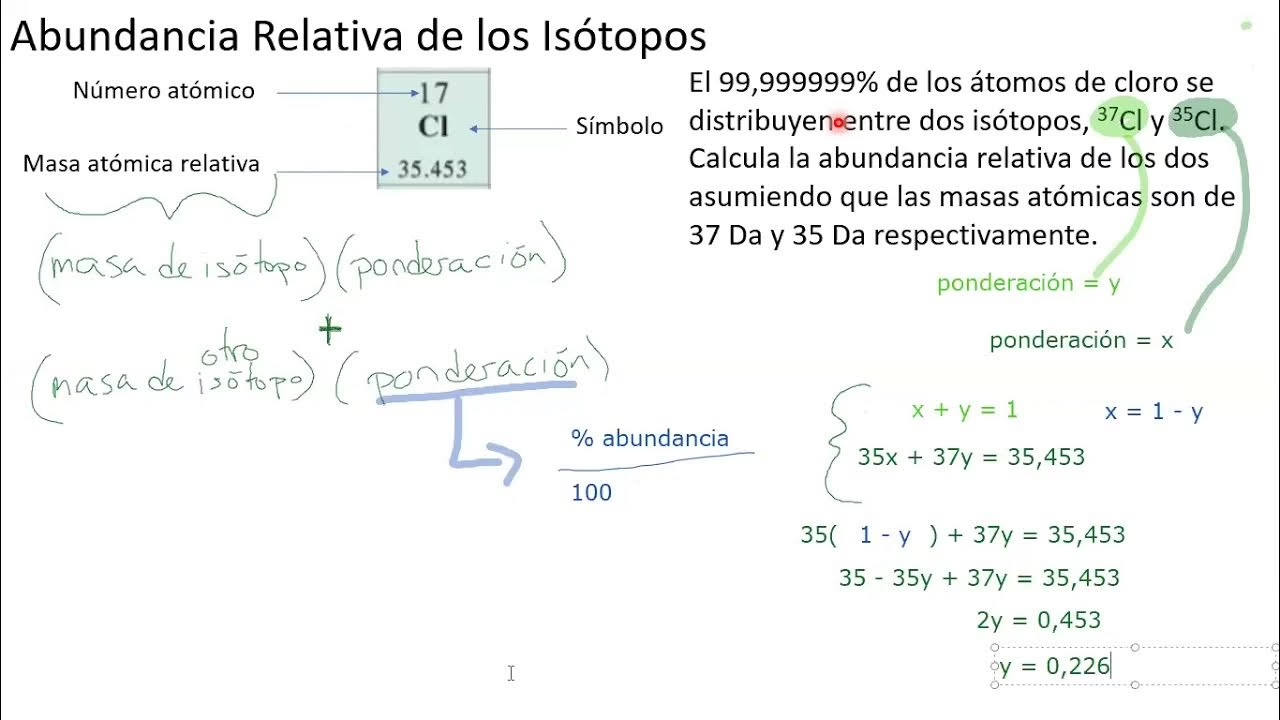
Ejemplo 2: Cloro
Determina el porcentaje de abundancia de los isótopos de cloro, 35Cl y 37Cl, dado que la masa atómica promedio del cloro es 35.45 uma.

Solución:
- Masa atómica promedio del Cloro (M(E)) = 35.45 uma
- Masa del isótopo 1 (M1, 35Cl) = 35 uma (se asume el número de masa como la masa atómica para simplificar, a menos que se den valores más precisos)
- Masa del isótopo 2 (M2, 37Cl) = 37 uma (se asume el número de masa como la masa atómica)
- Abundancia relativa de 35Cl = x (desconocida)
- Abundancia relativa de 37Cl = (1-x) (desconocida)
Aplicando la fórmula (M1)(x) + (M2)(1-x) = M(E):
35(x) + 37(1 - x) = 35.45
35x + 37 - 37x = 35.45
Combina términos similares:
(35 - 37)x + 37 = 35.45
-2x + 37 = 35.45
Resta 37 de ambos lados:
-2x = 35.45 - 37
-2x = -1.55
Divide por -2:
x = -1.55 / -2
x = 0.775
Por lo tanto, la abundancia en porcentaje para 'x' (35Cl) es 0.775 * 100% = 77.5%.
Y para (1-x) (37Cl) es (1 - 0.775) * 100% = 0.225 * 100% = 22.5%.
La abundancia del isótopo cloro-35 es 77.5%, mientras que la abundancia del isótopo cloro-37 es 22.5%.
Tabla Comparativa de los Ejemplos
| Elemento | Isótopo 1 (Masa) | Abundancia (%) | Isótopo 2 (Masa) | Abundancia (%) | Masa Atómica Promedio (uma) |
|---|---|---|---|---|---|
| Nitrógeno | 14N (14.003 uma) | 99.6% | 15N (15.000 uma) | 0.4% | 14.007 |
| Cloro | 35Cl (35 uma) | 77.5% | 37Cl (37 uma) | 22.5% | 35.45 |
Cálculo de la Masa Atómica Promedio a partir de la Abundancia Isótopica
Aunque el enfoque principal de este artículo es cómo encontrar la abundancia, es importante entender la relación inversa: cómo se calcula la masa atómica promedio si se conocen las masas de los isótopos y sus abundancias. Este es el principio subyacente de la masa atómica que aparece en la tabla periódica.
Para calcular la masa atómica promedio de un elemento, se multiplica la masa de cada isótopo por su abundancia (expresada como decimal) y luego se suman todos los productos.
Masa Atómica Promedio = (Masa Isótopo 1 × Abundancia 1) + (Masa Isótopo 2 × Abundancia 2) + ...
Por ejemplo, usando los datos del cloro:
- Masa 35Cl = 35 uma, Abundancia 35Cl = 77.5% (0.775)
- Masa 37Cl = 37 uma, Abundancia 37Cl = 22.5% (0.225)
Masa Atómica Promedio de Cloro = (35 uma × 0.775) + (37 uma × 0.225)
Masa Atómica Promedio de Cloro = 27.125 + 8.325
Masa Atómica Promedio de Cloro = 35.45 uma
Este cálculo demuestra cómo la masa atómica que consultamos en la tabla periódica es, de hecho, un valor ponderado que refleja la mezcla natural de los isótopos de un elemento. Es un testimonio de la precisión con la que la química puede describir la composición de la materia.
Aplicaciones de los Isótopos en la Vida Cotidiana y la Ciencia
La capacidad de comprender y calcular la abundancia de isótopos va mucho más allá de los ejercicios de química. Los isótopos son herramientas invaluables en diversas disciplinas, impactando directamente nuestra vida y el conocimiento científico.
Aplicaciones Médicas de los Isótopos
En el campo de la medicina, los isótopos, particularmente los radiactivos, son fundamentales. Un ejemplo destacado es el tecnecio-99m (99mTc), un isótopo radiactivo utilizado en medicina nuclear para técnicas de diagnóstico por imágenes, como la tomografía por emisión de fotón único (SPECT). El tecnecio-99m emite rayos gamma, que permiten a los profesionales médicos visualizar órganos internos e identificar anomalías con una claridad asombrosa, ayudando en la detección temprana de enfermedades.
Isótopos en las Ciencias Ambientales
Los isótopos también son esenciales para comprender el medio ambiente y los procesos naturales. El isótopo estable oxígeno-18 (18O), por ejemplo, se utiliza en estudios ambientales para rastrear el origen y las vías del agua, estudiar los ciclos hidrológicos y obtener información sobre el cambio climático. El análisis isotópico de los núcleos de hielo, por ejemplo, proporciona información valiosa sobre las condiciones climáticas pasadas y los cambios ambientales a largo plazo, revelando la historia de nuestro planeta.

Otro uso notable es la datación por carbono-14 (14C), que permite a los arqueólogos determinar la edad de artefactos antiguos y fósiles. Al medir la cantidad de carbono-14 restante en una muestra orgánica, pueden estimar cuándo murió el organismo, lo que es crucial para reconstruir la historia de la vida en la Tierra. Estas aplicaciones demuestran la versatilidad y la importancia de los isótopos en la comprensión de nuestro mundo.
Preguntas Frecuentes (FAQ)
A continuación, respondemos algunas de las preguntas más comunes sobre los isótopos y su abundancia.
¿Cómo se sabe la masa de un isótopo individual?
Las masas de los isótopos individuales se determinan con alta precisión mediante la espectrometría de masas. Esta técnica mide la relación masa-carga de los iones, lo que permite calcular la masa exacta de cada isótopo.
¿Por qué la abundancia de isótopos suma siempre 100%?
La abundancia relativa de los isótopos de un elemento representa la proporción de cada isótopo presente en una muestra natural. Dado que estos isótopos son las únicas formas de ese elemento que existen naturalmente, la suma de sus porcentajes individuales debe abarcar el total de la muestra, es decir, el 100%.
¿Cuál es la diferencia entre masa atómica y masa atómica promedio?
La masa atómica (o masa isotópica) se refiere a la masa de un único isótopo específico de un elemento (por ejemplo, la masa de un átomo de 14N). La masa atómica promedio (o peso atómico) es la media ponderada de las masas de todos los isótopos naturales de un elemento, tomando en cuenta sus respectivas abundancias. Es el valor que se encuentra en la tabla periódica y es el más relevante para la mayoría de los cálculos químicos.
¿Los isótopos tienen las mismas propiedades químicas?
Sí, los isótopos de un mismo elemento tienen prácticamente las mismas propiedades químicas porque estas están determinadas por el número de protones (y por lo tanto, el número de electrones) en el átomo, que es idéntico para todos los isótopos de un elemento. La única diferencia es su masa, lo que puede influir ligeramente en las tasas de reacción (efectos isotópicos cinéticos) o en las propiedades físicas como la densidad.
Conclusión
Dominar el cálculo de la abundancia de isótopos es una habilidad fundamental en química y ciencias afines. Hemos explorado no solo qué son los isótopos y cómo se identifican, sino también el método paso a paso para determinar su abundancia relativa a partir de la masa atómica promedio de un elemento. Desde la comprensión de la estructura atómica hasta la aplicación de fórmulas algebraicas, este proceso revela la composición precisa de los elementos en la naturaleza.
La importancia de los isótopos se extiende mucho más allá del aula, con aplicaciones prácticas que abarcan desde el diagnóstico médico hasta la investigación ambiental y la datación histórica. Al entender cómo se "pesan" y se "cuentan" estas variantes atómicas, obtenemos una visión más profunda de la materia que nos rodea y de los complejos procesos que ocurren en el universo. Esperamos que este artículo te haya proporcionado una comprensión clara y herramientas prácticas para desentrañar los secretos de la abundancia isotópica.
Si quieres conocer otros artículos parecidos a Descubre la Abundancia de Isótopos con Precisión puedes visitar la categoría Química.
