24/03/2022
En el vasto universo de la química, comprender la fuerza de ácidos y bases es fundamental. No todas las sustancias ácidas o básicas se comportan de la misma manera en solución acuosa. Algunas se disocian completamente, liberando o aceptando protones con avidez, mientras que otras apenas lo hacen. Para cuantificar esta característica esencial, los químicos utilizan una serie de constantes y escalas, siendo Ka, Kb, pKa y pKb las más relevantes. Estas herramientas nos permiten predecir el comportamiento de una sustancia en una reacción y son cruciales en campos que van desde la bioquímica hasta la farmacología. Acompáñenos en este viaje para desentrañar el significado y la interconexión de estas importantes constantes.
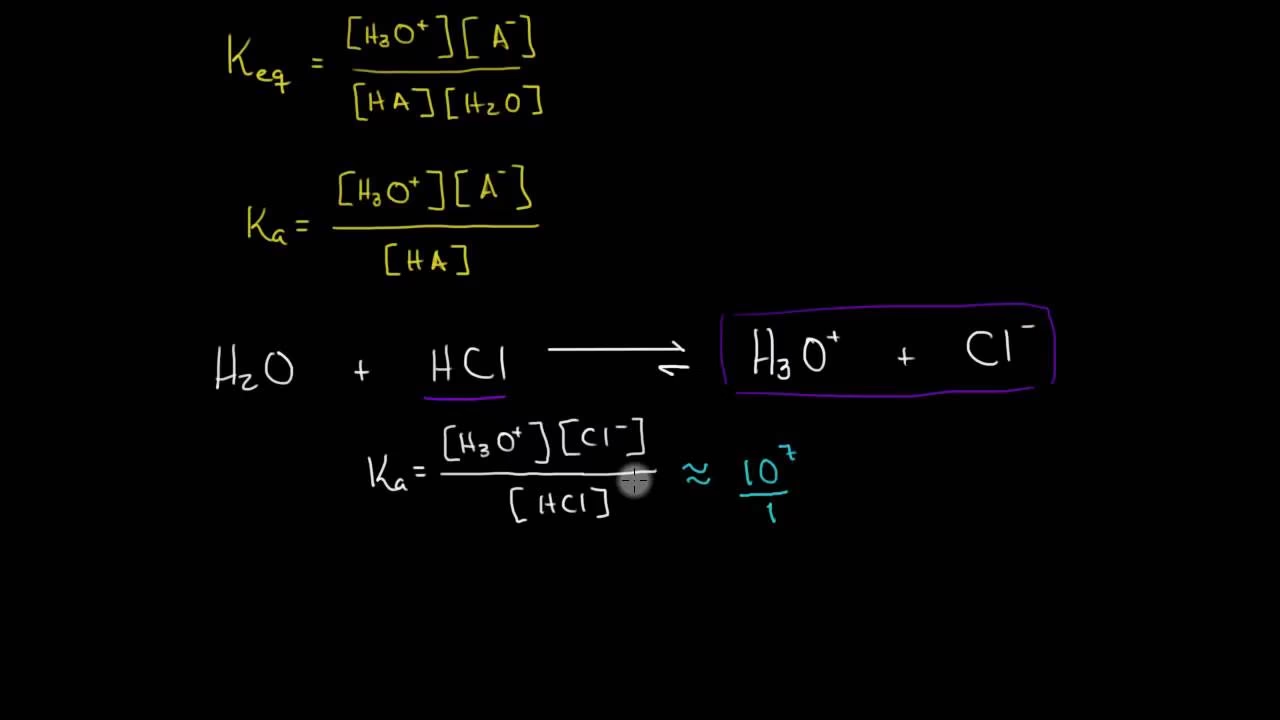
Comprendiendo Ka y Kb: La Fuerza de Ácidos y Bases
La constante de disociación ácida, conocida como Ka, es un valor numérico que mide la extensión en la que un ácido se disocia o ioniza cuando se disuelve en agua. Imagínese un ácido como un donante de protones (iones H+). Un valor de Ka alto indica que el ácido es fuerte, lo que significa que libera sus protones con gran facilidad y se disocia casi por completo en solución. Por el contrario, un valor de Ka bajo sugiere un ácido débil, que apenas se disocia y retiene la mayoría de sus protones. Esta constante es una medida directa de la tendencia de un ácido a ceder un protón.
De manera análoga, para las bases, tenemos la constante de disociación básica, Kb. Esta constante cuantifica la fuerza de una base midiendo su capacidad para aceptar protones (H+) o, equivalentemente, para disociarse y liberar iones hidroxilo (OH-) en agua. Una base fuerte tendrá un valor de Kb alto, indicando que acepta protones con gran avidez. En contraste, un valor de Kb bajo corresponde a una base débil, cuya capacidad para aceptar protones es limitada.
Existe una relación intrínseca entre Ka y Kb para un par ácido-base conjugado. El producto de Ka de un ácido y Kb de su base conjugada es igual a Kw, la constante de ionización del agua. El agua, aunque neutra, tiene la capacidad de autoionizarse, es decir, algunas de sus moléculas reaccionan entre sí para formar iones hidronio (H3O+) e iones hidroxilo (OH-). Este proceso de equilibrio se describe mediante Kw. A una temperatura estándar de 25 grados Celsius, el valor de Kw es de 1.0 x 10-14. Esta relación fundamental, Ka * Kb = Kw, nos permite calcular una constante si conocemos la otra, asumiendo condiciones de neutralidad a 25°C. Por ejemplo, si conocemos el Ka de un ácido, podemos determinar el Kb de su base conjugada simplemente dividiendo Kw (1.0 x 10-14) por el valor de Ka.
De la Constante a la Escala Logarítmica: Introduciendo pKa y pKb
Mientras que Ka y Kb nos dan valores directos de las constantes de disociación, estos números suelen ser muy pequeños y se expresan en notación científica, lo que puede resultar engorroso para comparar o trabajar. Para simplificar la representación de estas magnitudes, los químicos utilizan una escala logarítmica: pKa y pKb. El prefijo 'p' en pKa y pKb significa el logaritmo negativo en base 10 de la constante respectiva. Así, pKa se define como -log10(Ka), y pKb se define como -log10(Kb).
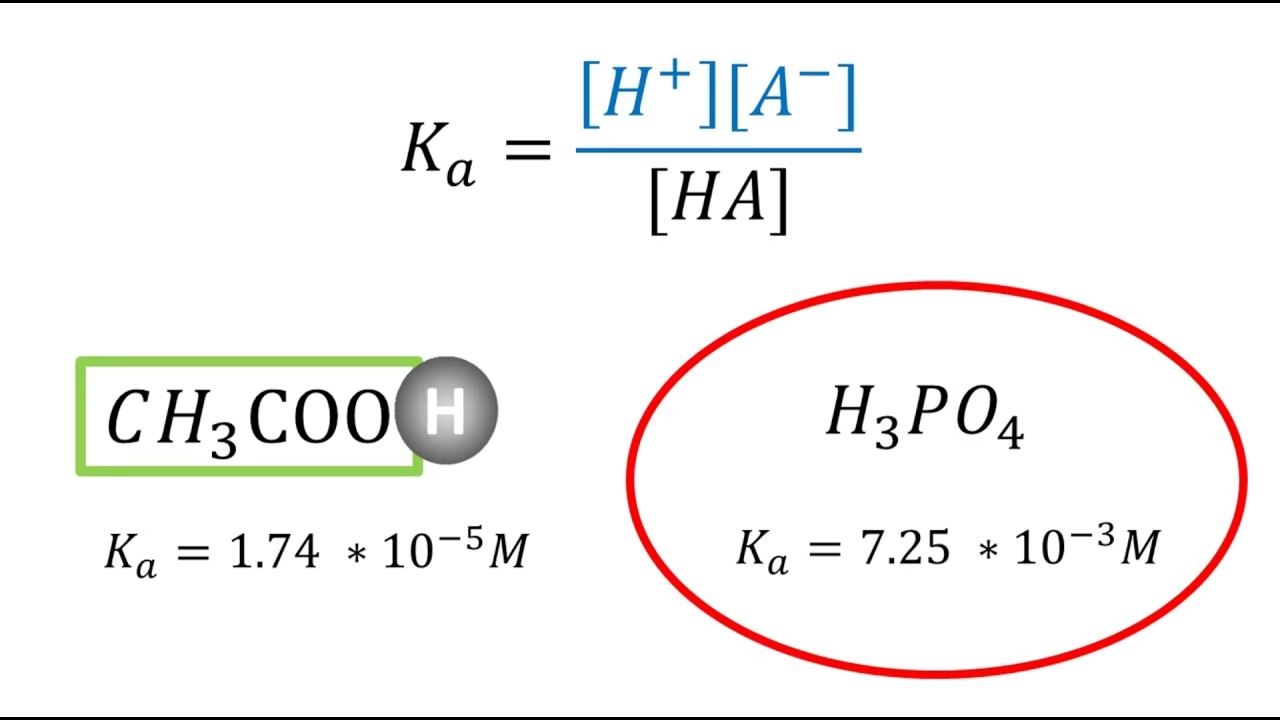
El uso de la escala logarítmica convierte números muy pequeños (como 10-5 o 10-9) en números más manejables y positivos (como 5 o 9). Esta transformación facilita la comparación de la fuerza relativa de diferentes ácidos y bases. Es crucial entender que, debido a la naturaleza del logaritmo negativo, la relación entre la magnitud de la constante y su valor 'p' es inversa. Un Ka grande (ácido fuerte) se traduce en un pKa pequeño. Por ejemplo, un ácido con Ka = 10-2 tendrá un pKa = 2, mientras que un ácido con Ka = 10-7 tendrá un pKa = 7. Un pKa menor indica un ácido más fuerte. De manera similar, un Kb grande (base fuerte) se corresponde con un pKb pequeño, indicando una base más fuerte. Por lo tanto, cuanto menor sea el valor de pKb, más fuerte será la base.
La Relación Fundamental: pKa + pKb = 14
La relación más directa y útil que vincula pKa y pKb es la ecuación pKa + pKb = 14.00. Esta fórmula deriva directamente de la relación entre Ka, Kb y Kw, tomando el logaritmo negativo de ambos lados de la ecuación Ka * Kb = Kw.
Si tomamos el logaritmo negativo de la ecuación Ka * Kb = Kw:
-log10(Ka * Kb) = -log10(Kw)
Aplicando la propiedad de los logaritmos (log(A*B) = log(A) + log(B)):
-(log10(Ka) + log10(Kb)) = -log10(Kw)
-log10(Ka) - log10(Kb) = -log10(Kw)
Sabemos que -log10(Ka) es pKa, -log10(Kb) es pKb, y -log10(Kw) es pKw.
Como Kw es 1.0 x 10-14 a 25°C, pKw es -log10(1.0 x 10-14) = 14.
Por lo tanto, la ecuación se simplifica a:
pKa + pKb = 14
Esta constante relación es increíblemente práctica en química. Significa que si conocemos el pKa de un ácido, podemos calcular fácilmente el pKb de su base conjugada, y viceversa, simplemente restando el valor conocido de 14. Esta ecuación es válida a 25 grados Celsius, la temperatura a la que Kw es 1.0 x 10-14. Si la temperatura cambia, el valor de Kw y, por lo tanto, de 14, también cambiaría ligeramente, pero para la mayoría de los cálculos estándar, 14 es el valor aceptado.

Cálculo Práctico: De Kb a pKa y Viceversa
La capacidad de convertir entre estas constantes es una habilidad esencial en química. Veamos algunos ejemplos prácticos.
Ejemplo 1: Convertir Kb a pKa
Supongamos que tenemos una base con un valor de Kb de 1.0 x 10-5. Nuestro objetivo es encontrar el pKa de su ácido conjugado.
- Calcular pKb: Usamos la definición de pKb:
pKb = -log10(Kb)
pKb = -log10(1.0 x 10-5)
pKb = 5 - Calcular pKa: Ahora usamos la relación fundamental:
pKa + pKb = 14
pKa + 5 = 14
pKa = 14 - 5
pKa = 9
Así, una base con un Kb de 1.0 x 10-5 tiene un ácido conjugado con un pKa de 9.
Ejemplo 2: Convertir Ka a pKb
Imaginemos que tenemos un ácido con un Ka de 1.0 x 10-3. Queremos encontrar el pKb de su base conjugada.
- Calcular pKa: Usamos la definición de pKa:
pKa = -log10(Ka)
pKa = -log10(1.0 x 10-3)
pKa = 3 - Calcular pKb: Usamos la relación fundamental:
pKa + pKb = 14
3 + pKb = 14
pKb = 14 - 3
pKb = 11
En este caso, un ácido con un Ka de 1.0 x 10-3 tiene una base conjugada con un pKb de 11.

Estos ejemplos demuestran la sencillez y la utilidad de la relación pKa + pKb = 14. Nos permite movernos fluidamente entre las propiedades de ácidos y bases conjugadas, facilitando la comprensión de su comportamiento en soluciones.
¿Por Qué es Importante Entender pKa y pKb?
Más allá de los cálculos, la comprensión de pKa y pKb tiene profundas implicaciones en diversas áreas. En bioquímica, el pKa de los grupos funcionales de las proteínas y aminoácidos es crucial para entender su estructura tridimensional y su función biológica, ya que el estado de ionización de estos grupos depende del pH del entorno. En farmacología, el pKa de un fármaco influye en su absorción, distribución, metabolismo y excreción en el cuerpo, ya que la forma ionizada o no ionizada de una molécula determina su capacidad para cruzar las membranas celulares. Por ejemplo, un fármaco con un pKa específico se absorberá mejor en un entorno con cierto pH (como el estómago ácido o el intestino más básico).
En química analítica, el pKa es esencial para diseñar y comprender las soluciones amortiguadoras (buffers), que son mezclas de un ácido débil y su base conjugada que resisten los cambios de pH. La capacidad de un buffer para mantener un pH estable está directamente relacionada con el pKa del ácido débil que lo compone. En la industria, desde la producción de alimentos hasta la fabricación de productos farmacéuticos y cosméticos, el control del pH es vital, y para ello se requiere un conocimiento profundo de las constantes de disociación de las sustancias involucradas. En resumen, pKa y pKb no son solo números abstractos; son herramientas poderosas que nos permiten predecir y manipular el comportamiento químico de las sustancias en una amplia gama de aplicaciones científicas y tecnológicas.
Tabla Comparativa
Para consolidar la información, la siguiente tabla resume las características clave de Ka/Kb y pKa/pKb:
| Característica | Ka / Kb (Constantes de Disociación) | pKa / pKb (Escalas Logarítmicas) |
|---|---|---|
| Definición | Cuantifican directamente la extensión de la disociación ácida (Ka) o básica (Kb) en agua. | Son el logaritmo negativo (base 10) de Ka o Kb, respectivamente (pKa = -log Ka, pKb = -log Kb). |
| Magnitud Típica | Valores muy pequeños, a menudo en notación científica (ej., 10-5, 10-9). | Valores más manejables y positivos (ej., 5, 9, 11). |
| Relación con la Fuerza del Ácido | Mayor Ka = Ácido más fuerte. | Menor pKa = Ácido más fuerte. |
| Relación con la Fuerza de la Base | Mayor Kb = Base más fuerte. | Menor pKb = Base más fuerte. |
| Relación entre Ácido y Base Conjugada | Ka (ácido) * Kb (base conjugada) = Kw (1.0 x 10-14 a 25°C). | pKa (ácido) + pKb (base conjugada) = 14 (a 25°C). |
| Uso Principal | Cálculos de equilibrio directos, comprensión de la concentración de iones. | Comparación rápida de fuerzas, diseño de buffers, relevancia biológica y farmacéutica. |
Preguntas Frecuentes (FAQs)
Para resolver cualquier duda persistente, abordemos algunas preguntas comunes:
¿Cuál es la fórmula para PKA KB?
- Para las constantes de disociación: Ka * Kb = Kw. Donde Kw es la constante de ionización del agua, igual a 1.0 x 10-14 a 25°C. Esta relación se aplica a un par ácido-base conjugado.
- Para las escalas logarítmicas: pKa + pKb = 14. Esta es la relación más comúnmente utilizada para convertir entre pKa y pKb de un par ácido-base conjugado a 25°C.
¿Cómo se calcula la pKa?
La pKa se puede calcular de dos maneras principales:
- A partir de Ka: Si conoces el valor de Ka (la constante de disociación ácida), calculas pKa usando la fórmula: pKa = -log10(Ka).
- A partir de Kb (o pKb): Si conoces el valor de Kb de la base conjugada, primero puedes calcular pKb (-log10(Kb)) y luego usar la relación pKa = 14 - pKb (a 25°C).
¿Cómo pasar de KB a pka?
Para convertir de Kb a pKa, sigue estos pasos:
- Primero, calcula el pKb a partir de Kb usando la fórmula: pKb = -log10(Kb). Por ejemplo, si Kb = 1.0 x 10-5, entonces pKb = -log10(1.0 x 10-5) = 5.
- Luego, usa la relación fundamental que conecta pKa y pKb: pKa + pKb = 14. Despeja pKa: pKa = 14 - pKb. Siguiendo el ejemplo anterior, pKa = 14 - 5 = 9.
¿PKA es lo mismo que KB?
No, pKa no es lo mismo que Kb. Son conceptos relacionados pero distintos. Kb es la constante de disociación básica, una medida directa de la fuerza de una base, expresada en notación científica. pKa, por otro lado, es la escala logarítmica negativa de la constante de disociación ácida (Ka), y se utiliza para medir la fuerza de un ácido. La relación que los conecta es a través de sus pares conjugados y la constante de ionización del agua (Kw), donde pKa y pKb de un par ácido-base conjugado suman 14 (pKa + pKb = 14) y Ka y Kb se relacionan por Ka * Kb = Kw.
Si quieres conocer otros artículos parecidos a Desentrañando pKa y Kb: La Fuerza de Ácidos y Bases puedes visitar la categoría Química.
