29/12/2022
En el vasto y fascinante universo de la química y la física, el átomo se erige como la unidad fundamental, un microcosmos de partículas que interactúan de formas complejas y determinantes. En el centro de cada átomo reside el núcleo, una diminuta pero densa región que concentra casi toda la masa del átomo y, crucialmente, su carga eléctrica positiva. Entender cómo se calcula y se interpreta esta carga es esencial para comprender la estructura atómica, el comportamiento de los electrones y, en última instancia, las propiedades de los elementos y las reacciones químicas. Este artículo te guiará a través de los diferentes conceptos de carga nuclear, desde la simple carga absoluta hasta la más compleja carga nuclear efectiva, e incluso la carga específica, proporcionándote las herramientas para desentrañar los misterios del núcleo atómico.

La capacidad de cuantificar la influencia del núcleo sobre sus electrones es una piedra angular de la química moderna. Sin una comprensión clara de la carga nuclear, sería imposible explicar por qué los átomos se unen de ciertas maneras, por qué los elementos exhiben sus propiedades periódicas características o incluso cómo funcionan las tecnologías que dependen de la manipulación de la materia a nivel atómico. Acompáñanos en este viaje para dominar estos cálculos fundamentales y expandir tu comprensión del mundo subatómico.
- Carga Nuclear Absoluta: El Corazón Eléctrico del Átomo
- Carga Nuclear Relativa: Una Perspectiva Comparativa de la Influencia
- Carga Nuclear Efectiva (Zeff): La Verdadera Atracción Electrónica
- Carga Específica de un Núcleo: La Relación Carga-Masa
- Preguntas Frecuentes sobre la Carga Nuclear
- Conclusión: Dominando los Fundamentos Atómicos
Carga Nuclear Absoluta: El Corazón Eléctrico del Átomo
Cuando hablamos de la carga nuclear de un átomo de la manera más directa y fundamental, nos referimos a la carga eléctrica total de su núcleo. Esta carga es intrínsecamente positiva y es el resultado de la presencia de protones dentro del núcleo. Los protones son partículas subatómicas que poseen una carga elemental positiva, igual en magnitud a la carga negativa de un electrón.
El cálculo de la carga nuclear es sorprendentemente sencillo y directo. Se basa en una propiedad fundamental de cada elemento químico: su Número Atómico. El Número Atómico, representado por la letra Z, no es otra cosa que el número de protones presentes en el núcleo de un átomo de ese elemento. Cada protón contribuye con una unidad de carga positiva, que es la carga elemental (e), cuyo valor es aproximadamente 1.602 x 10-19 Coulombs (C).
Por lo tanto, la fórmula para calcular la carga nuclear absoluta de un átomo es:
Carga Nuclear Absoluta = Número Atómico (Z) × Carga Elemental (e)
Por ejemplo, el carbono (C) tiene un Número Atómico (Z) de 6. Esto significa que un átomo de carbono posee 6 protones en su núcleo. Su carga nuclear absoluta sería 6 × (1.602 x 10-19 C) = 9.612 x 10-19 C.
Es importante destacar que los neutrones, las otras partículas que residen en el núcleo junto con los protones, no tienen carga eléctrica. Por lo tanto, no contribuyen a la carga nuclear, pero sí a la masa del átomo. La identidad de un elemento químico está definida únicamente por su Número Atómico, es decir, por la cantidad de protones que contiene en su núcleo. Cualquier cambio en el número de protones daría lugar a un átomo de un elemento diferente.
Esta carga positiva del núcleo es la fuerza principal que atrae a los electrones, que poseen carga negativa, manteniéndolos en órbitas alrededor del núcleo y formando el átomo como una entidad eléctricamente neutra (en el caso de un átomo neutro, el número de electrones es igual al número de protones). La magnitud de esta atracción es lo que impulsa muchos de los fenómenos químicos que observamos.
Carga Nuclear Relativa: Una Perspectiva Comparativa de la Influencia
El término “carga nuclear relativa” puede interpretarse de diversas maneras, pero en el contexto de la química y la física atómica, a menudo se refiere a la influencia de la carga nuclear en comparación con otros factores o en relación con diferentes elementos. Si bien la carga nuclear *absoluta* de un átomo es fija y se calcula directamente por el número de protones, su *efecto* sobre los electrones más externos puede ser percibido como "relativo" debido a la presencia de otros electrones que actúan como un escudo.
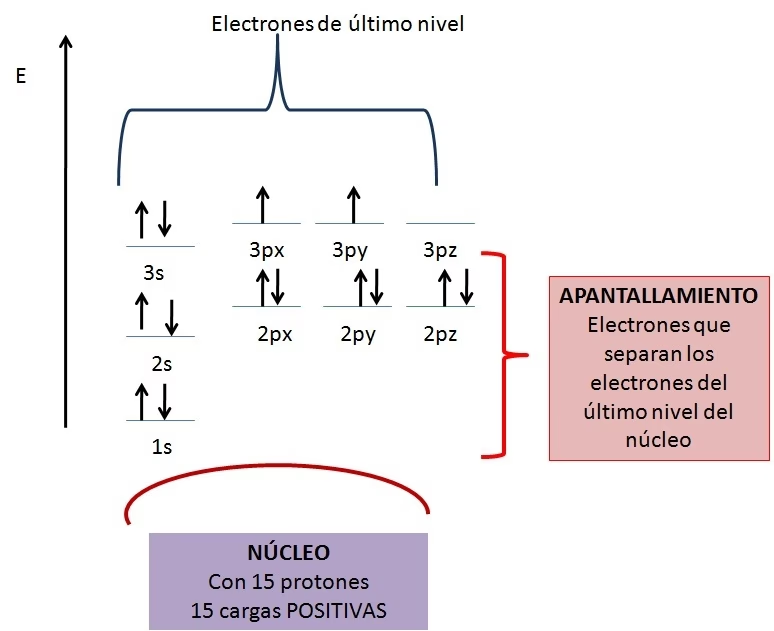
Cuando hablamos de la carga nuclear en un sentido relativo, no estamos cambiando la cantidad real de protones en el núcleo, sino cómo esa carga es percibida o experimentada por un electrón particular. Por ejemplo, la carga nuclear de un átomo de sodio (Z=11) es +11e. La carga nuclear de un átomo de cloro (Z=17) es +17e. En este sentido, la carga nuclear del cloro es "relativa" o comparativamente mayor que la del sodio. Esta diferencia en la magnitud de la carga nuclear absoluta es lo que impulsa muchas de las tendencias periódicas, como la electronegatividad o el tamaño atómico.
Sin embargo, el uso más común del concepto de “relatividad” en el contexto de la carga nuclear se da al considerar cómo la carga nuclear real es mitigada por la presencia de electrones internos. Este fenómeno se conoce como apantallamiento o efecto de pantalla. Los electrones más cercanos al núcleo (electrones internos o de carozo) tienden a repeler a los electrones más externos (electrones de valencia), disminuyendo la atracción neta que estos últimos sienten por el núcleo positivo. Es aquí donde el concepto de “carga nuclear relativa” se transforma en la fundamental “carga nuclear efectiva”.
En esencia, la carga nuclear absoluta es una propiedad intrínseca del núcleo, mientras que su "relatividad" surge al analizar cómo esa carga interactúa con el complejo entorno electrónico circundante. La fuerza con la que un electrón específico es atraído hacia el núcleo no depende únicamente del número de protones, sino también de cuántos electrones lo están 'protegiendo' de esa atracción. Esta consideración nos lleva directamente a uno de los conceptos más importantes en la química: la carga nuclear efectiva.
Carga Nuclear Efectiva (Zeff): La Verdadera Atracción Electrónica
La Carga Nuclear Efectiva (Zeff) es, sin duda, uno de los conceptos más cruciales en la química para entender el comportamiento de los electrones en un átomo polielectrónico (un átomo con más de un electrón). Como se mencionó anteriormente, la carga nuclear absoluta es simplemente el número de protones en el núcleo. Sin embargo, los electrones en un átomo no sienten la carga completa del núcleo debido al efecto de apantallamiento o cribado.
El apantallamiento ocurre porque los electrones internos, que están más cerca del núcleo, repelen a los electrones externos. Esta repulsión eléctrica actúa como una especie de 'escudo' o 'pantalla', disminuyendo la atracción neta que los electrones más alejados del núcleo experimentan. En otras palabras, la carga positiva del núcleo se 'enmascara' parcialmente por la presencia de electrones intermedios. Por lo tanto, la carga nuclear efectiva es la carga positiva neta del núcleo que un electrón de valencia experimenta en un átomo con múltiples electrones.
La definición clave de la carga nuclear efectiva es la carga que el núcleo *debería tener* para que, en ausencia de otros electrones, la atracción del núcleo sobre el electrón considerado fuera la misma que la atracción neta que experimenta el electrón en el átomo real. Esto la convierte en una medida más precisa de la fuerza de atracción que realmente sienten los electrones de valencia, que son los responsables de las interacciones químicas.
El cálculo de la carga nuclear efectiva se realiza mediante la siguiente fórmula:
Zeff = Z - S
Donde:
Zes el Número Atómico (la carga nuclear absoluta).Ses la constante de apantallamiento o constante de cribado.
La constante de apantallamiento (S) representa el grado en que los otros electrones 'apantallan' o 'escudan' al electrón de interés de la carga nuclear completa. Determinar el valor de S puede ser complejo y a menudo se estima utilizando métodos empíricos o semi-empíricos, como las Reglas de Slater. Estas reglas proporcionan un conjunto de pautas para asignar valores a S basándose en la configuración electrónica del átomo y la ubicación del electrón que se está considerando (es decir, en qué capa y subcapa se encuentra).
Aunque las Reglas de Slater son una simplificación y no proporcionan valores exactos, son una herramienta útil para comprender cómo los diferentes electrones contribuyen al apantallamiento. En términos generales, los electrones en capas más internas (con menor número cuántico principal, n) apantallan de manera más efectiva que los electrones en la misma capa o en capas más externas.

La carga nuclear efectiva es fundamental para explicar muchas tendencias periódicas, como:
- Tamaño Atómico: A medida que Zeff aumenta, la atracción del núcleo sobre los electrones de valencia se vuelve más fuerte, tirando de ellos más cerca del núcleo y disminuyendo el tamaño atómico.
- Energía de Ionización: Un mayor Zeff significa que se requiere más energía para remover un electrón de valencia, ya que está más fuertemente atraído por el núcleo.
- Afinidad Electrónica: Un mayor Zeff implica una mayor atracción por electrones adicionales, lo que generalmente resulta en una afinidad electrónica más negativa (más favorable).
- Electronegatividad: Los elementos con mayor Zeff tienden a atraer electrones con mayor fuerza en un enlace químico.
Comprender la carga nuclear efectiva nos permite ir más allá de la simple cantidad de protones y apreciar la dinámica real de las fuerzas eléctricas dentro de un átomo, lo que es esencial para predecir y explicar el comportamiento químico.
Carga Específica de un Núcleo: La Relación Carga-Masa
Más allá de la carga nuclear absoluta y efectiva, existe otro concepto importante en física atómica: la carga específica. En física, el término 'específico' generalmente se refiere a una propiedad de una sustancia por unidad de masa, longitud, área, volumen, etc. Por ejemplo, la capacidad calorífica específica se refiere a la energía térmica por unidad de masa de una sustancia.
En el contexto de la física atómica y nuclear, la carga específica se define como la relación entre la carga total de una partícula y su masa. Es una medida de cuán 'cargada' está una partícula en relación con su 'peso'.
Se puede calcular utilizando la ecuación:
Carga Específica = Carga Total / Masa Total
La carga específica se mide en unidades de Coulombs por kilogramo (C kg–1).
Para calcular la carga específica de un núcleo, necesitamos considerar su carga total y su masa total:
- Carga Total del Núcleo: Como ya sabemos, la carga de un núcleo proviene exclusivamente de sus protones. Cada protón tiene una carga elemental
e = 1.60 × 10–19 C. Por lo tanto, la carga total del núcleo esNúmero de Protones (Z) × e. - Masa Total del Núcleo: La masa de un núcleo se debe principalmente a la suma de las masas de sus protones y neutrones (colectivamente llamados nucleones). La masa de un protón (
mp) es aproximadamente1.67 × 10–27 kg, y la masa de un neutrón (mn) es muy similar, también aproximadamente1.67 × 10–27 kg. Por lo tanto, la masa total del núcleo esNúmero de Nucleones (Número Másico, A) × mp(aproximando la masa del neutrón a la del protón para este cálculo, ya que son muy cercanas). El número de nucleones es el número másico (A) del átomo, que es la suma de protones y neutrones.
Así, la fórmula para calcular la carga específica de un núcleo es:
Carga Específica del Núcleo = (Número de Protones × Carga Elemental) / (Número de Nucleones × Masa del Protón)
O, en símbolos:
Carga Específica del Núcleo = (Z × e) / (A × mp)
Por ejemplo, consideremos el núcleo de un átomo de Helio-4 (4He). Tiene Z=2 (2 protones) y A=4 (2 protones + 2 neutrones).
- Carga del núcleo = 2 × 1.60 × 10–19 C = 3.20 × 10–19 C
- Masa del núcleo = 4 × 1.67 × 10–27 kg = 6.68 × 10–27 kg
- Carga específica del núcleo de Helio-4 = (3.20 × 10–19 C) / (6.68 × 10–27 kg) ≈ 4.79 × 107 C kg–1
Los valores de la carga específica del electrón y del protón son datos fundamentales en física:
- La carga específica del electrón (e/me) = 1.76 × 1011 C kg–1
- La carga específica del protón (e/mp) = 9.58 × 107 C kg–1
La carga específica es un concepto importante en campos como la espectrometría de masas, donde se utiliza para identificar iones y núcleos basándose en su relación carga-masa, y en el estudio de partículas en campos eléctricos y magnéticos.
Comparación de Conceptos de Carga Nuclear
| Concepto | Definición | Cómo se Calcula | Importancia |
|---|---|---|---|
| Carga Nuclear Absoluta | Carga eléctrica total positiva del núcleo, debida a los protones. | Número Atómico (Z) × Carga Elemental (e) | Define la identidad del elemento y la atracción fundamental hacia los electrones. |
| Carga Nuclear Efectiva (Zeff) | Carga neta del núcleo que un electrón de valencia experimenta, considerando el apantallamiento de los electrones internos. | Z - S (donde S es la constante de apantallamiento) | Explica tendencias periódicas como tamaño atómico, energía de ionización y electronegatividad. |
| Carga Específica del Núcleo | Relación entre la carga total de un núcleo y su masa total. | (Z × e) / (A × mp) | Fundamental en espectrometría de masas y estudio de partículas cargadas. |
Preguntas Frecuentes sobre la Carga Nuclear
A continuación, respondemos algunas de las preguntas más comunes relacionadas con la carga nuclear y sus derivados.

¿Por qué es importante calcular la carga nuclear efectiva?
La carga nuclear efectiva es crucial porque la carga nuclear absoluta no refleja con precisión la atracción que los electrones más externos sienten por el núcleo en átomos con múltiples electrones. Los electrones internos 'apantallan' o 'escudan' parte de la carga nuclear, reduciendo la atracción neta sobre los electrones de valencia. Comprender la Zeff nos permite explicar y predecir una amplia gama de propiedades químicas y tendencias periódicas, como el tamaño de los átomos, la energía necesaria para remover electrones (energía de ionización) y la afinidad de un átomo por electrones adicionales.
¿Los neutrones afectan la carga nuclear?
No, los neutrones no afectan la carga nuclear. Los neutrones son partículas subatómicas eléctricamente neutras, lo que significa que no poseen carga eléctrica. La carga nuclear de un átomo depende exclusivamente del número de protones presentes en su núcleo. Los neutrones, sin embargo, contribuyen significativamente a la masa del átomo y son importantes para la estabilidad del núcleo.
¿La carga nuclear efectiva es siempre menor que la carga nuclear absoluta?
Sí, en la mayoría de los casos de átomos polielectrónicos, la carga nuclear efectiva que experimenta un electrón externo es siempre menor que la carga nuclear absoluta (el Número Atómico, Z). Esto se debe al efecto de apantallamiento que ejercen los electrones internos. La única excepción conceptual sería si consideráramos un átomo de hidrógeno (que solo tiene un protón y un electrón), donde el electrón no tiene otros electrones que lo apantallen, por lo que Zeff sería igual a Z (1).
¿Cómo influye la carga nuclear en la reactividad de un átomo?
La carga nuclear, y más específicamente la carga nuclear efectiva, tiene una influencia directa y profunda en la reactividad de un átomo. Un mayor Zeff significa que los electrones de valencia están más fuertemente atraídos hacia el núcleo. Esto hace que sea más difícil para el átomo perder electrones (menor tendencia a formar cationes) y más fácil para el átomo ganar electrones (mayor tendencia a formar aniones o atraer electrones en enlaces). Por lo tanto, elementos con alta Zeff (como los no metales en la parte superior derecha de la tabla periódica) tienden a ser más electronegativos y reactivos al ganar o compartir electrones, mientras que elementos con baja Zeff (como los metales alcalinos) tienden a perder electrones con facilidad.
Conclusión: Dominando los Fundamentos Atómicos
Hemos explorado las diversas facetas de la carga nuclear, desde su definición más básica como el número de protones en el núcleo hasta el concepto más matizado de la carga nuclear efectiva, que considera el impacto del apantallamiento electrónico. También hemos introducido la carga específica, una relación fundamental entre la carga y la masa que tiene aplicaciones en la física de partículas.
Comprender cómo calcular y aplicar estos conceptos es más que un simple ejercicio académico; es la clave para desentrañar las propiedades periódicas de los elementos, predecir la reactividad química y entender la interacción fundamental entre el núcleo y sus electrones. La carga nuclear efectiva, en particular, es una herramienta poderosa que nos permite ir más allá de la simple composición atómica para comprender las fuerzas reales que dan forma al comportamiento de la materia a nivel subatómico.
Ya sea que estés estudiando química, física o simplemente tengas curiosidad por el mundo que te rodea, la capacidad de calcular y conceptualizar estas cargas te proporcionará una base sólida para explorar fenómenos más complejos. El átomo, aunque pequeño, es un universo de interacciones eléctricas, y dominar el concepto de carga nuclear es el primer paso para comprender su vasto potencial.
Si quieres conocer otros artículos parecidos a Calculando la Carga Nuclear y su Impacto puedes visitar la categoría Cálculos.
