18/09/2024
En el vasto y fascinante universo de la química, la forma en que los átomos se unen para formar moléculas es fundamental para comprender las propiedades de la materia. Una de las herramientas más poderosas para predecir y entender la naturaleza de estos enlaces es el concepto de electronegatividad. Pero más allá de conocer el valor individual de cada átomo, la clave reside en la diferencia de electronegatividad entre los átomos enlazados. Esta diferencia nos revela la polaridad de un enlace y, en última instancia, el tipo de unión química, desde el enlace puramente covalente hasta el iónico, pasando por el covalente polar.
Este artículo te guiará a través de los principios de la electronegatividad, cómo se calcula su diferencia y qué implicaciones tiene esta para los enlaces químicos, proporcionando una comprensión clara de este concepto esencial.
- ¿Qué es la Electronegatividad?
- Cálculo de la Diferencia de Electronegatividad
- Clasificación de Enlaces según la Diferencia de Electronegatividad
- Carácter Iónico y Momentos Dipolares
- Electronegatividad en Metales, No Metales y Metaloides
- Preguntas Frecuentes (FAQ)
- ¿Cuál es la fórmula para la diferencia de electronegatividad?
- ¿Cómo saber cuál tiene más electronegatividad?
- ¿Cómo calcular la diferencia de electronegatividad entre C y O en CO2?
- ¿Existen otras escalas de electronegatividad además de la de Pauling?
- ¿Cómo afecta la diferencia de electronegatividad a las propiedades de un compuesto?
¿Qué es la Electronegatividad?
La electronegatividad, representada por la letra griega chi (χ), es una medida de la capacidad relativa de un átomo para atraer electrones hacia sí mismo en un compuesto químico. A diferencia de la energía de ionización o la afinidad electrónica, la electronegatividad no es una propiedad fija que se pueda medir directamente en un único experimento. En cambio, es una medida de la tendencia de un átomo a atraer electrones dentro de un enlace.
Los elementos con altas electronegatividades tienden a adquirir electrones en las reacciones químicas y se encuentran en la esquina superior derecha de la tabla periódica. Por el contrario, los elementos con bajas electronegatividades tienden a perder electrones en las reacciones químicas y se ubican en la esquina inferior izquierda de la tabla.
La electronegatividad de un átomo es una función de su energía de ionización (qué tan fuertemente el átomo retiene sus propios electrones) y su afinidad electrónica (qué tan fuertemente el átomo atrae otros electrones). Un elemento será altamente electronegativo si tiene una afinidad electrónica grande (negativa) y una alta energía de ionización (siempre endotérmica o positiva para átomos neutros). Así, atraerá electrones de otros átomos y resistirá que sus propios electrones sean atraídos.
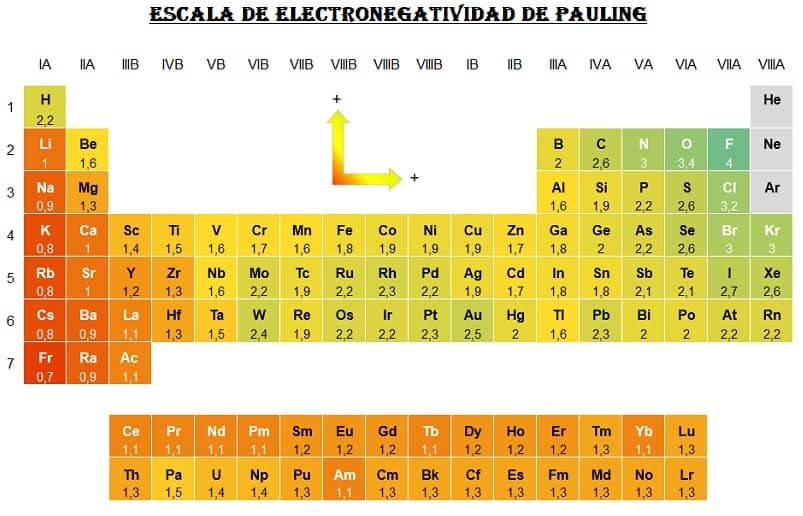
La Escala de Pauling
La escala de electronegatividad original, desarrollada en la década de 1930 por Linus Pauling, se basó en mediciones de las fuerzas de los enlaces covalentes entre diferentes elementos. Pauling estableció arbitrariamente la electronegatividad del flúor en 4.0 (aunque hoy en día se ha refinado a 3.98), creando así una escala en la que todos los elementos tienen valores entre 0 y 4.0. El elemento menos electronegativo no radiactivo es el cesio, con un valor de 0.79. El valor de referencia para el hidrógeno se define como 2.20.
Las variaciones periódicas en los valores de electronegatividad de Pauling muestran una tendencia clara: la electronegatividad generalmente aumenta diagonalmente desde la parte inferior izquierda hasta la parte superior derecha de la tabla periódica. Esto significa que los elementos en la esquina superior derecha (excluyendo los gases inertes) son los más electronegativos, mientras que los de la esquina inferior izquierda son los menos electronegativos.
Es importante señalar que Pauling no fue el único en desarrollar una escala de electronegatividad. Otras definiciones, como las escalas de Mulliken, Allred-Rochow y Allen, se han desarrollado para abordar el problema de que muchos elementos no forman compuestos covalentes estables, lo que limita la aplicación del método de Pauling. La electronegatividad de Mulliken, por ejemplo, es el promedio de la primera energía de ionización de un elemento y el valor absoluto de su afinidad electrónica, lo que muestra la relación entre la electronegatividad y estas otras propiedades periódicas.
Cálculo de la Diferencia de Electronegatividad
La diferencia de electronegatividad (Δχ) entre dos átomos enlazados es la clave para determinar la polaridad y el tipo de enlace químico. Se calcula simplemente restando los valores de electronegatividad de los dos átomos involucrados en el enlace:
Δχ = |χB − χA|
Donde χA y χB son los valores de electronegatividad de los dos átomos. Se utiliza el valor absoluto porque la diferencia es una magnitud, no una dirección.
La posición de los elementos en la tabla periódica nos da una pista visual sobre la posible diferencia de electronegatividad. En general, cuanto más separados se encuentren dos elementos en la tabla periódica (especialmente en diagonal desde la esquina inferior izquierda a la superior derecha), mayor será la diferencia de electronegatividades entre ellos. Esto se debe a la tendencia periódica de la electronegatividad.
Ejemplos de Cálculo de Diferencia de Electronegatividad:
- Unión entre Cesio (Cs) y Flúor (F): La electronegatividad del flúor es 3.98 (aproximadamente 4.0) y la del cesio es 0.79 (aproximadamente 0.7). La diferencia es 4.0 - 0.7 = 3.3. Este es uno de los valores más grandes posibles y caracteriza un enlace iónico.
- Unión entre Carbono y Azufre (Sulfuro de Carbono): La información indica que la diferencia de electronegatividad para esta unión es de 1.0. Este valor es característico de un enlace covalente polar.
- Unión entre Azufre y Carbono (Disulfuro de Carbono): Para esta unión, la diferencia de electronegatividad es de 0.0. Esto indica un enlace covalente no polar o puro, donde los electrones se comparten por igual entre los átomos.
Es importante recordar que los valores de electronegatividad pueden variar ligeramente entre diferentes escalas o incluso dentro de la misma escala dependiendo de la fuente. Sin embargo, las tendencias y la clasificación general de los enlaces se mantienen consistentes.
Clasificación de Enlaces según la Diferencia de Electronegatividad
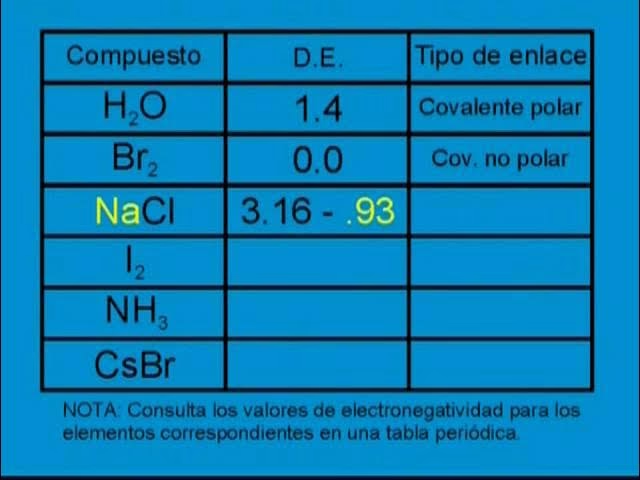
La diferencia de electronegatividad es una herramienta poderosa para predecir la naturaleza de un enlace químico. Aunque la transición entre los tipos de enlace es un continuo, podemos establecer rangos aproximados para clasificarlos:
| Diferencia de Electronegatividad (Δχ) | Tipo de Enlace | Características |
|---|---|---|
| Δχ < 0.4 | Covalente No Polar | Los electrones se comparten casi por igual entre los átomos. No hay separación significativa de carga. |
| 0.5 ≤ Δχ ≤ 1.6 | Covalente Polar | Los electrones se comparten de manera desigual; el átomo más electronegativo atrae más la densidad electrónica, creando cargas parciales (δ+ y δ-). |
| Δχ ≥ 1.7 | Iónico | La transferencia de electrones es prácticamente completa de un átomo a otro, formando iones con cargas opuestas que se atraen fuertemente. |
Es fundamental entender que estas clasificaciones son guías. Un enlace covalente no polar es aquel en el que los electrones se comparten por igual entre dos átomos. Un enlace covalente polar es aquel en el que un átomo tiene una mayor atracción por los electrones que el otro átomo, resultando en una distribución asimétrica de la densidad electrónica. Si esta atracción relativa es lo suficientemente grande, entonces el enlace es un enlace iónico, donde la transferencia de electrones es casi completa.
Por ejemplo, en la molécula de Cl2, la diferencia de electronegatividad es cero (ambos átomos de cloro tienen la misma electronegatividad), lo que resulta en un enlace covalente no polar donde los electrones se comparten equitativamente. En el NaCl, la diferencia es 2.23 (χCl = 3.16, χNa = 0.93), un valor alto que indica un enlace iónico, con transferencia de un electrón de sodio a cloro. Para el HCl, la diferencia es 0.96 (χCl = 3.16, χH = 2.20), lo que lo clasifica como un enlace covalente polar, con los electrones más atraídos hacia el cloro.

Carácter Iónico y Momentos Dipolares
La polaridad de un enlace, es decir, hasta qué punto es polar, está determinada en gran medida por las electronegatividades relativas de los átomos enlazados. Cuanto mayor sea la diferencia de electronegatividad, mayor será la separación de carga y, por lo tanto, mayor el carácter iónico del enlace.
Una forma de estimar el carácter iónico de un enlace, es decir, la magnitud de la separación de carga en un enlace covalente polar, es mediante el cálculo del momento dipolar. Un momento dipolar (µ) es el producto de la carga parcial (Q) en los átomos enlazados y la distancia (r) entre las cargas parciales:
µ = Qr
Donde Q se mide en culombios (C) y r en metros (m). La unidad para los momentos dipolares es el debye (D), donde 1 D = 3.3356 × 10-30 C·m.
Cuando una molécula con un momento dipolar se coloca en un campo eléctrico, tiende a orientarse con el campo debido a su distribución asimétrica de carga. Esto permite medir el momento dipolar y, a partir de él, calcular la carga parcial sobre los átomos y, en consecuencia, el porcentaje de carácter iónico.
Cálculo del Porcentaje de Carácter Iónico:
Si el enlace fuera puramente iónico, un electrón se transferiría completamente, resultando en una carga de +1 o -1. Comparando la carga calculada a partir del momento dipolar con la carga de un solo electrón (1.6022 × 10-19 C), podemos determinar el porcentaje de carácter iónico:
% Carácter Iónico = (Carga calculada / Carga de un electrón) × 100
- Ejemplo HCl: El momento dipolar del HCl es 1.109 D y la distancia H-Cl es 127.5 pm. Al calcular la carga parcial, se obtiene que el enlace H-Cl tiene aproximadamente un 18% de carácter iónico, lo que significa que es un 82% covalente. Esto concuerda con la diferencia de electronegatividad (0.96), que lo clasifica como un enlace covalente polar.
- Ejemplo NaCl (fase gaseosa): En la fase gaseosa, el NaCl tiene un momento dipolar de 9.001 D y una distancia Na-Cl de 236.1 pm. El cálculo revela un carácter iónico del 79.39% (aproximadamente 79%). Aunque es alto, demuestra que incluso un compuesto tan típicamente iónico no es 100% iónico en la fase gaseosa. Sin embargo, en estado sólido, las interacciones electrostáticas en la red cristalina aumentan la separación de carga, y el NaCl se comporta como un compuesto 100% iónico.
- Ejemplo AgCl (fase gaseosa): El cloruro de plata (AgCl) en fase gaseosa tiene un momento dipolar de 6.08 D y una distancia Ag-Cl de 228.1 pm. Su carácter iónico es del 55.5%.
Los datos muestran que las especies diatómicas con una diferencia de electronegatividad inferior a 1.5 tienen menos del 50% de carácter iónico, lo que es consistente con su descripción como enlaces covalentes polares.
Electronegatividad en Metales, No Metales y Metaloides
La electronegatividad de un elemento nos proporciona un valor único que podemos utilizar para caracterizar su química. Esta propiedad está intrínsecamente ligada al carácter metálico o no metálico de un elemento:
- Elementos con alta electronegatividad (χ ≥ 2.2): Generalmente son no metales y aislantes eléctricos. Tienen afinidades electrónicas muy negativas y grandes potenciales de ionización, lo que significa que tienden a ganar electrones en las reacciones químicas (es decir, son oxidantes). Se encuentran en la parte superior derecha de la tabla periódica.
- Elementos con baja electronegatividad (χ ≤ 1.8): Generalmente son metales y buenos conductores eléctricos. Tienen afinidades electrónicas positivas o pequeñas y potenciales de ionización bajos, lo que significa que tienden a perder sus electrones de valencia en las reacciones químicas (es decir, son reductores). Se encuentran en la parte inferior izquierda de la tabla periódica.
- Elementos con electronegatividades intermedias (χ ≈ 2.0): Entre los metales y no metales, a lo largo de la línea diagonal que va del boro (B) al ástato (At), se encuentran los metaloides (o semimetales). Estos elementos poseen algunas de las propiedades químicas tanto de los no metales como de los metales.
La distinción entre metales y no metales es una de las más fundamentales para categorizar los elementos y predecir su comportamiento químico. Los valores de electronegatividad también se utilizan para predecir las energías de enlace, las polaridades de enlace y los tipos de reacciones que experimentan los compuestos.
Preguntas Frecuentes (FAQ)
¿Cuál es la fórmula para la diferencia de electronegatividad?
La fórmula para calcular la diferencia de electronegatividad (Δχ) entre dos átomos enlazados es simple: se resta el valor de electronegatividad del átomo menos electronegativo del valor del átomo más electronegativo. Generalmente, se toma el valor absoluto de la resta: Δχ = |χB − χA|, donde χA y χB son las electronegatividades de los dos átomos.

¿Cómo saber cuál tiene más electronegatividad?
Para saber qué átomo tiene más electronegatividad, puedes consultar la tabla periódica. En general, la electronegatividad aumenta de izquierda a derecha a lo largo de un período y de abajo hacia arriba a lo largo de un grupo. Esto significa que los elementos más electronegativos se encuentran en la esquina superior derecha de la tabla (siendo el flúor el más electronegativo con un valor de 3.98 en la escala de Pauling), y los menos electronegativos en la esquina inferior izquierda (como el francio, con un valor de 0.7).
¿Cómo calcular la diferencia de electronegatividad entre C y O en CO2?
Para calcular la diferencia de electronegatividad entre el carbono (C) y el oxígeno (O) en el CO2, necesitarías los valores específicos de electronegatividad para cada uno de estos elementos. Si bien la metodología es la misma (restar los valores), los datos proporcionados para este artículo no incluyen los valores específicos de electronegatividad para el carbono y el oxígeno en la escala de Pauling, por lo que no podemos realizar el cálculo numérico exacto aquí. Sin embargo, si tuvieras esos valores, simplemente restarías el valor de electronegatividad del carbono del valor del oxígeno, ya que el oxígeno es más electronegativo.
¿Existen otras escalas de electronegatividad además de la de Pauling?
Sí, la escala de Pauling es la más conocida, pero existen otras escalas que abordan diferentes aspectos o se basan en distintos principios. Algunas de las más notables incluyen la escala de Mulliken, que se basa en la energía de ionización y la afinidad electrónica de un átomo; la escala de Allred-Rochow, que considera la carga nuclear efectiva y el radio atómico; y la escala de Allen, que utiliza las energías de configuración de los electrones de valencia.
¿Cómo afecta la diferencia de electronegatividad a las propiedades de un compuesto?
La diferencia de electronegatividad influye directamente en la polaridad de los enlaces dentro de un compuesto, lo que a su vez afecta una amplia gama de propiedades físicas y químicas. Los compuestos con enlaces polares o iónicos suelen tener puntos de fusión y ebullición más altos, son más solubles en disolventes polares (como el agua) y pueden conducir la electricidad (especialmente los iónicos en estado fundido o en disolución). La polaridad también es crucial para entender las interacciones intermoleculares, la reactividad química y la estructura tridimensional de las moléculas.
Comprender la diferencia de electronegatividad es, por tanto, un paso fundamental para desentrañar la complejidad del mundo molecular y predecir cómo se comportarán las sustancias en diversas condiciones.
Si quieres conocer otros artículos parecidos a Calculando la Diferencia de Electronegatividad puedes visitar la categoría Química.
