23/06/2023
La concentración es un concepto fundamental en la química, la biología y la vida cotidiana. Desde la etiqueta de un producto de limpieza hasta la preparación de una solución en un laboratorio, entender la concentración nos permite saber exactamente cuánto soluto hay disuelto en una cantidad determinada de solvente o solución. Pero, ¿qué significa realmente una solución concentrada o diluida, y cómo podemos expresar esta cantidad de manera precisa y cuantitativa?
En términos generales, una solución concentrada contiene una cantidad relativamente grande de soluto disuelto, mientras que una solución diluida contiene una cantidad relativamente pequeña. Sin embargo, estos términos son subjetivos y relativos. Para una comprensión más exacta, necesitamos métodos para cuantificar la concentración, y aquí es donde entran en juego las diferentes unidades de concentración, especialmente las basadas en porcentajes.
- Concentración Porcentual: Un Enfoque Detallado
- Más Allá del Porcentaje: Otras Unidades de Concentración
- Diluciones: Ajustando la Concentración
- ¿Qué Significa una Concentración al 5%?
- Cálculo de Concentraciones: Métodos y Herramientas
- Preguntas Frecuentes (FAQ)
- ¿Cuál es la diferencia entre una solución concentrada y una diluida?
- ¿Por qué es importante especificar el tipo de porcentaje (m/m, v/v, m/v)?
- ¿Cuándo se utilizan ppm o ppb en lugar de porcentajes?
- ¿Por qué la molaridad es la unidad de concentración preferida en las reacciones químicas?
- ¿Se pueden simplemente sumar los volúmenes del soluto y del solvente para obtener el volumen final de la solución?
Concentración Porcentual: Un Enfoque Detallado
Una de las formas más comunes y sencillas de describir la concentración de una solución es mediante el porcentaje de la solución que está compuesta por el soluto. Este porcentaje puede determinarse de tres maneras principales, y es crucial especificar cuál se está utilizando, ya que los valores pueden diferir significativamente.
Porcentaje Masa/Masa (% m/m o % p/p)
Cuando el soluto en una solución es un sólido, una forma conveniente de expresar la concentración es el porcentaje masa/masa. Esta unidad representa los gramos de soluto por cada 100 gramos de solución. Es particularmente útil en aplicaciones donde la masa es una propiedad clave, como en la formulación de productos alimenticios o farmacéuticos.
La fórmula para calcular el porcentaje masa/masa es la siguiente:
Porcentaje masa/masa = (masa del soluto / masa de la solución) × 100%
Es importante recordar que la masa de la solución es la suma de la masa del soluto y la masa del solvente. Por ejemplo, si se preparan 150 gramos de una solución disolviendo 30 gramos de azúcar en 120 gramos de agua, la concentración porcentual masa/masa sería:
Porcentaje masa/masa = (30 g azúcar / 150 g solución) × 100% = 20% m/m de azúcar
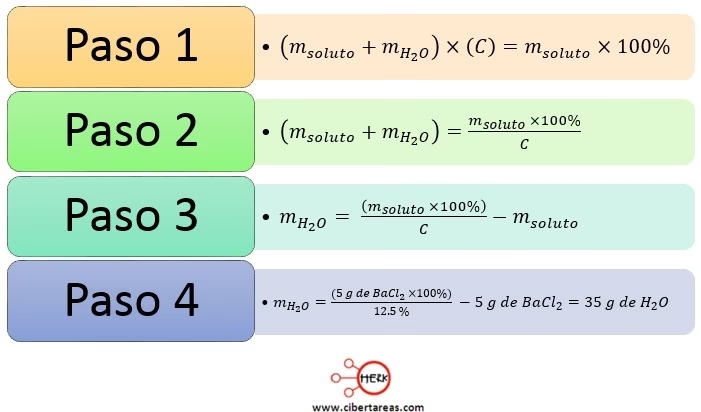
Si necesitas preparar una cantidad específica de solución con un cierto porcentaje masa/masa, puedes reorganizar la fórmula para calcular la masa de soluto necesaria. Por ejemplo, para hacer 500 gramos de una solución de sal al 10% m/m:
Masa de soluto = (Porcentaje masa/masa / 100%) × masa de la solución
Masa de soluto = (10 / 100) × 500 g = 50 g de sal
En este caso, necesitarías 50 gramos de sal y 450 gramos de agua (500 g - 50 g) para preparar la solución.
Porcentaje Volumen/Volumen (% v/v)
El porcentaje volumen/volumen se utiliza cuando tanto el soluto como el solvente son líquidos. Representa el volumen de soluto por cada 100 unidades de volumen de solución. Es común verlo en productos como bebidas alcohólicas (por ejemplo, el porcentaje de alcohol por volumen).
La fórmula para calcular el porcentaje volumen/volumen es:
Porcentaje volumen/volumen = (volumen del soluto / volumen de la solución) × 100%
Un punto crucial a tener en cuenta aquí es que, a diferencia de la masa, el volumen no siempre es aditivo. Es decir, el volumen final de una solución no es necesariamente la suma de los volúmenes del soluto y del solvente. Por lo tanto, al preparar una solución por volumen, generalmente se mide el volumen del soluto y luego se añade suficiente solvente para alcanzar el volumen final deseado de la solución. Por ejemplo, si se mezclan 25 mL de etanol y se añade agua hasta alcanzar un volumen total de 250 mL de solución:
Porcentaje volumen/volumen = (25 mL etanol / 250 mL solución) × 100% = 10% v/v de etanol
Si simplemente se mezclaran 25 mL de etanol con 225 mL de agua, el volumen final podría no ser exactamente 250 mL debido a interacciones intermoleculares.
Porcentaje Masa/Volumen (% m/v o % p/v)
El porcentaje masa/volumen se utiliza a menudo cuando un soluto sólido se disuelve en un solvente líquido. Representa la masa de soluto (generalmente en gramos) por cada 100 unidades de volumen de solución (generalmente en mililitros). Esta unidad es muy común en farmacia y en la preparación de soluciones para uso médico.
La fórmula para calcular el porcentaje masa/volumen es:
Porcentaje masa/volumen = (masa del soluto / volumen de la solución) × 100%
Por ejemplo, si se disuelven 5 gramos de cloruro de sodio (NaCl) en agua suficiente para preparar 200 mL de solución:
Porcentaje masa/volumen = (5 g NaCl / 200 mL solución) × 100% = 2.5% m/v de NaCl
Más Allá del Porcentaje: Otras Unidades de Concentración
Aunque los porcentajes son muy útiles, existen otras unidades de concentración que son más adecuadas para situaciones específicas, como soluciones muy diluidas o cálculos estequiométricos.
Partes por Millón (ppm) y Partes por Billón (ppb)
Para concentraciones extremadamente pequeñas de soluto, como la cantidad de contaminantes en el agua o el aire, se utilizan las unidades de partes por millón (ppm) y partes por billón (ppb). Se puede pensar en el porcentaje como "partes por cien". Siguiendo esta lógica, 15 ppm significa 15 partes de soluto por cada 1 millón de partes de solución. De manera similar, 22 ppb significa 22 partes de soluto por cada 1 billón de partes de solución.
Aunque pueden expresarse de varias maneras (por ejemplo, mg de soluto/kg de solución para ppm), comúnmente se interpretan como:
- 1 ppm = 1 mg de soluto por 1 Litro de solución (para soluciones acuosas diluidas, donde 1 L de agua pesa aproximadamente 1 kg).
- 1 ppb = 1 µg de soluto por 1 Litro de solución (donde 1 µg es una millonésima parte de un gramo).
Estas unidades son esenciales para monitorear la calidad ambiental y la seguridad alimentaria.
Molaridad (M)
En química, la molaridad es una de las unidades de concentración más importantes y utilizadas, especialmente en el contexto de las reacciones químicas. Esto se debe a que la molaridad relaciona la cantidad de soluto con el número de partículas (moles) presentes, lo cual es fundamental para la estequiometría de las reacciones. La molaridad (M) de una solución se define como el número de moles de soluto disueltos en un litro de solución.
La fórmula para calcular la molaridad es:
Molaridad (M) = moles de soluto / Litros de solución
La unidad de molaridad es M, que se lee como "molar". Por ejemplo, una solución etiquetada como 0.5 M de NaCl es una "solución 0.5 molar de cloruro de sodio".
Para calcular la molaridad, a menudo necesitarás convertir la masa del soluto a moles usando su masa molar. Por ejemplo, si se disuelven 29.22 gramos de NaCl (masa molar = 58.44 g/mol) en agua suficiente para hacer 0.500 litros de solución:
Moles de NaCl = 29.22 g / 58.44 g/mol = 0.500 moles
Molaridad = 0.500 moles / 0.500 L = 1.00 M
Equivalentes (Eq) y Miliequivalentes (mEq)
En el ámbito de la salud y la medicina, especialmente en soluciones intravenosas (IV) y análisis de fluidos corporales, a menudo se utilizan los conceptos de equivalentes (Eq) y miliequivalentes (mEq). Un equivalente es igual a un mol de carga en un ion. La valencia o carga del ion determina cuántos equivalentes hay por mol. El valor de los equivalentes siempre es positivo, independientemente de la carga del ion.
La importancia de los equivalentes radica en que la concentración de cargas es a menudo más relevante que la identidad específica de los iones para mantener el equilibrio eléctrico en los fluidos corporales.
Aquí tienes una tabla que muestra los equivalentes por mol para algunos iones comunes:
| Ion | Equivalentes por mol |
|---|---|
| Na+ | 1 |
| Mg2+ | 2 |
| Al3+ | 3 |
| Cl- | 1 |
| SO42- | 2 |
Dado que las concentraciones de iones en el cuerpo son a menudo muy bajas, se utiliza el miliequivalente (mEq), donde 1 Eq = 1000 mEq.
Por ejemplo, para calcular cuántos miliequivalentes de calcio (Ca2+) hay en 0.25 moles de Ca2+:
0.25 mol Ca2+ × (2 Eq / 1 mol Ca2+) × (1000 mEq / 1 Eq) = 500 mEq Ca2+
Diluciones: Ajustando la Concentración
En muchas ocasiones, es necesario reducir la concentración de una solución, un proceso conocido como dilución. Esto se logra añadiendo más solvente (comúnmente agua en soluciones acuosas). Durante la dilución, la cantidad de soluto (moles) permanece constante, pero el volumen total de la solución aumenta, lo que resulta en una disminución de la concentración.
La relación entre la concentración y el volumen antes y después de la dilución se expresa mediante la siguiente ecuación, conocida como la ecuación de dilución:
M1V1 = M2V2
Donde:
- M1 = Concentración inicial (o de la solución madre/stock)
- V1 = Volumen inicial (o de la solución madre/stock)
- M2 = Concentración final (o de la solución diluida)
- V2 = Volumen final (o de la solución diluida)
Es importante que las unidades de concentración (M) y volumen (V) sean las mismas en ambos lados de la ecuación.
Por ejemplo, si tienes 50 mL de una solución de HCl 4.0 M y la diluyes con agua hasta un volumen final de 200 mL, la nueva molaridad (M2) sería:
M2 = (M1V1) / V2 = (4.0 M × 50 mL) / 200 mL = 1.0 M
Otro problema común es determinar cuánto de una solución concentrada (solución madre o stock) se necesita para preparar una cantidad deseada de una solución más diluida. Por ejemplo, si necesitas preparar 5.0 L de una solución de ácido sulfúrico 0.25 M a partir de una solución stock 18 M:
V1 = (M2V2) / M1 = (0.25 M × 5.0 L) / 18 M = 0.0694 L (o 69.4 mL)
Esto significa que necesitarías tomar 69.4 mL de la solución stock de ácido sulfúrico y añadirle suficiente agua para alcanzar un volumen total de 5.0 L.
¿Qué Significa una Concentración al 5%?
La pregunta sobre qué significa una concentración al 5% es excelente, porque la respuesta es: depende. Como hemos visto, el término "porcentaje" por sí solo es ambiguo en el contexto de las concentraciones de soluciones. Una etiqueta que solo dice "5%" sin especificar si es m/m, v/v o m/v, puede llevar a confusiones y errores, especialmente en aplicaciones críticas.
- Si es 5% m/m (masa/masa): Significa que hay 5 gramos de soluto por cada 100 gramos de solución. Por ejemplo, 5 g de sal disueltos en 95 g de agua para obtener 100 g de solución.
- Si es 5% v/v (volumen/volumen): Significa que hay 5 mililitros de soluto por cada 100 mililitros de solución. Esto se aplica cuando tanto el soluto como el solvente son líquidos. Por ejemplo, 5 mL de alcohol en una solución total de 100 mL (completada con solvente hasta ese volumen).
- Si es 5% m/v (masa/volumen): Significa que hay 5 gramos de soluto por cada 100 mililitros de solución. Este es común para soluciones de sólidos disueltos en líquidos. Por ejemplo, 5 g de glucosa disueltos en agua suficiente para hacer un volumen final de 100 mL de solución.
Como puedes observar, aunque el número sea el mismo, la cantidad real de soluto presente en la solución y la forma de prepararla varían significativamente según el tipo de porcentaje al que se refiera.

Cálculo de Concentraciones: Métodos y Herramientas
Los métodos para calcular las concentraciones porcentuales, la molaridad, las ppm/ppb y los equivalentes han sido detallados en las secciones anteriores. Sin embargo, en el laboratorio, a veces la concentración de una de las soluciones es desconocida y se necesita determinar experimentalmente. Uno de los métodos más comunes para esto es la titulación.
La titulación es un método analítico que permite determinar la concentración de una solución desconocida (el analito) mediante su reacción con una solución de concentración conocida (el valorante). Se añade un volumen conocido de la solución valorante a la solución desconocida hasta que la reacción esté completa (el punto de equivalencia), lo cual a menudo se detecta con un indicador de color.
La fórmula general utilizada en titulaciones, basada en el principio de que los moles de soluto en el punto de equivalencia son proporcionales a sus coeficientes estequiométricos, se simplifica a menudo para reacciones 1:1 de la siguiente manera:
C1V1 = C2V2
Donde C1 y V1 son la concentración y el volumen de la solución conocida, y C2 y V2 son la concentración y el volumen de la solución desconocida. Al conocer tres de estas variables, se puede calcular la cuarta.
Preguntas Frecuentes (FAQ)
A continuación, respondemos algunas de las preguntas más comunes sobre la concentración de soluciones:
¿Cuál es la diferencia entre una solución concentrada y una diluida?
Una solución concentrada tiene una gran cantidad de soluto disuelto en relación con el solvente, mientras que una solución diluida tiene una pequeña cantidad. Son términos relativos, por lo que una solución puede ser concentrada en un contexto y diluida en otro. Las unidades cuantitativas de concentración (como el porcentaje o la molaridad) proporcionan una medida exacta.
¿Por qué es importante especificar el tipo de porcentaje (m/m, v/v, m/v)?
Es crucial porque la misma cifra porcentual puede representar cantidades muy diferentes de soluto y, por lo tanto, propiedades químicas y físicas distintas, dependiendo de si se basa en masa/masa, volumen/volumen o masa/volumen. No especificarlo puede llevar a errores significativos en la preparación o el uso de una solución.
¿Cuándo se utilizan ppm o ppb en lugar de porcentajes?
Las unidades de ppm y ppb se utilizan para expresar concentraciones extremadamente bajas de soluto, donde los porcentajes serían números muy pequeños (por ejemplo, 0.0001%). Son comunes en el análisis ambiental, la toxicología y el control de calidad de sustancias muy puras.
¿Por qué la molaridad es la unidad de concentración preferida en las reacciones químicas?
La molaridad es preferida en química porque se basa en el número de moles de soluto. Los moles son una medida directa del número de partículas (átomos, moléculas, iones) que pueden reaccionar. Esto facilita los cálculos estequiométricos y la predicción de la cantidad de producto que se formará en una reacción.
¿Se pueden simplemente sumar los volúmenes del soluto y del solvente para obtener el volumen final de la solución?
No siempre. Mientras que la masa es aditiva (masa de soluto + masa de solvente = masa de solución), el volumen no lo es necesariamente. Cuando se mezclan líquidos, las interacciones intermoleculares pueden causar que el volumen final sea ligeramente mayor o menor que la suma de los volúmenes individuales. Por eso, al preparar soluciones por volumen (como % v/v o molaridad), se recomienda añadir solvente hasta alcanzar el volumen final deseado en un matraz aforado.
Comprender las distintas formas de expresar la concentración de una solución es una habilidad esencial tanto para el estudiante como para el profesional. Ya sea que estemos calculando la fuerza de un desinfectante, la dosis de un medicamento o la pureza del agua, la capacidad de interpretar y calcular las concentraciones nos permite interactuar con el mundo de la química de manera informada y precisa. Cada unidad tiene su propósito y su aplicación específica, y saber cuándo y cómo utilizar cada una es clave para el éxito en cualquier campo que involucre la manipulación de sustancias.
Si quieres conocer otros artículos parecidos a Descifrando la Concentración Porcentual y Más puedes visitar la categoría Química.
